
牛奶蛋白过敏常见于婴幼儿,是由牛奶蛋白引起的异常免疫反应,发病机制可分为IgE或非IgE介导,亦或两者混合介导。目前我国已有多项牛奶蛋白过敏的专家共识,但这些共识均未对IgE和非IgE介导的牛奶蛋白过敏进行区分。鉴于两者在临床上有着明显不同,且婴儿时期非IgE介导的牛奶蛋白过敏更为常见,故中华预防医学会过敏病预防与控制专业委员会组织儿科消化、过敏/免疫、皮肤、营养和儿童保健专业专家,针对非IgE介导的牛奶蛋白过敏类型、临床特征、诊断和营养干预,参考国际指南并结合我国临床实践制定了本指南。本指南的建议更适合基层医师的理解和实践,涉及非IgE介导的牛奶蛋白过敏问题共7大类42条建议。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
牛奶蛋白过敏(cow′s milk protein allergy,CMPA)常见于婴幼儿,是一种由牛奶蛋白引起的异常免疫反应,其发病机制可通过IgE或非IgE介导,亦或两者混合介导。因诊断方法不同,各地报道的CMPA发病率也有所差别。文献报道,全球CMPA的发生率为2.5%~3.0%[1,2],国内报道0~3岁婴幼儿CMPA发生率为0.83%~3.50%[3]。因IgE介导的牛奶蛋白过敏(IgE mediated cow′s milk protein allergy,IgE-CMPA)表现为进食后出现症状的时间短[2],并可参考过敏原检测,故容易判断;而非IgE介导的牛奶蛋白过敏(non-IgE mediated cow′s milk protein allergy,non-IgE-CMPA)表现为进食后出现症状的时间不固定且较长[2],又缺乏实验室辅助诊断手段,故较难判断,往往需要通过试验性膳食回避-口服食物激发(experimental dietary avoidance-oral food challenge,EDA-OFC)来明确诊断。普遍共识牛奶蛋白EDA-OFC阳性的患儿,牛奶蛋白皮肤点刺试验(skin prick test,SPT)阳性或能检测到牛奶蛋白特异性IgE(specific IgE,sIgE)者为IgE-CMPA,牛奶蛋白SPT阴性或检测不到牛奶蛋白sIgE者为non-IgE-CMPA[4,5,6]。
目前我国已有多项涉及CMPA的专家共识,如2011版《婴幼儿食物过敏诊治建议》[7]、2013版《中国婴幼儿牛奶蛋白过敏诊治循证建议》[6]和2017版《食物过敏相关消化道疾病诊断与管理专家共识》[8]。这些共识均对CMPA的发生、临床表现、诊断及治疗进行了相关描述,但均未就IgE-CMPA和non-IgE-CMPA进行区分,鉴于IgE-CMPA和non-IgE-CMPA在临床上有着明显不同,并且婴儿时期non-IgE-CMPA更为常见,故本指南由中华预防医学会过敏病预防与控制专业委员会组织儿科消化、过敏/免疫、皮肤、营养和儿童保健专业专家,筛选相关文献对non-IgE-CMPA的类型、临床特征、诊断和营养干预,参考国际指南并结合我国临床实践做出了相应诊治建议。本指南的建议更适合基层医师理解和实践,简称为"中国牛奶过敏基层医师指南"(China-milk allergy in primary care guidelines),又称C-MAP指南。
本指南涉及non-IgE-CMPA问题共7大类42条建议。所有建议推荐的原则,除了根据文献的等级外,采用了专家投票方式进行等级推荐。专家参照2001年英国牛津循证医学证据分级和推荐意见强度[9]、相关指南推荐的强度和自我临床实践中的经验进行等级确定,最终以专家多数意见作为建议的等级推荐(附录1)。
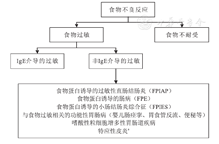
注:根据EAACI和NIAID命名法调整的非IgE介导的过敏性疾病的食物过敏细分;EAACI:欧洲过敏和临床免疫学学会;NIAID:美国国家过敏和传染病研究所;a特应性皮炎也可能由IgE介导,但通常与食物过敏无关 Food allergy subdivision of non-IgE mediated allergic diseases adjusted according to EAACI and NIAID nomenclature;EAACI:European Academy of Allergy and Clinical Immunology;NIAID:National Institute of Allergy and Infectious Diseases;aatopic dermatitis may also be IgE mediated,but it is usually not related to food allergy
non-IgE-CMPA与IgE-CMPA疾病谱明显不同。受累的器官主要以消化道和皮肤为主。在婴儿期,消化道受累包括了器质性病变和功能性胃肠病,而皮肤受累多以特应性皮炎(atopic dermatitis,AD)为主[10,11]。
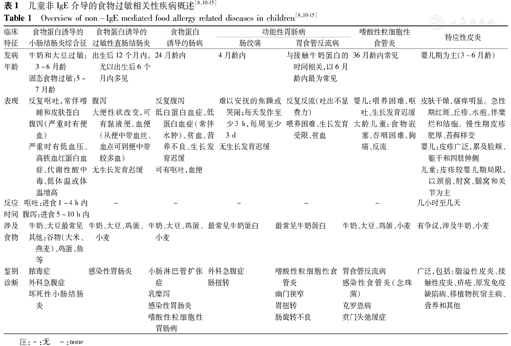
| 临床特征 | 食物蛋白诱导的小肠结肠炎综合征 | 食物蛋白诱导的过敏性直肠结肠炎 | 食物蛋白诱导的肠病 | 功能性胃肠病 | 嗜酸性粒细胞性食管炎 | 特应性皮炎发病 | |
|---|---|---|---|---|---|---|---|
| 肠绞痛 | 胃食管反流病 | ||||||
| 年龄 | 牛奶和大豆过敏:3~6月龄固态食物过敏:5~7月龄 | 出生后12个月内,尤以出生后6个月内多见 | 24月龄内 | 4月龄内 | 与接触牛奶蛋白的时间相关,以6月龄内最为常见 | 36月龄内常见 | 婴儿期为主(3~6月龄) |
| 表现 | 反复呕吐,常伴嗜睡和皮肤苍白 | 腹泻 | 反复腹泻 | 难以安抚的焦躁或哭闹;每天发作至少3 h,每周至少3 d | 反复反流(吐出不显费力) | 婴儿:喂养困难、呕吐、生长发育迟缓 | 皮肤干燥,瘙痒明显。急性期红斑、丘疹、水疱、伴糜烂和结痂。慢性期皮疹肥厚、苔藓样变 |
| 腹泻(严重时有便血) | 大便性状改变,可有黏液便、血便(从便中带血丝、血点可到便中带较多血) | 低白蛋白血症、低蛋白血症(常伴水肿)、贫血、营养不良、生长发育迟缓 | 无生长发育迟缓 | 喂养困难、生长发育受限、贫血 | 大龄儿童:食物嵌塞、吞咽困难、胸痛、反流 | 婴儿:皮疹广泛,累及脸颊、躯干和四肢伸侧 | |
| 严重时有低血压、高铁血红蛋白血症、代谢性酸中毒、低体温或体温增高 | 无生长发育迟缓 | 可有呕吐,血便 | 儿童:皮疹较婴儿期局限,以颈前、肘窝、腘窝和关节为主 | ||||
| 反应 | 呕吐:进食1~4 h内 | - | - | - | - | - | 几小时至几天 |
| 时间 | 腹泻:进食5~10 h内 | ||||||
| 涉及 | 牛奶、大豆最常见 | 牛奶、大豆、鸡蛋、小麦 | 牛奶、大豆、鸡蛋、小麦 | 最常见牛奶蛋白 | 最常见牛奶蛋白 | 牛奶、大豆、鸡蛋、小麦 | 有争议,涉及牛奶、小麦 |
| 食物 | 其他:谷物(大米、燕麦)、鸡蛋、鱼等 | ||||||
| 鉴别诊断 | 脓毒症外科急腹症坏死性小肠结肠炎 | 感染性胃肠炎 | 小肠淋巴管扩张症乳糜泻感染性胃肠炎嗜酸性粒细胞性胃肠病 | 外科急腹症肠扭转 | 嗜酸性粒细胞性食管炎幽门狭窄胃扭转肠旋转不良 | 胃食管反流病感染性食管炎(念珠菌)克罗恩病贲门失弛缓症 | 广泛,包括:脂溢性皮炎、接触性皮炎、疥疮、原发免疫缺陷病、移植物抗宿主病、营养和其他 |
注:-:无
-:none
特别需要注意的是,食物蛋白诱导的各种肠道病变的判断,其中食物蛋白诱导的小肠结肠炎综合征(food protein-induced enterocolitis syndrome,FPIES)少见、严重[13,14];食物蛋白诱导的过敏性直肠结肠炎(food protein-induced allergic proctocolitis,FPIAP)多为母乳喂养,且以血便为主[12,13];食物蛋白诱导的肠病(food protein-induced enteropathy,FPE)较少见,以反复腹泻、小肠吸收功能降低为主,严重时可伴有生长发育迟缓[15]。
病史采集是判断CMPA的重要依据,不同机制介导的CMPA存在着明显不同的特征,不论是在进食牛奶蛋白后到出现症状的时间以及喂养方式和临床表现均有一定差异。婴儿轻中度IgE-CMPA和non-IgE-CMPA的特征见表2。
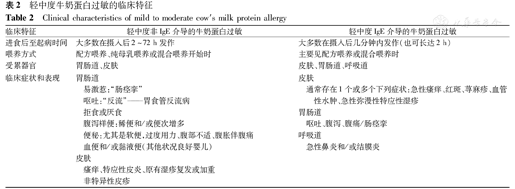
轻中度牛奶蛋白过敏的临床特征
Clinical characteristics of mild to moderate cow′s milk protein allergy
轻中度牛奶蛋白过敏的临床特征
Clinical characteristics of mild to moderate cow′s milk protein allergy
| 临床特征 | 轻中度非IgE介导的牛奶蛋白过敏 | 轻中度IgE介导的牛奶蛋白过敏 | ||
|---|---|---|---|---|
| 进食后至起病时间 | 大多数在摄入后2~72 h发作 | 大多数在摄入后几分钟内发作(也可长达2 h) | ||
| 喂养方式 | 配方喂养、纯母乳喂养或混合喂养开始时 | 主要见配方喂养或混合喂养时 | ||
| 受累器官 | 胃肠道、皮肤 | 皮肤、胃肠道、呼吸道 | ||
| 临床症状和表现 | 胃肠道 | 皮肤 | ||
| 易激惹:"肠痉挛" | 通常存在1个或多个下列症状:急性瘙痒、红斑、荨麻疹、血管性水肿、急性弥漫性特应性湿疹 | |||
| 呕吐:"反流"——胃食管反流病 | 胃肠道 | |||
| 拒食或厌食 | 呕吐、腹泻、腹痛/肠痉挛 | |||
| 腹泻样便:稀便和/或便次增多 | 呼吸道 | |||
| 便秘:尤其是软便,过度用力、腹部不适、腹胀伴腹痛 | 急性鼻炎和/或结膜炎 | |||
| 血便和/或黏液便(其他状况良好婴儿) | ||||
| 皮肤 | ||||
| 瘙痒、特应性皮炎、原有湿疹复发或加重 | ||||
| 非特异性皮疹 | ||||
一般婴儿non-IgE-CMPA临床表现多以胃肠道受累为主,皮肤表现往往以AD为主,且基本不会引起呼吸道受累[5,16]。而婴儿IgE-CMPA往往以皮肤受累为主,表现为急性红斑、风团和血管性水肿为主,且可表现出呼吸道症状[17]。一般纯母乳喂养的婴儿呼吸道受累少见。
根据临床表现可将CMPA分为轻中度过敏和重度过敏,但non-IgE-CMPA和IgE-CMPA的分度依据不同。重度与轻中度non-IgE-CMPA的区分不是以临床表现的轻重为依据,而是以是否因过敏造成了营养不良(如血红蛋白、白蛋白降低)和生长发育障碍,或以消化道是否存在病理性的病变为依据。而重度与轻中度IgE-CMPA的区分则是以是否存在严重的过敏反应,如呼吸困难(如喉头水肿)或过敏性休克等为依据[5,18],见表3。

重度牛奶蛋白过敏的临床特征
Clinical characteristics of severe cow′s milk protein allergy
重度牛奶蛋白过敏的临床特征
Clinical characteristics of severe cow′s milk protein allergy
| 临床特征 | 重度非IgE介导的牛奶蛋白过敏 | 重度IgE介导的牛奶蛋白过敏 | ||
|---|---|---|---|---|
| 进食后至起病时间 | 大多数在摄入后2~72 h发作 | 即刻出现严重反应 | ||
| 喂养方式 | 配方喂养、纯母乳喂养或混合喂养开始时 | - | ||
| 受累器官 | 胃肠道、皮肤 | 全身、呼吸道 | ||
| 临床症状和表现 | 胃肠道 | 过敏性反应 | ||
| 由于慢性腹泻或拒绝吃奶或呕吐引起发育迟缓 | 呼吸道 | |||
| 肠道潜血或镜下血便导致的缺铁性贫血 | 急性喉部水肿或支气管阻塞导致的呼吸困难 | |||
| 低蛋白血症 | ||||
| 内窥镜或病理证实的肠炎或严重的溃疡性结肠炎 | ||||
| 皮肤 | ||||
| 中重度特应性皮炎合并低蛋白血症、贫血、发育迟缓 | ||||
注:-:无
-:none
婴儿功能性胃肠病包括婴儿肠痉挛(表现为哭闹和易激惹)、胃食管反流、功能性腹泻和功能性便秘等[17,19,20]。临床上在判断这些症状是否与CMPA有关时存在一定困难。一般的原则为:不以单纯存在某一功能性胃肠病来考虑其与CMPA的相关性,而是以是否伴随有其他相关的CMPA的症状进行综合考虑[21]。
CoMiSS评分是欧洲建立的一种CMPA相关症状的认知工具,可帮助临床医师进行早期CMPA的诊断[19]。鉴于我国生活习惯和方式的不同,在临床实践中发现CMPA的婴儿很难达到CoMiSS评分推荐的12分标准[22],且对基层医师来说短暂的就诊过程也不易做出评分。因此本指南在CoMiSS评分基础上进行了改良,使其在婴儿功能性胃肠病与CMPA相关性的判定上更为简单易行,见表4。

非IgE介导的牛奶蛋白过敏与婴儿功能性胃肠病的相关性评分
Relevance scoring between non-IgE mediated cow′s milk protein allergy and infant functional gastrointestinal disease
非IgE介导的牛奶蛋白过敏与婴儿功能性胃肠病的相关性评分
Relevance scoring between non-IgE mediated cow′s milk protein allergy and infant functional gastrointestinal disease
| 症状 | 评分 | 程度 |
|---|---|---|
| 腹泻 | 1 | 不成形便,便次增多(>4次) |
| 2 | 稀便,便次增多(>4次)(排除感染) | |
| 3 | 稀便带有较多黏液(排除感染) | |
| 血便 | 3 | 血丝/血点/便中带有较多血 |
| 特应性皮炎 | 1 | vIGA 2分a |
| 2 | vIGA 3分a | |
| 3 | vIGA 4分a | |
| 呼吸道 | 1 | 轻微表现b |
| 2 | 轻度表现b | |
| 3 | 重度表现b |
注:avIGA评分(经验证的研究者整体评估)是特应性皮炎临床研究中广泛使用的一种严重程度评估方法,由国际湿疹协会进行标准化并推广。临床医师可根据皮疹的总体外观(不涉及面积)进行评分,简便快捷(https://www.eczemacouncil.org/assets/docs/vIGA-AD%E2%84%A2CH.pdf)。0分-清除:无特应性皮炎的炎症体征(无红斑、无硬结/丘疹、无苔藓化、无渗出/结痂),可能存在炎症后色素沉着和/或色素减退;1分-基本清除:几乎无法察觉的红斑、几乎无法察觉的硬结/丘疹和/或极轻微的苔藓化,无渗出或结痂;2分-轻度:轻微但明显的红斑(粉红色)、轻微但明显的硬结/丘疹和/或轻微但明显的苔藓化,无渗出或结痂;3分-中度:明显可见的红斑(暗红色)、明显可见的硬结/丘疹和/或明显可见的苔藓化,可能存在渗出和结痂;4分-重度:明显红斑(深或鲜红色)、明显硬结/丘疹和/或明显苔藓化,病变广泛存在,可能存在渗出或结痂。b指流涕、眼痒、咳嗽或喘息等
aThe Validated Investigator Global Assessment (vIGA) is a widely used severity assessment method in clinical studies of atopic dermatitis,which is standardized and promoted by the International Eczema Council.Clinicians can score according to the overall appearance of the rash (not involving the area),which is simple and fast (https://www.eczemacouncil.org/assets/docs/vIGA-AD%E2%84%A2CH.pdf).Score 0-clear:no inflammatory signs of atopic dermatitis (no erythema,no induration/papulation,no lichenification,no oozing/crusting),post-inflammatory hyperpigmentation and/or hypopigmentation may be present;score 1-almost clear:barely perceptible erythema,barely perceptible induration/papulation and/or minimal lichenification,no oozing or crusting;score 2-mild:slight but definite erythema (pink),slight but definite induration/papulation and/or slight but definite lichenification,no oozing or crusting;score 3-moderate:clearly perceptible erythema (dull red),clearly perceptible induration/papulation,and/or clearly perceptible lichenification,oozing and crusting may be present;score 4-severe:marked erythema (deep or bright red),marked induration/papulation,and/or marked lichenification,disease is widespread in extent,oozing or crusting may be present.brefers to runny nose,itchy eyes,coughing or wheezing,etc
本指南"non-IgE-CMPA与婴儿功能性胃肠病的相关性评分"强调是否伴有腹泻、血便、AD和呼吸道症状来进行评分,血便单项评分3分,其余每项评分1~3分,总计最高为12分。建议功能性胃肠病的婴儿评分应达到4分或以上才能考虑与CMPA的相关性,但最终的诊断仍以EDA-OFC结果为准。
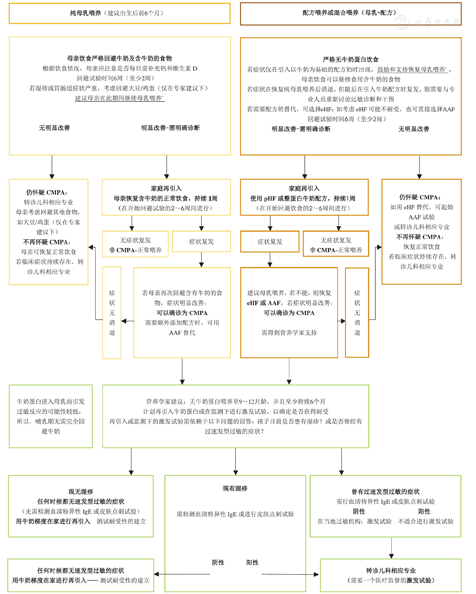

注:eHF:深度水解牛奶蛋白配方;AAF:氨基酸配方;CMPA:牛奶蛋白过敏;pHF:部分水解配方;a母乳是婴儿的最佳营养来源,应尽可能鼓励母乳喂养,世界卫生组织建议母乳喂养至2岁以上;b来自iMAP指南,iMAP指南是2017年英国牵头发布的,针对非IgE牛奶蛋白过敏婴儿的识别、诊断和治疗指南
eHF:extensively hydrolyzed protein formula;AAF:amino acid formula;CMPA:cow′s milk protein allergy;pHF:partially hydrolyzed formula;abreast milk is the best nutrition source for infants,as breastfeeding is encouraged as much as possible,the World Health Organization recommends breastfeeding up to 2 years of age or beyond;bfrom the iMAP guideline,which is a guideline developed primarily by the United Kingdom in 2017 for the identification,diagnosis and treatment of infants with non-IgE mediated cow′s milk protein allergy
non-IgE-CMPA的诊断依赖于详细病史(包括饮食记录)、体格检查以及EDA-OFC的反应[12,17]。但单纯的病史和体格检测不能诊断non-IgE-CMPA,并且non-IgE-CMPA也无可参考的标准实验室诊断方法,因此最终诊断应以牛奶蛋白EDA-OFC结果为准。
膳食回避可明确慢性胃肠道症状和AD对饮食控制的反应。膳食回避牛奶蛋白后,过敏症状显著改善所需的时间,一般在消化道受累的情况下,急性FPIES可在数小时内呕吐和腹泻显著改善,而慢性FPIES需要数天内呕吐和腹泻才能显著改善;FPIAP粪便中可见的血液需要在几天内消失;FPE的症状通常需要1~4周才能消失;而胃肠道的黏膜修复和双糖酶活性恢复则可能需要几个月的时间[23];AD症状的明显改善可能需要2~6周[24]。因此EDA的时间推荐为2~6周,而全程CMPA的膳食回避时间原则上不能少于6个月,且年龄越小建议回避的时间越长,一般需要回避至9~12月龄[4,5]。
IgE-CMPA需要在医院有急救条件的情况下进行OFC[21](方法可见相关指南)。轻中度non-IgE-CMPA可在家里做家庭再引入的OFC[25](附iMAP指南-配方奶喂养再引入牛奶蛋白实例,见表5)。但是如果临床经验不足,无法从临床特征判断出IgE-CMPA或non-IgE-CMPA的情况下,必须是过敏原检测牛奶蛋白sIgE阴性且既往也未发生过速发型过敏反应的婴儿才可以进行家庭再引入的OFC[17]。而重度non-IgE-CMPA的婴儿仍需在医院有急救条件的情况下进行OFC[17,21]。

非IgE介导的牛奶蛋白过敏婴儿配方奶喂养时牛奶蛋白再引入实例
Examples of reintroduction of milk protein in formula fed infant with non-IgE mediated cow′s milk protein allergy
非IgE介导的牛奶蛋白过敏婴儿配方奶喂养时牛奶蛋白再引入实例
Examples of reintroduction of milk protein in formula fed infant with non-IgE mediated cow′s milk protein allergy
| 天数 | 奶瓶液体体积(mL) | 低敏配方(mL) (仅第1瓶) | 牛奶配方(mL) (仅第1瓶) |
|---|---|---|---|
| 第1天 | 210 | 180 | 30 |
| 第2天 | 210 | 150 | 60 |
| 第3天 | 210 | 120 | 90 |
| 第4天 | 210 | 90 | 120 |
| 第5天 | 210 | 60 | 150 |
| 第6天 | 210 | 30 | 180 |
| 第7天 | 210 | 0 | 210 |
注:每天以第1瓶(顿)奶做口服食物激发,即将低敏配方(深度水解牛奶蛋白配方或氨基酸配方)转换为整蛋白牛奶配方。如婴儿第1瓶的奶量为200 mL或以上,经7 d转换过程以确定婴儿是否已经耐受整蛋白牛奶配方,如能耐受则可将一天的全部低敏配方转换为整蛋白牛奶配方;如婴儿第1瓶的奶量未达到200 mL,则需在第1瓶奶转换后,继续转化第2瓶奶,直到达到奶量为200 mL或以上才可以将一天的全部低敏配方转换为整蛋白牛奶配方
When converting from hypoallergenic formula (extensively hydrolyzed protein formula or amino acid formula) to intact protein formula,use the first bottle (feed) of milk of the day as oral food challenge.If a baby′s first bottle of milk is 200 mL or more,a 7-day conversion process is needed to determine whether the baby can tolerate intact protein formula;if tolerated,all hypoallergenic formulas of the day can be converted to intact protein formula.If a baby′s first bottle of milk is below 200 mL,after the conversion of the first bottle,another bottle of milk needs to be converted until the volume of milk reaches 200 mL or more,at which all hypoallergenic formulas of the day can be converted to intact protein formula
牛奶蛋白EDA-OFC是诊断non-IgE-CMPA的唯一可靠方法[4,16,17]。但需要注意以下几点:(1)一般non-IgE-CMPA不能以EDA症状改善作为最终诊断的参考,一定要以EDA时症状改善、OFC时症状再现作为最终的诊断参考[5];(2)non-IgE-CMPA在EDA时,不要求症状完全缓解,只要是症状明显改善即可考虑行OFC[17,26];(3)non-IgE-CMPA行OFC时可能会受到过敏原的量和分子大小的影响,因此不能用煮沸的牛奶行OFC[25]。
SPT和血清sIgE检测过敏原仅对IgE-CMPA具有诊断参考价值,对non-IgE-CMPA不具有诊断参考价值[6,16,27],即牛奶蛋白过敏原SPT和sIgE阴性者仍然不能排除non-IgE-CMPA。也不建议以特异性IgG和IgG4水平来诊断non-IgE-CMPA,也不能以单纯血中嗜酸性粒细胞增高作为诊断指标[14,20]。如果临床表现和进食牛奶蛋白后症状出现的时间明确指向non-IgE-CMPA时,也可不做过敏原筛查[21,27]。
non-IgE-CMPA所致的AD,EDA时应以特应性皮炎积分指数(SCORAD)评分来判断AD症状严重程度的改善(SCORAD评分下降≥10分)[28]。症状改善后应进行OFC,并在OFC前和至少16~24 h后进行SCORAD评分来确定非IgE介导的湿疹反应。AD婴儿行OFC时应注意:(1)应在无症状的间歇期或皮疹稳定期进行,如果皮疹仅靠EDA没有达到稳定,则必须在开始OFC前加强局部治疗;(2)EDA-OFC期间,不应改变伴随治疗和个人环境因素;(3)如果无法避免外用激素,建议每日使用低效外用皮质类固醇激素并持续整个OFC过程[28]。而其他抗炎药物、抗组胺药物或紫外线疗法不能同时使用。
出生后纯母乳喂养是所有婴儿的首选。世界卫生组织(World Health Organization,WHO)建议纯母乳喂养至出生后6个月,之后可继续母乳喂养至2岁或2岁以上,并辅以适当的辅食[4]。不论是IgE-CMPA还是non-IgE-CMPA,母乳喂养的婴儿一般不建议停母乳。但考虑母亲饮食可能是导致婴儿产生过敏反应的原因,建议母亲行EDA-OFC,以观察婴儿过敏反应的情况。只有当母亲EDA时婴儿过敏症状明显改善,且母亲OFA时婴儿过敏反应再现才需要母亲持续的膳食回避。鉴于婴儿期食物过敏以牛奶和鸡蛋过敏的概率最高[29],因此建议母亲行EDA时首先回避牛奶和鸡蛋,如果回避后症状改善不明显,再考虑其他食物过敏。另外,国外有提出考虑到母亲膳食回避,可能存在摄入营养不足会导致母亲和婴儿的营养不良,母亲也可以选择进食深度水解牛奶蛋白配方(extensively hydrolyzed protein formula,eHF)和氨基酸配方(amino acid formula,AAF)[17],但在国内还存在争议。
如有下列情况可考虑暂停母乳,改为AAF替代喂养[8]:(1)尽管母亲膳食回避,婴儿症状仍持续存在且很严重;(2)婴儿生长迟缓和其他营养缺乏;(3)母亲饮食回避导致自身严重体质量减少和影响健康;(4)母亲无法应对心理负担。但停母乳的前提一定是婴儿EDA-OFC结果符合CMPA才可以持续地使用AAF替代喂养。
在纯母乳喂养婴儿停母乳后的低敏配方选择,既往多建议选择eHF喂养,但新近认为母乳与牛奶整蛋白相比是低敏的,并含有一定量的小分子蛋白水解片段,婴儿仍不能耐受,故可能也存在着对eHF不耐受的风险增高,现多推荐AAF替代喂养,以提高耐受的比率。
CMPA婴儿因无法进食整蛋白配方,需要选择低敏配方进行营养替代。对于轻中度CMPA的婴儿初始治疗时,一般国际上建议使用eHF替代,但考虑到轻中度CMPA的婴儿仍然存在着一定比例对eHF的不耐受,而AAF配方是无敏配方,100% CMPA的婴儿均能耐受,因此在国内习惯上在EDA的2~6周可考虑使用AAF替代[30]。
重度CMPA婴儿和不能耐受eHF的CMPA婴儿原则上建议使用AAF进行替代治疗[26]。
在膳食回避到足够长的时间后,是否已经耐受整蛋白配方,需要重新行OFC予以确认[26]。在行OFC之前需要询问病史和过敏原检测,以确定是否可行OFC和行OFC地点的选择[17,31,32](图2)。
世界过敏组织(World Allergy Organization,WAO)和欧洲儿科胃肠病学肝病学和营养学学会(The European Society for Paediatric Gastroenterology Hepatology and Nutrition,ESPGHAN)关于CMPA的其他配方建议[2]:(1)部分水解配方(partially hydrolyzed formula,pHF)可能仍含有免疫反应性表位,不适合用于CMPA婴儿的替代治疗;(2)由于>90%的CMPA婴儿可能同时伴有羊奶过敏反应,因此不建议使用羊奶配方替代治疗;(3)由于30%~50%的CMPA婴儿可能同时伴有大豆过敏反应,不建议使用大豆配方替代治疗,特别是6个月内的婴儿。
non-IgE-CMPA的婴儿再行OFC时,可将pHF作为普通配方先行激发,如能耐受的婴儿可利用pHF持续喂养,也可在此基础上再行整蛋白配方OFC。该选择的意义在于,在不能耐受整蛋白配方的non-IgE-CMPA婴儿中,有一定比例的婴儿可以耐受pHF,从而可减少eHF和AAF的使用[4]。如果要做pHF序贯转换承接,其时间点一定要遵循指南推荐做OFC时先行进行,而不是在6个月干预过程中随意转换承接。
non-IgE-CMPA婴儿应在过敏症状,尤其是胃肠道症状得到良好控制时,开始添加辅食。辅食添加的时间和原则与正常婴儿相同[6]。
纯母乳喂养的non-IgE-CMPA婴儿,鼓励纯母乳喂养至满6月龄[33,34],在继续母乳喂养的基础上添加辅食。基于花生过敏的早期了解(learning early about peanut allergy,LEAP)研究[35]和耐受探索(enquiring about tolerance,EAT)研究[36]以及对辅食添加研究的系统性回顾[37],非纯母乳喂养的non-IgE-CMPA婴儿,可以在婴儿满4月龄后,且能安全进食固体食物时(如抬头稳、能靠坐,伸舌反射消失),开始添加辅食,且应持续、规律摄入多样化的食物[38]。
non-IgE-CMPA婴儿辅食添加也应从富铁的泥糊状食物开始,如婴儿营养米粉、瘦肉等,逐渐增加食物种类及进食量。引入新食物时,应密切观察是否有过敏现象[39],但不应盲目回避易过敏食物,如鸡蛋、花生、鱼、虾等[27]。如尝试某种新食物出现不良反应,须及时停止,3个月后再尝试从更低剂量开始少量引入。辅食添加初期(4~9月龄),建议以引入新的食物为重点,尽量减少不必要的配方转换。
轻中度non-IgE-CMPA婴儿可在家庭中进行牛奶蛋白的再引入,家庭再引入可从致敏性低的含有牛奶蛋白的烘焙食物开始。依据iMAP指南[16]的"牛奶蛋白梯度引入"实例,并结合中国婴儿奶制品选择习惯,建议在婴儿序贯转换至pHF后,逐渐从少量开始再引入牛奶蛋白。
引入牛奶蛋白可遵循以下五个步骤:第一步,引入少许含牛奶蛋白的饼干开始,逐渐增加进食量;第二步,引入其他含牛奶蛋白较高的烘烤产品;第三步,引入奶酪;第四步,引入酸奶;第五步,巴氏消毒奶。在重新引入牛奶蛋白期间,不应引入任何其他新的食物,如果期间出现任何过敏症状应立即停止,返回上一步。
过敏预防应分级预防,所谓一级预防是指出生后未发生过敏时,作为过敏的高风险人群应采取的营养策略。因此有关过敏高风险人群的筛查和确认,应该在孕期和围生期就开始。
国际上研究通常以家族过敏史(包括父母和/或兄弟姐妹过敏史)来定义婴儿发生过敏的高危因素[40]。研究表明,有家族过敏史的婴儿,其CMPA的发病率较正常人群高出3倍。若家族中有AD或哮喘病史,婴儿发生CMPA的风险更高[41]。
母乳喂养可降低婴儿食物过敏风险[42,43]。母乳蛋白质为同种蛋白质,对婴儿免疫系统无刺激,而且母乳中还存在少量来自哺乳母亲的食物特异性抗原,如卵清蛋白(ovalbumin)、β-乳球蛋白(β-lactoglobulin)、麦醇溶蛋白(gliadin)及花生(peanut)等,可适当刺激婴儿的免疫系统,促进免疫发育和免疫耐受[44,45]。母乳中丰富的低聚糖、分泌性IgA、细胞因子、益生菌等均有助于降低婴儿食物过敏风险[46,47]。因此,建议婴儿出生早期纯母乳喂养,鼓励纯母乳喂养至婴儿满6月龄,随后在继续母乳喂养的基础上添加辅食[39]。
当不能母乳喂养或母乳不足时,过敏高风险的婴儿可选择有循证依据的pHF预防过敏[48,49]。关于pHF是否能有效预防过敏或AD仍存在一定争议[50]。但2020年德国婴儿营养干预(Germany infant nutrition intervention,GINI)研究公布了其20年随访结果,仍提示水解蛋白配方具有一定的预防AD作用,远期也可降低呼吸道过敏的风险[51]。
过敏高风险婴儿辅食添加原则和方法与正常婴儿相同。依据LEAP研究[35]和EAT研究[36]以及对辅食添加研究的系统性回顾[37],建议非纯母乳喂养的过敏高风险婴儿在4~6月龄间可引入鸡蛋,而牛奶、鱼、小麦、大豆等其他易过敏食物也应在适当时间引入;出生第1年引入食物种类多,可降低食物过敏风险。
膳食回避是目前治疗食物过敏的唯一有效方法[7],但膳食回避致使可食用的食物种类减少,有可能影响婴儿能量、蛋白质和微量营养素的摄入,导致其出现营养不均衡,严重的可致营养不良。由于婴儿期母乳和/或婴儿配方乳为婴儿的唯一(或)主要营养来源,CMPA的婴儿母亲或自身回避了牛奶蛋白,故发生营养不足或缺乏的风险更高。因此在婴儿CMPA的治疗和管理中,需要进行定期的营养评估,并根据具体情况给予个性化的喂养和营养指导,以保证正常的生长发育。
生长良好是婴儿营养充足的最佳指标,因此身高、体质量的测量是简单评价CMPA婴儿营养状况的主要内容。
在儿童的营养评价中推荐使用Z评分。Z值评分法可比较不同年龄、不同性别儿童生长发育情况,是最常用的儿童体格生长评价方法。根据婴儿的实际体质量和身高,结合WHO儿童生长标准图表(0~2岁)的Z评分(https://www.who.int/tools/child-growth-standards),可确定婴儿生长指标的Z值。通过评价年龄的身长Z评分(length-for-age Z score,LAZ)、年龄的体质量Z评分(weight-for-age Z score,WAZ)和身长的体质量Z评分(weight-for-length Z score,WLZ)来判断儿童的营养状况[52]。
由于生长速度对机体营养状况敏感,采用生长曲线图来评估连续的生长变化非常必要。通过将测量的体质量和身长值标注于生长曲线上以评估生长发育状态,监测生长发育趋势,对发现生长发育异常起到帮助作用。0~2岁婴幼儿推荐使用WHO的多中心生长曲线作为生长的参考依据。
仅有单个时间点的数据时,鉴别及诊断指标均为Z评分,包括WLZ、LAZ、WAZ。有2个以上时间点的数据时,强调生长曲线的应用,指标包括体质量增长速率(2岁以下),WLZ下降等(附录2)。
另外,血红蛋白和血浆白蛋白的检测在评估营养不良时也具有重要的意义[52]。
指南制定机构 中华预防医学会过敏病预防与控制专业委员会
所有作者均声明不存在利益冲突

| 序号 | 建议 | 推荐等级 |
|---|---|---|
| 1 | Non-IgE-CMPA相关疾病类型及特征 | |
| 2 | 婴儿non-IgE-CMPA与IgE-CMPA的临床表现、鉴别和分度 | |
| 3 | Non-IgE-CMPA相关功能性胃肠病诊断 | |
| (1) | 功能性胃肠病与CMPA的相关性取决于是否伴有功能性胃肠病之外的CMPA相关症状 | C |
| (2) | "Non-IgE-CMPA与婴儿功能性胃肠病的相关性评分"是通过是否伴有腹泻、血便、特应性皮炎和呼吸道症状来进行评分 | C |
| (3) | "Non-IgE-CMPA与婴儿功能性胃肠病的相关性评分"应达到4分或4分以上才可考虑其与CMPA相关 | C |
| 4 | 轻中度non-IgE-CMPA诊断流程 | |
| (4) | Non-IgE-CMPA的最终诊断应以牛奶蛋白EDA-OFC结果为准 | A |
| (5) | EDA时间为2~6周,全程膳食回避时间原则上不能少于6个月;对于小月龄婴儿,一般建议回避至其9~12月龄 | A |
| (6) | IgE-CMPA需要在医院有急救条件的情况下进行OFC | A |
| (7) | 明确的轻中度non-IgE-CMPA可在家里做家庭再引入的OFC | A |
| (8) | 不能判定IgE-或non-IgE-CMPA时,须在过敏原检测牛奶蛋白sIgE阴性且既往无速发型过敏反应,才可在家庭进行再引入的OFC | B |
| (9) | 重度non-IgE-CMPA需在医院有急救条件的情况下进行OFC | A |
| (10) | Non-IgE-CMPA须以EDA时症状改善、OFC时症状再现作为最终的诊断参考 | A |
| (11) | Non-IgE-CMPA在EDA时,症状明显改善即可考虑做OFC | B |
| (12) | Non-IgE-CMPA不能用煮沸的牛奶做OFC | B |
| (13) | SPT和血清sIgE检测过敏原对non-IgE-CMPA的诊断不具有参考价值 | B |
| (14) | 特异性IgG和IgG4水平不能作为non-IgE-CMPA的诊断依据 | A |
| (15) | 单纯血中嗜酸性粒细胞增高不能作为non-IgE-CMPA诊断指标 | B |
| (16) | AD婴儿行EDA时,应以SCORAD评分来判断症状严重程度的改善(SCORAD评分下降≥10分) | B |
| (17) | AD婴儿症状改善后应进行OFC,并在16~24 h后进行SCORAD评分以确定非IgE介导的湿疹反应 | B |
| (18) | AD婴儿须在无症状的间歇期或皮疹稳定期才可进行OFC | A |
| (19) | AD婴儿在EDA-OFC期间,不应改变伴随的治疗和个人环境因素 | B |
| (20) | 纯母乳喂养non-IgE-CMPA的婴儿,一般不建议停母乳喂养 | A |
| (21) | 怀疑婴儿过敏与母亲饮食有关,只有当母亲做EDA-OFC的结果符合CMPA时,母亲才可持续膳食回避 | B |
| (22) | 母亲进行EDA时,应首先回避牛奶和鸡蛋,如症状改善不明显,再考虑其他食物的回避 | B |
| (23) | 在膳食回避过程中,母亲亦可选择进食eHF或AAF,以降低母亲与婴儿可能发生营养不良的风险 | D |
| (24) | 不能耐受母乳喂养的CMPA婴儿,可直接使用AAF替代喂养,以避免可能存在的对eHF不耐受的风险 | B |
| (25) | 确诊为CMPA的婴儿,在以下特殊情况下可考虑AAF替代母乳喂养:①尽管母亲膳食回避,婴儿症状仍持续且很严重;②婴儿生长迟缓和存在其他营养缺乏;③由于饮食回避导致母亲体质量严重减少;④母亲无法应对心理负担 | B |
| (26) | 人工(或混合)喂养的轻中度CMPA婴儿,国际上建议首选eHF替代喂养治疗,国内习惯在EDA阶段的2~6周可考虑使用AAF替代喂养治疗 | B |
| (27) | 人工(或混合)喂养的重度CMPA婴儿,建议直接使用AAF替代喂养治疗 | B |
| (28) | CMPA婴儿持续膳食回避6个月后,需通过OFC确认是否已耐受整蛋白配方 | B |
| (29) | 不建议使用pHF替代喂养治疗CMPA | A |
| (30) | 不建议使用羊奶配方替代喂养治疗CMPA | B |
| (31) | 不建议使用大豆配方替代喂养治疗CMPA,特别是6个月内的婴儿 | B |
| (32) | Non-IgE-CMPA患儿在做OFC时,可将pHF作为普通配方先行做激发,也可在此基础上再做整蛋白配方OFC | C |
| 5 | CMPA婴儿的辅食添加 | |
| (33) | Non-IgE-CMPA婴儿应在过敏症状,尤其是胃肠道症状得到良好控制时,才可开始添加辅食 | B |
| (34) | 纯母乳喂养的non-IgE-CMPA婴儿,鼓励纯母乳喂养至满6月龄,在继续母乳喂养的基础上添加辅食 | A |
| (35) | 非纯母乳喂养的non-IgE-CMPA婴儿,可在满4月龄后,且能安全进食固体食物时,开始添加辅食 | A |
| (36) | CMPA婴儿在辅食添加初期(4~9月龄),建议以引入新食物为重点,尽量减少不必要的配方转换 | B |
| (37) | CMPA婴儿在辅食添加时不应盲目回避易过敏食物,但应在引入新食物时,密切观察是否有不良反应。如有不良反应,须及时停止,3个月后再从低剂量开始少量引入 | B |
| (38) | 轻中度non-IgE-CMPA婴儿可在家中从致敏性低的含有牛奶蛋白的烘焙食物开始再引入牛奶蛋白 | B |
| (39) | 轻中度non-IgE-CMPA婴儿在序贯转换至pHF后,可从少量开始逐渐引入牛奶蛋白 | B |
| 6 | 过敏预防营养策略 | |
| (40) | 对于过敏高风险人群,提倡母乳喂养,预防过敏的发生 | A |
| (41) | 对于过敏高风险人群,不能母乳喂养或母乳不足时,可使用有循证依据的pHF喂养来预防过敏 | B |
| (42) | 过敏高风险婴儿辅食添加原则和方法与正常婴儿相同 | B |
| 7 | CMPA婴儿营养及生长发育评估 |
注:推荐等级是根据循证证据、相关指南推荐意见,结合专家自我临床实践经验进行等级确定,最终以专家多数意见作为建议的等级推荐。推荐等级分为高等强度(A)、中等强度(B)、低等强度(C)、不推荐(D)。结果的评定:9名专家参与了等级评定;8名专家评定结果集中在同一等级,以该等级为最终推荐;8名专家评定结果集中在2个等级或3个等级,以低的等级为最终推荐结果;有2名专家评定结果为不推荐的,以不推荐为最终推荐等级

单一时间点的儿科营养不良鉴别指标(SD)
单一时间点的儿科营养不良鉴别指标(SD)
| 指标 | 轻度营养不良 | 中度营养不良 | 重度营养不良 |
|---|---|---|---|
| 身长的体质量Z评分 | -2.0~-1.0 | -3.0~-2.0 | <-3.0 |
| 年龄的身高Z评分 | 无数据 | 无数据 | <-3.0 |

2个或多个时间点来源数据的营养不良鉴别指标
2个或多个时间点来源数据的营养不良鉴别指标
| 指标 | 轻度营养不良 | 中度营养不良 | 重度营养不良 |
|---|---|---|---|
| 体质量增长速度(<2岁) | 正常体质量增长速度的50%~<75% | 正常体质量增长速度的25%~<50% | <正常体质量增长速度25% |
| 身长的体质量Z评分下降 | 下降1个Z评分 | 下降2个Z评分 | 下降3个Z评分 |



























