
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
囊性部分分化性肾母细胞瘤(cystic partially differentiated nephroblastoma,CPDN)是临床上较罕见的儿童肾源性肿瘤,属于良性或潜在低度恶性肿瘤,预后良好。现将华中科技大学同济医学院附属同济医院收治1例病例报告如下。
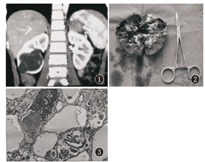
患儿,男,7岁9个月,因腹痛伴呕吐体检发现右肾囊肿伴结石2个月收入院。患儿入院时已无腹痛及呕吐等症状。查体:腹部平软,未触及包块,双侧肾区无叩击痛,心肺无异常。化验检查血常规:WBC 5.34×109/L,RBC 4.72×1012/L,血红蛋白135.0 g/L,红细胞比容44%,血小板278×109/L;生化:丙氨酸氨基转移酶23 U/L,天冬氨酸氨基转移酶28 U/L,尿素4.91 mmol/L,肌酐63 μmol/L,电解质及尿常规均正常。2个月前的多层螺旋CT尿路造影提示:右肾中下极多发低密度灶,范围约5.1 cm×4.0 cm,其内可见高密度影,边界欠清,腹膜后未见明显肿大淋巴结,左肾正常,考虑多发性肾囊肿可能,右肾结石(图1)。本次入院复查彩超提示:右肾囊性病灶,右肾多发结石伴右肾轻度积水,左肾正常;胸片未见异常,腹部平片未见阳性结石征象。术前诊断:右肾囊性病变:肾囊肿?囊性肾瘤?囊性肾母细胞瘤?治疗行右肾切除及肿瘤切除术,术中见右肾绝大部分被瘤体占据,仅上极有部分正常肾组织存留,集合系统受侵犯,瘤体包膜完整,质地较硬,剖面呈多房性,囊液清黄色,囊肿壁呈白色纤维状,无正常肾实质结构,瘤体中心可见少许坏死灶,未见结石(图2)。病理报告:CPDN(输尿管断端未见肿瘤组织)。免疫组织化学:波形蛋白、Wilms肿瘤蛋白-1、胶质纤维酸性蛋白、上皮膜抗原均为(+),结蛋白灶性(+),神经元特异性烯醇化酶、酸性钙结合蛋白S-100(-),蛋白Ki-67标记指数约60%(图3)。术后患儿恢复良好,未进行放化疗,8个月随访,无复发及转移。

CPDN是一种好发于婴幼儿相对少见的肾源性肿瘤,文献报告年龄多<24个月[1]。在囊性肾肿瘤中,多囊性肾瘤(MCN)和囊性肾母细胞瘤(CWT)容易与CPDN混淆[2]。
临床上CPDN术前诊断困难,本报告患儿只因腹痛及呕吐行体检发现右肾囊性占位性病变,多数病例主要表现是发现腹部包块。术前影像学检查无法与其他肾脏囊性占位相鉴别,最终需病理确诊,有学者做过针吸活检诊断,但其可能导致局部扩散复发和不能确定诊断等风险,未得到推广[3]。
对于CPDN的治疗同样难以确定,Joshi和Beckwith[2]认为如术中与其他囊性肾肿瘤难区别,可经术中冷冻切片病理诊断,如诊断为MCN,可仅行肿瘤切除,保留部分肾实质,可避免全肾切除。Baker等[4]报道1例Ⅲ期CPDN术后复发,考虑复发原因与术中肿瘤破溃污染有关,强调肿瘤完整切除的重要性和术后随诊复查的必要性。Green[5]将CPDN划分为肾母细胞瘤的一种特殊类型,如Ⅰ期,年龄﹤6个月,肿瘤质量﹤550 g,一般不伴微小转移灶,将仅行单纯肾脏切除术,不行化疗。Blakely等[6]报道21例患儿治疗结果发现:所有患儿都存活,均未发现复发及转移,Ⅰ级CPDN行单纯肾切除与肾切除加用术后化疗的疗效无差别,Ⅱ级以上的患儿在患肾及肿瘤切除后加用长春新碱和放线菌素D的化疗取得良好的效果。van den Hoek等[7]对6例MCN、CPDN和CWT患儿回顾性分析发现,如在影像学中发现的囊性肾肿瘤无明显实质性肿瘤成分时,应采取手术优先治疗方案。本组1例术后经病理科及肿瘤科综合会诊意见,肿瘤包膜完整,已行患肾完全切除,无侵犯征象,考虑伴微小转移灶可能性小、化疗不良反应大,术后未化疗,现已随访8个月未见复发,但需进一步密切随访。


























