
探讨口服补充乳清蛋白制剂对儿童重度肝损害的安全性和营养治疗作用。
病理确诊为重度肝损害患儿50例,男26例,女24例;年龄4~14岁,采取前瞻性随机对照研究,分为试验组和对照组,各25例。完善伦理和知情同意后,对照组服用自然食物,试验组予自然食物+乳清蛋白粉,2组热量换算保持相同。分别于治疗前1 d和治疗后4周内,观察2组耐受性、营养治疗、肝细胞损伤指标和体质量变化情况。组间比较采用SPSS 17.0软件进行统计学分析。
研究期间,试验组有2例(8.6%),对照组有1例(4.8%)患儿发生轻微的恶心、腹胀症状。与对照组比较,第2周开始试验组清蛋白[(35.6±4.1) g/L比(30.2±3.6) g/L,P<0.05]和前清蛋白[(169.7±40.9) g/L比(103.3±54.8) g/L,P<0.05]显著高于对照组,4周后作用仍然持续。总蛋白自第3周开始显示出类似差异[(67.8±6.5) g/L比(59.1±6.6) g/L,P<0.05]。2组体质量变化差异有统计学意义[(0.20±0.04) kg比(-0.80±0.05) kg,P<0.05]。丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)均较干预前下降,尽管组间比较差异有统计学意义,但试验组ALT[(72.2±30.8) U/L比(88.8±33.5) U/L,P<0.05]和AST[(60.6±20.4) U/L比(70.8±27.3) U/L,P<0.05]特定时间下降更为明显。2组血红蛋白始终未显示出统计学差异。
分离乳清蛋白粉是一种安全有效的蛋白补充制剂,可作为蛋白补充剂在临床营养治疗中推荐使用。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肝脏是人体重要的代谢器官,儿童因器官发育不成熟更易受多种因素影响,导致肝损害同时伴有不同程度的低蛋白血症和营养摄入不足[1]。分离乳清蛋白其安全性已在成人肝病临床试验中取得满意效果[2,3]。但该营养制剂对儿童肝病是否具有良好的耐受性,尚缺乏临床多次连续使用的相关研究。在临床营养治疗中,对低蛋白血症且清蛋白≤28 g/L重度肝损害患儿,常规采用人血清蛋白注射液作为蛋白质补充,能取得较好的疗效。但对清蛋白值<35 g/L患儿经口膳食补充蛋白制剂较少,根据欧洲肠外肠内营养学会(ESPEN)关于肝病肠内营养的指南推荐,对于慢性肝病患者,建议采用经口摄入营养补充剂的肠内营养方式补充所需能量。肝损害患儿往往胃肠道功能较完整,具备进行肠内营养的生理条件。因此,本研究通过随机对照的方法,观察肝损害患儿口服补充乳清蛋白制剂的疗效和安全性,旨在探讨适宜肝损害患儿合理有效地营养支持治疗方案,为临床患者安全使用提供依据。
纳入解放军第三〇二医院2013年6月至2014年6月病理确诊为重度肝损害[4]的50例患儿作为研究对象。男26例,女24例;年龄4~14岁;丙氨酸氨基转移酶(ALT)与天冬氨酸氨基转移酶(AST)均高于正常值,总胆红素≤85 μmol/L,所有患者经肝活检病理确诊为重度肝损害;血清蛋白,<35 g/L且≥28 g/L,符合低清蛋白血症诊断标准,病情暂不需要输注人血清蛋白。患儿家长知情同意并签署知情同意书,本试验获医院医学伦理委员会批准。
(1)依从性差,无法按要求口服乳清蛋白粉制剂的患儿;(2)3个月内合并其他严重心、肺、脑病史,恶性肿瘤,糖尿病史;(3)治疗上需静脉输注人血清清蛋白或应用氨基酸制剂;(4)血氨高需禁止高蛋白质食物摄入;(5)同时参加了其他药物的临床研究;(6)因经济或其他原因不能接受正规治疗或未明显好转自动出院者,将排除研究对象。
入选患儿按随机数字表法分为对照组和试验组,各25例,研究期间共有6例因无法按要求口服乳清蛋白而退出研究,余44例中药物性肝损害17例,慢性乙型病毒性肝炎9例,EB病毒性肝炎8例,先天性肝纤维化6例,自身免疫性肝炎4例,2组年龄、性别、病情及治疗等方面比较差异均无统计学意义(P均>0.05),见表1。
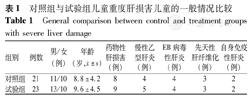
对照组与试验组儿童重度肝损害儿童的一般情况比较
General comparison between control and treatment groups with severe liver damage
对照组与试验组儿童重度肝损害儿童的一般情况比较
General comparison between control and treatment groups with severe liver damage
| 组别 | 例数 | 男/女(例) | 年龄(岁, ±s) ±s) | 药物性肝损害(例) | 慢性乙型肝炎(例) | EB病毒性肝炎(例) | 先天性肝纤维化(例) | 自身免疫性肝炎(例) |
|---|---|---|---|---|---|---|---|---|
| 对照组 | 21 | 11/10 | 8.8±4.2 | 8 | 4 | 4 | 3 | 2 |
| 试验组 | 23 | 13/10 | 9.6±4.5 | 9 | 5 | 4 | 3 | 2 |
干预前按肝病和儿童饮食要求给予患儿适宜热量的优质蛋白、低脂肪易消化饮食,热量按照1 000+年龄×系数(60~100,年龄越小系数越大)提供,蛋白质占总热量的18%,其中一半以上来自优质蛋白,脂肪低于总热量的25%。试验组在对照组的基础上口服增加博普里奥分离乳清蛋白(美国戴维斯柯国际食品公司,生产批号:LI2J201)10 g/d(蛋白质含量91%),每日分2次随餐或餐后0.5 h服用,5 g/次。对照组服用等热量的自然食物,2组总能量摄入量及蛋白质摄入量差异无统计学意义。填表评估受试者饮食情况,对填写中存在的问题及时予以指导,同时密切注意受试者的依从性,以保证试验结果真实可靠。
采用SPSS 17.0软件进行统计学分析,计量资料用 ±s表示。采用重复测量的多因素方差分析2组间的差异,同一时间点2组差异采用多变量方差分析,组内比较采用重复测量的单因素方差分析,P≤0.05为差异有统计学意义。
±s表示。采用重复测量的多因素方差分析2组间的差异,同一时间点2组差异采用多变量方差分析,组内比较采用重复测量的单因素方差分析,P≤0.05为差异有统计学意义。
试验组2例(8.6%),对照组1例(4.8%)患儿发生轻微的恶心、腹胀症状。余患儿均未出现不耐受的症状。对照组和试验组受试者胃肠道不耐受症状的发生率比较差异无统计学意义。
试验组14 d(后2周)患儿前清蛋白与干预前比较差异有统计学意义,对照组差异未见统计学意义,试验组第21天清蛋白、总蛋白与干预前比较差异有统计学意义,对照组除前清蛋白外差异无统计学意义。试验组在第21天体质量变化不显著,对照组体质量下降(表2)。
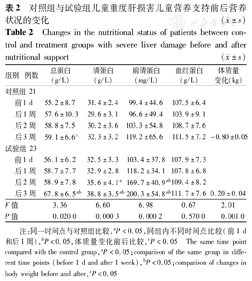
对照组与试验组儿童重度肝损害儿童营养支持前后营养状况的变化 ( ±s)
±s)
Changes in the nutritional status of patients between control and treatment groups with severe liver damage before and after nutritional support ( ±s)
±s)
对照组与试验组儿童重度肝损害儿童营养支持前后营养状况的变化 ( ±s)
±s)
Changes in the nutritional status of patients between control and treatment groups with severe liver damage before and after nutritional support ( ±s)
±s)
| 组别 例数 | 总蛋白(g/L) | 清蛋白(g/L) | 前清蛋白(mg/L) | 血红蛋白(g/L) | 体质量变化(kg) | |
|---|---|---|---|---|---|---|
| 对照组21 | ||||||
| 前1 d | 55.2±8.7 | 31.4±2.4 | 99.4±44.6 | 107.5±6.4 | ||
| 后1周 | 57.6±10.3 | 29.6±3.1 | 96.6±49.4 | 103.9±9.1 | ||
| 后2周 | 58.8±7.5 | 30.2±3.6 | 103.3±54.8 | 108.7±7.6 | ||
| 后3周 | 59.1±6.6c | 32.3±3.2 | 119.2±65.6 | 111.5±7.2 | -0.80±0.05 | |
| 试验组23 | ||||||
| 前1 d | 56.1±6.2 | 32.5±3.3 | 103.4±37.8 | 107.9±7.3 | ||
| 后1周 | 58.7±7.7 | 32.9±2.8 | 118.2±34.1 | 107.8±6.8 | ||
| 后2周 | 58.9±7.8 | 35.6±4.1a | 169.7±40.9ab | 109.4±8.2 | ||
| 后3周 | 67.8±6.5ab | 38.8±3.5ab | 200.3±54.8ab | 111.7±7.6 | 0.20±0.04 | |
| F值 | 3.36 | 6.60 | 6.98 | 0.67 | 2.01 | |
| P值 | 0.020 0 | 0.000 3 | 0.000 2 | 0.570 0 | 0.001 0 | |
注:同一时间点与对照组比较,aP<0.05,同组内不同时间点比较(前1 d和后1周),bP<0.05,体质量变化前后比较,cP<0.05 The same time point compared with the control group,aP<0.05;comparison of the same group in diffe-rent time points (before 1 d and after 1 week),bP<0.05;comparison of changes in body weight before and after,cP<0.05
ALT、AST均较干预前下降,尽管组间比较下降差异无统计学意义,但试验组下降在特定时间更为明显(P<0.05)。2组血红蛋白未显示出统计学差异(表3)。
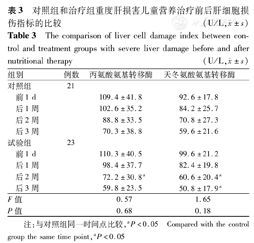
对照组和治疗组重度肝损害儿童营养治疗前后肝细胞损伤指标的比较(U/L, ±s)
±s)
The comparison of liver cell damage index between control and treatment groups with severe liver damage before and after nutritional therapy(U/L, ±s)
±s)
对照组和治疗组重度肝损害儿童营养治疗前后肝细胞损伤指标的比较(U/L, ±s)
±s)
The comparison of liver cell damage index between control and treatment groups with severe liver damage before and after nutritional therapy(U/L, ±s)
±s)
| 组别 | 例数 | 丙氨酸氨基转移酶 | 天冬氨酸氨基转移酶 | |
|---|---|---|---|---|
| 对照组 | 21 | |||
| 前1 d | 109.4±41.8 | 92.6±17.8 | ||
| 后1周 | 102.6±35.2 | 84.2±25.7 | ||
| 后2周 | 88.8±33.5 | 70.8±27.3 | ||
| 后3周 | 70.3±38.8 | 59.6±21.6 | ||
| 试验组 | 23 | |||
| 前1 d | 110.3±40.5 | 99.6±21.2 | ||
| 后1周 | 98.4±37.7 | 82.4±19.8 | ||
| 后2周 | 72.2±30.8a | 60.6±20.4a | ||
| 后3周 | 59.8±23.5 | 50.8±17.9a | ||
| F值 | 0.57 | 1.65 | ||
| P值 | 0.68 | 0.18 | ||
注:与对照组同一时间点比较,aP<0.05 Compared with the control group the same time point,aP<0.05
儿童时期肝脏结缔组织发育不全,与成人相比对外界的刺激更为敏感,容易受到各种有害因素的影响而使肝细胞发生肿胀、变性甚至坏死、导致不同程度的肝损害[5]。严重肝损害患儿普遍存在低蛋白血症和营养不良,一方面是由于患儿本身能量消耗快,伴随疾病的发生出现食欲下降、正常进食量的减少,导致摄入不足,体质量下降;另一方面由于小儿肝脏对一些必需酶合成能力低下,其分解、合成、储存和解毒能力不完善,肝损害以后易出现低蛋白血症和凝血酶原活力下降,影响某些激素和微量元素的生成[6]。因此,营养支持治疗已成为这类患儿综合治疗的重要组成部分。分离乳清蛋白被称为蛋白之王,是公认的人体优质蛋白质补充剂之一。本研究结果显示,口服蛋白制剂的患儿仅有3例出现轻微恶心、腹胀症状,其他时间未发生任何胃肠道不耐受的表现。分析原因可能与儿童肝损害本身临床症状有关。
本研究试验组和对照组的总能量摄入及蛋白质摄入量差异无统计学意义,但试验组第2周患儿前清蛋白与干预前比较差异有统计学意义,第3周时前清蛋白、清蛋白、总蛋白与干预前比较差异有统计学意义,而对照组除3周时前清蛋白与干预前比较差异有统计学意义,余未见统计学差异。这主要是因为乳清蛋白纯度高、消化吸收率高、氨基酸组成合理,对机体安全无刺激[7]。对于临床使用乳清蛋白,可有助于血清清蛋白的恢复,减少静脉人血清蛋白的使用量,一方面节约了资源,另一方面减轻了家长经济负担。试验结束时2组体质量变化差异有统计学意义,对照组体质量在4周内体质量丢失明显,而试验组体质量基本没有改变。因此认为,体质量的丢失与营养物质摄入不足和肝脏合成清蛋白的功能障碍相关,而在就餐后0.5 h内口服分离乳清蛋白粉是可以补充机体所需能量,防止体质量的进一步丢失,本试验也验证了这一点。因此,乳清蛋白是肝损害患儿补充蛋白质能量的良好来源。
乳清蛋白所含必需氨基酸,能通过抗脂质过氧化作用快速有效地合成身体所需蛋白质以修复坏死肝细胞,促进肝功能恢复并促进肝脏细胞恢复和新生,促进防止变性肝细胞坏死而发展为肝硬化[8]。同时,乳清蛋白脂肪含量低,在满足蛋白质需求时,不会因脂肪摄入过多造成肝功能进一步损害。2组患儿营养治疗前后肝细胞损伤结果比较显示,尽管组间比较差异无统计学意义,但在药物治疗方法不变的情况下,试验组在特定时间下降更为明显,这提示膳食补充乳清蛋白在改善肝损害患儿肝功能方面具有一定作用。合理的营养支持可促进受损的肝组织修复,保护肝功能,减少致病因素对肝脏的进一步损害[9]。
综上,分离乳清蛋白是一种安全有效的蛋白质营养补充剂,对改善肝损害患儿的营养状况切实有效,对促进患儿肝功能恢复、节约积极资源方面有着重要的意义。



























