
2020年5月7日,国际儿科肾脏病学会发布了国际最新的儿童激素耐药型肾病综合征诊治建议。该建议提出了一些新的诊断名称/定义用于指导治疗。对激素耐药型肾病综合征的诊断流程、非免疫抑制剂和免疫抑制剂治疗的适应证、禁忌证和方案、并发症和终末期肾脏病的管理均提出了明确的建议。现主要介绍该建议要点。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
2020年5月7日,国际儿科肾脏病学会(the International Pediatric Nephrology Association,IPNA)发布了国际上最新的儿童激素耐药型肾病综合征(steroid-resistant nephrotic syndrome,SRNS)诊治建议[1]。该建议提出了一些新的诊断名称/定义用于指导治疗,如多药耐药型SRNS(multi-drug resistant SRNS)、肾移植后复发型肾病综合征等。对SRNS的诊断治疗及终末期肾脏病(end-stage kidney disease,ESKD)阶段的管理均提出了更为明确的建议。现主要介绍建议要点。
该建议根据美国儿科学会证据分级系统评估证据质量[2]。证据等级分为高(A)、中(B)、低(C)、极低(D)或不适用(X)。X是指因明显的利或弊占主导不能进行验证性研究的例外情况。推荐级别分为强推荐、中度推荐、弱推荐和自主决定。
建议在确定SRNS前或调整免疫抑制剂治疗前至少检测1次晨尿或24 h尿尿蛋白/肌酐比(urinary protein/creatinine ratio,UPCR),建议以UPCR作为基线值用于评估治疗反应[3](A,强推荐)。
相关定义见表1(B,中度推荐),其中NS的诊断标准为肾病水平蛋白尿伴低白蛋白血症(血清白蛋白<30 g/L)或水肿(若无血清白蛋白数据)。

儿童肾病综合征相关定义
Definitions relating to nephrotic syndrome in children
儿童肾病综合征相关定义
Definitions relating to nephrotic syndrome in children
| 专业术语 | 定义 |
|---|---|
| 肾病水平蛋白尿 | 晨尿UPCR ≥200 mg/mmol(2 mg/mg)或24 h尿尿蛋白≥1 000 mg/m2,试纸检测尿蛋白3+或4+ |
| 肾病综合征 | 肾病水平蛋白尿伴低白蛋白血症(血清白蛋白<30 g/L)或水肿(若无血清白蛋白数据) |
| SSNS | PDN标准剂量[60 mg/(m2·d)或2 mg/(kg·d),最大量60 mg/d]治疗4周内完全缓解 |
| SRNS | PDN标准剂量治疗4周后未达完全缓解 |
| 确认期 | 从开始PDN标准剂量治疗4~6周。在此期间,对于经4周PDN治疗获部分缓解者继续口服PDN和/或静脉甲泼尼龙冲击同时加用RAASi治疗,评估治疗反应。若6周时完全缓解则判定为迟发激素敏感,若未完全缓解则判定SRNS |
| 完全缓解 | 至少连续3次UPCR(晨尿或24 h尿)≤20 mg/mmol(0.2 mg/mg)或试纸检测尿蛋白微量或阴性 |
| 部分缓解 | UPCR (晨尿或24 h尿)>20 mg/mmol但<200 mg/mmol,如有检测,血清白蛋白≥30 g/L |
| 复发 | 既往曾达部分缓解或完全缓解的患儿再次出现肾病水平蛋白尿。连续3 d试纸检测尿蛋白≥3+或晨尿UPCR ≥200 mg/mmol(2 mg/mg),伴或不伴水肿 |
| CNI-耐药型SRNS | 1种CNI足量治疗6个月后未达至少部分缓解 |
| 多药耐药型SRNS | 用2种不同作用机制的激素替代药物标准剂量治疗12个月未达完全缓解 |
| 继发激素耐药 | 初治激素敏感者在随后复发中进展为SRNS |
| 肾移植后复发型肾病综合征 | SRNS患儿肾移植后无明确病因再次出现肾病水平蛋白尿和/或足突融合。若既往无尿者移植后出现持续性蛋白尿(UPCR≥100 mg/mmol)(1 mg/mg),或移植时有蛋白尿者移植后无明确病因UPCR增加≥100 mg/mmol(1 mg/mg),应考虑此诊断 |
注:UPCR:尿蛋白/肌酐比;SSNS:激素敏感型肾病综合征;PDN:泼尼松或泼尼松龙;SRNS:激素耐药型肾病综合征;RAASi:肾素-血管紧张素-醛固酮系统拮抗剂;CNI:钙调磷酸酶抑制剂 UPCR:urine protein/creatinine ratio;SSNS:steroid-sensitive nephrotic syndrome;PDN:Prednisone/Prednisolone;SRNS:steroid-resistant nephrotic syndrome;RAASi:inhibitors of renin-angiotensin-aldosterone system;CNI:calcineurin inhibitor
即开始标准剂量泼尼松/泼尼松龙(Prednisone/Prednisolone,PDN)治疗后4~6周这段时间为确认期,用于进一步确定患儿对PDN的治疗反应(C,弱推荐)。建议在确认期考虑基因检测和/或肾活检(B,中度推荐)。
建议详细询问肾和肾外表现的家族史及近亲婚配史。若有肾脏疾病家族史,应尽可能询问患病家庭成员发病年龄、临床过程及对药物治疗反应、肾功能、肾活检和基因检测结果(A,强推荐)。
仔细查体,确定有无肾外表现如骨骼、神经系统、眼、耳和泌尿生殖系统发育畸形,确定有无可致NS的继发性病因如感染灶(表2)(A,强推荐)。
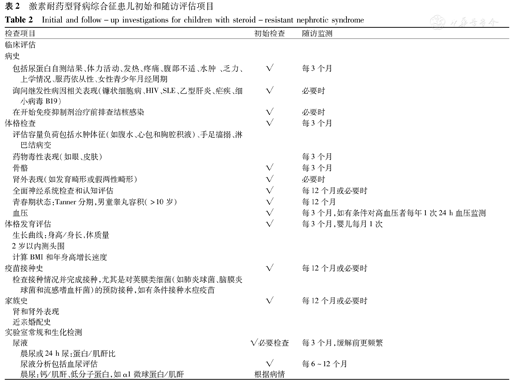
激素耐药型肾病综合征患儿初始和随访评估项目
Initial and follow-up investigations for children with steroid-resistant nephrotic syndrome
激素耐药型肾病综合征患儿初始和随访评估项目
Initial and follow-up investigations for children with steroid-resistant nephrotic syndrome
| 检查项目 | 初始检查 | 随访监测 | ||
|---|---|---|---|---|
| 临床评估 | ||||
| 病史 | ||||
| 包括尿蛋白自测结果、体力活动、发热、疼痛、腹部不适、水肿、乏力、上学情况、服药依从性、女性青少年月经周期 | √ | 每3个月 | ||
| 询问继发性病因相关表现(镰状细胞病、HIV、SLE、乙型肝炎、疟疾、细小病毒B19) | √ | 必要时 | ||
| 在开始免疫抑制剂治疗前排查结核感染 | √ | 必要时 | ||
| 体格检查 | √ | 每3个月 | ||
| 评估容量负荷包括水肿体征(如腹水、心包和胸腔积液)、手足搐搦、淋巴结病变 | ||||
| 药物毒性表现(如眼、皮肤) | 每3个月 | |||
| 骨骼 | √ | 每3个月 | ||
| 肾外表现(如发育畸形或假两性畸形) | √ | 必要时 | ||
| 全面神经系统检查和认知评估 | √ | 每12个月或必要时 | ||
| 青春期状态:Tanner分期,男童睾丸容积(>10岁) | √ | 每12个月 | ||
| 血压 | √ | 每3个月,如有条件对高血压者每年1次24 h血压监测 | ||
| 体格发育评估 | √ | 每3个月,婴儿每月1次 | ||
| 生长曲线:身高/身长,体质量 | ||||
| 2岁以内测头围 | ||||
| 计算BMI和年身高增长速度 | ||||
| 疫苗接种史 | √ | 每12个月或必要时 | ||
| 检查接种情况并完成接种,尤其是对荚膜类细菌(如肺炎球菌、脑膜炎球菌和流感嗜血杆菌)的预防接种,如有条件接种水痘疫苗 | ||||
| 家族史 | √ | 每12个月或必要时 | ||
| 肾和肾外表现 | ||||
| 近亲婚配史 | ||||
| 实验室常规和生化检测 | ||||
| 尿液 | √必要检查 | 每3个月,缓解前更频繁 | ||
| 晨尿或24 h尿:蛋白/肌酐比 | ||||
| 尿液分析包括血尿评估 | √ | 每6~12个月 | ||
| 晨尿:钙/肌酐、低分子蛋白,如α1微球蛋白/肌酐 | 根据病情 | |||
| 血液 | √必要检查 | 每3个月,缓解前和CKD 4~5期检测更频繁 | ||
| 全血细胞计数 | ||||
| 肌酐、尿素氮、或尿素 | ||||
| 电解质(包括离子钙、钾) | 使用大量利尿剂时每日1次或隔日1次 | |||
| 血清白蛋白、总蛋白 | ||||
| 血气分析(HCO3) | ||||
| C-反应蛋白 | √ | 必要时 | ||
| 估算肾小球滤过率 | √ | 每3个月,CKD 4期时更频繁 | ||
| ALP、PTH、25(OH)维生素D | √ | 每12个月,CKD 3~5期时更频繁 | ||
| 脂代谢检查(LDL-胆固醇和HDL-胆固醇、三酰甘油) | √ | 每12个月或必要时 | ||
| 凝血功能检测(凝血酶原时间、INR、aPTT、纤维蛋白原、抗凝血酶Ⅲ);对既往有血栓史、中心静脉置管、持续肾病水平蛋白尿和/或血栓家族史者进行细致的血栓筛查 | √ | 诊断时,之后在必要时尤其复发时 | ||
| 甲状腺功能(T3、FT4、TSH) | √ | 每12个月或必要时,尤其是持续蛋白尿者 | ||
| 免疫球蛋白G | √ | 反复感染时 | ||
| 糖/空腹血糖 | √ | 每6个月或必要时 | ||
| 糖化血红蛋白 | √ | 每12个月或必要时 | ||
| C3、抗核抗体 | √ | 必要时 | ||
| 抗ds-DNA、ENA、ANCA | 根据病情 | 必要时 | ||
| HBs-Ag、抗HCV抗体、梅毒和HIV检测 | √ | 在泼尼松/泼尼松龙治疗前及必要时 | ||
| 疫苗接种状况,包括抗体滴度测定 | √ | 每年1次或必要时 | ||
| 基因检测 | ||||
| 二代测序/全外显子测序 | 对已知致病基因进行全面检测(表3);若拟肾移植者可行全外显子测序 | |||
| 药物监测 | ||||
| 环孢素A和他克莫司:谷浓度测定 | 调药阶段每周1次连测4周。之后每3个月1次或必要时 | |||
| 霉酚酸酯:霉酚酸动力学分析(2 h) | 治疗4周后测AUC值,之后每6~12个月1次或必要时 | |||
| 利妥昔单抗 | 给药前和首次给药后1个月(最低点)分析CD19 B细胞计数,每1~3个月检测1次直至B细胞恢复 | |||
| 他汀类药物:肌酸激酶 | 若用他汀类药物,每6个月检测1次 | |||
| 长期糖皮质激素治疗 | 根据病情 | 眼科检查白内障和眼压,腰椎双能X线骨密度检测 | ||
| 影像学 | ||||
| 肾脏超声:肾脏回声和大小 | √ | 起病时(肾活检前必行超声检查) | ||
| 腹部和胸膜腔超声(腹水、积液、血栓) | √ | 必要时 | ||
| 心脏超声(左心室质量指数、积液) | √ | 高血压者每12个月1次或严重水肿时 | ||
| 胸部X线 | √ | 必要时 | ||
| 左腕X线检查(>5岁儿童的骨龄评估、骨矿化评估) | √ | 每12个月或必要时 | ||
| 组织病理学(肾活检) | √ | 见正文 | ||
| 营养咨询 | ||||
| 营养师对盐、钾、热卡和蛋白质摄入提出建议 | √ | 每3个月1次(婴儿、营养不良和CKD 4~5期患儿更频繁) | ||
| 肾外表现评估(根据所患疾病和肾外异常表现) | √必要时 | 必要时 | ||
| 头颅磁共振(如有小头畸形、运动发育落后、智力发育迟缓、肌阵挛性癫痫、震颤、共济失调和肌张力低下表现) | ||||
| 眼科(如白内障、青光眼、视神经萎缩、圆锥角膜、黄斑病变、圆锥形晶体、眼球震颤) | ||||
| 心脏(如先天性心脏病) | ||||
| 内分泌(如有假两性畸形、青春期延迟、原发性闭经、糖尿病) | ||||
| 皮肤科(如大疱性表皮松解) | ||||
| 骨科(如髌骨缺如或发育不全,脊柱骨骺发育不良) | ||||
| 免疫评估(T淋巴细胞免疫缺陷) | ||||
| 血液学(如巨血小板减少症,Döhle体) | ||||
| 听力(感音神经性耳聋) | ||||
注:HIV:人类免疫缺陷病毒;SLE:系统性红斑狼疮;BMI:体质量指数;CKD:慢性肾脏病;ALP:碱性磷酸酶;PTH:甲状旁腺激素;LDL:低密度脂蛋白;HDL:高密度脂蛋白;INR:国际标准化比值;aPTT:活化部分凝血活酶时间;T3:三碘甲状腺原氨酸;FT4:游离甲状腺素;TSH:促甲状腺激素;ds-DNA:双链DNA;ENA:可提取核抗原;ANCA:抗中性粒细胞胞浆抗体;HBs-Ag:乙型肝炎病毒表面抗原;HCV:丙型肝炎病毒 HIV:human immunodeficiency virus;SLE:systemic lupus erythematosus;BMI:body mass index;CKD:chronic kidney disease;ALP:alkaline phosphatase;PTH:parathyroid hormone;LDL:low density lipoprotein;HDL:high density lipoprotein;INR:international normalized ratio;aPTT:activated partial thromboplastin time;T3:tri-iodothyronine;FT4:free thyroxine;TSH:thyroid stimulating hormone;ds-DNA:double strand DNA;ENA:extractable nuclear antigen;ANCA:anti-neutrophil cytoplasmic antibodies;HBs-Ag:hepatitis B virus surface antigen;HCV:hepatitis C virus
建议行表2列出的血液和尿液检测,寻找SRNS相关免疫病因或感染因素,评估蛋白尿程度、估算肾小球滤过率(estimated glomerular filtration rate,eGFR)和肾脏病理改变(B,中度推荐)。建议在基因检测前完成患儿兄弟姐妹的尿液检测。
若疑似结核感染或有流行地区旅居史,建议根据国家有关指南行相关检测评估亚临床结核感染,如胸部X线检查、结核菌素试验或干扰素释放试验(C,中度推荐)。为排除继发性病因及在开始免疫抑制剂尤其是利妥昔单抗治疗前,建议检测乙型肝炎病毒、丙型肝炎病毒、梅毒和人类免疫缺陷病毒(C,弱推荐)。
建议对所有诊断为原发性SRNS者行基因检测(B,中度推荐)[4]。对有蛋白尿/血尿或不明原因慢性肾脏病(chronic kidney disease,CKD)家族史、肾外表现或拟行肾移植者优先检测(C,弱推荐)。若很快(数周内)可获得基因检测结果,建议在肾活检前完成,尤其对需优先行基因检测者(D,弱推荐)。不建议对初治激素敏感继发激素耐药者行基因检测(C,中度推荐)。
建议行全面基因检测,包含全部已知SRNS致病基因(表3)的二代测序是目前性价比最高的检测方案[5]。若临床表型提示特定基因也可行单基因检测(B,中度推荐)。建议根据美国医学遗传学会指南分析遗传变异的致病性[6](B,中度推荐)。建议为患儿及家人提供遗传咨询,解释检测结果(B,中度推荐)。
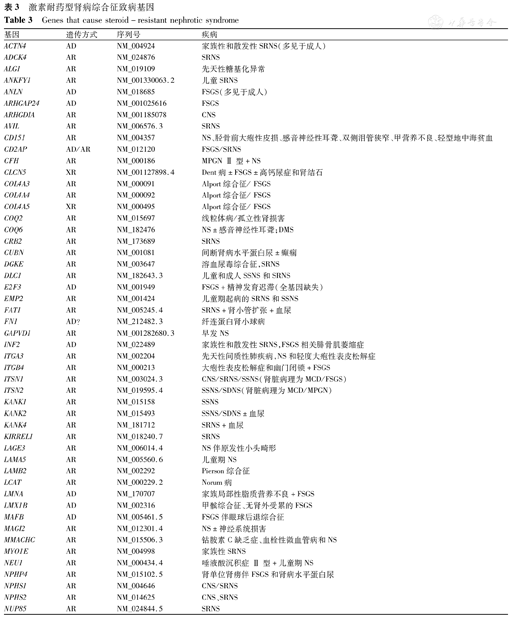
激素耐药型肾病综合征致病基因
Genes that cause steroid-resistant nephrotic syndrome
激素耐药型肾病综合征致病基因
Genes that cause steroid-resistant nephrotic syndrome
| 基因 | 遗传方式 | 序列号 | 疾病 |
|---|---|---|---|
| ACTN4 | AD | NM_004924 | 家族性和散发性SRNS(多见于成人) |
| ADCK4 | AR | NM_024876 | SRNS |
| ALG1 | AR | NM_019109 | 先天性糖基化异常 |
| ANKFY1 | AR | NM_001330063.2 | 儿童SRNS |
| ANLN | AD | NM_018685 | FSGS(多见于成人) |
| ARHGAP24 | AD | NM_001025616 | FSGS |
| ARHGDIA | AR | NM_001185078 | CNS |
| AVIL | AR | NM_006576.3 | SRNS |
| CD151 | AR | NM_004357 | NS、胫骨前大疱性皮损、感音神经性耳聋、双侧泪管狭窄、甲营养不良、轻型地中海贫血 |
| CD2AP | AD/AR | NM_012120 | FSGS/SRNS |
| CFH | AR | NM_000186 | MPGN Ⅱ型+NS |
| CLCN5 | XR | NM_001127898.4 | Dent病±FSGS±高钙尿症和肾结石 |
| COL4A3 | AR | NM_000091 | Alport综合征/ FSGS |
| COL4A4 | AR | NM_000092 | Alport综合征/ FSGS |
| COL4A5 | XR | NM_000495 | Alport综合征/ FSGS |
| COQ2 | AR | NM_015697 | 线粒体病/孤立性肾损害 |
| COQ6 | AR | NM_182476 | NS±感音神经性耳聋;DMS |
| CRB2 | AR | NM_173689 | SRNS |
| CUBN | AR | NM_001081 | 间断肾病水平蛋白尿±癫痫 |
| DGKE | AR | NM_003647 | 溶血尿毒综合征,SRNS |
| DLC1 | AR | NM_182643.3 | 儿童和成人SSNS和SRNS |
| E2F3 | AD | NM_001949 | FSGS+精神发育迟滞(全基因缺失) |
| EMP2 | AR | NM_001424 | 儿童期起病的SRNS和SSNS |
| FAT1 | AR | NM_005245.4 | SRNS+肾小管扩张+血尿 |
| FN1 | AD? | NM_212482.3 | 纤连蛋白肾小球病 |
| GAPVD1 | AR | NM_001282680.3 | 早发NS |
| INF2 | AD | NM_022489 | 家族性和散发性SRNS,FSGS相关腓骨肌萎缩症 |
| ITGA3 | AR | NM_002204 | 先天性间质性肺疾病,NS和轻度大疱性表皮松解症 |
| ITGB4 | AR | NM_000213 | 大疱性表皮松解症和幽门闭锁+FSGS |
| ITSN1 | AR | NM_003024.3 | CNS/SRNS/SSNS(肾脏病理为MCD/FSGS) |
| ITSN2 | AR | NM_019595.4 | SSNS/SDNS(肾脏病理为MCD/MPGN) |
| KANK1 | AR | NM_015158 | SSNS |
| KANK2 | AR | NM_015493 | SSNS/SDNS±血尿 |
| KANK4 | AR | NM_181712 | SRNS+血尿 |
| KIRREL1 | AR | NM_018240.7 | SRNS |
| LAGE3 | AR | NM_006014.4 | NS伴原发性小头畸形 |
| LAMA5 | AR | NM_005560.6 | 儿童期NS |
| LAMB2 | AR | NM_002292 | Pierson综合征 |
| LCAT | AR | NM_000229.2 | Norum病 |
| LMNA | AD | NM_170707 | 家族局部性脂质营养不良+FSGS |
| LMX1B | AD | NM_002316 | 甲髌综合征、无肾外受累的FSGS |
| MAFB | AD | NM_005461.5 | FSGS伴眼球后退综合征 |
| MAGI2 | AR | NM_012301.4 | NS±神经系统损害 |
| MMACHC | AR | NM_015506.3 | 钴胺素C缺乏症、血栓性微血管病和NS |
| MYO1E | AR | NM_004998 | 家族性SRNS |
| NEU1 | AR | NM_000434.4 | 唾液酸沉积症Ⅱ型+儿童期NS |
| NPHP4 | AR | NM_015102.5 | 肾单位肾痨伴FSGS和肾病水平蛋白尿 |
| NPHS1 | AR | NM_004646 | CNS/SRNS |
| NPHS2 | AR | NM_014625 | CNS、SRNS |
| NUP85 | AR | NM_024844.5 | SRNS |
| NUP93 | AR | NM_014669 | 儿童期SRNS |
| NUP107 | AR | NM_020401 | 儿童期SRNS |
| NUP160 | AR | NM_015231.2 | SRNS |
| NUP205 | AR | NM_015135 | 儿童期SRNS |
| NXF5 | XR | NM_032946 | FSGS伴心脏传导阻滞 |
| OCRL | XR | NM_000276 | Dent病2型、Lowe综合征、±FSGS、±肾病水平蛋白尿 |
| OSGEP | AR | NM_017807.4 | NS伴原发性小头畸形 |
| PAX2 | AD | NM_003987 | 无肾外表现的成年期发病的FSGS |
| PDSS2 | AR | NM_020381 | Leigh综合征 |
| PLCe1 | AR | NM_016341 | CNS/SRNS |
| PMM2 | AR | NM_000303 | 先天性糖基化异常 |
| PODXL | AD | NM_005397 | FSGS |
| PTPRO | AR | NM_030667 | NS |
| SCARB2 | AR | NM_005506 | 动作性肌阵挛-肾衰综合征±听力下降 |
| SGPL1 | AR | NM_003901.4 | 原发性肾上腺皮质功能不全和SRNS |
| SMARCAL1 | AR | NM_014140 | Schimke免疫-骨发育不良 |
| SYNPO | AD | NM_007286 | 散发FSGS(启动子突变) |
| TBC1D8B | XR | NM_017752.3 | 早发SRNS和FSGS |
| TNS2 | AR | NM_170754.3 | SSNS/SDNS(肾脏病理为MCD/FSGS/DMS) |
| TP53RK | AR | NM_033550.4 | NS伴原发性小头畸形 |
| TPRKB | AR | NM_001330389.1 | NS伴原发性小头畸形 |
| TRPC6 | AD | NM_004621 | 家族性和散发性SRNS(主要是成人) |
| TTC21B | AR | NM_024753 | FSGS伴肾小管间质病变 |
| WDR73 | AR | NM_032856 | Galloway-Mowat综合征(小头畸形和SRNS) |
| WT1 | AD | NM_024426 | 散发SRNS(儿童:可能有生殖器异常)、Denys-Drash综合征和Frasier综合征 |
| XPO5 | AR | NM_020750 | 儿童期SRNS |
| ZMPSTE24 | AR | NM_005857 | 下颌骨锁骨发育不全伴FSGS |
| MYH9 | AD | NM_002473 | MYH9相关疾病、Epstein和Fechtner综合征 |
| APOL1 | G1,G2易感基因 | NM_003661 | 非洲裔美国人、西班牙裔美国人和非洲人易发生FSGS和终末期肾脏病 |
注:AD:常染色体显性遗传;SRNS:激素耐药型肾病综合征;AR:常染色体隐性遗传;FSGS:局灶节段性肾小球硬化;CNS:先天性肾病综合征;NS:肾病综合征;MPGN:膜增生性肾小球肾炎;XR:X连锁遗传;DMS:弥漫性系膜硬化;SSNS:激素敏感型肾病综合征;MCD:微小病变;SDNS:激素依赖型肾病综合征;MYH9:肌球蛋白重链9 AD:autosomal dominant;SRNS:steroid-resistant nephrotic syndrome;AR:autosomal recessive;FSGS:focal segmental glomerulosclerosis;CNS:congenital nephrotic syndrome;NS:nephrotic syndrome;MPGN:membranoproliferative glomerulonephritis;XR:X-linked recessive;DMS:diffuse mesangial sclerosis;SSNS:steroid-sensitive nephrotic syndrome;MCD:minimal change disease;SDNS:steroid-dependent nephrotic syndrome;MYH9:myosin heavy chain 9
建议对所有SRNS患儿行肾活检,除非已确定SRNS继发于感染或恶性肿瘤、或患儿为家族性和/或综合征性或遗传性SRNS(A,强推荐)。
建议诊断SRNS后立即开始RAASi治疗[7,8](B,中度推荐)。建议开始血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitors,ACEi)/血管紧张素受体拮抗剂(angiotensin receptor blockers,ARBs)治疗后监测晨尿蛋白变化(D,弱推荐)。药量目标值为患儿可耐受的最大允许剂量(表4)(C,弱推荐)。

血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂剂量推荐
Recommendations for the dosage of angiotensin converting enzyme inhibitors/angiotensin receptor blockers
血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂剂量推荐
Recommendations for the dosage of angiotensin converting enzyme inhibitors/angiotensin receptor blockers
| 药物 | 年龄 | 初始剂量 | 最大量 | |
|---|---|---|---|---|
| 血管紧张素转换酶抑制剂 | ||||
| 禁忌证:妊娠期、血管神经性水肿 | ||||
| 常见不良反应:咳嗽、头痛、头晕、乏力 | ||||
| 严重不良反应:高钾血症、急性肾损伤、血管神经性水肿、胎儿毒性 | ||||
| 贝那普利 | ≥6岁a | 0.2 mg/(kg·d)(≤10 mg/d) | 0.6 mg/(kg·d)(≤40 mg/d) | |
| 卡托普利 | 婴儿 | 0.05 mg/(kg·次) | 6 mg/(kg·d),1~4次/d | |
| 儿童 | 0.5 mg/(kg·次) | 6 mg/(kg·d),3次/d | ||
| 依那普利 | ≥1个月a | 0.08 mg/(kg·d) (≤5 mg/d) | 0.6 mg/(kg·d) (≤40 mg/d),1~2次/d | |
| 福辛普利 | ≥6岁 | |||
| <50 kg | 0.1 mg/(kg·d)(≤5 mg/d) | 40 mg/d | ||
| ≥50 kga | 5 mg/d | 40 mg/d | ||
| 赖诺普利 | ≥6岁a | 0.07 mg/(kg·d)(≤5 mg/d) | 0.6 mg/(kg·d) (≤40 mg/d) | |
| 雷米普利b | - | 1.6 mg/(m2·d) | 6 mg/(m2·d) | |
| 喹那普利 | - | 5 mg/d | 80 mg/d | |
| 血管紧张素受体拮抗剂b | ||||
| 禁忌证:妊娠期 | ||||
| 常见不良反应:头痛、头晕 | ||||
| 严重不良反应:高钾血症、急性肾损伤、胎儿毒性 | ||||
| 坎地沙坦b | 1~5岁a | 0.2 mg/(kg·d)(≤ 4 mg/d) | 0.4 mg/(kg·d)(≤16 mg/d) | |
| ≥6岁a | ||||
| <50 kg | 4 mg/d | 16 mg/d | ||
| ≥50 kg | 8 mg/d | 32 mg/d | ||
| 厄贝沙坦b | 6~12岁 | 75 mg/d | 150 mg/d | |
| ≥13岁 | 150 mg/d | 300 mg/ d | ||
| 氯沙坦b | ≥6岁a | 0.7 mg/kg (≤50 mg) | 1.4 mg/kg(≤100 mg) | |
| 奥美沙坦b | ≥6岁a | |||
| <35 kg | 10 mg | 20 mg | ||
| ≥35 kg | 20 mg | 40 mg | ||
| 缬沙坦b | ≥6岁a | 1.3 mg/kg(≤40 mg) | 2.7 mg/kg (≤160 mg) | |
注:a美国食品药品监督管理局批准用于儿童;b主要经肝脏代谢,晚期慢性肾脏病患儿无需减量;-不适用 aFood and Drug Administration pediatric labeling;bmainly metabolized by the liver,thus no dose reduction in patients with advanced chronic kidney disease necessary; -:not applicable/available
对CKD 4期者用ACEi或ARBs治疗需谨慎,在患儿存在血容量不足、急性肾损伤(acute kidney injury,AKI)、高钾血症或频繁呕吐/腹泻时不应服用此类药物或停用[9](X,强推荐)。建议用非单一经肾排泄的药物(如雷米普利和ARBs),以避免肾衰时药物排泄障碍导致蓄积(D,弱推荐)。青少年女性患儿服用RAASi类药物期间应严格避孕,以避免药物致畸作用(X,强推荐)。
推荐CNIs如环孢素(Cyclosporine A,CsA)或他克莫司(Tacrolimus,TAC)为一线用药[10]。确认SRNS后开始CNIs治疗(图1)(B,中度推荐)。
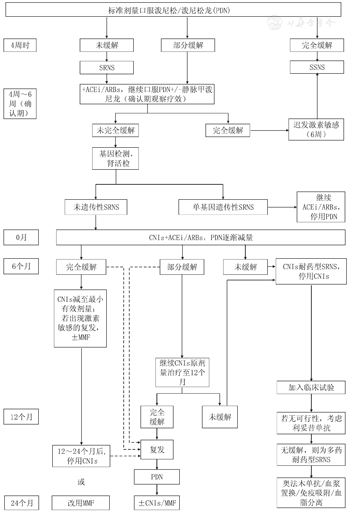

注:PDN:泼尼松/泼尼松龙;SRNS:激素耐药型肾病综合征;SSNS:激素敏感型肾病综合征;ACEi:血管紧张素转换酶抑制剂;ARBs:血管紧张素受体拮抗剂;CNIs:钙调磷酸酶抑制剂;MMF:霉酚酸酯 PDN:Prednisone/Prednisolone;SRNS:steroid-resistant nephrotic syndrome;SSNS:steroid-sensitive nephrotic syndrome;ACEi:angiotensin-converting enzyme inhibitors;ARBs:angiotensin-receptor blockers;CNIs:calcineurin inhibitors;MMF:Mycophenolate mofetil
对于存在eGFR<30 mL/(min·1.73 m2)、AKI和/或未控制的高血压患儿,建议停用或延缓CNIs治疗(X,强推荐)。对确诊单基因遗传性SRNS者,建议停用CNIs和PDN(B,中度推荐)。
建议CsA起始剂量3~5 mg/(kg·d)(最大起始量250 mg/d),每日分2次口服(B,弱推荐)。采用串联质谱分析方法检测CsA全血浓度,目标谷浓度80~120 μg/L(B,弱推荐)。
建议TAC起始剂量0.1~0.2 mg/(kg·d)(最大起始剂量5 mg/d),每日分2次口服(B,弱推荐)。目标谷浓度4~8 μg/L(B,弱推荐)。
建议每周检测1次CsA/TAC谷浓度,直至达目标水平,之后每1~3个月检测1次,同时检测血肌酐以监测药物安全性(D,弱推荐)。若eGFR降至<30 mL/(min·1.73 m2),建议CNIs减量或停用(X,强推荐)。
建议CNIs至少应用6个月以判定疗效(B,弱推荐)。若6个月未达部分缓解,建议停用(B,中度推荐)。若6个月达完全缓解,将CNIs减量至维持缓解所需最低剂量。为减低肾毒性风险,建议疗程12~24个月(C,弱推荐)。可将CNIs转换至霉酚酸酯(mycophenolate mofetil,MMF)治疗以最大程度降低CNIs肾毒性风险并维持缓解。若停用CNIs后NS复发,建议重新开始CNIs联合足量PDN治疗4周,或考虑MMF治疗(C,弱推荐)。若治疗6个月后获部分缓解,建议继续原剂量CNIs治疗至少12个月(C,弱推荐)。
当患儿无法获得或无法负担CNIs治疗时,建议静脉或口服环磷酰胺治疗,联用/不联用大剂量激素(D,弱推荐)。
由于CNIs有肾毒性风险,对于eGFR<30 mL/(min·1.73 m2)者,建议用MMF而非CNIs治疗(C,弱推荐)。若患儿经CNIs治疗缓解后出现激素敏感型NS复发,在复发缓解后建议用MMF维持缓解(C,弱推荐)。若CNIs治疗后NS完全缓解至少12个月,建议用MMF替代CNIs(C,弱推荐)。
不建议长期(> 6个月)常规联用PDN、CNIs和RAASi治疗(C,中度推荐)。建议开始CNIs治疗后PDN按以下方式减量:40 mg/m2隔日服用4周,30 mg/m2隔日服用4周,20 mg/m2隔日服用4周,10 mg/m2隔日服用8周,之后停用(D,弱推荐)[11]。一些SRNS患儿经CNIs治疗达完全缓解后表现为激素依赖型NS,可联用小剂量隔日PDN治疗。
若在随访期间出现无法解释的eGFR下降或尿蛋白增加,建议重复肾活检评估CNIs肾毒性[12](C,弱推荐)。建议对长期使用CNIs(> 2年)或开始第2疗程CNIs治疗者行重复肾活检(C,弱推荐)。
建议让患儿和家属知晓免疫抑制剂不良反应(X,强推荐)。
建议经CNIs治疗后未达至少部分缓解且无遗传性或综合征性疾病的患儿加入SRNS新治疗临床试验(未分级)。
建议对所有患儿检测已知足细胞病基因以决定后续免疫抑制剂的应用(X,强推荐)。对遗传性和/或多药耐药型患儿,告知患儿和父母患儿存在进展至ESKD的高风险(X,强推荐)。停用无效的免疫抑制剂治疗,继续非免疫抑制剂治疗管理,包括RAASi和支持治疗(X,强推荐)。对于非遗传性SRNS患儿,建议加入新治疗临床试验(X,强推荐)。
对存在遗传缺陷但经免疫抑制剂治疗获得部分缓解或完全缓解者,建议重新评估基因变异类型,确定变异类型是否致病或可能致病(A,强推荐)。告知患儿父母用药的利(缓解症状、降低疾病进展风险)、弊(药物不良反应、感染)和治疗费用,共同商定是否继续进行免疫抑制剂治疗(A,强推荐)。
避免高盐饮食(C,弱推荐)。如有条件,咨询营养师适合患儿的低盐饮食和应避免的高盐饮食(D,弱推荐)。无证据支持SRNS患儿增加蛋白质摄入量(未分级)。
不建议常规限制液体量(C,弱推荐)。建议根据尿量、容量状态和血钠确定液体入量,维持出入量平衡(C,弱推荐)。建议根据患儿能力和CKD分期进行体育锻炼,保证适合CKD分期的营养需求。建议禁烟(C,中度推荐)。
建议对有严重水肿者应用袢利尿剂(如呋塞米)。对顽固性水肿者,也可考虑加用美托拉宗、噻嗪类利尿剂或保钾利尿剂(C,中度推荐)。由于有导致血栓形成和AKI风险,对于有血容量不足征象(包括毛细血管再充盈时间延长、心动过速、低血压和少尿)者不应使用利尿剂(X,强推荐)[19]。
建议人血白蛋白输注用于治疗具有难治性水肿(心包/胸腔积液、全身水肿、生殖器水肿)和/或症状性低血容量或有肾前危象(因血容量不足导致的少尿)者(C,中度推荐)。建议应用20%~25%的白蛋白起始剂量0.5~1.0 g/kg静脉输注4~8 h,输注过程中和/或输注结束后静脉注射呋塞米1~2 mg/kg(C,弱推荐)。输注白蛋白期间每30 min监测1次血压和心率,若出现任何容量负荷过重征象应减慢输注或停药(X,强推荐)。
建议监测并发症和药物不良反应(表5)(B,中度推荐)。
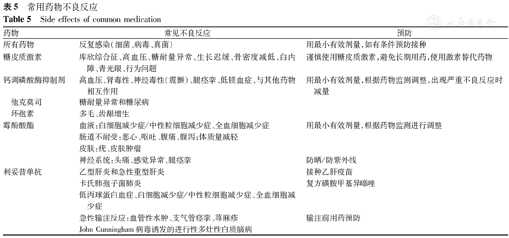
常用药物不良反应
Side effects of common medication
常用药物不良反应
Side effects of common medication
| 药物 | 常见不良反应 | 预防 | |
|---|---|---|---|
| 所有药物 | 反复感染(细菌、病毒、真菌) | 用最小有效剂量,如有条件预防接种 | |
| 糖皮质激素 | 库欣综合征、高血压、糖耐量异常、生长迟缓、骨密度减低、白内障、青光眼、行为问题 | 谨慎使用糖皮质激素,避免长期用药,使用激素替代药物 | |
| 钙调磷酸酶抑制剂 | 高血压、肾毒性、神经毒性(震颤)、腿痉挛、低镁血症、与其他药物相互作用 | 用最小有效剂量,根据药物监测调整,出现严重不良反应时减量 | |
| 他克莫司 | 糖耐量异常和糖尿病 | ||
| 环孢素 | 多毛、齿龈增生 | ||
| 霉酚酸酯 | 血液:白细胞减少症/中性粒细胞减少症、全血细胞减少症 | 用最小有效剂量,根据药物监测进行调整 | |
| 肠道不耐受:恶心、呕吐、腹痛、腹泻;体质量减轻 | |||
| 皮肤:疣、皮肤肿瘤 | |||
| 神经系统:头痛、感觉异常、腿痉挛 | 防晒/防紫外线 | ||
| 利妥昔单抗 | 乙型肝炎和急性重型肝炎 | 接种乙肝疫苗 | |
| 卡氏肺孢子菌肺炎 | 复方磺胺甲基异 唑 唑 | ||
| 低丙球蛋白血症、白细胞减少症/中性粒细胞减少症、全血细胞减少症 | |||
| 急性输注反应:血管性水肿、支气管痉挛、荨麻疹 | 输注前用药预防 | ||
| John Cunningham病毒诱发的进行性多灶性白质脑病 | |||
对存在低血清IgG且有反复感染和/或严重感染者考虑静脉输注丙种球蛋白(D,弱推荐)。不建议常规预防性应用抗生素(C,弱推荐)。对接受利妥昔单抗治疗者,建议根据患儿B细胞恢复情况和联合应用免疫抑制剂情况考虑预防性应用复方磺胺甲基异 唑3~6个月(C,弱推荐)。
唑3~6个月(C,弱推荐)。
建议在起病时全面评估预防接种史,尽快完成所有预防接种,尤其是对荚膜类细菌(肺炎球菌、脑膜炎球菌和流感嗜血杆菌)的预防接种。如有可能,接种水痘疫苗(A,强推荐)。建议每年接种灭活流感疫苗(A,强推荐)。对免疫缺陷患儿的灭活疫苗和减毒活疫苗的接种原则建议遵循国家指南(A,强推荐)。每日应用免疫抑制剂包括CNIs、MMF和PDN治疗期间不能接种活疫苗(X,强推荐)。建议对水痘易感者(未接种水痘疫苗或对水痘无免疫和水痘暴露者)应用水痘-带状疱疹免疫球蛋白(A,强推荐)。如无水痘-带状疱疹免疫球蛋白,建议在水痘暴露后7~10 d内口服阿昔洛韦[10 mg/(kg·次),每日4次,连用7 d](C,中度推荐)。建议对水痘无免疫力的患儿在NS缓解期且未用免疫抑制剂时接种水痘疫苗(A,强推荐)。
建议患儿尽可能活动。除必要短时应用外不建议行中心静脉置管(X,强推荐)。无充分证据支持对既往无血栓史或血栓风险者预防性抗凝治疗(未分级)。建议对既往有血栓史者给予预防性应用低分子肝素或口服抗凝药物。对有额外血栓高危因素者(如中心静脉置管、遗传性易栓症、急性疾病、感染或脱水风险)考虑预防性抗凝治疗(C,弱推荐)。建议对有血栓高危因素(如中心静脉置管、持续性肾病水平蛋白尿、阳性血栓家族史)者进行血栓筛查(C,弱推荐)。
建议根据年龄对持续不缓解的多药耐药型患儿在低密度脂蛋白胆固醇持续>130 mg/dL(3.4 mmol/L)时考虑降脂治疗[20](C,弱推荐)。
若根据离子钙和/或白蛋白矫正后存在低钙血症,建议口服钙剂(C,弱推荐)。若血25(OH)维生素D<30 μg/L,建议补充维生素D3或维生素D2(C,中度推荐)。建议在症状性低镁血症时口服镁剂治疗(D,弱推荐)。
对持续大量蛋白尿者尤其需监测促甲状腺素和游离T4,若促甲状腺素>10 mU/L和游离T4降低,建议用T4治疗(A,强推荐)。
建议根据现有指南治疗高血压和CKD合并症,如贫血、代谢性酸中毒和甲状旁腺功能亢进(A,强推荐)。
尚无可用于预测SRNS复发风险的临床指标或病理指标(未分级)。
在CNIs治疗期间复发时,建议通过测定血药谷浓度监测患儿对CNIs治疗的依从性(C,中度推荐)。建议口服PDN 60 mg/(m2·d),直至NS缓解或最长疗程4周,缓解后逐渐减量(C,弱推荐)。对治疗无反应、频复发或药物不良反应突出者,建议遵循难治性SRNS方案(未分级)。
停用免疫抑制剂治疗后复发时,建议口服PDN60 mg/(m2·d)直至缓解或最长疗程4周,达缓解后逐渐减量。或再次应用可预防复发的免疫抑制剂(D,弱推荐)。若用药后4周内未达完全缓解、频复发或出现药物不良反应,建议遵循难治性SRNS方案(未分级)。
建议对有残存肾功能者在移植前检测尿蛋白,以便在移植后准确监测复发(A,强推荐)。建议在肾脏替代治疗期间与家长讨论肾移植后复发风险(A,强推荐)。若拟对ESKD患儿在NS未缓解前进行移植,建议移植前考虑行肾切除术(D,弱推荐)。
建议在移植前行基因检测,告知移植后SRNS复发风险(B,中度推荐)。建议为SRNS所致ESKD患儿提供肾移植治疗,无论其病因是遗传性还是非遗传性(B,中度推荐)。对于既往有肾移植后SRNS复发史者,需在移植团队内部及与患儿和父母讨论再次肾移植的利弊(A,强推荐)。
如有可能,建议对候选活体肾移植供者行基因检测,评估是否存在SRNS遗传背景(X,强推荐)。不建议将显性基因致病变异或可能致病变异携带者(无论是否有症状)作为肾移植供者(X,强推荐)。
经遗传咨询后,隐性基因杂合变异携带者(除外COL4A5、COL4A3和COL4A4致病性变异携带者)可考虑作为肾移植供者(C,弱推荐)。若无其他供者选择时,无症状未知致病性基因变异携带者在经过详细的评估和咨询后可考虑作为移植供者(C,弱推荐)。
在选择移植供者时,需考虑移植后复发和移植失败风险(A,强推荐)。
在非遗传性SRNS患儿首次肾移植时,活体供肾和尸体供肾移植均可考虑(B,中度推荐)。对第1次肾移植后NS复发者不建议活体供肾移植(B,中度推荐)。对有移植后NS复发导致移植肾失功史者考虑尸体供肾移植,尤其对于透析难以维持或发生过危及生命的事件、重症感染、生长障碍和/或生活质量低下者(C,弱推荐)。
无足够证据用于推荐预防首次肾移植后NS复发的方案(未分级)。对既往有移植后NS复发导致移植肾失功史者,建议再次移植时行预防性血浆置换或免疫吸附或血脂分离及围术期输注利妥昔单抗治疗(C,弱推荐)。
建议在肾移植当天开始监测尿蛋白,在首次移植住院期间每日监测UPCR,然后定期监测(如每周1次连续4周,每月1次连续1年,之后每季度1次)(C,中度推荐)。
若既往无尿者移植后UPCR≥100 mg/mmol(1 mg/mg),提示可能有早期复发、感染或其他情况,需评估(C,弱推荐)。若移植时有蛋白尿者在移植后UPCR增加≥100 mg/mmol(1 mg/mg),提示可能有早期复发、感染或其他情况,需评估(C,弱推荐)。
建议将早期出现的急性肾小管坏死或移植物无功能/功能障碍作为复发早期征象(C,弱推荐)。不必要通过移植肾活检诊断移植后NS快速复发,但若患儿出现非肾病水平蛋白尿、移植后48 h复发或移植肾功能延迟时建议行移植肾活检以鉴别病因(B,中度推荐)。
对于出现晚期NS复发(移植后≥3个月)者,建议在调整免疫抑制治疗方案前进行评估感染情况、血清供体特异性抗体和肾脏病理包括电镜检查结果(B,中度推荐)。
一旦确诊复发,尽快针对NS复发进行治疗(X,强推荐)。建议增加CNIs剂量、静脉甲泼尼龙冲击和/或血浆置换治疗(或免疫吸附)。可联用/不联用利妥昔单抗治疗(C,弱推荐)。建议对经靶向治疗未达完全缓解者开始RAASi治疗(C,弱推荐)。
总之,该建议基于最新临床研究证据对儿童SRNS的多个诊治问题提出了全面的推荐。在诊断方面,将用于NS诊断的血清白蛋白标准定义为<30 g/L。明确提出"确认期"概念用于评估激素治疗效应。对CNI-耐药型SRNS和多药耐药型SRNS提出了明确定义。在治疗方面,仍建议CNIs为一线用药,但也提出应尽可能降低肾毒性风险。明确提出了不适用或停用PDN及其他免疫抑制剂的指征。在预防接种方面,建议在起病时完成必要的预防接种。该建议指出,由于所基于的临床研究样本量偏小,文中的建议存在局限性,多为弱推荐或中度推荐。本文可能存在疏漏或不当,仅供参考,详细内容请见英文原文。
所有作者均声明不存在利益冲突



























