
分析早产儿出生早期外周血中γδ-T淋巴细胞亚群的水平与脑损伤的关系,探讨外周血淋巴细胞亚群对早产儿脑损伤的早期预测价值。
采用前瞻性研究方法,选取2021年1月1日至6月1日在郑州大学第三附属医院新生儿科住院的106例胎龄<34周的早产儿为研究对象,采用流式细胞术检测其出生24 h外周血γδ-T、CD4+T、CD8+T、CD3+T及总淋巴细胞的比例,根据出生后连续头颅超声及纠正胎龄36~37周头颅磁共振成像检查结果,将患儿分为脑损伤组(36例)及无脑损伤组(70例),采用t检验或χ2检验比较2组患儿一般情况及淋巴细胞亚群的差异;将脑损伤组进一步按照不同脑损伤类型分为颅内出血组(8例)、脑室周围白质软化组(6例)及弥散性脑白质损伤组(22例),采用单因素方差分析和LSD-t检验比较各组间淋巴细胞亚群的差异。
脑损伤组早产儿出生24 h外周血中γδ-T淋巴细胞水平[(0.09±0.12)%]低于无脑损伤组早产儿[(0.15±0.13)%],差异有统计学意义(t=-2.445,P=0.016),2组早产儿CD4+、CD8+等T淋巴细胞亚群无差异。脑损伤组患儿中,脑室周围白质软化组或弥散性脑白质损伤组早产儿出生24 h外周血γδ-T淋巴细胞占比[(0.03±0.05)%、(0.07±0.09)%]低于无脑损伤组早产儿[(0.15±0.13)%],差异均有统计学意义(t=-2.190、-2.659,均P<0.05)。
γδ-T淋巴细胞可能与早产儿脑损伤的发生有关;出生早期外周血γδ-T淋巴细胞对早产儿脑损伤,特别是脑白质软化及弥散性脑白质损伤具有预测价值。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
近年来早产发生率较高,随着围生医学及新生儿重症监护技术的进步,早产儿的存活率也显著提高[1]。在中国及全球范围内,早产及其相关并发症,尤其是早产儿脑损伤仍然是导致新生儿死亡和残疾的主要原因。在胎龄<34周或出生体质量<1 500 g的存活早产儿中,5%~15%会遗留神经系统后遗症,包括脑性瘫痪、认知障碍、语言障碍及心理行为问题等[2]。早产儿脑损伤主要包括颅内出血(ICH)、脑室周围白质软化(PVL)及弥散性脑白质损伤[3]。早期预测早产儿脑损伤并及时进行干预和治疗,对降低早产儿脑损伤发生率,从而提高早产儿生存质量至关重要,但目前临床上尚缺乏有效进行早期筛查和预测的指标。
近年来的多项研究发现,淋巴细胞介导的炎症反应参与了多种早产儿疾病,包括脑损伤的形成及发展[4,5,6,7]。根据T淋巴细胞受体(TCR)的不同,人体T淋巴细胞分为αβ-T淋巴细胞和γδ-T淋巴细胞。γδ-T淋巴细胞在出生早期即具备活性,并参与维持新生儿免疫稳态。本课题组研究表明,γδ-T而非αβ-T淋巴细胞促进脓毒血症引起的新生大鼠脑白质损伤并影响后期的运动行为[8]。本研究旨在探讨外周血淋巴细胞亚群,尤其是γδ-T淋巴细胞与早产儿脑损伤的关系,以明确早产儿脑损伤的机制,并筛选早产儿脑损伤的早期预测指标。
采用前瞻性研究方法,选取2021年1月1日至6月1日于郑州大学第三附属医院产科出生并于出生24 h内转至新生儿科治疗的122例早产儿(胎龄28~34周,出生体质量700~2 500 g)为研究对象。
排除标准:先天发育异常、遗传代谢性疾病、红细胞增多症、血小板减少症、出生后首次血常规感染指标存在异常及未完成影像学检查的早产儿。
患儿监护人对所做研究均知情同意,并签署知情同意书,本研究通过郑州大学第三附属医院医学伦理委员会批准(批准文号:2021-027-1)。
研究对象按照出生1 d、3 d、7 d及以后每周1次头颅超声检查和纠正胎龄36~37周头颅磁共振成像(MRI)检查结果分为脑损伤组和无脑损伤组;前者进一步分为ICH组、PVL组及弥散性脑白质损伤组。脑损伤组诊断标准如下:(1) ICH诊断参考第5版《实用新生儿学》[9]。(2) PVL MRI表现为侧脑室前角和中央部、侧脑室后角三角区周围白质的1个或多个囊性图像,T1WI显示低信号,T2WI则显示高信号。(3)弥散性脑白质损伤MRI表现为脑白质中无>1 mm的囊性异常(主要标准);胼胝体变薄;侧脑室扩张;脑室周围白质密度减低形成T2WI高信号;双侧交叉突触间变性导致小脑大小/体积双侧对称减少[10]。
入组后剔除早产儿16例。其中,流式细胞术检测结果分群不清3例,纠正胎龄不足36周治愈出院6例,死亡7例,最终106例纳入研究,脑损伤组36例(ICH组8例,PVL组6例,弥散性脑白质损伤组22例),无脑损伤组70例。
收集入组早产儿以下资料:(1)围生期情况:产前激素应用、生产方式、母亲孕期情况(妊娠合并症、羊水及胎盘情况)等。(2)早产儿基本情况:性别、出生胎龄、出生体质量、1 min Apgar及5 min Apgar评分。(3)早产儿并发症情况,如支气管肺发育不良(BPD)、新生儿坏死性小肠结肠炎(NEC)、早产儿视网膜病(ROP)、肺炎、新生儿持续性肺动脉高压(PPHN)、脓毒症、新生儿胆汁淤积症及脑膜炎。早产儿并发症诊断参考第5版《实用新生儿学》[9]。
对纳入研究的早产儿于出生24 h内留静脉血1 mL,留样后8 h内进行检测。采用美国eBioscience公司的三色免疫荧光单克隆抗体试剂盒,运用美国Beckman-Coulter流式细胞仪进行检测。于100 μL肝素钠抗凝血中依次加入荧光标记单克隆抗体推荐量,常温避光孵育20 min,加入红细胞裂解液2 mL,振匀后室温避光10 min,500×g离心5 min,弃上清,再以磷酸盐缓冲液(PBS)洗涤2次,置流式细胞仪上进行分析,每个样本收集2×105个细胞。为保证数据的准确性,仪器的质量控制、标本的处理和测试、数据分析均由同一实验员操作。
应用SPSS 26.0统计软件进行数据处理。计数资料以例(%)表示,组间比较采用χ2检验或校正χ2检验;符合正态分布的计量资料以 ±s表示,采用t检验,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验,P<0.05为差异有统计学意义。
±s表示,采用t检验,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验,P<0.05为差异有统计学意义。
2组早产儿在产前激素应用、生产方式、母孕期情况等方面比较,差异均无统计学意义(均P>0.05),见表1。
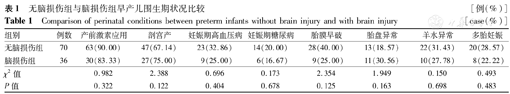
无脑损伤组与脑损伤组早产儿围生期状况比较[例(%)]
Comparison of perinatal conditions between preterm infants without brain injury and with brain injury[case(%)]
无脑损伤组与脑损伤组早产儿围生期状况比较[例(%)]
Comparison of perinatal conditions between preterm infants without brain injury and with brain injury[case(%)]
| 组别 | 例数 | 产前激素应用 | 剖宫产 | 妊娠期高血压病 | 妊娠期糖尿病 | 胎膜早破 | 胎盘异常 | 羊水异常 | 多胎妊娠 |
|---|---|---|---|---|---|---|---|---|---|
| 无脑损伤组 | 70 | 63(90.00) | 47(67.14) | 23(32.86) | 14(20.00) | 28(40.00) | 13(18.57) | 22(31.43) | 20(28.57) |
| 脑损伤组 | 36 | 30(83.33) | 27(75.00) | 9(25.00) | 6(16.67) | 9(25.00) | 11(30.56) | 10(27.78) | 8(22.22) |
| χ2值 | 0.982 | 2.388 | 0.696 | 0.173 | 2.354 | 1.949 | 0.150 | 0.493 | |
| P值 | 0.322 | 0.122 | 0.404 | 0.678 | 0.125 | 0.163 | 0.698 | 0.483 |
2组早产儿在性别、出生胎龄、出生体质量、出生1 min Apgar评分、出生5 min Apgar评分等方面比较,差异均无统计学意义(均P>0.05),见表2。
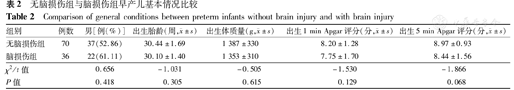
无脑损伤组与脑损伤组早产儿基本情况比较
Comparison of general conditions between preterm infants without brain injury and with brain injury
无脑损伤组与脑损伤组早产儿基本情况比较
Comparison of general conditions between preterm infants without brain injury and with brain injury
| 组别 | 例数 | 男[例(%)] | 出生胎龄(周, ±s) ±s) | 出生体质量(g, ±s) ±s) | 出生1 min Apgar评分(分, ±s) ±s) | 出生5 min Apgar评分(分, ±s) ±s) |
|---|---|---|---|---|---|---|
| 无脑损伤组 | 70 | 37(52.86) | 30.44±1.69 | 1 387±330 | 8.20±1.28 | 8.97±0.93 |
| 脑损伤组 | 36 | 22(61.11) | 30.10±1.40 | 1 353±310 | 7.75±1.70 | 8.44±1.56 |
| χ2/t值 | 0.656 | -1.031 | -0.505 | -1.530 | -1.866 | |
| P值 | 0.418 | 0.305 | 0.615 | 0.129 | 0.068 |
2组早产儿住院期间各种新生儿并发症发生率比较,差异均无统计学意义(均P>0.05),见表3。
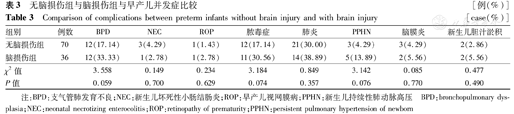
无脑损伤组与脑损伤组与早产儿并发症比较[例(%)]
Comparison of complications between preterm infants without brain injury and with brain injury[case(%)]
无脑损伤组与脑损伤组与早产儿并发症比较[例(%)]
Comparison of complications between preterm infants without brain injury and with brain injury[case(%)]
| 组别 | 例数 | BPD | NEC | ROP | 脓毒症 | 肺炎 | PPHN | 脑膜炎 | 新生儿胆汁淤积 |
|---|---|---|---|---|---|---|---|---|---|
| 无脑损伤组 | 70 | 12(17.14) | 3(4.29) | 1(1.43) | 12(17.14) | 21(30.00) | 3(4.29) | 3(4.29) | 2(2.86) |
| 脑损伤组 | 36 | 12(33.33) | 1(2.78) | 1(2.78) | 11(30.56) | 14(38.89) | 5(13.89) | 2(5.56) | 2(5.56) |
| χ2值 | 3.558 | 0.149 | 0.234 | 3.184 | 0.849 | 3.142 | 0.085 | 0.477 | |
| P值 | 0.059 | 0.700 | 0.629 | 0.074 | 0.357 | 0.076 | 0.770 | 0.490 |
注:BPD:支气管肺发育不良;NEC:新生儿坏死性小肠结肠炎;ROP:早产儿视网膜病;PPHN:新生儿持续性肺动脉高压
BPD:bronchopulmonary dysplasia;NEC:neonatal necrotizing enterocolitis;ROP:retinopathy of prematurity;PPHN:persistent pulmonary hypertension of newborn
脑损伤组早产儿出生24 h内外周血中γδ-T淋巴细胞百分比明显低于无脑损伤组早产儿,差异有统计学意义(P<0.05),见表4。2组早产儿出生24 h内外周血CD4+T淋巴细胞、CD8+ T淋巴细胞、CD4+/CD8+、CD3+ T淋巴细胞及总淋巴细胞百分比分布比较,差异均无统计学意义(均P>0.05),见表4。
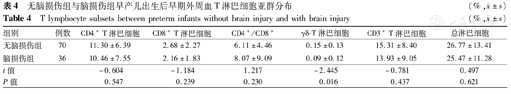
无脑损伤组与脑损伤组早产儿出生后早期外周血T淋巴细胞亚群分布(%, ±s)
±s)
T lymphocyte subsets between preterm infants without brain injury and with brain injury(%, ±s)
±s)
无脑损伤组与脑损伤组早产儿出生后早期外周血T淋巴细胞亚群分布(%, ±s)
±s)
T lymphocyte subsets between preterm infants without brain injury and with brain injury(%, ±s)
±s)
| 组别 | 例数 | CD4+ T淋巴细胞 | CD8+ T淋巴细胞 | CD4+/CD8+ | γδ-T淋巴细胞 | CD3+ T淋巴细胞 | 总淋巴细胞 |
|---|---|---|---|---|---|---|---|
| 无脑损伤组 | 70 | 11.30±6.39 | 2.68±2.27 | 6.11±4.46 | 0.15±0.13 | 15.31±8.40 | 26.77±13.41 |
| 脑损伤组 | 36 | 10.46±7.55 | 2.16±1.83 | 8.07±9.09 | 0.09±0.12 | 13.93±9.05 | 25.47±11.28 |
| t值 | -0.604 | -1.184 | 1.217 | -2.445 | -0.781 | 0.497 | |
| P值 | 0.547 | 0.239 | 0.230 | 0.016 | 0.437 | 0.621 |
ICH组[(0.18±0.19)%]、PVL组[(0.03±0.05)%]及弥散性脑白质损伤组[(0.07±0.09)%]出生早期外周血γδ-T淋巴细胞占比的差异有统计学意义(F=3.737,P=0.014),且PVL组及弥散性脑白质损伤组较无脑损伤组降低,差异均有统计学意义(t=-2.190、-2.659,均P<0.05)。ICH组与无脑损伤组比较差异无统计学意义(t=0.397,P=0.693)。各组与无脑损伤组出生早期外周血CD4+T淋巴细胞、CD8+ T淋巴细胞、CD4+/CD8+、CD3+ T淋巴细胞及总淋巴细胞百分比比较,差异均无统计学意义(均P>0.05)。
早产儿脑损伤可能会破坏关键的结构和功能连接网络,造成神经发育障碍。随着近年来早产儿保健逐渐从保生存向促发展转变,早产儿脑损伤越来越受到新生儿界的关注。目前早产儿脑损伤的发病机制尚不完全清楚,除了与早产儿自身神经系统发育不成熟相关以外,缺氧缺血、感染/炎症和兴奋性毒性等均可能导致早产儿脑损伤。此外,感染/炎症或预先暴露在低氧环境等前驱因素会加强大脑的脆弱性及易损性[11]。相关实验数据表明,如果在脑损伤后数小时、数天甚至数周内进行干预,对改善预后有显著效果[12,13]。然而早产儿脑损伤早期往往缺乏典型临床特征,目前主要依据后期影像学检查进行诊断,往往会让患儿错失最佳治疗时机,因此探索出生早期生物学指标对于预测早产儿脑损伤、给予及时干预及治疗至关重要。本研究对脑损伤早产儿出生早期外周血中的γδ-T淋巴细胞亚群水平进行研究,以寻求一种敏感简便、能在早期反映脑损伤的检测指标。
γδ-T淋巴细胞是人体最先发育的一种T淋巴细胞,虽仅占外周血T淋巴细胞的5%左右,但在新生儿期即处于活跃状态[14]。在没有成熟的αβ-T淋巴细胞的情况下,γδ-T淋巴细胞可能会使新生儿产生强烈的细胞介导的反应。它具有非组织相容性复合体(MHC)限制性,不需抗原提呈细胞(APC),可直接识别并结合抗原分子,溶解靶细胞,在固有免疫及适应性免疫中起桥梁作用,并可通过产生白细胞介素17A(IL-17A)、干扰素(IFN)、肿瘤坏死因子-α(TNF-α)等多种细胞因子调节免疫应答,从而帮助限制损伤的扩散,并促进损伤部位的内稳态[15,16]。γδ-T淋巴细胞区别于传统T淋巴细胞的特性及其在新生儿围生期及出生后免疫中的独特作用成为目前研究的热点。研究发现,γδ-T淋巴细胞与早产儿宫内窒息、围生期感染等脑损伤重要病因密切相关,Królak-Olejnik和Mazur[17]发现具有胎膜早破等感染高危因素的早产儿脐血中γδ-T淋巴细胞显著降低。有研究证明,在成年或新生大鼠缺血性脑损伤中,γδ-T淋巴细胞在脑组织中释放可加重或修复损伤的抗炎细胞因子,从而直接参与到脑损伤的发生与发展中[18,19]。本研究结果显示,脑损伤组早产儿出生24 h内外周血中,γδ-T淋巴细胞明显低于无脑损伤组。推测可能与存在脑损伤高危因素的早产儿神经免疫及神经内分泌系统较其他早产儿更加不成熟有关。脑损伤早产儿出生早期固有免疫功能低下,免疫抑制肽内源性前列腺素2 (PGE2)释放,诱导淋巴细胞凋亡机制异常启动,淋巴细胞凋亡加速。同时,PGE2激活下丘脑-垂体-肾上腺轴(HPA),导致机体内多种神经内分泌肽类物质合成、储藏、运输与分泌释放等过程紊乱[20],表达的抗炎细胞因子和其他能够局限或下调炎症过程的蛋白减少,而促炎细胞因子水平升高,这些蛋白及细胞因子通过干扰神经元及少突胶质细胞的分化,对发育中的大脑造成直接损伤[21]。本研究中2组早产儿出生早期外周血CD3+T、CD4+T和CD8+T等淋巴细胞亚群水平未发现差异,证实了出生早期检测γδ-T淋巴细胞较其他淋巴细胞亚群对早产儿免疫的紊乱状态更加敏感,对预测早产儿脑损伤具有重要意义。
本研究进一步按照早产儿脑损伤不同类型进行划分,并探究其与出生早期外周血γδ-T淋巴细胞水平的关系。既往研究表明,CD4+T、CD8+T、CD3+T等外周免疫细胞与缺血性脑损伤密切相关,并可通过脑室周围组织及血管周围间隙浸润脑组织[7]。传统淋巴细胞在白质软化灶中通过产生自由基,调控细胞因子和兴奋性毒性作用参与激活小胶质细胞、中性粒细胞及脑内皮细胞,并最终作用于24~34周妊娠期脑室周围占优势的少突胶质细胞前体(preOL)[22]。Albertsson等[23]在新生大鼠脓毒症介导的脑白质损伤模型及死亡早产儿尸检中发现,γδ-T淋巴细胞在白质软化灶附近显著增多,并推测γδ-T淋巴细胞从外周募集进入脑组织。但尚未有研究探索脑白质损伤患儿出生早期外周血中γδ-T淋巴细胞变化及机制。本研究中,PVL组及弥散性脑白质损伤组早产儿出生早期外周血γδ-T淋巴细胞水平较无脑损伤组显著降低,是否系由于γδ-T淋巴细胞从外周转移至中枢神经系统,尚需要进一步研究。这一结果表明了γδ-T淋巴细胞对早产儿脑白质损伤具有早期预测价值。
目前研究发现,除影像学方法外,外周血中性粒细胞与淋巴细胞比值(NLR)可以反映成人及新生儿ICH病情进展及严重程度[24],与ICH伴行的免疫抑制综合征主要以淋巴细胞减少和功能抑制为主要特征[25]。但不同淋巴细胞亚群的情况似乎不尽相同,Gao等[26]发现成年脑出血大鼠中,脑组织和外周血γδ-T淋巴细胞较对照组均明显增多,目前尚缺乏新生儿ICH疾病与γδ-T淋巴细胞的相关性研究。本研究发现,ICH组早产儿出生早期外周血γδ-T淋巴细胞水平与无脑损伤组比较差异无统计学意义。因此,出生早期外周血γδ-T淋巴细胞对胎龄<34周早产儿ICH的预测价值有待进一步研究。
综上所述,γδ-T淋巴细胞对胎龄<34周早产儿脑损伤早期预测有重要价值,出生早期γδ-T淋巴细胞水平越低,后期发生脑损伤,特别是PVL及弥散性脑白质损伤的可能性越大,为早产儿脑损伤早期筛查和预测提供了依据,可进行早期干预以遏制脑损伤进一步发展。但由于本研究样本量较少,仅测定出生后早期外周血各淋巴亚群及γδ-T淋巴细胞水平,随访时间较短,因此有必要进一步研究γδ-T淋巴细胞与神经发育预后的关系。
感谢郑州大学第三附属医院检验科袁恩武主任、石瑛主任和新生儿科李文丽医师对本研究提供的指导与帮助
所有作者均声明不存在利益冲突



























