
分析川崎病(KD)患儿合并中小型冠状动脉瘤(CAA)持续时间的高危因素,为早期、足疗程治疗提供临床指导。
回顾性分析2018年1月至2021年1月在新乡医学院第一附属医院儿科确诊为KD的68例患儿临床资料,根据CAA持续时间分为CAA持续时间≥8周组及CAA持续时间<8周组,采用单因素分析筛选出与CAA持续时间相关危险因素,进而采用多因素Logistic回归分析KD患儿CAA持续时间的独立危险因素。
68例住院KD患儿中,男45例(66.18%),女23例(33.82%);发病年龄3个月~10岁,中位发病年龄1.59(1.02~3.19)岁。CAA持续时间≥8周组31例,CAA持续时间<8周组37例。单因素分析发现,CAA持续时间≥8周组总热程>10 d[45.16%(14/31例)比21.62%(8/37例)]、静脉注射免疫球蛋白(IVIG)前病程>10 d[54.84%(17/31例)比16.22%(6/37例)]、血小板计数>600×109/L[32.26%(10/31例)比10.81%(4/37例)]、超敏C反应蛋白>100 mg/L[38.71%(12/31例)比13.51%(5/37例)]者显著多于CAA持续时间<8周组,2组比较差异均有统计学意义(均P<0.05);2组间性别、年龄、KD类型、病原学证据、激素应用情况、IVIG应用前热程、IVIG敏感情况、IVIG应用方式、尿白细胞情况、白细胞计数、血红蛋白、中性粒细胞比例、红细胞沉降率、谷丙转氨酶比较,差异均无统计学意义(均P>0.05)。多因素Logistic回归分析提示IVIG应用前病程>10 d(OR=6.589,95%CI:1.678~25.867,P=0.007)、超敏C反应蛋白>100 mg/L(OR=7.949,95%CI:1.947~32.461,P=0.004)分别为预测KD合并中小型CAA持续时间≥8周的独立危险因素。
IVIG应用前病程>10 d及超敏C反应蛋白>100 mg/L是KD合并中小型CAA持续时间≥8周的独立危险因素。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
川崎病(Kawasaki disease,KD)是一种儿童时期急性自限性发热性疾病,其病理特征为全身性、系统性血管炎,易累及中小动脉,尤以冠状动脉最为常见。KD冠状动脉损害在我国和发达国家已成为获得性心脏病的主要原因[1,2]。KD急性期冠状动脉损害主要表现为冠状动脉扩张,分为小型、中型及巨大冠状动脉瘤(coronary artery aneurysm,CAA),且以中小型CAA最为常见,Z值< 2.5的CAA多于4~8周内恢复正常[3],但部分患者持续时间更长,且冠状动脉管腔狭窄、血栓形成等CAA后期主要不良心血管事件发生的风险随CAA持续时间的推移持续增加[4]。因此,尽早预测KD患儿CAA持续时间,并给予及时、足疗程治疗至关重要。目前有关CAA持续时间危险因素的研究较少,本研究回顾性分析68例KD并中小型CAA患儿的临床资料及实验室指标,探讨KD合并中小型CAA持续时间的危险因素,为早期预警KD患儿CAA持续存在提供依据,亦为早期、足疗程治疗提供临床支持。
回顾性分析。以2018年1月至2021年1月在新乡医学院第一附属医院儿科诊断,且合并中小型CAA的68例KD患儿为研究对象。其中男45例(66.18%),女23例(33.82%);发病年龄3个月~10岁。入选标准:(1)KD诊断标准符合2017年美国心脏协会(AHA)制定的《川崎病的诊断、治疗及远期管理——美国心脏协会对医疗专业人员的科学声明》[3];(2)年龄<14岁;(3)急性期入院,临床及实验室资料完整。排除标准:排除其他发热出疹性疾病、肿瘤、急性淋巴结炎、遗传代谢病、结缔组织病及心血管疾病者。本研究通过新乡医学院第一附属医院医学伦理委员会批准(批准文号:2021029)。均获得患儿监护人知情同意,并签署知情同意书。
(1)一般临床资料:包括性别、年龄、静脉注射免疫球蛋白(IVIG)前热程、IVIG前病程、发病时临床表现、是否为完全KD、是否有病原体感染证据、IVIG应用方法、是否应用糖皮质激素、既往病史及转归情况;(2)IVIG前(病程10 d内)实验室检查结果:白细胞计数(WBC)、血红蛋白(Hb)、血小板计数(PLT)、中性粒细胞百分比(NE%)、超敏C反应蛋白(HsCRP)、尿常规、红细胞沉降率(ESR)、谷丙转氨酶(ALT)、超声心动图等。
应用超声心动图进行冠状动脉检查,分别于起病时、IVIG后1周内,并于病程8周内根据病情每1~2周进行1次,后根据病情每1~6个月进行1次。并根据超声心动图检查结果进行分类,超声心动图正常指冠状动脉壁光滑,回声细薄,无任何部位扩张。冠状动脉内径正常值[5]:年龄≤3岁:<2.5 mm;3岁<年龄≤9岁:<3.0 mm;9岁<年龄≤14岁:<3.5 mm。冠状动脉瘤标准[6]:冠状动脉内径<4 mm为小型CAA,4~8 mm为中型CAA,>8 mm为巨大CAA。
根据CAA持续时间是否≥8周,分为CAA持续时间≥8周组及CAA持续时间<8周组。
采用SPSS 19.0软件进行统计学分析。计数资料以百分比表示,组间比较采用χ2检验或Fisher′s精确概率法进行单因素筛选,采用Logistic回归分析KD合并中小型CAA持续时间的独立危险因素。P<0.05为差异有统计学意义。
68例KD并中小型CAA患儿,中位发病年龄1.59(1.02~3.19)岁;其中<3岁48例,3~5岁13例,>5岁7例;完全型KD 24例,不完全型KD 44例;25例有病原学证据,尿白细胞>10/高倍镜视野(HPF)者9例。其中CAA持续时间≥8周组31例,CAA持续时间<8周组37例。2组患儿在性别、年龄、KD类型、病原学证据、尿白细胞>10/HPF情况比较,差异均无统计学意义(均P>0.05)。结果见表1。
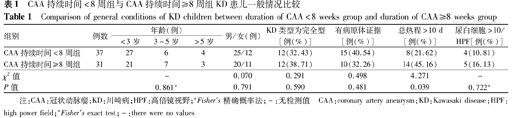
CAA持续时间<8周组与CAA持续时间≥8周组KD患儿一般情况比较
Comparison of general conditions of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group
CAA持续时间<8周组与CAA持续时间≥8周组KD患儿一般情况比较
Comparison of general conditions of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group
| 组别 | 例数 | 年龄(例) | 男/女(例) | KD类型为完全型[例(%)] | 有病原体证据[例(%)] | 总热程>10 d[例(%)] | 尿白细胞>10/ | ||
|---|---|---|---|---|---|---|---|---|---|
| <3岁 | 3~5岁 | >5岁 | |||||||
| HPF[例(%)] | |||||||||
| CAA持续时间<8周组 | 37 | 27 | 6 | 4 | 25/12 | 12(32.43) | 15(40.54) | 8(21.62) | 4(10.81) |
| CAA持续时间≥8周组 | 31 | 21 | 7 | 3 | 20/11 | 12(38.71) | 10(32.26) | 14(45.16) | 5(16.13) |
| χ2值 | - | 0.070 | 0.291 | 0.498 | 4.271 | - | |||
| P值 | 0.861a | 0.791 | 0.590 | 0.481 | 0.039 | 0.722a | |||
注:CAA:冠状动脉瘤;KD:川崎病;HPF:高倍镜视野;aFisher′s精确概率法;-:无检测值
CAA:coronary artery aneurysm;KD:Kawasaki disease;HPF:high power field;aFisher′s exact test;-:there were no values
CAA持续时间≥8周组总热程>10 d者14例,CAA持续时间<8周组总热程>10 d者8例,2组比较差异有统计学意义(P<0.05)。结果见表1。
IVIG应用剂量为1 g/(kg·d),连用2 d者57例;IVIG剂量为2 g/kg,一次性应用者11例;IVIG应用前热程≥6 d者39例,<6 d者29例;IVIG敏感者59例,IVIG抵抗9例;共26例在病程中应用糖皮质激素。2组在IVIG应用方式、IVIG应用前热程、IVIG敏感情况、激素应用情况方面比较,差异均无统计学意义(均P>0.05)。结果见表2。

CAA持续时间<8周组与CAA持续时间≥8周组KD患儿治疗情况比较
Comparison of treatment of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group
CAA持续时间<8周组与CAA持续时间≥8周组KD患儿治疗情况比较
Comparison of treatment of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group
| 组别 | 例数 | IVIG应用方式(例) | IVIG应用前热程≥6 d[例(%)] | IVIG应用前病程>10 d[例(%)] | IVIG敏感[例(%)] | 应用糖皮质激素[例(%)] | |
|---|---|---|---|---|---|---|---|
| 1 g/( kg·d),2 d | 2 g/(kg·d),1 d | ||||||
| CAA持续时间<8周组 | 37 | 30 | 7 | 21(56.76) | 6(16.22) | 34(91.89) | 16(43.24) |
| CAA持续时间≥8周组 | 31 | 27 | 4 | 18(58.06) | 17(54.84) | 25(80.65) | 10(32.26) |
| χ2值 | 0.450 | 0.012 | 11.241 | - | 0.862 | ||
| P值 | 0.502 | 0.914 | 0.001 | 0.282a | 0.353 | ||
注:CAA:冠状动脉瘤;KD:川崎病;IVIG:静脉注射免疫球蛋白;aFisher′s精确概率法;-:无检测值
CAA:coronary artery aneurysm;KD:Kawasaki disease;IVIG:intravenous immunoglobulin;aFisher′s exact test;-:there were no values
CAA持续时间≥8周组IVIG应用前病程>10 d者17例,所占比例明显高于CAA持续时间<8周组,2组比较差异有统计学意义(P<0.05)。结果见表2。
CAA持续时间≥8周组与CAA持续时间<8周组患儿WBC、Hb、NE%、ESR、ALT水平比较,差异均无统计学意义(均P>0.05)。2组患儿PLT及HsCRP水平比较,差异均有统计学意义(均P<0.05)。结果见表3。
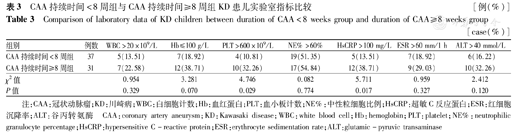
CAA持续时间<8周组与CAA持续时间≥8周组KD患儿实验室指标比较[例(%)]
Comparison of laboratory data of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group [case(%)]
CAA持续时间<8周组与CAA持续时间≥8周组KD患儿实验室指标比较[例(%)]
Comparison of laboratory data of KD children between duration of CAA<8 weeks group and duration of CAA≥8 weeks group [case(%)]
| 组别 | 例数 | WBC>20×109/L | Hb≤100 g/L | PLT>600×109/L | NE%>60% | HsCRP>100 mg/L | ESR>60 mm/1 h | ALT>40 mmol/L |
|---|---|---|---|---|---|---|---|---|
| CAA持续时间<8周组 | 37 | 5(13.51) | 7(18.92) | 4(10.81) | 19(51.35) | 5(13.51) | 7(18.92) | 6(16.22) |
| CAA持续时间≥8周组 | 31 | 7(22.58) | 12(38.71) | 10(32.26) | 17(54.84) | 12(38.71) | 9(29.03) | 10(32.26) |
| χ2值 | 0.954 | 3.281 | 4.746 | 0.082 | 5.711 | 0.959 | 2.412 | |
| P值 | 0.329 | 0.070 | 0.029 | 0.774 | 0.017 | 0.327 | 0.120 |
注:CAA:冠状动脉瘤;KD:川崎病;WBC:白细胞计数;Hb:血红蛋白;PLT:血小板计数;NE%:中性粒细胞比例;HsCRP:超敏C反应蛋白;ESR:红细胞沉降率;ALT:谷丙转氨酶
CAA:coronary artery aneurysm;KD:Kawasaki disease;WBC:white blood cell;Hb:hemoglobin;PLT:platelet;NE%:neutrophilic granulocyte percentage;HsCRP:hypersensitive C-reactive protein;ESR:erythrocyte sedimentation rate;ALT:glutamic-pyruvic transaminase
将表1,表2,表3中P<0.05的变量作为自变量,KD合并中小型CAA持续时间≥8周作为因变量,进行多因素Logistic回归分析,结果显示,IVIG应用前病程>10 d(OR=6.589,95%CI:1.678~25.867,P=0.007)、HsCRP>100 mg/L(OR=7.949,95%CI:1.947~32.461,P=0.004)分别是预测KD合并中小型CAA持续时间≥8周的独立危险因素。结果见表4。
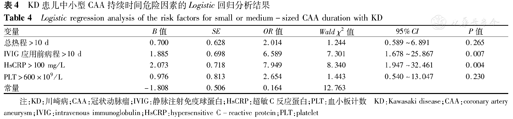
KD患儿中小型CAA持续时间危险因素的Logistic回归分析结果
Logistic regression analysis of the risk factors for small or medium-sized CAA duration with KD
KD患儿中小型CAA持续时间危险因素的Logistic回归分析结果
Logistic regression analysis of the risk factors for small or medium-sized CAA duration with KD
| 变量 | B值 | SE | OR值 | Wald χ2值 | 95%CI | P值 |
|---|---|---|---|---|---|---|
| 总热程>10 d | 0.700 | 0.628 | 2.014 | 1.244 | 0.589~6.891 | 0.265 |
| IVIG应用前病程>10 d | 1.885 | 0.698 | 6.589 | 7.301 | 1.678~25.867 | 0.007 |
| HsCRP>100 mg/L | 2.073 | 0.718 | 7.949 | 8.340 | 1.947~32.461 | 0.004 |
| PLT>600×109/L | 0.976 | 0.813 | 2.654 | 1.443 | 0.540~13.047 | 0.230 |
| 常量 | -1.808 | 0.506 | 0.164 | 12.763 |
注:KD:川崎病;CAA:冠状动脉瘤;IVIG:静脉注射免疫球蛋白;HsCRP:超敏C反应蛋白;PLT:血小板计数
KD:Kawasaki disease;CAA:coronary artery aneurysm;IVIG:intravenous immunoglobulin;HsCRP:hypersensitive C-reactive protein;PLT:platelet
目前KD病因尚不明确,对于其远期预后更不清楚,而CAA是影响KD远期预后的最主要因素,CAA进一步发展可导致冠状动脉血栓及冠状动脉狭窄,甚至冠状动脉闭塞,严重者可导致死亡[7]。未经有效治疗的KD患儿,约25%可发生CAA,对于KD合并CAA的预测及相关危险因素研究较多,但对于KD患儿CAA持续时间的预测及相关因素认识明显不足。本研究选取合并中小型CAA的68例KD患儿为研究对象,分析影响CAA持续时间的相关危险因素,为早期预警KD患儿CAA持续存在提供依据,亦为早期、足疗程治疗提供临床支持。
发热为KD首要症状,亦是炎症反应最直接、最主要的临床表现。国内外已有多项研究[8,9,10]证实发热持续时间是KD并发CAA的危险因素,认为发热时间越长,机体产生炎症介质可能越多,那么血管炎症损伤也越重,并发CAA的风险越大。但这并不意味着热程越长,CAA持续时间一定越长,本研究单因素分析发现CAA持续时间≥8周组总热程>10 d者明显高于CAA持续时间<8周组,但多因素回归分析并未发现二者相关,与近期韩国的一项研究[9]一致。并且本研究发现,IVIG应用前热程亦与CAA持续时间无关。因此,无论是总热程或是IVIG应用前热程均不是CAA持续存在的独立危险因素。另外糖皮质激素可抑制炎症反应、缩短热程,但在KD中的应用一直存在争议。早期研究发现,糖皮质激素应用对KD并无益处,甚至可促进CAA形成,然而,近年来更倾向于接受糖皮质激素对缩短热程、降低冠状动脉病变风险的正向作用[11],因此AHA于2017年首次提出糖皮质激素可用于预估IVIG无反应和CAA高风险患者的初始治疗[3],本研究中部分患儿亦加用糖皮质激素治疗,且发现加用糖皮质激素并未导致CAA持续时间延长。
血小板可释放多种趋化因子、细胞因子等炎症介质,进而加重机体炎症反应,是介导全身炎症反应的因子之一[12],KD急性期PLT可明显增高,但KD患儿PLT水平与CAA发生、发展的相关性,目前尚无一致意见。近期韩国一项对392例KD的研究发现,高PLT是预测早期CAA发展的独立因素,但与中晚期CAA持续存在并无关联[9]。本研究亦得出类似结论,单因素分析表明PLT>600×109/L为CAA持续时间≥8周的危险因素,但多因素分析未发现PLT明显增高与CAA持续存在相关。并且一项KD合并CAA危险因素的Meta分析[13]认为,PLT并非KD合并CAA的独立危险因素。但也有学者持不同的观点,Qiu等[14]最近研究表明较高的PLT是持续性冠状动脉病变的独立危险因素。分析原因,考虑可能是各临床研究均为单中心病例,所纳入的临床病例资料可能不完全一致,期待多中心的联合研究。
IVIG是目前公认的KD急性期一线治疗用药,并且其用法、用量、用药时机至关重要,宜于发病10 d内应用,多项研究[13,15,16]表明,于发病10 d后应用IVIG可明显增加CAA发生风险。一项美国流行病学调查资料显示,5%~25%的KD患儿对首次IVIG耐药,是发生冠状动脉损害的独立危险因素[17]。本研究进一步比较CAA持续时间≥8周组和CAA持续时间<8周组IVIG应用情况,发现IVIG应用前病程>10 d是CAA持续时间≥8周的独立危险因素,与既往研究[14]结果一致。另外一项为期3年的随访研究发现,IVIG前病程>10 d、IVIG抵抗是KD患儿CAA持续存在的危险因素[18],而本研究中IVIG抵抗情况在CAA持续时间≥8周组和CAA持续时间<8周组分布并无明显差异,分析原因可能与本研究中部分患儿联合糖皮质激素应用而影响IVIG抵抗情况判断有关。另外,本研究还比较了不同IVIG应用方式对CAA持续时间的影响,发现不同IVIG应用方式并不影响CAA持续时间。因此,早期诊断并于病程10 d内应用IVIG至关重要,否则易导致CAA发生并可能持续存在。
C反应蛋白为具有多种生物效应的急相反应蛋白,是临床中常用的炎症指标之一。一项对来自韩国38家医院的5 151例KD患者的调查研究发现,仅C反应蛋白与KD患儿CAA发生独立相关,而NE%、ALT、谷草转氨酶等均与KD患儿CAA发生无关[19],本研究单因素分析与多因素回归分析均提示HsCRP>100 mg/L是KD患儿CAA持续时间≥8周的独立危险因素,提示KD患儿HsCRP与CAA持续时间相关,与日本一项研究[20]相符,因此,对于HsCRP>100 mg/L的KD患儿,需警惕CAA发生,且需重视CAA持续存在风险,可定期并频繁复查超声心动图,监测冠状动脉病情演变,并予足疗程治疗,预防KD不良心血管事件发生。
综上,本研究结果提示,IVIG前病程>10 d、HsCRP>100 mg/L是KD患儿合并中小型CAA持续时间≥8周的独立危险因素,临床上对于符合上述条件的KD患儿,需高度警惕CAA持续存在,早期需及时给予干预,且需足疗程治疗,预防严重心血管不良事件发生,为KD患儿长期管理提供临床依据。但本研究为回顾性研究,且样本量略少,未来需要更深入的大规模前瞻性、多中心研究进一步探讨。
所有作者均声明不存在利益冲突



























