
探讨儿童癫痫持续状态严重程度评分(STEPSS)和END-IT评分对癫痫持续状态(SE)患儿短期预后的预测价值。
回顾性分析。纳入2012年1月1日至2022年1月1日青岛大学附属青岛妇女儿童医院收治的SE患儿103例。根据出院时格拉斯哥预后评分量表分为预后良好组(78例)和预后不良组(25例),应用Logistic回归分析SE患儿预后不良的危险因素,采用受试者工作特征(ROC)曲线评估STEPSS评分和END-IT评分对SE患儿短期预后的预测价值。
预后不良组患儿年龄较小[16(9,58)个月比56(21,84)个月,Z=-3.068,P=0.002]、血乳酸水平更高[3.16(2.43,4.01) mmol/L比1.67(1.32,2.10) mmol/L,Z=-6.085,P<0.001]、STEPSS评分和END-IT评分增高[3.0(3.0,4.0)分比1.0(1.0,2.0)分、3.0(1.5,4.0)分比1.0(0,1.0)分,Z=-6.956、-5.502,均P<0.001]、合并发育迟缓的比例增高(χ2=16.756,P<0.001)、脑磁共振检查异常比例增高(χ2=5.860,P=0.015)、启动抗SE治疗时间长(Z=1.488,P=0.024)、治疗中应用呼吸机的比例和应用多种抗癫痫药物的比例均增高(均P<0.001)。二分类Logistic回归分析显示血乳酸增高(OR=7.975,95%CI:2.705~23.518)、药物种类增多(OR=14.562,95%CI:2.035~104.173)、STEPSS评分(OR=8.914,95%CI:2.824~28.140)和END-IT评分(OR=2.209,95%CI:1.046~4.667)是影响SE患儿预后的危险因素。ROC曲线分析显示STEPSS评分和END-IT评分用于预测SE患儿不良预后时,曲线下面积(AUC)分别为0.939、0.853,截断值分别为2.5分(敏感度96.0%,特异度85.9%)和1.5分(敏感度76.0%,特异度75.6%),约登指数分别为0.82和0.52。STEPSS评分的AUC值较END-IT评分的AUC值增高(U=36.91,P<0.05)。2种评分联合试验预测SE患儿不良预后时,并联试验的敏感度和阴性预测值均达100.0%,串联试验的特异度为94.9%,阳性预测值为81.8%。
STEPSS评分和END-IT评分对SE患儿的短期预后具有良好的预测价值,2种评分系统联合应用更有利于SE患儿不良预后的预测。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
癫痫持续状态(status epilepticus,SE)是儿科最常见的神经系统急症之一,病因错综复杂,有较高的住院率和致残率,因此,在对SE患者的管理中,早期应用预警指标评估预后,有助于临床医师及时调整SE的管理决策和制定针对性处理措施[1]。许多研究尝试建立与临床相关、简单全面且具有良好预测价值的评分系统来预测SE患者的短期预后,如针对成人SE患者建立并应用广泛的癫痫持续状态严重程度评分(the Status Epilepticus Severity Score,STESS)和SE病死率评分[2],但由于儿童病理生理的特殊性,上述评分系统在儿童SE中的应用受到限制。Sharma团队2019年优化了STESS指标,并重新定义为儿童癫痫持续状态严重程度评分量表(the Status Epilepticus in Pediatric Patients Severity Score,STEPSS),从年龄、发作形式和意识状态等方面对患儿病情进行评估[3]。END-IT评分包含患者的临床特征、惊厥形式、影像学特点及治疗等,2021年Kapoor等[4]发现其对印度SE患儿的预后有一定的预测价值,但也有其局限性[4]。目前,上述SE评分系统在国内SE患儿中的应用少见,对SE患儿预后的预测价值尚不清楚。本研究通过比较STEPSS和END-IT评分系统对SE患儿不良预后的预测价值,旨在为SE患儿的预后评估提供参考依据。
回顾性分析2012年1月1日至2022年1月1日青岛大学附属青岛妇女儿童医院儿童重症监护室和神经内科收治的SE患儿的资料。SE诊断符合国际抗癫痫联盟修订的诊断标准[5]:强直-阵挛SE>5 min,局灶性SE伴意识损害>10 min,失神SE>15 min。难治性癫痫持续状态(refractory status epilepticus,RSE)指经一线药物(苯二氮 类)联合一种二线抗癫痫药物治疗后仍不能控制。超难治性癫痫持续状态(super refractory status epilepticus,SRSE)指应用麻醉药物治疗24 h后,发作仍不缓解或脑电图(electroencephalogram,EEG)痫样放电仍无法终止或发作已终止但维持麻醉剂减量过程中再次复发。排除年龄<28 d和年龄>14岁患儿及癔症等心理性疾病患儿。本研究通过医院医学伦理委员会批准(批准文号:QFELL-YJ-2022-40)。患儿监护人均知情同意。
类)联合一种二线抗癫痫药物治疗后仍不能控制。超难治性癫痫持续状态(super refractory status epilepticus,SRSE)指应用麻醉药物治疗24 h后,发作仍不缓解或脑电图(electroencephalogram,EEG)痫样放电仍无法终止或发作已终止但维持麻醉剂减量过程中再次复发。排除年龄<28 d和年龄>14岁患儿及癔症等心理性疾病患儿。本研究通过医院医学伦理委员会批准(批准文号:QFELL-YJ-2022-40)。患儿监护人均知情同意。
收集患儿性别、年龄、是否合并发育迟缓、惊厥发作形式、启动抗惊厥治疗时间、控制癫痫药物种类、是否使用呼吸机以及治疗效果。所有患儿入院2 h内采集外周静脉血标本以测定血乳酸,住院期间完善EEG、心电图;经监护人同意的患儿完善脑脊液、脑磁共振成像(magnetic resonance imaging,MRI)、血尿串联质谱和基因检测。
(1)已知病因:急性(如中毒、疟疾、脑炎、代谢、出血等)、远期(如创伤后、脑炎后、卒中后等)、进行性(如脑肿瘤、免疫性疾病等)、明确的临床综合征等;(2)未知病因(隐源性)。
入院后对所有患儿按照STEPSS和END-IT评分量表进行评分(表1、表2)。

儿童癫痫持续状态严重程度评分量表
The Status Epilepticus in Pediatric Patients Severity Score
儿童癫痫持续状态严重程度评分量表
The Status Epilepticus in Pediatric Patients Severity Score
| 项目 | 类型 | 计分 |
|---|---|---|
| 意识 | 清醒、嗜睡、意识模糊 | 0 |
| 昏迷 | 1 | |
| 发作形式 | 局限性发作、肌阵挛发作 | 0 |
| 全面性发作 | 1 | |
| 非惊厥SE,SE伴昏迷 | 2 | |
| 既往发作史 | 有 | 0 |
| 无或不知道 | 1 | |
| 年龄 | ≥2岁 | 0 |
| <2岁 | 2 |
注:SE:癫痫持续状态 SE:status epilepticus
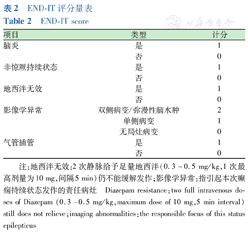
END-IT评分量表
END-IT score
END-IT评分量表
END-IT score
| 项目 | 类型 | 计分 |
|---|---|---|
| 脑炎 | 是 | 1 |
| 否 | 0 | |
| 非惊厥持续状态 | 是 | 1 |
| 否 | 0 | |
| 地西泮无效 | 是 | 1 |
| 否 | 0 | |
| 影像学异常 | 双侧病变/弥漫性脑水肿 | 2 |
| 单侧病变 | 1 | |
| 无局灶病变 | 0 | |
| 气管插管 | 是 | 1 |
| 否 | 0 |
注:地西泮无效:2次静脉给予足量地西泮(0.3~0.5 mg/kg,1次最高剂量为10 mg,间隔5 min)仍不能缓解发作;影像学异常:指引起本次癫痫持续状态发作的责任病灶 Diazepam resistance:two full intravenous doses of Diazepam (0.3-0.5 mg/kg,maximum dose of 10 mg,5 min interval) still does not relieve;imaging abnormalities:the responsible focus of this status epilepticus
出院时应用格拉斯哥预后评分量表(Glasgow Outcome Scale,GOS)评估患儿预后[6]。GOS内容:5分为恢复良好(恢复正常生活,尽管有些轻微缺陷);4分为轻度残疾(可独立生活,可在保护下工作);3分为重度残疾(日常生活不能独立,需要照顾);2分为植物生存(仅有最小反应,可随着睡眠/清醒周期,眼睛能睁开);1分为死亡。其中,4~5分定义为预后良好组,<4分定义为预后不良组。
应用SPSS 20.0软件进行统计学分析。符合正态分布的计量资料以 ±s表示,组间比较采用t检验。非正态分布数据以M(Q1,Q3)表示,应用非参数检验(秩和检验)进行比较。计数资料以率或构成比表示,组间比较应用χ2检验。应用二分类Logistic回归分析SE患儿预后不良的危险因素。采用受试者工作特征(receiver operating characteristic curve,ROC)曲线评价评分系统对SE患儿短期预后的预测价值。P<0.05为差异有统计学意义。
±s表示,组间比较采用t检验。非正态分布数据以M(Q1,Q3)表示,应用非参数检验(秩和检验)进行比较。计数资料以率或构成比表示,组间比较应用χ2检验。应用二分类Logistic回归分析SE患儿预后不良的危险因素。采用受试者工作特征(receiver operating characteristic curve,ROC)曲线评价评分系统对SE患儿短期预后的预测价值。P<0.05为差异有统计学意义。
共收治109例SE患儿,排除6例(年龄>14岁2例,心理疾病4例)。符合纳入标准者103例,其中男43例,女60例;年龄1个月至11岁,中位年龄48个月。其中RSE 18例(17.5%),SRSE 6例(5.8%)。根据GOS评分,预后良好组78例,预后不良组25例,其中死亡5例,死亡原因为中枢性呼吸衰竭,病因为颅内出血和重症脑炎。103例SE患儿的病因基线资料见表3,其中61例患儿完成脑脊液检查,55例患儿完成基因、代谢病筛查。病因明确者仅占36.9%,63.1%的患儿病因不明。感染性疾病中以病毒性脑炎最多见,非感染疾病中以基因病和染色体病为主,其中确诊为线粒体疾病2例。代谢性疾病2例,分别为甲基丙二酸血症和鸟氨酸氨甲酰转移酶缺乏症。
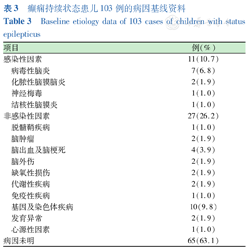
癫痫持续状态患儿103例的病因基线资料
Baseline etiology data of 103 cases of children with status epilepticus
癫痫持续状态患儿103例的病因基线资料
Baseline etiology data of 103 cases of children with status epilepticus
| 项目 | 例(%) |
|---|---|
| 感染性因素 | 11(10.7) |
| 病毒性脑炎 | 7(6.8) |
| 化脓性脑膜脑炎 | 2(1.9) |
| 神经梅毒 | 1(1.0) |
| 结核性脑膜炎 | 1(1.0) |
| 非感染性因素 | 27(26.2) |
| 脱髓鞘疾病 | 1(1.0) |
| 脑肿瘤 | 2(1.9) |
| 脑出血及脑梗死 | 4(3.9) |
| 脑外伤 | 2(1.9) |
| 缺氧性损伤 | 2(1.9) |
| 代谢性疾病 | 2(1.9) |
| 免疫性疾病 | 1(1.0) |
| 基因及染色体疾病 | 10(9.8) |
| 发育异常 | 2(1.9) |
| 心源性因素 | 1(1.0) |
| 病因未明 | 65(63.1) |
预后不良组患儿年龄较小(Z=-3.068,P=0.002)、血乳酸水平更高(Z=-6.085,P<0.001)、STEPSS评分和END-IT评分增高(Z=-6.956、-5.502,均P<0.001)、脑MRI异常比例增高(χ2=5.860,P=0.015)、合并发育迟缓的比例增高(χ2=16.756,P<0.001)、启动抗SE治疗时间长(Z=1.488,P=0.024)、治疗中应用呼吸机的比例和应用多种抗癫痫药物的比例均增高(均P<0.001)。但2组患儿在性别、惊厥发作形式、EEG和脑脊液检查异常的比例方面差异均无统计学意义(均P>0.05)(表4)。
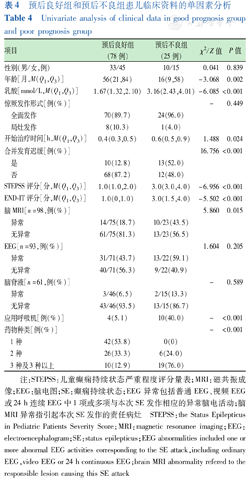
预后良好组和预后不良组患儿临床资料的单因素分析
Univariate analysis of clinical data in good prognosis group and poor prognosis group
预后良好组和预后不良组患儿临床资料的单因素分析
Univariate analysis of clinical data in good prognosis group and poor prognosis group
| 项目 | 预后良好组(78例) | 预后不良组(25例) | χ2/Z值 | P值 |
|---|---|---|---|---|
| 性别(男/女,例) | 33/45 | 10/15 | 0.041 | 0.839 |
| 年龄[月,M(Q1,Q3)] | 56(21,84) | 16(9,58) | -3.068 | 0.002 |
| 乳酸[mmol/L,M(Q1,Q3)] | 1.67(1.32,2.10) | 3.16(2.43,4.01) | -6.085 | <0.001 |
| 惊厥发作形式[例(%)] | - | 0.449 | ||
| 全面发作 | 70(89.7) | 24(96.0) | ||
| 局灶发作 | 8(10.3) | 1(4.0) | ||
| 开始治疗时间[h,M(Q1,Q3)] | 0.4(0.3,0.5) | 0.6(0.5,0.9) | 1.488 | 0.024 |
| 合并发育迟缓[例(%)] | 16.756 | <0.001 | ||
| 是 | 10(12.8) | 13(52.0) | ||
| 否 | 68(87.2) | 12(48.0) | ||
| STEPSS评分[分,M(Q1,Q3)] | 1.0(1.0,2.0) | 3.0(3.0,4.0) | -6.956 | <0.001 |
| END-IT评分[分,M(Q1,Q3)] | 1.0(0,1.0) | 3.0(1.5,4.0) | -5.502 | <0.001 |
| 脑MRI[n=98,例(%)] | 5.860 | 0.015 | ||
| 异常 | 14/75(18.7) | 10/23(43.5) | ||
| 无异常 | 61/75(81.3) | 13/23(56.5) | ||
| EEG[n=93,例(%)] | 1.604 | 0.205 | ||
| 异常 | 31/71(43.7) | 13/22(59.1) | ||
| 无异常 | 40/71(56.3) | 9/22(40.9) | ||
| 脑脊液[n=61,例(%)] | - | 0.589 | ||
| 异常 | 3/46(6.5) | 2/15(13.3) | ||
| 无异常 | 43/46(93.5) | 13/15(86.7) | ||
| 应用呼吸机[例(%)] | 4(5.1) | 10(40.0) | - | <0.001 |
| 药物种类[例(%)] | - | <0.001 | ||
| 1种 | 42(53.8) | 0(0) | ||
| 2种 | 26(33.3) | 6(24.0) | ||
| 3种及3种以上 | 10(12.9) | 19(76.0) |
注:STEPSS:儿童癫痫持续状态严重程度评分量表;MRI:磁共振成像;EEG:脑电图;SE:癫痫持续状态;EEG异常包括普通EEG、视频EEG或24 h连续EEG中1项或多项与本次SE发作相应的异常脑电活动;脑MRI异常指引起本次SE发作的责任病灶 STEPSS:the Status Epilepticus in Pediatric Patients Severity Score;MRI:magnetic resonance imaging;EEG:electroencephalogram;SE:status epilepticus;EEG abnormalities included one or more abnormal EEG activities corresponding to the SE attack,including ordinary EEG,video EEG or 24 h continuous EEG;brain MRI abnormality refered to the responsible lesion causing this SE attack
将SE预后结果作为因变量,赋值:预后不良=1,预后良好=0;将单因素分析中有差异的临床指标(血乳酸、是否合并发育迟缓、药物种类、MRI异常、启动抗SE治疗时间、应用呼吸机、STEPSS评分、END-IT评分)作为自变量,进行二分类Logistic回归分析,选择LR向前逐步回归法,逐步筛选出具有统计意义的指标,发现血乳酸水平增高、药物种类增多、STEPSS评分和END-IT评分增高是影响SE患儿预后的危险因素(表5)。
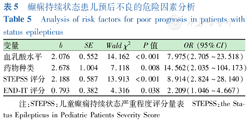
癫痫持续状态患儿预后不良的危险因素分析
Analysis of risk factors for poor prognosis in patients with status epilepticus
癫痫持续状态患儿预后不良的危险因素分析
Analysis of risk factors for poor prognosis in patients with status epilepticus
| 变量 | b | SE | Wald χ2 | P值 | OR (95%CI) |
|---|---|---|---|---|---|
| 血乳酸水平 | 2.076 | 0.552 | 14.162 | <0.001 | 7.975(2.705~23.518) |
| 药物种类 | 2.678 | 1.004 | 7.118 | 0.008 | 14.562(2.035~104.173) |
| STEPSS评分 | 2.188 | 0.587 | 13.913 | <0.001 | 8.914(2.824~28.140) |
| END-IT评分 | 0.793 | 0.382 | 4.316 | 0.038 | 2.209(1.046~4.667) |
注:STEPSS:儿童癫痫持续状态严重程度评分量表 STEPSS:the Status Epilepticus in Pediatric Patients Severity Score
分别绘制STEPSS评分和END-IT评分预测SE患儿预后的ROC曲线,计算曲线下面积(area under the curve,AUC)和截断值。STEPSS评分和END-IT评分用于预测SE患儿发生不良预后时,截断值分别为2.5分和1.5分,约登指数分别为0.82和0.52,AUC(95%CI)分别为0.939(0.895~0.983)和0.853(0.769~0.936)。STEPSS评分组的AUC值较END-IT评分组增高(U=36.91,P<0.05)。STEPSS评分的敏感度、特异度、准确性、阴性预测值均高于END-IT评分,2种评分的阴性预测分别为98.5%、90.8%,但阳性预测值分别为68.6%、50.0%;2种评分联合试验评估SE患儿发生不良预后时,并联试验和串联试验的AUC(95%CI)分别为0.833(0.758~0.908)和0.834(0.724~0.944)。并联试验的敏感度和阴性预测值均达100.0%,串联试验的特异度为94.9%,阳性预测值为81.8%,均高于单项评分指标。STEPSS评分、END-IT评分、并联试验和串联试验的约登指数进行比较,STEPSS评分组最高(Z=6.818,P<0.01)(表6,图1)。
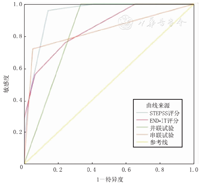

注:ROC:受试者工作特征;STEPSS:儿童癫痫持续状态严重程度评分量表 ROC:receiver operating characteristic;STEPSS:the Status Epilepticus in Pediatric Patients Severity Score
STEPSS和END-IT评分系统评估价值的比较
Comparison of the assessed value of STEPSS and END-IT scoring systems
STEPSS和END-IT评分系统评估价值的比较
Comparison of the assessed value of STEPSS and END-IT scoring systems
| 评分 | 敏感度[%(例)] | 特异度[%(例)] | 假阳性[%(例)] | 假阴性[%(例)] | 阳性预测值[%(例)] | 阴性预测值[%(例)] | 准确性[%(例)] | 约登指数 | 约登指数J方差 |
|---|---|---|---|---|---|---|---|---|---|
| STEPSS评分 | 96.0(24/25) | 85.9(67/78) | 14.1(11/78) | 4.0(1/25) | 68.6(24/35) | 98.5(67/68) | 88.3(91/103) | 0.820 | 0.005 2 |
| END-IT评分 | 76.0(19/25) | 75.6(59/78) | 24.4(19/78) | 24.0(6/25) | 50.0(19/38) | 90.8(59/65) | 75.7(78/103) | 0.520 | 0.008 8 |
| 联合试验 | |||||||||
| 并联 | 100.0(25/25) | 66.7(52/78) | 33.3(26/78) | 0(0/25) | 49.0(25/51) | 100.0(52/52) | 74.8(77/103) | 0.667 | 0.008 8 |
| 串联 | 72.0(18/25) | 94.9(74/78) | 5.1(4/78) | 28.0(7/25) | 81.8(18/22) | 91.4(74/81) | 89.3(92/103) | 0.669 | 0.004 5 |
注:STEPSS:儿童癫痫持续状态严重程度评分量表;约登指数=敏感度+特异度-1;约登指数J方差=α(1-α)/(a+b)+β(1-β)/(c+d),α为假阳性率,β为假阴性率,a+b为金标准确诊的例数,c+d为金标准排除的例数;并联:STEPSS评分≥2.5或END-IT评分≥1.5;串联:STEPSS评分≥2.5和END-IT评分≥1.5 STEPSS:the Status Epilepticus in Pediatric Patients Severity Score;Youden index=sensitivity+specificity-1;J variance of Youden index=α(1-α)/(a+b)+β(1-β)/(c+d);α was false positive rate,β was false negative rate,a+b was the number of cases confirmed by gold standard,c+d was the number of cases excluded by gold standard;parallel test:STEPSS score≥2.5 or END-IT score≥1.5;series test:STEPSS score≥2.5 and END-IT score≥1.5
SE总体死亡率高,及早识别导致SE预后不良的危险因素,对降低SE患者的致残、致死率具有重要意义[7]。多项研究致力于探讨影响SE不良预后的危险因素,包括急性症状性病因(如中枢神经系统感染、创伤、缺氧等)、年龄、惊厥持续时间、应用机械通气、神经影像学异常、RSE、发育落后等[8,9]。本研究结果显示,患儿死亡病因以重症脑炎和颅内出血多见,预后不良者年龄更小、脑MRI异常比例和应用气管插管的比例增高,且控制惊厥药物种类增多,与文献报道[8,9,10]一致。同时,本研究显示,血乳酸水平增高是影响SE患儿预后的危险因素,血乳酸为机体在缺血、缺氧状态时无氧酵解的产物,是反映组织灌注的敏感指标,对颅脑损伤具有重要的提示意义[11]。本研究结果提示,上述临床指标可在预测SE患儿不良预后的临床实践中参考应用。但由于影像学、血标志物等检查的复杂性和不确定性,临床工作中需要更稳定可靠的评估方法,将患者根据预后风险进行分层以便及时调整治疗策略[12]。
STESS从意识、发作形式、既往发作史及年龄4个方面对患者进行预后评估,在成人中广泛应用且具有较好的指导价值[13]。2019年有学者将其应用于儿科,并对年龄界值设定为2岁,定义为STEPSS,发现预测不良预后的截断值为3分(敏感度93%,特异度81%)[3]。张群群等[14]研究发现,STEPSS预测SE患者不良预后的截断值为2.38分。本研究中,STEPSS评分增高是影响SE患儿预后的危险因素,其预测截断值为2.5分,敏感度96.0%,特异度85.9%,提示STEPSS评分对SE患儿的不良预后具有较高的预测价值。END-IT评分在2016年提出[15],其中加入了治疗因素,是目前可对SE患者出院后的功能恢复进行预测的评分,最初适用于12岁以上SE患者的远期预后评估。2021年Kapoor等[4]将其用于评估印度SE患儿的短期预后,发现预后不良的预测截断值为2分(敏感度73%,特异度94%),对SE患儿的短期预后也有较好的预测价值。本研究发现END-IT评分预测SE患儿发生不良预后的AUC在0.7以上,提示有一定的评估作用,其预测截断值为1.5分;但其敏感度仅为76.0%,特异度也未达到80%,阳性预测值较低,提示END-IT评分预测SE患儿短期不良预后的可靠性偏低,与文献报道的结果不一致[4,15],考虑可能与所研究人群的种族和人口学特征不同有关。
本研究比较STEPSS评分和END-IT评分对SE患儿短期预后的预测价值,发现STEPSS评分的AUC值高,且敏感度、特异度和准确性均高于END-IT评分,约登指数最高,其整体预测效能优于END-IT评分。2种评分系统的阴性预测值均较高,能够较准确地预测SE患儿的良好结局,可用于指导SE患儿的早期治疗策略,避免过度治疗;但2种评分系统的阳性预测值均较低,预测SE患儿不良结局的可靠性偏低。因此,本研究进一步通过并联试验和串联试验进行联合分析,发现2种评分系统联合试验评估SE患儿预后时,并联试验的敏感度和阴性预测值均可达100.0%,能准确地预测SE患儿的良好结局并指导早期治疗;串联试验的特异度为94.9%,阳性预测值为81.8%,对SE患儿短期不良预后预测的可靠性高,有助于高危患儿的分层治疗,其评估效能优于单项评分系统。
总之,STEPSS和END-IT操作简单,对SE患儿的短期预后具有一定的预测价值。2种评分系统联合应用更有利于SE患儿短期预后的评估。本研究的不足:(1)纳入的SE患儿均来自本院,为单中心研究,且病例数偏少;(2)未进行SE患儿的长期预后评估和记录治疗过程中的动态变化。这是未来需进一步完善的方向。
所有作者均声明不存在利益冲突



























