
探讨MR内耳水成像技术在人工耳蜗植入术中的应用价值。
回顾性分析2015年4月—2016年3月在黑龙江省医院和哈尔滨医科大学附属第四医院行人工耳蜗植入术的128例患者的影像资料,其中男68例、女60例,年龄4~48岁,右耳植入101例、左耳植入27例。患者术前、术后均行头颅内听道螺旋CT及MR内耳水成像检查,并比较两种检测方法对患者内耳、中耳畸形及病变的检出率。
MR内耳水成像内听道总体异常检出率90.63%(116/128),CT检出率为76.56%(98/128),二者比较差异有统计学意义(χ2=9.228,P<0.05)。在前庭导水管异常、耳蜗畸形、内听道狭窄、耳蜗纤维化等疾病,MR诊断的灵敏度、特异度、准确度、阳性预测值和阴性预测值均高于CT,但差异均无统计学意义(P值均>0.05)。
在人工耳蜗植入术前、术后进行MR内耳水成像技术检查,可有效了解患者内听道解剖学信息,对治疗方案的选择具有指导性意义,值得临床进一步推广应用。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
随着人工耳蜗植入技术的日趋成熟,术前检查、术式等不断完善,目前人工耳蜗植入术已普及至各大医院当中[1]。因需要行人工耳蜗植入的患者内耳解剖结构不同,以及对内耳疾病严重程度评估差异等因素,使得该术式的临床效果存在一定的不确定性,因此,术前检查显得极为重要。除常规耳科专项、听力学评价外,影像学检查也是术前必要的检查项目[2]。以往临床中常使用螺旋CT对该疾病患者进行术前检查,但由于内耳道解剖结构较为复杂,当出现内耳道狭窄、耳蜗畸形等情况时,CT无法进行检测[3]。近年来,MR内耳水成像技术应用于临床内耳疾病检查,并取得了较好的诊断效果。本研究中,分别应用螺旋CT及MR内耳水成像技术对128例行人工耳蜗植入术的患者进行检查,并比较两者的检查结果,旨在分析MR内耳水成像技术在人工耳蜗植入术中的应用价值。
纳入标准:双耳重度或极重度感音神经性聋者;配戴合适助听器,经听力康复训练3~6个月听觉言语能力无明显改善者;患者本人及家属知情且同意入组观察者。
排除标准:伴其他心、肝、肾等重要脏器病变者;伴发精神疾病,依从性较差者;患者本人或家属不知情或知情后拒绝入组观察者。
纳入2015年4月—2016年3月黑龙江省医院和哈尔滨医科大学附属第四医院128例行人工耳蜗植入术患者的临床资料进行回顾性分析,其中男68例,女60例;年龄4~48岁;右耳植入101例,左耳植入27例。人工耳蜗类型分别为:美国AB人工耳蜗90k型68例,澳大利亚Neuclear24M型32例,奥地利Med-EL40+型24例,国产耳蜗诺尔康CS-10A 4例。纳入患者均先行常规听力学检查,包括耳声发射、声阻抗、脑干诱发电位、多频稳态等检查,同时依据情况补充40 Hz相关电位、电测听检查;患者均行MR内耳水成像和CT检查。
本研究得到黑龙江省医院医学伦理委员会批准(批准文号:HLJSYY20150312),患者或患儿家长均签署知情同意书。
选择美国GE HDx 3.0 T MR扫描仪。MR检查:嘱患者保持仰卧位,头部位于正中位置,双耳对称。儿童患者若可合作则无需行干预;若患者年龄较小,需于检查前减少睡眠,并于检查前0.5 h内应用苯巴比妥进行镇定。扫描范围包括头部及颞骨岩部。患者均行3D高级快速自旋回波序列进行横断面扫描,参数如下:TE 2.5 ms、TR 6.5 ms, FOV 16 mm×16 mm,矩阵448 mm×256 mm,间距0.4 mm,层厚0.8 mm。对患者颞骨原始图像进行最大密度投影3D重建,删除低信号组织,保留双侧内耳。
CT设备选择日本东芝Aquilion 64排螺旋CT。扫描范围包括面神经、前庭水管、前庭、半规管、耳蜗等;扫描参数:层距1.0 mm,层厚1.0 mm,管电流200 mA,管电压120 kV,窗位500 HU,窗宽3 500 HU。
患者全身麻醉。植入电极后进行电极阻抗测试和神经反应遥测,其中内耳畸形患者使用EBAR监测和面神经监测。采用耳后切口、面隐窝进路。切口分为两层,表层为皮肤皮下,深层为颞筋膜。将皮瓣向后翻开,暴露乳突区骨皮质。用电钻于乳突后上方颅骨表面打磨接受刺激器骨床。行单纯乳突切除术,暴露砧骨短脚;以此为标志开放面隐窝,于圆窗龛前下方打开耳蜗鼓阶。将接受刺激器入位骨床,将刺激电极插入耳蜗鼓阶[4],参考电极置于颞肌下的颅骨表面。
观察MR内耳水成像与螺旋CT两种检查方法对内耳畸形的检出结果,并以手术诊断为金标准,比较两种方法检测的灵敏度、特异度、准确度、阳性预测值和阴性预测值[5]。
应用SPSS 16.0软件对研究数据进行统计学分析。计数资料比较采取配对χ2检验和Fisher确切概率法检验。以P<0.05为差异有统计学意义。
128例患者均成功完成微创人工耳蜗植入术。手术诊断:前庭导水管异常51例,耳蜗畸形42例,内听道狭窄19例,耳蜗纤维化16例。
MR内耳水成像内耳畸形检出率为90.63%(116/128),螺旋CT的检出率为76.56%(98/128),二者比较差异有统计学意义(χ2=9.228,P<0.01)。与手术诊断金标准比较,MR内耳水成像与螺旋CT对不同内耳畸形诊断的灵敏度、特异度、准确度、阳性预测值、阴性预测值等分别见表1、表2。
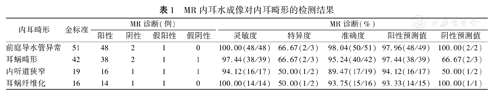
MR内耳水成像对内耳畸形的检测结果
MR内耳水成像对内耳畸形的检测结果
| 内耳畸形 | 金标准 | MR诊断(例) | MR诊断(%) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 阳性 | 阴性 | 假阳性 | 假阴性 | 灵敏度 | 特异度 | 准确度 | 阳性预测值 | 阴性预测值 | ||
| 前庭导水管异常 | 51 | 48 | 2 | 1 | 0 | 100.00(48/48) | 66.67(2/3) | 98.04(50/51) | 97.96(48/49) | 100.00(2/2) |
| 耳蜗畸形 | 42 | 38 | 2 | 1 | 1 | 97.44(38/39) | 66.67(2/3) | 95.24(40/42) | 97.44(38/39) | 66.67(2/3) |
| 内听道狭窄 | 19 | 16 | 1 | 1 | 1 | 94.12(16/17) | 50.00(1/2) | 89.47(17/19) | 94.12(16/17) | 50.00(1/2) |
| 耳蜗纤维化 | 16 | 14 | 1 | 1 | 0 | 100.00(14/14) | 50.00(1/2) | 93.75(15/16) | 93.33(14/15) | 100.00(1/1) |
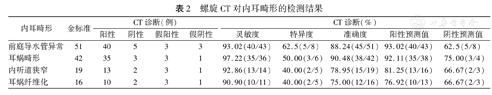
螺旋CT对内耳畸形的检测结果
螺旋CT对内耳畸形的检测结果
| 内耳畸形 | 金标准 | CT诊断(例) | CT诊断(%) | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 阳性 | 阴性 | 假阳性 | 假阴性 | 灵敏度 | 特异度 | 准确度 | 阳性预测值 | 阴性预测值 | ||
| 前庭导水管异常 | 51 | 40 | 5 | 3 | 3 | 93.02(40/43) | 62.5(5/8) | 88.24(45/51) | 93.02(40/43) | 62.5(5/8) |
| 耳蜗畸形 | 42 | 35 | 3 | 3 | 1 | 97.22(35/36) | 50.00(3/6) | 90.48(38/42) | 92.11(35/38) | 75.00(3/4) |
| 内听道狭窄 | 19 | 13 | 2 | 3 | 1 | 92.86(13/14) | 40.00(2/5) | 78.95(15/19) | 81.25(13/16) | 66.67(2/3) |
| 耳蜗纤维化 | 16 | 10 | 2 | 3 | 1 | 90.90(10/11) | 40.00(2/5) | 75.00(12/16) | 76.92(10/13) | 66.67(2/3) |
CT与MR内耳水成像各指标比较,MR内耳水成像诊断内耳各种畸形的灵敏度、特异度、准确度、阳性预测值和阴性预测值均高于CT,但差异均无统计学意义(P值均>0.05)。见表3、图1。
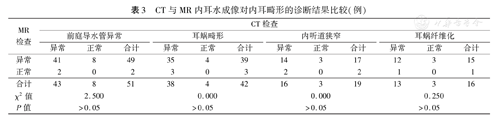
CT与MR内耳水成像对内耳畸形的诊断结果比较(例)
CT与MR内耳水成像对内耳畸形的诊断结果比较(例)
| MR检查 | CT检查 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 前庭导水管异常 | 耳蜗畸形 | 内听道狭窄 | 耳蜗纤维化 | |||||||||
| 异常 | 正常 | 合计 | 异常 | 正常 | 合计 | 异常 | 正常 | 合计 | 异常 | 正常 | 合计 | |
| 异常 | 41 | 8 | 49 | 35 | 4 | 39 | 14 | 3 | 17 | 12 | 3 | 15 |
| 正常 | 2 | 0 | 2 | 3 | 0 | 3 | 2 | 0 | 2 | 1 | 0 | 1 |
| 合计 | 43 | 8 | 51 | 38 | 4 | 42 | 16 | 3 | 19 | 13 | 3 | 16 |
| χ2值 | 2.500 | 0.000 | 0.000 | 0.250 | ||||||||
| P值 | >0.05 | >0.05 | >0.05 | >0.05 | ||||||||
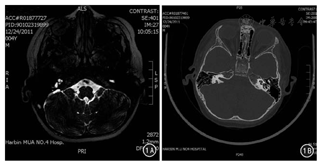

MR水成像技术[6,7]就是将标准头部正交线圈放在患者双耳,应用缓慢流动的液体进行成像,利用较长的重复时间及长回波时间,获得重T2WI,使得富含水的脂肪与周围组织对比更为明显。同时,进行最大密度投影3D重建,可将患者耳蜗形态清晰呈现,与周边低信号组织形成对比,不含水或含水量较少的组织随着回波时间的不断延长而衰减;与内耳造影效果相似,可直接将患者内耳膜迷路、淋巴囊、淋巴管等显像,同时易于发现较小的肿瘤,为临床提供了有利的影像依据。该技术不使用任何造影剂,检出率也明显高于其它检查方式,对行人工耳蜗植入术患者的评估有重要指导意义。目前,MRI检查颞骨主要有以下3种方法[8]:增强T1WI、2D自旋回波序列及3D梯度回波翻转。
本组研究中,对内耳病变患者,以手术诊断为金标准,对采用螺旋CT和MR内耳水成像检测结果进行对比观察。本研究结果显示:(1)MR内耳水成像诊断具有较高的诊断灵敏度、特异度、准确度、阳性预测值和阴性预测值,并且在诊断前庭导水管异常和耳蜗纤维化疾病中,灵敏度与阴性预测值可以达到100%。(2)整体上,CT诊断各种内耳畸形的灵敏度、特异度、准确度、阳性预测值和阴性预测值均低于MR内耳水成像诊断,但两种方法比较差异均无统计学意义(P值均>0.05)。虽然螺旋CT对骨性病变诊断方面优势明显,但其对软组织成像能力极低,而MR内耳水成像技术则可将其清晰显示,能为手术提供依据。
正常内耳MRI表现大致如下:内听道处于颞骨深处,于重T2WI上表现为椎管状高信号,直径大约在5 mm左右;内部脑脊液表现为高信号,可清楚观察到患者神经走行及与周围血管间关联[9]。半规管多为边缘光滑的C形结构,除椭圆囊处的半规管略微胀大外,其余部位较为均匀。耳蜗多呈高信号"蜗牛状"表现,球囊及椭圆囊结构可清晰呈现。而先天性内耳畸形、发育不全的患者于MR内耳水成像检测中多表现为影像缺失现象[10]。导水管综合征患者多表现为淋巴管、囊的扩张,于T2WI上内淋巴管多位于乙状窦的前方,表现为高信号,可于内耳的测量中显像,其中点宽度为0.1~1.4 mm,若其最大宽度超过1.5 mm则可诊断为淋巴囊扩张,该类型患者术中可出现搏动性脑脊液漏,严重者出现甚至出现井喷显像[11]。正常人体内听道于MRI中多为管、椎状高信号;血管、神经间隔、走行极为清晰;耳蜗形似蜗牛,球囊、椭圆囊较为完全,呈高信号;半规管表现为边缘光滑的C字形[12]。病理状态下MRI多表现为内耳Michel畸形、Mondini畸形等[13];前庭水管异常者多表现为淋巴囊异常增大,且呈高信号。相比螺旋CT,MR内耳水成像可更为精准地对耳蜗神经进行评价,对手术方案的制定意义重大[14]。
对人工耳蜗植入术患者手术前后进行MR内耳水成像检查,可有效了解患者内听道解剖学结构,对治疗方案的选择具有指导性意义,值得于临床中进一步推广使用。本研究中,MR内耳水成像相对于螺旋CT检查,能够提供更为准确的诊断信息,值得临床借鉴。但本次研究持续时间较短,样本数量较小,所得结论尚需要进一步验证。在今后的研究中需采集大量样本,以期得到可靠的研究数据,为临床提供有利依据。



























