
比较Tri-Lock骨保留型股骨柄(BPS)与Corail股骨柄治疗成人发育性髋关节发育不良(DDH)的临床应用价值。
回顾性分析。纳入2015年1月—2019年4月贵州省人民医院骨关节外科病区Crowe Ⅰ型DDH患者35例(40髋),其中男5例(5髋)、女30例(35髋),年龄26~77(60.81±11.72)岁,均采用全髋关节置换术(THA)治疗。按照使用的股骨柄假体类型不同分为两组:观察组17例20髋,采用Tri-Lock BPS;对照组18例20髋,采用Corail股骨柄。对比两组患者的性别、年龄、髓腔闪烁指数(CFI),比较两组患者术后股骨柄初始稳定性、手术前后双下肢绝对长度差及股骨小转子最宽部骨量保留的面积,使用Mimics 17.0测量大小转子间骨量保留体积,并记录与股骨柄相关并发症。术后第2日使用视觉模拟评分(VAS)评估髋部疼痛程度,术后12周按照Harris髋关节评分(HHS)标准评价整体疗效。
两组患者性别、年龄、CFI等一般资料比较差异均无统计学意义(P值均>0.05)。术后随访6~18个月,平均12.6个月。患者的股骨柄初始稳定性以及术前术后双下肢绝对长度差组间比较,差异均无统计学意义(P值均>0.05);观察组患者的股骨小转子最宽部骨量保留的面积[(6.28±0.32)cm2]、大小转子间骨量保留体积[(30.25±0.81)cm3]均大于对照组患者[(5.63±0.14)cm2、(17.74±0.33)cm3],差异均有统计学意义(t=8.313、64.099, P值均<0.01)。术后第2天髋部疼痛VAS、双下肢绝对长度差、股骨柄的初始稳定性观察指标组间比较,差异均无统计学意义(P值均>0.05);术后12周,观察组与对照组HHS总分及其中髋部疼痛评分比较差异均有统计学意义(t=2.098、2.432, P值均<0.05),但髋关节功能、运动及肢体畸形评分比较差异均无统计学意义(P值均>0.05)。观察组患者并发症发生率(5.0%,1/20)低于对照组(25.0%, 5/20),但差异无统计学意义(χ2=1.765, P>0.05)。
Tri-Lock BPS较Corail股骨柄假体用于治疗Crowe Ⅰ型DDH THA中,具有更加微创、更好的临床效果和更多的股骨近端骨量保留的优势,且不增加手术并发症。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
发育性髋关节发育不良(developmental dysplasia of the hip, DDH )患者由于髋臼发育异常、髋臼覆盖不足,导致髋关节负重区软骨退变、骨质增生,最终引发髋骨关节炎[1],常常需要行全髋关节置换术(total hip arthroplasty, THA)治疗[2]。继发于DDH的髋骨关节炎常见于中青年人群,为尽可能延长假体使用寿命,同时为未来可能的翻修手术留有余地,应尽可能选择生物型假体,并最大限度地保留原始骨量。Tri-Lock骨保留型股骨柄(bone preservation stem, BPS)具有微创置入、解剖匹配等优点,能够满足上述要求。本研究中,分析采用THA治疗的35例(40侧)CroweⅠ型DDH患者临床和影像学资料,重点比较分别使用Tri-Lock BPS与经典Corail股骨柄两种类型假体的患者的临床预后、骨量保留情况及并发症发生率,旨在为Tri-Lock BPS的临床应用提供参考。
纳入标准:(1)Crowe Ⅰ型DDH患者,保守治疗无效、严重髋骨关节炎;(2)接受初次THA的患者;(3)无髋部活动性感染或炎性病变。排除标准:(1)既往有髋关节手术史;(2)有严重的心脑血管方面疾病、糖尿病、免疫系统疾病、长期酗酒吸烟史等;(3)不能按时随访的患者;(4)接受双侧手术患者两次手术时间间隔小于3个月。
回顾性研究。纳入2015年1月—2019年4月贵州省人民医院骨关节外科病区Crowe Ⅰ型DDH患者35例(40髋),其中男5例(5髋)、女30例(35髋),年龄26~77(60.81±11.72)岁。根据使用的股骨柄假体类型不同将患者分为观察组(采用Tri-Lock BPS)和对照组(采用Corail股骨柄)。
本研究符合《赫尔辛基宣言》的要求,所有患者术前签署手术知情同意书。
患者均全身麻醉,取常规后外侧入路(Gibson入路)。观察组使用50°导板截骨、对照组使用传统的45°导板截断股骨颈,两组患者均使用Pinnacle髋臼杯(Depuy,美国强生),根据患者术前要求选择陶瓷或高交联聚乙烯内衬。股骨髓腔开口,依次扩髓至合适深度后,观察组使用Tri-Lock BPS(Depuy,美国强生),对照组使用Corail股骨柄(Depuy,美国强生)。安装陶瓷头并复位髋关节。
两组患者术前30 min预防性使用抗生素,术后继续应用24 h,并予以氟比洛芬酯镇痛、低分子肝素钙皮下注射预防深静脉血栓形成。自麻醉完全苏醒后即床旁指导患者行大腿肌肉收缩锻炼。术后24 h后指导患者下地负重行走并指导卧床坐位姿势防脱位。
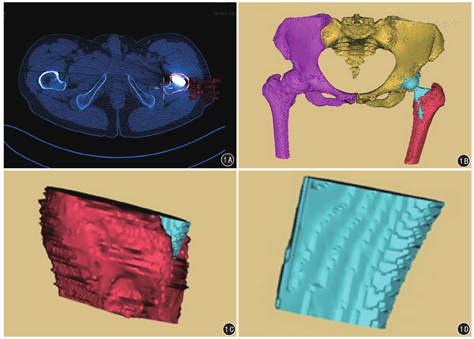
(1)一般资料:比较两组患者性别、年龄及髓腔闪烁指数(canal flare index, CFI)等。(2)治疗效果:对患者术后第2日髋部疼痛改善情况进行VAS评估;术后12周使用Harris髋关节评分(harris hip score, HHS)标准评价患者髋部的整体功能,具体从疼痛、功能、髋关节活动和肢体畸形四个方面来评估,90~100分为优、80~89分较好,70~79分为尚可,<70分为差。(3)股骨假体位置及稳定性评估:参考Mulliken标准,术后即刻采用X线测量评估股骨假体置换后股骨柄的初始位置,以股骨柄居中或内外翻角度≤3°,同时股骨柄压配率于X线正位片达80%、侧位片达70%为股骨柄初始稳定性优良,未达此标准的为差。(4)双下肢绝对长度差:在手术前后双髋X线正位片上,分别测量双侧小转子基底部到坐骨结节连线的高度,记录两侧差值。(5)两组假体骨量保留参数比较:基于CT三维重建影像,于股骨小转子最宽部层面,测量股骨外层皮质、假体外层平面的面积,两者差值即为小转子最宽部骨量保留面积;应用Mimics 17.0软件重建并测量大转子最宽部至小转子最宽部容量体积,减去对应部位的假体体积,即为大小转子间骨量保留体积。见图1。(6)术中及术后早期并发症:股骨近端医源性骨折、大腿远端疼痛等。

采用SPSS 20.0统计软件进行数据分析。服从近似正态分布的计量资料用 ±s表示,两组间比较采用独立样本t检验,组内比较采用配对t检验;分类资料比较采用χ2检验。以P<0.05为差异有统计学意义。
±s表示,两组间比较采用独立样本t检验,组内比较采用配对t检验;分类资料比较采用χ2检验。以P<0.05为差异有统计学意义。
观察组和对照组两组患者均为Crowe Ⅰ型DDH,性别、年龄及CFI等指标组间比较差异均无统计学意义(P值均>0.05)。见表1。
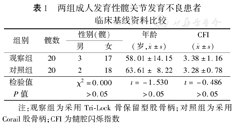
两组成人发育性髋关节发育不良患者临床基线资料比较
两组成人发育性髋关节发育不良患者临床基线资料比较
| 组别 | 髋数 | 性别(髋) | 年龄(岁, ±s) ±s) | CFI( ±s) ±s) | |
|---|---|---|---|---|---|
| 男 | 女 | ||||
| 观察组 | 20 | 3 | 17 | 58.01±14.15 | 3.38±1.16 |
| 对照组 | 20 | 2 | 18 | 63.61± 8.22 | 3.28±0.78 |
| 检验值 | χ2=0.000 | t=-1.530 | t=-0.486 | ||
| P值 | >0.05 | >0.05 | >0.05 | ||
注:观察组为采用Tri-Lock骨保留型股骨柄;对照组为采用Corail股骨柄;CFI为髓腔闪烁指数
观察组THA术后股骨柄初始稳定性优良率略高于对照组,差异无统计学意义(P>0.05)。两组患者双下肢绝对长度差术后较术前均有改善,差异均有统计学意义(P值均<0.01);但术前和术后组间比较,差异均无统计学意义(P值均>0.05)。观察组术后股骨小转子最宽部骨量保留面积、大小转子间骨量保留体积均优于对照组,差异均有统计学意义(P值均<0.01)。见表2。
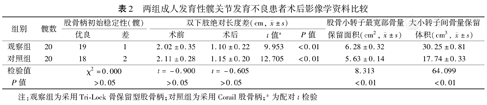
两组成人发育性髋关节发育不良患者术后影像学资料比较
两组成人发育性髋关节发育不良患者术后影像学资料比较
| 组别 | 髋数 | 股骨柄初始稳定性(髋) | 双下肢绝对长度差(cm,  ±s) ±s) | 股骨小转子最宽部骨量保留面积(cm2,  ±s) ±s) | 大小转子间骨量保留体积(cm3,  ±s) ±s) | ||||
|---|---|---|---|---|---|---|---|---|---|
| 优良 | 差 | 术前 | 术后 | t值a | P值 | ||||
| 观察组 | 20 | 19 | 1 | 2.02±0.35 | 1.10±0.22 | 9.953 | <0.01 | 6.28±0.32 | 30.25±0.81 |
| 对照组 | 20 | 18 | 2 | 2.11±0.28 | 1.15±0.20 | 12.705 | <0.01 | 5.63±0.14 | 17.74±0.33 |
| 检验值 | χ2 =0.000 | t=-0.900 | t=-0.605 | 8.313 | 64.099 | ||||
| P值 | >0.05 | >0.05 | >0.05 | <0.01 | <0.01 | ||||
注:观察组为采用Tri-Lock骨保留型股骨柄;对照组为采用Corail股骨柄;a为配对t检验
两组患者术后均获随访,随访时间6~18个月,平均12.6个月。术后12周,观察组与对照组HHS总分及髋部疼痛评分比较,差异均有统计学意义(P值均<0.05);但HHS评分系统中的髋关节功能、活动及肢体畸形评分,以及术后第2天髋部疼痛VSA,组间比较差异均无统计学意义(P值均>0.05)。见表3。
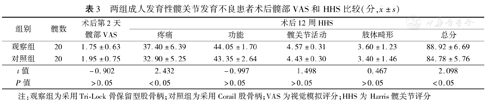
两组成人发育性髋关节发育不良患者术后髋部VAS和HHS比较(分, ±s)
±s)
两组成人发育性髋关节发育不良患者术后髋部VAS和HHS比较(分, ±s)
±s)
| 组别 | 髋数 | 术后第2天髋部VAS | 术后12周HHS | ||||
|---|---|---|---|---|---|---|---|
| 疼痛 | 功能 | 髋关节活动 | 肢体畸形 | 总分 | |||
| 观察组 | 20 | 1.75±0.63 | 37.40±6.39 | 44.05±1.70 | 4.57±0.31 | 3.60±1.23 | 88.92±6.69 |
| 对照组 | 20 | 1.95±0.75 | 32.90±5.25 | 43.35±2.64 | 4.43±0.30 | 3.40±1.46 | 84.78±5.76 |
| t值 | -0.902 | 2.432 | -0.997 | 1.498 | 0.467 | 2.098 | |
| P值 | >0.05 | <0.05 | >0.05 | >0.05 | >0.05 | <0.05 | |
注:观察组为采用Tri-Lock骨保留型股骨柄;对照组为采用Corail股骨柄;VAS为视觉模拟评分;HHS为Harris髋关节评分
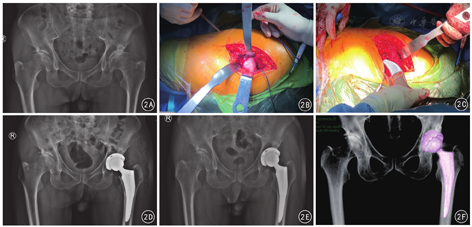
两组患者均未发生切口感染;对照组2髋因术中锉磨髓腔时出现股骨近端医源性骨折采取近端钢丝加固,观察组未见上述情况发生;对照组3例、观察组1例出现大腿远端疼痛。术后并发症总体发生率观察组(5.0%,1/20)低于对照组(25.0%,5/20),但差异无统计学意义(χ2 =1.765,P>0.05)。典型病例见图2。

DDH患者因髋臼与股骨头匹配不良,容易出现髋部关节负重区软骨退变、骨质增生,最终导致髋骨关节炎的发生[1]。既往受到人工关节使用寿命的限制,DDH患者常采取相对保守的治疗策略。随着手术技术的发展以及人工关节摩擦界面的革新,DDH患者继发终末期髋骨关节炎患者选择THA作为终极治疗日益受到认可和推广。这类患者一方面有着更高的功能需求,另一方面存在日后潜在翻修的可能。因此,手术中充分匹配并尽可能地保留骨量具有重要意义[3]。
临床广泛使用的经典生物型全涂层股骨柄(Corail柄)已历时30余载,其近、远期的临床疗效优良,但在临床应用中发现其依然存在下述问题[4,5]:(1)矩形贴边设计力求紧贴皮质,为获得更好的初始稳定性却牺牲了股骨近端大部分骨量,并容易导致股骨距皮质破裂即股骨近端医源性骨折的发生,术中需使用钢丝环扎以加强假体的稳定性;(2)直柄的设计导致应力集中于股骨峡部,部分患者术后出现大腿远端疼痛[6]。
Tri-Lock BPS具有如下特点[6]:(1)采用股骨柄扁平、双面锥化设计,更加匹配股骨髓腔的生理解剖形态,即近端膨大、远端狭窄,能在股骨颈及近端干骺端区域获得良好的填充压配,提供了优良的初始稳定性[7]。(2)缩小股骨柄远端长度和宽度,减少或不扩大远端峡部髓腔,保留远端峡部骨量。(3)较之传统的45°截骨线,50°截骨线可有效保留股骨距部骨量。Hammer[8]指出,股骨距为人体负重的重要构成部分,它作为真正的股骨颈起到承上启下重要作用,股骨距部骨量的增加减少了操作过程中股骨近端医源性骨折的发生。(4)削肩设计,锉磨过程中远离了大转子区域,保留更多的股骨近端大转子部骨量,并避免了磨锉过程中对臀中肌的大转子止点部潜在损伤。(5)股骨柄的远端采取应力分散的设计,减少了因应力集中于股骨柄远端而导致近端大粗隆部失应力的骨量流失[9],也减少了术后大腿远端疼痛的发生率[6]。针对上述特点,本研究中采用股骨小转子最宽部区域骨量的面积,并重点数字重建股骨大小转子最宽部间区域,以此来观察具体骨量保留情况,将抽象的骨量保留概念数字化,证实了观察组较对照组能在此区域内有效保留骨量,可为后期翻修预留切实可靠的骨量空间。
在DDH患者的治疗中,不仅存在臼-头覆盖差、髋臼纤维环扁平翻转、髋臼外倾角增大等髋臼侧的问题,往往还合并存在股骨髓腔狭窄、股骨前倾角增大等股骨侧的问题[10,11],即使扩髓也仍难达到常规股骨髓腔的宽度。特别是CFI大于4.7的DDH患者,使用Corail股骨柄常出现股骨远端难以扩髓,即使强行扩髓插入股骨柄,其近端也会出现压配不足的问题。而Tri-Lock BPS的远端更细长,有利于将假体柄充分打入,从而避免了因假体置入深度不够导致的双下肢不等长。研究显示,短柄较长柄能更好地恢复双下肢长度[12],而双下肢等长的患者更是能在关节置换术后较早的进行运动[13,14],有效提高了生活质量。由于Tri-Lock BPS扁平化趋势明显,置入后股骨前后方空间较Corail股骨柄置入后的空间大,当出现股骨发育性前倾角增大的时候,术中可以通过柄的适当旋转,灵活调整前倾角的位置。
Tri-Lock BPS也有一定的缺点:其新型的Gription微孔涂层较Corail股骨柄的生物活性涂层增加了36%的摩擦系数,仅需覆盖股骨柄近端63%的表面即可获得与全涂层股骨柄相同的固定效果[15]。微孔涂层结构方便周围骨生长进而增加股骨柄的长期稳定性,但因涂层摩擦系数较大,置入时术者对于股骨柄的初始稳定性判断有时会产生偏差;特别在年轻且骨质较好的DDH患者关节置换时,术中测试股骨柄稳定后再透视,会发现整体压配率欠佳即股骨柄-骨皮质间存在明显间隙,为了提高压配率需再次击打或更换加大一号的股骨柄,相对增加了手术时间。
本研究尚存在以下局限性:总体样本较少,部分患者随访时间不足,无法观察假体中远期的稳定性;同时,观察期内本组尚无一例需要翻修,保留的骨量是否会发生流失尚无法判断。目前的临床观察结果显示,THA中采用Tri-Lock BPS与经典Corail股骨柄假体在相同入路(后外侧入路)下治疗DDH的效果相当,但Tri-Lock BPS同时具备更多的初始有效骨量保留、灵活调整股骨前倾角等优点,相对减少术后并发症的发生,因此临床应用价值较高。
所有作者均声明不存在利益冲突



























