
在人口老龄化的背景下,神经系统变性疾病呈逐年上升趋势,神经系统变性疾病生物样本与数据库建设对疾病研究及转化应用至关重要。由于目前国内在此领域尚未建立统一共识,中国研究型医院学会临床数据与样本资源库专业委员会联合金域医学及全国部分三级甲等医院神经病学科与生物样本库领域专家,制订本专家共识,旨在推动神经系统变性疾病高质量生物样本与数据库建设,促进我国神经病学的研究与转化医学的发展。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
在社会老龄化加重、人口平均寿命延长的背景下,神经变性疾病患者呈上升趋势,将占用大量医疗护理资源,对我国医疗卫生体系构成显著挑战。据WHO预测,到2040年,神经变性疾病将取代癌症成为人类第二大致死疾病。目前,全球有超过5 000万人受痴呆症(dementia)影响,这一数值到2050年可能上升至1.3亿,且尚无有效药物[1]。以帕金森病(Parkinson disease,PD)为例,我国>65岁人群中患病率约1.7%。目前,全国至少有200万例PD患者;预计到2030年,我国的患者约占世界患者的57.0%[2]。随着老龄化的加剧,神经系统变性疾病患者总数将持续增加,对我国公共卫生健康构成严重威胁。本共识将统一神经系统变性疾病相关样本与信息采集标准,以提高样本质量、实现神经系统疾病生物样本资源共享以及联合研究。这对神经系统变性疾病研究中,严格遵照相关标准规范操作、提高其临床和科研水平、加强临床疑难疾病的一线诊治、推动其基础研究与临床转化具有重要意义。本共识中规定了神经系统变性疾病生物样本和数据库建设要求,包括基于神经系统变性疾病的科研项目立项、伦理与知情同意、患者入组与排除标准以及脑脊液(cerebrospinal fluid,CSF)、脑组织、皮肤、血液、尿液等生物样本与数据采集、处理、存储与质量控制等内容。本共识适用于开展神经系统变性疾病基础和临床研究的机构,以及基于神经系统变性疾病研究的生物样本库。
下列术语和定义适用于本共识。(1)腰椎穿刺(lumbar puncture):从腰椎L3~L5间隙推进腰椎穿刺针,穿透进入蛛网膜下腔,提取CSF的过程。(2)CSF:一种存在于脑室以及蛛网膜下腔内的无色透明液体,主要由双侧侧脑室脉络丛分泌,经室间孔入第三、四脑室,通过第四脑室的中间孔与侧孔分布于脑和脊髓表面的蛛网膜下腔和脑池,大部分经脑穹窿面的蛛网膜颗粒吸收至静脉窦,进入血液循环。(3)采集(collection):直接获取所需要的人类生物样本及其相关数据的过程。(4)无菌技术(aseptic technology):在实验室,用于防止细胞、试剂、物料、人员受到微生物感染的操作。(5)生物样本信息(biological specimen information):生物样本的附属信息,包括但不限于研究数据、表型数据、临床数据、流行病学数据和生物样本处理过程相关数据等。
基于神经系统变性疾病的科研立项应经申报申请、科学审查、伦理审查。审查批准之后才能确定该科研项目获得立项。科研项目负责人应向本单位或上级单位的科学技术管理部门和伦理审查机构提交立项书与生物样本入库申请书。申请书内容包括但不限于以下内容:(1)研究目的、意义和创新性、预期研究目标;(2)研究方案、技术路线、拟解决的关键科学问题等;(3)项目负责人及团队信息;(4)神经系统变性疾病患者入组和排除标准;(5)研究的样本量和统计学数据。
科学委员会对项目申请进行科学技术审查,提出学术意见和建议,作出学术评估,保障项目研究方案的科学性。伦理审查委员会遵照GB/T 38736[3],进行伦理审查并签发书面意见。所有会议及其决议均应有书面记录并归档。
项目负责人应向生物样本库管理者提交相关样本入库申请书。申请书包括但不限于以下信息与资料:(1)项目基本信息(立项申请书副本及立项批复);(2)伦理审查委员会批复(副本);(3)伦理审查委员会批准的知情同意书版本;(4)预期样本规模及计算依据;(5)拟入库样本信息,包括但不限于入库病种、病例数(例/年)、样本类型、样本量(份/年)、预计每年使用量(份/年);(6)样本操作规程,包括样本采集、处理、保存与质量控制;(7)拟采集的信息(最小数据集);(8)随机抽查样本进行质控检测的频次。
相关生物样本与信息收集需获得供者的知情同意。对于未成年人、无民事行为能力及遗体供者,应获得其法定代理人或监护人的知情同意。在法定代理人或监护人知情同意的情况下,如未获得供者的知情同意,不得收集生物样本与信息。在样本与信息收集前应确保供者充分知情、理解相关风险和权益,全面和准确地认识相关告知内容。签署的《知情同意书》一式3份,分别由供者、采集机构和生物样本库三方保存或备份保存。
应根据立项范围确定和选择样本库重点收集的病种样本。常见的神经系统变性疾病包括但不限于阿尔茨海默病(Alzheimer disease,AD)、PD、额颞叶变性(frontotemporal lobar degeneration,FTLD)、路易体痴呆(dementia with Lewy body,DLB)、肌萎缩侧索硬化症(amyotrophic lateral sclerosis,ALS)、多系统萎缩(multiple system atrophy,MSA)、进行性核上性麻痹(progressive supranuclear palsy,PSP)。疾病分类和编码应遵照《国际疾病分类》第11版(ICD-11)[4]的规定;诊断应符合国内外认可的共识。基于神经系统变性疾病连续进展的特点,宜采用分层操作将入组标准进行相应扩展,建立涵盖疾病临床前期的队列。如对AD的研究,宜包括临床前期、临床早期(mild cognitive impairment,MCI)和临床晚期(痴呆)各个病程阶段的患者,并进行纵向随访。
1. AD:诊断标准参考美国国家衰老研究所(National Institute of Aging,NIA)和阿尔茨海默病学会(Alzheimer Association,AA)于2011年4月19日发表的NIA-AA诊断标准[5]。符合痴呆诊断标准,并且具有以下特点者:(1)隐匿起病,症状缓慢进展,长达数月乃至数年,并非发生于数小时或数天之内。(2)具有明确的认知功能恶化史,并且在询问病史和体检中发现的早期和最显著的认知损害有以下表现。①遗忘表现:为AD最常见症状,即学习和回忆新近习得知识的功能受损,以及至少一项其他认知功能(如语言、视空间、执行、计算和理解判断等方面)缺损的证据。②非遗忘表现:一是语言障碍,最突出的缺损是找词困难,同时还应存在其他认知功能缺损;二是视空间障碍,最突出的缺损是空间认知受损,包括:物体失认、面容识别损害、动作失认、失读,同时还表现其他认知区域的缺损;三是执行功能障碍,最突出的缺损是推理、判断以及解决问题的能力受损,同时还表现其他认知区域的缺损。有以上3项中≥1项的表现。(3)需排除其他原因引起的痴呆。(4)影像及实验室检查结果异常,包括:①与年龄匹配的正常人群相比,定性和定量MRI分析显示双侧颞叶、海马萎缩。②CSF和血液标志物异常,如淀粉样蛋白(Aβ)42含量降低,Aβ42/Aβ40比值下降、总tau和(或)过磷酸化tau升高等。③PET等分子神经影像检查提示特定脑区代谢异常,如双侧颞顶皮质糖代谢下降,额叶、颞叶、顶叶、后扣带回及纹状体Aβ滞留增加。④家族性AD致病基因突变,位于21号染色体的淀粉样前体蛋白(amyloid precursor protein,APP)基因、14号染色体的早老素-1(presenilin1,PSEN-1)基因以及1号染色体的PSEN2基因异常。排除标准:(1)伴发严重的脑血管疾病,定义为卒中病史与认知缺损的发生或恶化有短暂的关联,或出现多发,或严重脑梗死,或重度脑白质病变。(2)具有DLB核心特征。(3)具有行为变异的额颞叶痴呆的显著特征。(4)具有原发性进行性语义型失语,或原发性进行性非流利性,或显著的语法错乱型失语特征。(5)有其他活动性神经疾病并发症,或非神经系统疾病表现并发症,或具有药物性严重认知障碍的证据。
2. PD:PD的诊断分为临床确诊PD、临床很可能PD。入组与排除标准详见《中国帕金森病的诊断标准(2016版)》[6]。
3. FTLD:根据临床特征,目前国际上将FTLD分为3种主要的临床亚型,包括行为变异型额颞叶痴呆、语义性痴呆和进行性非流利性失语。入组与排除标准详见《额颞叶变性专家共识》[7]。
4. DLB:根据DLB的核心临床特征和提示性生物标志物,DLB的诊断分为很可能的DLB、可能的DLB。入组与排除标准详见《中国路易体痴呆诊断与治疗指南》[8]。
5. ALS:临床类型包括经典类型,如ALS、进行性肌萎缩、进行性延髓麻痹,以及连枷臂综合征、连枷腿综合征、ALS伴额颞叶痴呆。入组与排除标准详见《肌萎缩侧索硬化诊断和治疗中国专家共识2022》[9]。
6. MSA:目前临床上将MSA分为以帕金森症状为突出表现的MSA-P亚型和以小脑性共济失调症状为突出表现的MSA-C亚型,入组与排除标准详见《多系统萎缩诊断标准中国专家共识》[10]。
7. PSP:诊断分为确诊PSP、很可能PSP、可能PSP以及提示PSP,入组与排除标准详见国际运动障碍学会(International Parkinson and Movement Disorder Society,MDS)PSP协作组2017年发表更新的PSP诊断标准[11]和《进行性核上性麻痹的诊断新认识》[12]。
神经系统变性疾病的样本应遵循GB/T 40352.1-2021[13]、ISO/TS 20658-2017[14]、GB/T 39767-2021[15]、GB/T 37864-2019[16]进行采集与处理。采集样本主要为CSF、脑组织、血液、尿液、肌肉活检组织等。采集CSF时,应同时配对采集血液样本(血清和血浆),血浆抗凝剂选择乙二胺四乙酸(EDTA)类。样本采集时间应根据研究计划要求制定,如:手术前后、治疗前后、不同疾病阶段等;根据研究目的及神经系统变性疾病的靶标种类的不同,确定经验证的采集与处理方法。
1. CSF采集要求:(1)应由具有采集资质的临床医师执行无菌采集。(2)采集前应对供者适当地解释与安抚,以消除疑虑和恐惧。检查供者有无颅内压增高症状和体征、做眼底检查排除CSF采集禁忌者,告知供者腰椎穿刺的风险及相关注意事项。(3)采集量应标准化并在文件中规定,采集量应≥12 ml。最初采集的1~2 ml CSF可用于常规分析,后续采集的置于聚丙烯材质(polypropylene,PP)管中处理后保存。(4)正常采集的CSF为无色、清澈、透明、不凝结的液体,如有肉眼可见的血液污染,不作为样本库保存的样本,污染的红细胞数量>500个/μl为CSF不保存的标准。CSF采集后需在2 h内处理保存。
2. CSF处理要求:(1)CSF处理应由培训合格的生物样本库技术人员执行。(2)脑脊液经分离、分装,上清与沉淀分开保存。分装应在生物无菌柜中进行,避免交叉污染。(3)冻存管应配唯一代码(2D)的标签(耐低温标签)以便于检索。标识内容不含可识别的身份信息,有助于盲分析及供者隐私保护。(4)CSF转运应遵循ISO/TS 20658-2017[14],放于干冰中运输。干冰量应能确保样本保持在适当的温度≥3 d。CSF最好在周一开始运输,以便样本在同一周内到达目的地。
3. CSF采集与处理标准操作规程:(1)查看知情同意书,并确认已签署、不存在采集禁忌证。(2)核对供者姓名、病历号等以确认与知情同意书上的供者身份信息保持一致。(3)准备腰穿包、穿戴个人防护装备,至少两层手套,并强烈建议在一次性手套下佩戴耐切割手套。(4)标记注射器,并根据供者体型选择合适的腰椎穿刺针。建议肥胖者使用长度>90 mm的穿刺针、一般体型者使用长度<90 mm的穿刺针,标准型号为21~23 G的非创伤性针头。(5)选择合适的穿刺部位。具体:①活体供者,建议于腰椎L3~L5间隙进行穿刺采集;行脑室引流的患者直接从脑室外引流管的接入口获取CSF。②尸体供者,通常在尸检过程中收集CSF。对于需要进行完整尸检的供者,或在局部解剖中枢神经系统的情况下[有或没有附加器官系统和(或)体腔限制],在移除颅骨后直接从侧脑室获取。将穿刺针插入大脑半球背侧的副矢状面(正中线正外侧)至合适的深度,至可见柱塞缩回液体流出。CSF采集应在病理学家详细检查大脑并记录其特征和所有异常后进行。若尸检不对颅内内容物进行评估(如颅骨和颅底、硬脑膜、软脑膜、脑、垂体、颅神经),仍可以通过腰椎穿刺收集CSF。尸体腰椎穿刺的位置可不必局限于脊髓的腰部区域。(6)最初采集的1~2 ml CSF用于常规分析评估,后续收集CSF样本置于PP管中留存。(7)采集容器应为旋盖无菌的PP材质离心管。CSF应采集多管,分别满足常规生化、微生物、细胞学检测及生物样本库的前瞻性保藏;(8)采集结束后应彻底清洁工作站、冲洗使用过的手术器械,并进行手消毒。一次性手术刀片必须放在指定的锋利物容器内,所有个人防护设备脱下后按医疗废弃物进行统一处置。(9)采集的CSF应按照不同要求于室温或低温进行转运。(10)采集的CSF应即时离心(离心力2 000×g,室温10 min);若离心有红色沉淀不保存该样本,如需要保存细胞(离心力400×g,室温离心10 min)。(11)使用校准过的移液管将CSF等量分装到PP存储管中。建议每根冻存管以0.2、0.5或1.0 ml量分装,最小分装量为0.1 ml(尽量保证多复份分装,如10.0 ml CSF样本,0.5 ml/管,可分装20管)。CSF量应达冻存管总容量的75%,以防止冷冻干燥。(12)样本置于-80 ℃环境长期保存。建议将样本分放于2个或多个不同设备中存储,并记录样本冻融次数。冻融次数应<3次。(13)按液体样本的标准分析前变量编码(standard PRE-analytical code,SPREC)(如采集时间、采集量、采集部位、主要添加剂、离心前延迟时间、离心次数、离心速度与时间、存储容器、长期存储时间等)要求完善记录,并录入样本数据库系统定期备份。
1. 脑组织采集总要求:脑组织来源于神经系统变性疾病患者或正常人(对照)的遗体捐赠。对于捐献遗体,应确认供者死亡时间、原因,记录死亡前(濒死)表现,评价危险因素(是否有感染性疾病等)。取材地点可在医院病理解剖室或遗体志愿捐献接收站专用解剖室。如不能及时采集,应将遗体低温保存。取材人员应记录供者信息、固体样本SPREC及取材过程。
2.脑组织处理总要求:脑组织处理常规行大脑半脑固定。优势半脑取新鲜组织速冻,确定新鲜半脑取材的内容(表1),特殊情况下左右脑轮流固定与冻存。以下情形需双侧脑全部固定:(1)供体死亡时间>24 h;(2)两侧大脑半球可能受疾病影响不同,需要双侧脑组织病理诊断者;(3)有HIV、克雅病、活动性耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus,MRSA)感染等患者。
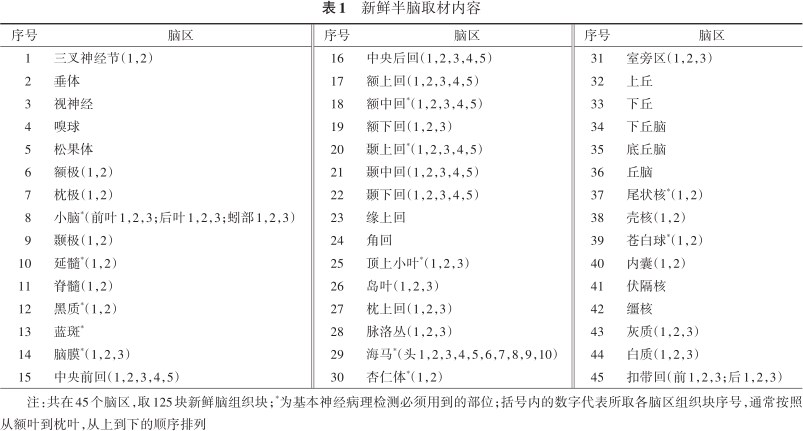
新鲜半脑取材内容
新鲜半脑取材内容
| 序号 | 脑区 | 序号 | 脑区 | 序号 | 脑区 |
|---|---|---|---|---|---|
| 1 | 三叉神经节(1,2) | 16 | 中央后回(1,2,3,4,5) | 31 | 室旁区(1,2,3) |
| 2 | 垂体 | 17 | 额上回(1,2,3,4,5) | 32 | 上丘 |
| 3 | 视神经 | 18 | 额中回*(1,2,3,4,5) | 33 | 下丘 |
| 4 | 嗅球 | 19 | 额下回(1,2,3) | 34 | 下丘脑 |
| 5 | 松果体 | 20 | 颞上回*(1,2,3,4,5) | 35 | 底丘脑 |
| 6 | 额极(1,2) | 21 | 颞中回(1,2,3,4,5) | 36 | 丘脑 |
| 7 | 枕极(1,2) | 22 | 颞下回(1,2,3,4,5) | 37 | 尾状核*(1,2) |
| 8 | 小脑*(前叶1,2,3;后叶1,2,3;蚓部1,2,3) | 23 | 缘上回 | 38 | 壳核(1,2) |
| 9 | 颞极(1,2) | 24 | 角回 | 39 | 苍白球*(1,2) |
| 10 | 延髓*(1,2) | 25 | 顶上小叶*(1,2,3) | 40 | 内囊(1,2) |
| 11 | 脊髓(1,2) | 26 | 岛叶(1,2,3) | 41 | 伏隔核 |
| 12 | 黑质*(1,2) | 27 | 枕上回(1,2,3) | 42 | 缰核 |
| 13 | 蓝斑* | 28 | 脉洛丛(1,2,3) | 43 | 灰质(1,2,3) |
| 14 | 脑膜*(1,2,3) | 29 | 海马*(头1,2,3,4,5,6,7,8,9,10) | 44 | 白质(1,2,3) |
| 15 | 中央前回(1,2,3,4,5) | 30 | 杏仁体*(1,2) | 45 | 扣带回(前1,2,3;后1,2,3) |
注:共在45个脑区,取125块新鲜脑组织块;*为基本神经病理检测必须用到的部位;括号内的数字代表所取各脑区组织块序号,通常按照从额叶到枕叶,从上到下的顺序排列
3.脑组织采集与处理标准操作规程如下:(1)查看知情同意书,确认已签署并了解是否存在采集上的限制。(2)核对供者姓名、病历号等以确认与知情同意书上的供者身份信息一致。(3)准备取材医疗器械以及摄像机。(4)判断是否有颅脑外伤。如有大范围损伤,应放弃取脑。(5)沿耳后至颅顶,冠状切开头皮、翻折、暴露颅骨。(6)开颅,沿眉弓到枕外隆突环行线上约1 cm锯开颅骨,避免切口过深损伤脑组织。(7)用解剖刀小心剥离硬脑膜,离断脑与颅骨联系。(8)完整取出大脑、小脑、脑干以及相连的部分颈髓;然后沿大脑、小脑、脑干中线矢状切开,将整个脑等分为两部分,一部分置入6%甲醛溶液固定、另一部分冷冻处理。(9)脑组织冷冻处理步骤:①将冷冻的新鲜半脑称重,测量并拍照。②沿上丘脑水平或乳头体后方去除中脑及相连接的脑干、小脑部分,沿小脑脚分离脑干、小脑。③按照表1中取材内容和部位分别顺序取材。④完成取材后按次序排列摄片,并将组织速冻后装入标记好的自封袋,放入冻存盒,-80 ℃环境保存。(10)脑组织固定处理步骤:①置入6%甲醛溶液的半脑组织固定3 d后,固定液换为4%甲醛溶液固定2周;然后取出固定好的半脑,去除所有脑膜及血管。②肉眼观察脑组织是否有萎缩、梗死、出血等病理表现,若发现明显病灶则在原有取材部位基础上,取病灶处用于神经病理检查;沿上丘水平或乳头体后方去除中脑及相连接的脑干、小脑;沿小脑脚分离脑干、小脑。③小脑半球沿矢状平行切面切片,由额叶至枕叶顺序编号,并摄片;脑干及脊髓横断面切片,按顺序编号并摄片。④肉眼观察切片组织是否有出血、梗死、损伤等病理变化。⑤按表1中取材内容分别取大脑及脑干各部位组织,脱水包埋用于病理诊断与科研;其余组织继续于4% NBF固定液中保存。固定液每2年更换一次。
应遵循WS/T 225[21]和GB/T 38576-2020[22]要求采集处理血液样本,分离获得血清、血浆、血细胞、血凝块,抗凝剂优先选择EDTA。血液经分离(离心力2 000×g、室温10 min)、分装(生物无菌柜环境)于冻存管,保存于-80 ℃超低温冰箱。血液样本应在24 h内完成处理和贮存,建议最佳在2 h内完成。因特殊情况延迟处理时,应在2~8 ℃环境冷藏并记录SPREC。
遵循GB/T 38735-2020[23]要求采集供者的中段尿。采集后的尿液样本,经分离(离心力400×g、室温5 min),分装上清、尿沉渣,保存于-80 ℃超低温冰箱。
1.皮肤组织采集:应准备好采集皮肤组织的医疗器械、容器。适当解释安抚供者,告知皮肤活检的目的、部位及方式,有遗留瘢痕、疼痛等风险。如多点取材或样本需分割多块,则应对样本编号进行记录,必要时可画图标记。皮肤组织采集的标准操作规程如下:(1)准备取材医疗器械(带有盖子的立式托盘、乙醇垫、局部麻醉剂、手套、镊子、短剪刀、缝合材料、纱布、针头、打孔器)和盛装组织的容器。容器包括含40%甲醛溶液的样本瓶、无菌杯(含生理盐水预湿的无菌纱布)。(2)充分暴露拟作活检部位皮肤、常规乙醇消毒,左手固定皮肤,右手用取皮器在取材部位一边旋转,一边向下用力,钻到适当深度时(达到皮下组织)取出。(3)用带齿小镊子夹起样本边缘,将样本提起,用小剪刀将样本从底部剪断。(4)压迫创口止血,常规消毒,必要时缝合伤口。
2.皮肤组织处理:应根据研究目的及样本用途对采集后的皮肤组织进行相应处理,如加入相应的保存介质、选取相应的保存方法,以维持组织细胞的活性、核酸的完整性和基因表达的稳定性等。具体处理方式包括(1)石蜡组织:应立即将采集的皮肤组织放入盛有体积是样本10倍以上固定液的容器进行固定,经脱水、透明、包埋制成组织蜡块于室温保存。(2)冰冻组织:采集的皮肤组织(直径约3 mm的圆柱形皮肤样本),立即放入Zamboni液或过碘酸盐-赖氨酸-多聚甲醛(PLP)固定液,4 ℃固定16~24 h;然后于低温防护液中过夜并且置于液氮保存,以备后续进行冰冻切片。(3)新鲜冷冻组织:应立即将采集的皮肤组织置于冻存管放液氮中速冻,转运至样本库,置于气相液氮罐长期保存。(4)细胞分离与培养:将采集的皮肤组织放入组织保养液中,以确保组织具有高细胞活性和基因信息的完整,同时不改变组织细胞基因的表达及后续的培养与扩增等。
1.肌肉组织采集总要求:肌肉采集部位的选择通常取决于病程阶段,同时兼顾取材方便、安全的原则。常用的肌肉取材部位包括肱二头肌、三角肌、腓肠肌、胫骨前肌、股外侧肌、股四头肌等,其中最常选取的是肱二头肌。这主要是由于肱二头肌取材方便、安全,并且肌纤维类型比较均衡[慢肌纤维(Ⅰ)∶快肌纤维(Ⅱa)∶Ⅱx≈1∶1∶1]。
2.肌肉组织采集与处理标准操作规程:(1)选定活检部位后进行常规消毒,铺洞巾。(2)采用2%利多卡因5 ml进行局部麻醉。(3)切口长度为2.0~3.0 cm,脂肪层厚的供者切口适当延长,钝性分离皮下组织至深筋膜,切开、分离并充分暴露肌肉组织,确定没有大血管、神经进入肌束。(4)用弯止血钳轻柔挑取肌束,取直径0.5 cm,长1.0~1.5 cm的肌束(避免肌肉过度牵拉)。用粗线结扎肌束一端,先剪断另一端,提起结扎线,再剪断结扎的一端,用生理盐水浸透的纱布轻轻包起。(5)纱布压迫止血,分层缝合深筋膜和皮肤,用无菌纱布及弹力绷带加压包扎以防止术野渗血;但要在3 h后放松绷带,避免包扎部位远端肿胀。(6)用生理盐水纱布包裹肌肉组织置于冰盒内干冰保存,并迅速送至样本库进行处理,防止酶活性降低、DNA消耗和RNA降解。(7)采用异戊烷速冻法冻存肌肉。将新鲜肌肉样本用黄蓟胶固定在直径1.5 cm、厚0.5 cm的圆形软木块上;将盛有20 ml异戊烷的小烧杯置于液氮内,并用玻璃棒不停地搅拌异戊烷,待烧杯底部出现白色结晶时,将准备好的样本投入异戊烷中,并不停搅拌10~20 s即可。(8)肌肉放置在预先以液氮冷却至-160 ℃的异戊烷溶液中快速冻存。
1. DNA:组织进行DNA提取时,应控制组织的体积约0.5 cm×0.5 cm×0.5 cm。对于新鲜的手术组织样本,用流水及预冷生理盐水快速将其表面和腔面的血液、黏液以及污物冲洗干净;血液及细胞样本进行DNA提取时按试剂盒说明书的方法操作。按照流程提取的DNA,置PP冻存管中并完善标识,置于-80 ℃或气相液氮中长期保存。
2. RNA:进行RNA提取的组织厚度应<0.5 cm。手术切除的样本组织应尽快浸入装有RNA later溶液的冻存管中,置于4 ℃的冰箱过夜。盛组织样本的容器中,RNA later溶液量至少是组织块体积的5~10倍,可使组织完全浸没于RNA later液内。RNA later使用根据试剂说明书的方法进行。血液及细胞样本进行RNA提取时按试剂盒说明书的方法操作。按照流程提取的RNA,置于PP冻存管、并配以完整标识,置于-80 ℃环境或气相液氮中长期保存。
样本的存储应遵循GB/T 37864-2019中7.7、GB/T 39766-2021[25]进行神经系统变性疾病样本的存储管理。(1)不同样本(CSF、血液、皮肤、肌肉、脑组织)的保存温度,应满足相应的标准,选择合适的容器和存储设备。(2)存储容器必须稳定,应能承受骤然降温至超低温,在低温下可以密封并长时间存储。(3)来自同一样本的多个备份样本应尽量存储在不同的设备中,有条件的可以异地分散存储,以备其中某个设备出现问题时备用。(4)存储地点和流程的设计应保证将污染风险降至最低,并确保生物样本的内在完整性。样本存储的设备,存储样本的每一级货架或容器都应该有唯一的编号,确保样本存储位置的唯一性和可追溯性。以上信息应与样本信息库系统实时关联,实时反映每个样本的存储位置和出入库信息。(5)应该对存储环境进行实时监控。专用冷链监控系统应24 h实时监控存储环境温度,并在超出预设温度范围时发出声光警报和远程报警信息。(6)应定期核实库存,保证至少每年一次。
样本库应利用信息管理系统管理神经系统变性疾病相关信息与数据,遵循GB/T 39725-2020[26]原则进行数据采集、处理与存储管理,确保数据的保密性、完整性和可用性以及数据使用和披露过程的合法性和合规性。应建立标准的神经系统变性疾病样本相关数据的传输和接收程序,并按照标准实施。数据传输应确保其完整性并防止受侵犯或隐私泄露,传输前应针对数据的采集和接收与利益相关方达成协议。
应建立神经系统变性疾病最小数据集标准和信息收集标准模板。神经系统变性疾病相关信息与数据的获取可通过多系统间的端口对接与关联自动获取,如样本库信息管理系统与医院信息系统和实验室信息系统(laboratory information management system,LIS)等信息系统实施链接后自动采集。临床数据收集时间为血液或CSF等样本采集前后6个月内。神经系统变性疾病数据库应收集包括样本源(供者)、生物样本、实验分析及随访等相关数据与信息。
1.样本源(供者)相关数据与信息:应包括但不仅限于(1)基本人口统计数据:包括供者姓名、出生日期、性别、民族、身份识别号、教育背景、籍贯、健康状况、常住地、联系方式等。(2)体检信息:如血压、身高、体质量和体质量指数(body mass index,BMI)等。(3)临床病史信息:如遗传信息、既往病史、常见共病疾病(心血管、脑血管、神经、内分泌、躯体和精神疾病)、用药史、吸烟习惯和酒精摄入等。(4)用药情况:应详细记录常用药物、用法和持续时间等,特别是对生物标志物的表达有影响的药物,最好在收集CSF前至少一年开始。(5)临床症状与关键体征:一般认知、记忆、语言流利性、视觉空间结构、注意力和执行功能领域的神经心理测试量表等结果。神经心理学测验评估包括简易精神状态量表(mini-mental state examination,MMSE)、蒙特利尔认知评估量表(montreal cognitive assessment,MoCA)、临床痴呆评定量表(clinical dementia rating,CDR)和全面衰退量表(global deterioration scale,GDS)等。应收集可能影响CSF和血液分析结果的其他相关生理变量,包括是否禁食、怀孕和潜在的非神经性疾病,如感染等。(6)诊断与治疗信息:治疗方法、疗程信息等。(7)辅助检查信息:特别是影像检查数据,MRI、正电子放射断层摄影术显像(PIB-PET)、1-{6-[(2-18F-氟乙基)-甲氨基]-2-萘基}-亚乙基丙二氰PET脑显像(18F-FDDNP)、单光子发射计算机断层成像(SPECT)等。
2.生物样本相关信息与数据:包括但不限于(1)项目基本信息:伦理委员会的批件与所有供者签署的知情同意书。(2)样本采集与处理信息:如样本收集和处理程序,样本分析前变量。(3)样本存储与管理:为了便于跟踪和快速重新定位样本,存储信息应包括样本标识信息(唯一ID)、冰箱位置、冰箱标识和样本位置。数据库应包括样本存储过程的监控数据(存储时间、存储温度、冷链与环境监测数据、冻融循环次数等)。(4)样本包装、转运、销毁信息与数据质量控制:按GB/T39766-2021[25]规定要求实施。在样本装运前,样本库管理者应与样本使用方签署材料转移协议信息。
3.实验室检测与分析数据信息:包括但不限于(1)应收集CSF常规检测数据(细胞计数,糖、氯化物、蛋白质含量等)以及各类样本生物标志物检测数据。如体液指标的检测主要包括CSF、血液及尿液中相关指标的检测(表2)。(2)应用脑组织进行免疫组织化学、荧光染色以及Western blot等方法所获得的信息。(3)脑组织的遗传信息(如RNA、DNA测序等)以及蛋白组学信息。
| 疾病名称 | 脑脊液 | 血液 | 尿液 |
|---|---|---|---|
| 阿尔茨海默病 | Aβ42、Aβ40、T-tau、P-tau181,以及Aβ42/Aβ40、Aβ42/T-tau、Aβ42/P-tau、NFL、P-tau181/Aβ42的比值 | miRNA(miR-34a、miR-81b和let-7f)、Aβ蛋白、炎症标志物(TNF-1、TNF-α、IL-1β、IFN-γ和TGF-β)、氧化应激生物标志物(游离脂肪酸、蛋白质硝化产物、DNA氧化产物、脂质过氧化产物、HNE和晚期糖基化终产物)、致病基因APP、PSEN1或PSEN2;易感基因APOEε4等位基因 | AD7c-NTP |
| 帕金森病 | P-tau/T-tau、P-tau/Aβ42、Aβ42/T-tau比值,及α-syn、NfL/Aβ42、FABP3、GCase、高香草酸、PARK7、多巴胺及其代谢产物 | α-syn、T-tau、儿茶酚胺、BDNF、IGF-1 | KYN、VGF、ENPEP |
| 肌萎缩侧索硬化 | BDNF、GDNF、pNFH、NFL、DPRs、MCP-1、SOD、TDP-43 | 血清磷酸肌酸激酶、乙酰胆碱酯酶、BDNF、GDNF、血清肌酐;血清肌酐/胱抑素C比值、IL-8、MCP-1、血清尿酸、SOD、TNF-α | p75ECD、8-羟基-2'- 脱氧鸟苷(8-OH-2,- dG) |
| 额颞叶痴呆 | tau蛋白、TDP-43、NFL | tau蛋白、TDP-43、NFL | AD7c-NTP |
| 多系统萎缩 | α-syn、NFL、T-tau | α-syn、NFL | 尿酸 |
| 进行性核上性麻痹 | NFL | NFL |
注:Aβ为β样淀粉蛋白,T-tau为总tau蛋白,P-tau181为Tau磷酸化181蛋白,NFL为神经丝蛋白轻链,TNF为肿瘤坏死因子,IL-1β为白细胞介素1β,IFN-γ为干扰素-γ,TGF-β为转化生长因子-β,HNE为4-羟基2反式壬烯醛,PSEN为早老素,APOE为载脂蛋白E,AD7c-NTP为阿尔茨海默相关神经丝蛋白,NfL为神经丝轻链,α-syn为α-突触核蛋白,FABP3为重组人脂肪酸结合蛋白-3,GCase为GBA编码的葡糖脑苷脂酶,PARK7为DJ1蛋白,BDNF为脑源性神经营养因子,IGF-1为胰岛素样生长因子-1,KYN为犬尿氨酸,VGF为神经生长因子,ENPEP为谷氨酰氨基肽酶,GDNF为胶质细胞源性神经营养因子,pNFH为磷酸化神经丝蛋白重链,DPRs为二肽重复蛋白,MCP-1为单核细胞趋化蛋白-1,SOD为超氧化物歧化酶,TDP-43为反式激活应答DNA结合蛋白43,p75ECD为神经营养素受体,8-OH-2,-dG为8-羟基-2'-脱氧鸟苷
4.随访信息:应建立随访机制,在项目研究过程中、结束后,分别在不同时间段(1、2、5年)对活体供者临床结局(致残、死亡)、用药情况以及卫生经济学信息进行随访调查,并将随访数据纳入数据库管理。
应根据数据与信息类型、数据对象(基因组、转录组、表观组等)、数据类别(生物测序和生物信息分析数据)进行分类处理。对于采集的生物信息数据,如DNA、RNA处理过程应包括核酸序列数据格式转换和生物基因信息原始数据分析。不同的数据类型应采用不同的分析流程和分析软件。
应合理规划数据与信息的存储方式、数据的承载容量与存储地点(主系统、专用服务器或云平台)。信息与数据应≥2个副本,且存储在不同位置。神经系统变性疾病数据库应定期备份,必要时采用多种介质实行异地备份存储、专人管理。存储数据时,应建立数据间的逻辑与物理对应关系以确保数据的可追溯性。应妥善保管数据专用存储介质,保证存储物理环境的稳定性。设定数据访问权限,避免对备份数据的非授权访问。应遵循GBT37864-2019[16]文件规定的数据获得、内部或外部转移程序实施。数据的弃用应遵循书面协议或文件(如合同、书面或签署的承诺、有约束力的网络接收条款和条件)。所有存储事件均应记录在存储日志表中。数据存储日志应包含数据类别、数据存放介质、数据时效性、数据完整性、数据更新情况和数据管理人员等。生物样本库应确保将识别出的问题清晰记录并传达给接收者或用户。在生物样本及相关数据分发过程中,如发现生物样本及相关数据存在问题,应书面告知接收方或用户,并由其决定是否接收。
生物样本与数据的质量控制遵循ISO 20387中7.8要求,每批次样本处理过程均应执行质量控制程序;应保留质量控制活动和结果的记录,以证明样本及相关数据能满足预期要求。具体:(1)应对数据进行分析和质量控制,对不能满足既定要求的不合格生物样本及相关数据进行有效标识,并采取措施控制其报告和分发范围。(2)生物样本库还应定期分析质量控制结果的趋势,作为持续改进过程的输入内容。(3)原始样本(如脑组织、CSF、血液、尿液、皮肤组织等)经过多步处理获得复杂衍生物,如DNA、RNA等。应针对影响这些衍生物质量的关键步骤,建立规范的质量控制程序,评估衍生物的重要质量特性,包括稳定性、完整性、浓度与纯度等。(4)定期进行样本外部评价和室间比对。应使用能提供客观证据的方法(适当时可获得)以证明生物样本质量(如处理或检测结果)的可比性。这些方法包括相关的外部质量评价(EQA)计划、能力验证计划及室间比对或生物样本库自行建立的方法,如生物样本库参加室间比对计划。当其未满足预定的评价准则时,应监控室间比对的相关结果并实施和记录纠正措施。
共识执笔人员(按作者贡献大小排序):周红梅(广州金域医学检验集团股份有限公司生物资源中心)、龙玲(中山大学附属第三医院神经内科)、何新月(广州金域医学检验集团股份有限公司生物资源中心)、唐闻晶(解放军总医院第一医学中心神经内科)、康晓楠(上海交通大学附属仁济医院临床生物样本库)、汤媛媛(广州金域医学检验集团股份有限公司神经疾病与衰老检测中心)
共识参与专家(按姓氏笔画排序):毛志锋(广州金域医学检验集团股份有限公司神经疾病与衰老检测中心)、仇文颖(中国医学科学院基础医学研究所国家发育和功能人脑组织资源库)、田亚平(解放军总医院医学创新研究部)、李慧源(广州金域医学检验集团股份有限公司实验室管理中心)、吴景文(同济大学附属东方医院功能神经科)、张玉虎(广东省人民医院神经内科)、陈曲波(广州中医药大学第二附属医院生物资源中心)、罗文婷(广州医科大学附属第一医院生物样本库)、赵秀梅(解放军总医院医学创新研究部)、徐群(上海交通大学医学院附属仁济医院神经内科)、韩晓燕(中山大学附属第三人民医院生物样本库)、程凯汀(广州金域医学检验集团股份有限公司神经疾病与衰老检测中心)、蔡彦宁(北京宣武医院神经生物室)
所有参与共识制订的专家之间无利益冲突



























