
探讨血硫胺素水平与极低出生体重儿喂养不耐受(feeding intolerance,FI)的相关性。
选择2018年7月至2020年7月生后2 h内入住佛山市妇幼保健院新生儿科的极低出生体重儿(1 000 g≤出生体重<1 500 g)为研究对象进行前瞻性研究,根据是否存在FI分为FI组和喂养耐受(feeding tolerance,FT)组,比较两组患儿临床资料及血硫胺素水平。
共纳入极低出生体重儿160例,FI组76例(47.5%),FT组84例(52.5%)。FI组血硫胺素水平低于FT组[(45.3±8.1)nmol/L比(57.4±7.7)nmol/L],差异有统计学意义(P<0.05)。多因素Logistic回归分析表明硫胺素水平降低、胎龄<28周、开奶延迟(>3 d)、母亲绒毛膜羊膜炎、人工喂养是极低出生体重儿发生FI的危险因素。
极低出生体重儿易发生FI,硫胺素水平降低是其发生FI的危险因素。

随着我国新生儿重症监护技术的进步,早产儿尤其是极低/超低出生体重儿存活率逐渐升高,喂养不耐受(feeding intolerance,FI)成为新生儿医学中的常见问题。FI指新生儿因胃肠功能严重紊乱而导致喂养计划中断的一组临床症状,表现为呕吐、腹胀等,多见于极低/超低出生体重儿[1]。早产儿FI发生率约为30%,极低出生体重儿FI发生率高达76%[2]。硫胺素又称维生素B1,是人体重要的生物催化剂,缺乏时会造成小肠、结肠蠕动缓慢,消化腺分泌减少[3, 4]。极低出生体重儿生后因禁食或奶量摄入不足会导致硫胺素摄入减少,肠外营养补充的葡萄糖或脂肪乳会导致硫胺素需求增加,另外部分极低出生体重儿合并感染可能会导致硫胺素水平进一步下降。本研究通过观察FI极低出生体重儿血硫胺素水平的变化,探讨血硫胺素水平与极低出生体重儿FI的相关性,为临床治疗FI提供依据。
选择2018年7月至2020年7月生后2 h内入住佛山市妇幼保健院新生儿科的极低出生体重儿(1 000 g≤出生体重<1 500 g)进行前瞻性研究,根据是否发生FI分为FI组及喂养耐受(feeding tolerance,FT)组。排除标准:(1)先天性消化道畸形;(2)遗传代谢性疾病;(3)出生时重度窒息;(4)新生儿坏死性小肠结肠炎;(5)确诊新生儿败血症;(6)严重小于胎龄儿(出生体重低于同性别同胎龄体重3个标准差);(7)住院时间<14 d;(8)住院期间死亡/放弃治疗;(9)家属不同意参加本研究。本研究通过佛山市妇幼保健院医学伦理委员会批准,患儿家长均签署知情同意书。
1.资料收集:记录患儿性别、胎龄、出生体重、身长、头围、Apgar评分;记录患儿母亲分娩方式、产前激素使用及妊娠期并发症情况,如胎膜早破>18 h、绒毛膜羊膜炎、胎盘早剥、前置胎盘、子痫前期等。
2.硫胺素水平检测:所有患儿生后10 d采动脉血1 ml,离心后取血清0.5 ml置于EP管中备用,采用高效液相色谱法检测血硫胺素水平(岛津液相色谱仪LC-20A、色谱柱C18、美国GENMED血液硫胺素高效液相色谱法定量检测试剂盒)。
3.硫胺素水平判定:目前缺乏早产儿硫胺素正常值范围标准。本研究参考黄钰君等[3]研究结果,0~3岁儿童硫胺素水平45.6~88.1 nmol/L为正常范围,低于46 nmol/L为硫胺素水平降低。
4.FI诊断标准及营养策略:所有患儿于生后10 d内判断是否发生FI。目前国际上FI尚无统一临床诊断标准,本研究采用的FI临床诊断标准如下[2,4]:①胃残留量>喂养量的50%;②呕吐≥3次/d;③胃残液或呕吐物为胆汁或咖啡样液体;④腹胀(24 h内腹围增加≥1.5 cm,有肠型),并除外经鼻持续气道正压通气引起的腹胀;⑤禁食>2次;⑥便血或大便潜血阳性,但需排除新生儿坏死性小肠结肠炎。符合以上一种情况即诊断FI。
营养支持遵循2013年《中国新生儿营养支持临床应用指南》[5]及《极低出生体重儿喂养指南》[6],经充分评估患儿病情及吸吮-吞咽-呼吸功能后选择经口喂养或经口/鼻胃管喂养,结合患儿实际情况制定个体化喂养目标及肠外营养方案。患儿生后48 h内均常规静脉补充水溶性维生素(限肠外营养期间,达全肠道喂养后停止静脉补充水溶性维生素),按照药品说明书所给剂量为0.1瓶/(kg·d)(山东罗欣药业,复方制剂),含硫胺素0.31 mg/(kg·d),稍低于2013年《中国新生儿营养支持临床应用指南》推荐的硫胺素摄入量0.35~0.5 mg/(kg·d)。
应用SPSS 20.0统计软件进行数据分析。正态分布的计量资料以±s表示,组间比较采用t检验;计数资料以例(%)表示,组间比较采用χ2检验;采用Logistic回归分析硫胺素水平与FI的相关性。P<0.05为差异有统计学意义。
研究期间共收治极低出生体重儿232例,排除家属拒绝参加研究50例、新生儿败血症10例、坏死性小肠结肠炎4例、先天性消化道畸形3例、住院期间死亡3例、遗传代谢性疾病2例,最终纳入160例,FI组76例,FT组84例。两组患儿性别、胎龄、出生体重、身长、头围、剖宫产比例比较,差异均无统计学意义(P>0.05)。见表1。
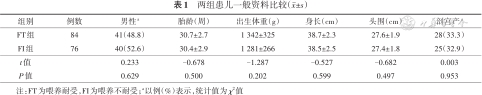
两组患儿一般资料比较(±s)
两组患儿一般资料比较(±s)
| 组别 | 例数 | 男性a | 胎龄(周) | 出生体重(g) | 身长(cm) | 头围(cm) | 剖宫产a |
|---|---|---|---|---|---|---|---|
| FT组 | 84 | 41(48.8) | 30.7±2.7 | 1 342±325 | 38.7±2.3 | 27.6±1.9 | 28(33.3) |
| FI组 | 76 | 40(52.6) | 30.4±2.9 | 1 281±266 | 38.5±2.5 | 27.4±1.8 | 25(32.9) |
| t值 | 0.233 | -0.678 | -1.287 | -0.527 | -0.682 | 0.003 | |
| P值 | 0.629 | 0.500 | 0.202 | 0.599 | 0.497 | 0.953 |
注:FT为喂养耐受,FI为喂养不耐受;a以例(%)表示,统计值为χ2值
FI组患儿生后10 d血硫胺素水平为(45.3±8.1)nmol/L,FT组为(57.4±7.7)nmol/L,两组比较差异有统计学意义(P<0.001)。
单因素分析结果显示,FI组胎龄<28周、小于胎龄儿、母亲绒毛膜羊膜炎、窒息、抗生素使用时间>7 d、开奶延迟(>3 d)、硫胺素水平降低(<46 nmol/L)比例高于FT组(P<0.001)。两组母亲产前使用激素、胎膜早破(>18 h)、机械通气(>96 h)、使用咖啡因、新生儿贫血、动脉导管未闭方面比较差异无统计学意义(P>0.05)。见表2。
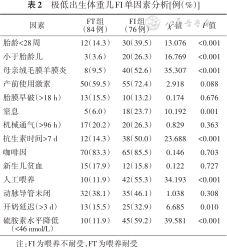
极低出生体重儿FI单因素分析[例(%)]
极低出生体重儿FI单因素分析[例(%)]
| 因素 | FT组(84例) | FI组(76例) | χ2值 | P值 |
|---|---|---|---|---|
| 胎龄<28周 | 12(14.3) | 30(39.5) | 13.076 | <0.001 |
| 小于胎龄儿 | 3(3.6) | 20(26.3) | 16.769 | <0.001 |
| 母亲绒毛膜羊膜炎 | 8(9.5) | 40(52.6) | 35.307 | <0.001 |
| 产前使用激素 | 50(59.5) | 55(72.4) | 2.918 | 0.088 |
| 胎膜早破(>18 h) | 13(15.5) | 10(13.2) | 0.174 | 0.676 |
| 窒息 | 5(6.0) | 18(23.7) | 10.192 | 0.001 |
| 机械通气(>96 h) | 17(20.2) | 20(26.3) | 0.829 | 0.363 |
| 抗生素时间>7 d | 12(14.3) | 38(50.0) | 23.688 | <0.001 |
| 咖啡因 | 70(83.3) | 65(85.5) | 0.146 | 0.703 |
| 新生儿贫血 | 15(17.9) | 12(15.8) | 0.122 | 0.727 |
| 人工喂养 | 10(11.9) | 42(55.3) | 34.193 | <0.001 |
| 动脉导管未闭 | 32(38.1) | 35(46.1) | 1.038 | 0.308 |
| 开奶延迟(>3 d) | 13(15.5) | 25(32.9) | 6.685 | 0.010 |
| 硫胺素水平降低(<46 nmol/L) | 10(11.9) | 45(59.2) | 39.581 | <0.001 |
注:FI为喂养不耐受,FT为喂养耐受
以极低出生体重儿是否发生FI为因变量,以单因素分析结果中有统计学意义的影响因素(胎龄<28周、小于胎龄儿、窒息、开奶延迟、抗生素使用时间>7 d、母亲绒毛膜羊膜炎、人工喂养、硫胺素水平降低)为自变量纳入Logistic回归模型中,结果显示胎龄<28周、人工喂养、母亲绒毛膜羊膜炎、开奶延迟(>3 d)、硫胺素水平降低是极低出生体重儿FI的危险因素。见表3。
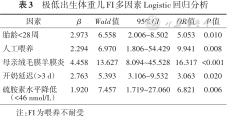
极低出生体重儿FI多因素Logistic回归分析
极低出生体重儿FI多因素Logistic回归分析
| 因素 | β | Wald值 | 95%CI | OR值 | P值 |
|---|---|---|---|---|---|
| 胎龄<28周 | 2.973 | 6.558 | 2.006~8.502 | 5.053 | 0.010 |
| 人工喂养 | 2.294 | 6.970 | 1.806~54.429 | 9.941 | 0.008 |
| 母亲绒毛膜羊膜炎 | 4.458 | 13.627 | 8.094~45.528 | 16.317 | <0.001 |
| 开奶延迟(>3 d) | 2.763 | 5.393 | 3.106~9.532 | 3.063 | 0.020 |
| 硫胺素水平降低(<46 nmol/L) | 1.920 | 7.457 | 1.719~27.060 | 6.821 | 0.006 |
注:FI为喂养不耐受
早产儿FI是指在肠内喂养后出现奶汁消化障碍,导致腹胀、呕吐、胃潴留等情况,被认为是多因素导致的常见现象,但病因尚不明确,可能与早产致肠道发育不成熟有关,也可能是坏死性小肠结肠炎或败血症等严重疾病的早期临床表现,常发生于胎龄<32周或出生体重<1 500 g的早产儿[7]。余章斌等[8]的Meta分析指出,我国早产儿FI与胎龄、氨茶碱使用、出生窒息、机械通气、宫内窘迫、出生体重、开奶时间等因素密切相关。本研究发现,胎龄<28周、开奶延迟(>3 d)、母亲绒毛膜羊膜炎、人工喂养、硫胺素水平降低是极低出生体重儿FI的危险因素。
胎儿胃肠动力发育相对迟缓,胎龄33周以后胃才逐渐发育成熟[9],小肠的移行性复合运动波到35周左右才出现[10],因此,新生儿胎龄越小,FI发生率越高。临床研究表明,生后24 h内进行早期喂养可能促进新生儿胃肠激素分泌、胃电生理活动成熟、胃肠蠕动[11];而极低出生体重儿生后因病情危重、缺氧等常开奶延迟,可能会导致胃肠道黏膜萎缩以及乳糖酶缺乏,进一步导致FI。母亲发生绒毛膜羊膜炎时释放各种炎性介质,造成胎儿多系统损伤(包括肺、皮肤、胃肠道)[12],可能会导致新生儿生后出现FI。本研究中人工喂养的极低出生体重儿FI发生率是母乳喂养儿的4.64倍,与以往研究结果一致[13],母乳易于消化,含有多种营养物质及免疫因子,是极低出生体重儿开奶的最佳选择。
硫胺素是人体重要的生物催化剂,它参与细胞的氧化活动,是体内丙酮酸氧化脱羧中的辅酶,参与糖代谢中丙酮酸的氧化脱羧反应,对于维持人体正常糖代谢及心脏、神经、消化系统的正常功能有重要作用,可促进碳水化合物代谢,修复受损神经,并能促进机体血清胃动素的有效释放[14]。硫胺素缺乏时胆碱酯酶活性增高,加速乙酰胆碱水解,导致胆碱能神经系统功能障碍,尤其影响支配胃肠道、腺体等处的神经传导,造成小肠、结肠蠕动缓慢,消化腺分泌减少。国外研究表明,硫胺素缺乏会导致恶心、呕吐、腹痛以及乳酸中毒[15]。极低出生体重儿生后因禁食或奶量摄入不足导致硫胺素摄入减少,部分极低出生体重儿合并严重感染可能会导致硫胺素水平低下,进而影响胃肠激素有效释放及胃肠道蠕动,导致FI。为消除感染因素对硫胺素水平的影响,本研究未纳入坏死性小肠结肠炎及败血症患儿,结果发现FI组极低出生体重儿血硫胺素水平明显低于FT组。
综上所述,胎龄<28周、开奶延迟(>3 d)、母亲绒毛膜羊膜炎、人工喂养、硫胺素水平降低是极低出生体重儿FI的危险因素。极低出生体重儿血硫胺素水平与FI密切相关,临床对此类患儿需密切监测血硫胺素水平,将来还需更多研究明确补充硫胺素是否会减轻FI症状。
所有作者均声明不存在利益冲突



























