
探讨新生儿胃穿孔的临床特点及死亡的危险因素。
回顾性分析2015年1月至2021年12月广东省妇幼保健院新生儿内科和新生儿外科重症监护室收治的临床确诊胃穿孔患儿,根据预后分为存活组和死亡组,比较两组患儿临床特点,采用多因素logistic回归分析死亡危险因素。
共纳入50例,男38例,女12例;早产儿34例,低出生体重儿30例;存在窒息史5例;存活组41例,死亡组9例。患儿主要表现为腹胀、呼吸急促、发绀、反应差、发热、肠鸣音减弱、腹壁潮红等,腹部X线均显示气腹,实验室检查主要表现为血白细胞升高或降低、血小板降低、C反应蛋白及降钙素原升高、血pH降低、乳酸升高。穿孔部位主要为胃大弯(30例),大于3 cm的穿孔40例,伴肠坏死14例。部分患儿存在败血症、呼吸衰竭、肺出血、休克、凝血功能障碍等相关并发症。死亡组呼吸困难、发热、降钙素原升高、pH<7.3、肠坏死、出现症状至手术时间>24 h及有败血症、肺出血、呼吸衰竭、休克、凝血功能障碍等并发症的比例均高于存活组,差异有统计学意义(P<0.05)。多因素logistic回归分析显示,pH<7.3(OR=9.755,95%CI 1.363~69.800)、出现症状至手术时间>24 h(OR=11.831,95%CI 1.305~107.301)和合并败血症(OR=29.622,95%CI 3.728~235.369)为新生儿胃穿孔死亡的危险因素。
新生儿胃穿孔以腹胀、气腹为主要表现,合并败血症、pH<7.3及出现症状至手术时间>24 h提示死亡风险增加。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
胃穿孔是新生儿期急腹症,活产新生儿发病率1∶5 000[1]。新生儿胃穿孔的发生与早产、窒息、先天发育异常、出生时应激、高压力通气复苏、远端梗阻引起的胃内压升高、医源性损伤(胃管置入)、胃解剖异常、类固醇的使用等相关[2]。其起病急,进展迅速,病情复杂,救治难度大,需多学科联合救治。有研究显示男性、代谢性酸中毒、早产、低出生体重可导致胃穿孔预后不良[3]。本研究回顾性分析本院2015—2021年收治的新生儿胃穿孔患儿临床资料,探讨导致患儿死亡的危险因素,以提高救治成功率。
选取广东省妇幼保健院2015年1月至2021年12月新生儿内科及新生儿外科重症监护室收治的临床确诊胃穿孔患儿进行回顾性研究。入选标准:发病日龄<28 d;经手术确诊新生儿胃穿孔。排除入院前诊治过程不详、病例资料不完整者。所有患儿观察到死亡或出院。根据预后分为存活组和死亡组。本研究获得广东省妇幼保健院伦理委员会批准(医伦第[202201300]号)。
通过查阅电子病历收集患儿胃穿孔相关临床表现(腹胀、呕吐、发热、呼吸困难、腹壁潮红、腹肌紧张度)、辅助检查(腹部侧位X线片、血常规、C反应蛋白、降钙素原、血气分析、乳酸)、手术方式及术中所见、病理检查、术后恢复情况等。对两组临床资料进行比较,分析死亡危险因素。
应用SPSS 26.0统计软件对数据进行分析。符合正态分布的计量资料以±s表示,两组比较采用独立样本t检验;非正态分布的计量资料以M(Q1,Q3)表示,两组比较采用非参数Wilcoxon秩和检验;计数资料以例(%)表示,两组比较采用χ2检验或Fisher精确概率法。采用logistic回归进行危险因素分析。P<0.05为差异有统计学意义。
研究期间新生儿内科及新生儿外科重症监护室共收治新生儿约3.5万例,其中诊断胃肠道穿孔265例,手术确诊胃穿孔55例,排除资料不完整5例(包括2例放弃治疗),共纳入50例。患儿发病均在生后1周内,男38例,女12例;早产儿34例(68.0%),低出生体重儿30例(60.0%);有窒息史5例。存活41例(82.0%),死亡9例(18.0%),存活组与死亡组一般资料比较差异无统计学意义(P>0.05),见表1。
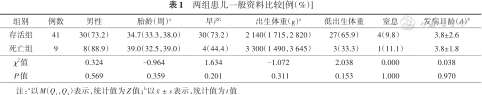
两组患儿一般资料比较[例(%)]
两组患儿一般资料比较[例(%)]
| 组别 | 例数 | 男性 | 胎龄(周)a | 早产 | 出生体重(g)a | 低出生体重 | 窒息 | 发病日龄(d)b |
|---|---|---|---|---|---|---|---|---|
| 存活组 | 41 | 30(73.2) | 34.7(33.3,38.0) | 30(73.2) | 2 140(1 715,2 820) | 27(65.9) | 4(9.8) | 3.8±2.6 |
| 死亡组 | 9 | 8(88.9) | 39.0(32.5,39.0) | 4(44.4) | 3 300(1 490,3 645) | 3(33.3) | 1(11.1) | 3.8±1.8 |
| χ2值 | 0.324 | -0.964 | 1.634 | -1.072 | 2.038 | 0.000 | 0.038 | |
| P值 | 0.569 | 0.359 | 0.201 | 0.311 | 0.153 | 1.000 | 0.970 |
注:a以M(Q1,Q3)表示,统计值为Z值;b以表示,统计值为t值
50例患儿表现为腹胀49例、精神萎靡30例、呕吐27例、呼吸困难21例、发绀18例、发热14例、肠鸣音减弱或无肠鸣音37例、腹壁潮红17例。死亡组呼吸困难、发热比例高于存活组,差异有统计学意义(P<0.05);两组其他临床表现比较,差异无统计学意义(P>0.05)。见表2。
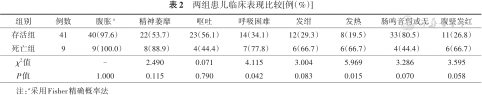
两组患儿临床表现比较[例(%)]
两组患儿临床表现比较[例(%)]
| 组别 | 例数 | 腹胀a | 精神萎靡 | 呕吐 | 呼吸困难 | 发绀 | 发热 | 肠鸣音弱或无 | 腹壁发红 |
|---|---|---|---|---|---|---|---|---|---|
| 存活组 | 41 | 40(97.6) | 22(53.7) | 23(56.1) | 14(34.1) | 12(29.3) | 8(19.5) | 33(80.5) | 11(26.8) |
| 死亡组 | 9 | 9(100.0) | 8(88.9) | 4(44.4) | 7(77.8) | 6(66.7) | 6(66.7) | 4(44.4) | 6(66.7) |
| χ2值 | - | 2.490 | 0.071 | 4.115 | 3.004 | 5.969 | 3.286 | 3.595 | |
| P值 | 1.000 | 0.115 | 0.790 | 0.042 | 0.083 | 0.015 | 0.070 | 0.058 |
注:a采用Fisher精确概率法
患儿诊断胃穿孔时白细胞异常21例,血小板减少14例,C反应蛋白升高33例,降钙素原升高17例,pH<7.3 10例,乳酸>2.5 mmol/L 33例,腹部X线片提示气腹50例。死亡组血小板减少、降钙素原升高、pH<7.3比例高于存活组,差异有统计学意义(P<0.05);两组其他检查指标差异无统计学意义(P>0.05)。见表3。
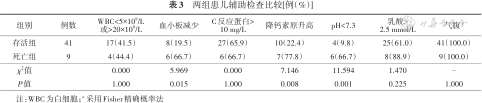
两组患儿辅助检查比较[例(%)]
两组患儿辅助检查比较[例(%)]
| 组别 | 例数 | WBC<5×109/L或>20×109/L | 血小板减少 | C反应蛋白>10 mg/L | 降钙素原升高 | pH<7.3 | 乳酸>2.5 mmol/L | 气腹a |
|---|---|---|---|---|---|---|---|---|
| 存活组 | 41 | 17(41.5) | 8(19.5) | 27(65.9) | 10(22.4) | 4(9.8) | 25(61.0) | 41(100.0) |
| 死亡组 | 9 | 4(44.4) | 6(66.7) | 6(66.7) | 7(77.8) | 6(66.7) | 8(88.9) | 9(100.0) |
| χ2值 | 0.000 | 5.969 | 0.000 | 7.146 | 11.594 | 1.470 | - | |
| P值 | 1.000 | 0.015 | 1.000 | 0.008 | 0.001 | 0.225 | 1.000 |
注:WBC为白细胞;a 采用Fisher精确概率法
两组患儿穿孔部位、穿孔大小、是否合并其他消化道畸形、腹水量>100 ml比例比较,差异无统计学意义(P>0.05);死亡组出现症状至手术时间>24 h及伴肠坏死比例高于存活组,差异有统计学意义(P<0.05)。见表4。
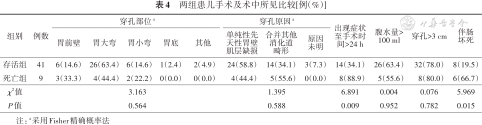
两组患儿手术及术中所见比较[例(%)]
两组患儿手术及术中所见比较[例(%)]
| 组别 | 例数 | 穿孔部位a | 穿孔原因a | 出现症状至手术时间>24 h | 腹水量>100 ml | 穿孔>3 cm | 伴肠坏死 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 胃前壁 | 胃大弯 | 胃小弯 | 胃底 | 其他 | 单纯性先天性胃壁肌层缺损 | 合并其他消化道畸形 | 原因未明 | |||||||
| 存活组 | 41 | 6(14.6) | 26(63.4) | 6(14.6) | 1(2.4) | 2(4.9) | 24(58.8) | 14(34.1) | 3(7.3) | 14(34.1) | 26(63.4) | 32(78.0) | 8(19.5) | |
| 死亡组 | 9 | 3(33.3) | 4(44.4) | 2(22.2) | 0(0.0) | 0(0.0) | 4(44.4) | 5(55.6) | 0(0.0) | 8(88.9) | 5(55.6) | 8(80.0) | 6(66.7) | |
| χ2值 | 3.163 | 1.395 | 6.891 | 0.004 | 0.076 | 5.969 | ||||||||
| P值 | 0.564 | 0.588 | 0.009 | 0.952 | 0.782 | 0.015 | ||||||||
注: a采用Fisher精确概率法
合并败血症15例,呼吸衰竭9例,肺出血6例,休克9例,凝血功能障碍13例。死亡组合并败血症、呼吸衰竭、肺出血、休克及凝血功能障碍比例高于存活组,差异有统计学意义(P<0.05),见表5。根据术中及术后病理,单纯性先天性胃壁肌层缺损28例,死亡4例;合并其他消化道畸形19例,死亡5例;原因不明3例,均存活。其中合并先天性肠旋转不良8例,死亡2例;合并先天性食管闭锁伴气管食管瘘7例,死亡3例;合并美克尔憩室并肠坏死3例、合并胎粪性肠梗阻1例,无死亡。
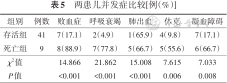
两患儿并发症比较[例(%)]
两患儿并发症比较[例(%)]
| 组别 | 例数 | 败血症 | 呼吸衰竭 | 肺出血 | 休克 | 凝血障碍 |
|---|---|---|---|---|---|---|
| 存活组 | 41 | 7(17.1) | 2(4.9) | 1(65.9) | 4(9.8) | 7(17.1) |
| 死亡组 | 9 | 8(88.9) | 7(77.8) | 5(66.7) | 5(55.6) | 6(66.7) |
| χ2值 | 14.866 | 21.862 | 15.008 | 7.615 | 7.033 | |
| P值 | <0.001 | <0.001 | <0.001 | 0.006 | 0.008 |
50例患儿均进行手术治疗,其中2例因胃穿孔复发接受二次手术。将单因素分析有意义的因素进行多因素logistic回归分析,结果显示合并败血症、出现症状至手术时间>24 h、诊断胃穿孔时pH<7.3是导致预后不良的危险因素,见表6。
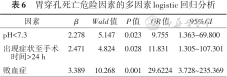
胃穿孔死亡危险因素的多因素logistic回归分析
胃穿孔死亡危险因素的多因素logistic回归分析
| 因素 | β | Wald值 | P值 | OR值 | 95%CI |
|---|---|---|---|---|---|
| pH<7.3 | 2.278 | 5.147 | 0.023 | 9.755 | 1.363~69.800 |
| 出现症状至手术时间>24 h | 2.471 | 4.824 | 0.028 | 11.831 | 1.305~107.301 |
| 败血症 | 3.389 | 10.268 | 0.001 | 29.6224 | 3.728~235.369 |
新生儿胃穿孔是新生儿期威胁生命的急腹症之一,约占新生儿胃肠道穿孔的7%~12%,国外研究显示胃穿孔的病死率达30%~70%[4, 5]。本研究数据来自广东省妇幼保健院新生儿内科及外科,新生儿内科为广东省危重症救治中心,接收外院转诊的早产危重病例,因此本组新生儿胃穿孔约占新生儿胃肠道穿孔的20%,比例较高,但胃穿孔病死率为18.0%,较文献低。国内研究显示胃穿孔中早产儿比例占新生儿期胃穿孔的57.8%[6],本组病例中早产儿占68.0%,较国内研究高。早产和低体重是新生儿胃穿孔最常见且始终相关的诱发因素,但早产和低出生体重是否为新生儿胃穿孔死亡的危险因素仍存在争议[2,7]。本研究中,死亡组早产儿和低出生体重比例虽低于存活组,但差异无统计学意义。
新生儿胃穿孔与肠道穿孔临床表现相似,主要表现为突然出现并进行性加重的腹胀,因合并其他消化道畸形或因疾病严重程度不同而伴有呕吐、发热、精神萎靡、呼吸困难及腹膜炎体征,可早期行腹部X线检查确诊,典型的X线片表现为膈下游离气体影,以“足球征”为特点[8]。本研究显示死亡组发热及呼吸困难比例高于存活组,分析原因可能为穿孔后炎性物质及细菌侵入导致腹膜炎,从而出现体温异常,同时大量腹腔积气、膈肌升高影响胸腔容积进而影响呼吸系统,导致呼吸困难。因此,新生儿胃穿孔患儿出现发热及呼吸困难时往往提示预后不良。台湾长庚医院的一项研究显示,新生儿胃穿孔死亡患儿入院时白细胞减少、48 h内血小板减少、酸中毒、术后持续血小板减少和存在腹膜炎与严重后遗症显著相关[9]。还有研究显示降钙素原水平与患儿发生不良预后的风险相关[10]。Yang等[11]报道了白细胞计数异常与新生儿胃穿孔的高病死率相关,Huang等[12]研究显示,白细胞计数<5×109/L或>20×109/L、血小板减少、pH<7.3、血清乳酸>2.5 mmol/L、低钠血症患儿预后不良的几率较高。本研究显示死亡组pH<7.3、血小板减少及降钙素原升高比例高于存活组,提示内环境紊乱、感染可能与死亡相关。乳酸升高可显示组织灌注不足,是临床危重症观察指标之一,但本研究中死亡组和存活组胃穿孔患儿乳酸水平差异并无统计学意义,可能与病例数较少有关。
本研究中死亡组和存活组穿孔部位、穿孔>3 cm及腹水量>100 ml比例差异均无统计学意义,但死亡组出现症状至手术时间>24 h、伴肠坏死比例更高。Byun等[13]研究显示出现症状与手术干预之间的时间间隔是影响生存的唯一预后因素。Lee等[14]研究显示从确诊到手术的时间与预后和病死率相关。Yang等[9]研究显示严重的肠道缺血坏死可能是死亡的潜在原因。此外,由于胃穿孔后渗漏至腹腔的胃酸和胃蛋白酶对腹部脏器产生强烈的刺激及腐蚀作用,胃内细菌从消化道穿孔部位进入腹腔,可引起肠坏死及腹腔感染[15]。
国内王凯等[5]研究显示单纯性先天性胃壁肌层缺损约占新生儿胃穿孔的44.4%,赵宝红等[8]研究显示先天性胃壁肌层缺损约占新生儿胃穿孔的71.4%,本研究中先天性胃壁肌层缺损占胃穿孔患儿的58.0%,与以上研究相符。先天性肠旋转不良、食道闭锁等结构异常极易导致新生儿胃穿孔。有研究表明先天性肠旋转不良合并胃穿孔是患儿死亡原因之一,与大段肠坏死及严重感染相关;先天性食管闭锁合并胃穿孔病死率高,且由于手术复杂,救治难度大,术后感染率高,易致家属放弃治疗,进一步增加病死率[16, 17, 18]。本研究中新生儿胃穿孔合并先天性肠旋转不良、合并先天性食管闭锁患儿病死率较国内研究高,可能与孕早期不规律产检未及时发现结构异常,未能及时转诊至有救治条件的医疗机构有关。此外,本研究发现胃穿孔合并消化道畸形并不影响预后,合并败血症、呼吸衰竭、肺出血、休克、凝血功能障碍与死亡相关,logistic回归分析显示出现症状至手术时间>24 h、pH<7.3及合并败血症为新生儿胃穿孔死亡的危险因素。这与国内外研究一致[7,14,19]。这表明合并败血症、内环境紊乱可增加胃穿孔患儿死亡风险,出现临床表现后越晚行手术治疗,死亡风险越高。
综上所述,新生儿胃穿孔以腹胀、气腹为主要表现,出现相关症状至手术时间>24 h、pH<7.3、合并败血症的患儿病死率高。因此,尽早确诊并及时手术治疗,对合并败血症者积极抗感染治疗对提高新生儿胃穿孔患儿存活率有积极意义。但本研究为回顾性病例对照研究,病例数较少,研究结果存在局限性,还应进一步扩大样本量并行前瞻性研究进一步分析探讨。
钟迪, 龙芳, 康朦梦, 等. 新生儿胃穿孔临床特点及死亡危险因素分析[J]. 中华新生儿科杂志, 2023, 38(5): 278-282. DOI: 10.3760/cma.j.issn.2096-2932.2023.05.005.
所有作者声明无利益冲突



























