
评价常规口服利尿剂治疗后仍有液体潴留(心原性水肿)的心力衰竭(心衰)患者联用托伐普坦片的有效性和安全性。
研究采用随机、双盲、安慰剂平行对照的方法,2012年8月~2013年7月间在中国27家医院入选常规口服利尿剂治疗后仍心原性水肿的心衰患者,左心室射血分数不限。在常规治疗基础上给予托伐普坦片15 mg/d或安慰剂治疗7 d。主要有效性指标为服药第8天体重与基线体重相比的变化量;次要有效性指标为服药后体重变化率及心原性水肿体征变化。
本研究共随机入选托伐普坦组124例,安慰剂组120例。两组患者基线资料比较差异无统计学意义。服药第8天,托伐普坦组体重下降值[(-1.48±1.95)kg比(-0.54±1.51)kg,P<0.01]、下肢水肿改善率(86.60%比70.79%,P=0.008)及颈静脉怒张消失率(39.58%比15.91%,P=0.012)显著高于安慰剂组。与安慰剂相比,托伐普坦组服药第8天的24 h尿量、摄水量、血清钠升高值均显著增加(P均<0.01),液体负平衡较基线的变化量于第1、2、6天均显著增加(P均<0.05)。两组所有测量时点血清钠均<155 mmol/L,不良事件发生率两组比较差异无统计学意义。
在常规治疗基础上联用托伐普坦片可有效减轻心原性水肿患者的体重、增加尿量、减轻充血体征,安全性良好。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
容量负荷增加是心力衰竭(心衰)患者住院的主要原因。目前常用的减轻容量负荷药物包括襻利尿剂和噻嗪类利尿剂,但近30%心衰患者对这两类药物存在抵抗[1]。血管加压素(argininevasopressin,AVP)非渗透性分泌增高是心衰容量负荷过重的重要机制之一,它作用于肾脏集合管细胞基底膜侧的V2受体促进自由水的吸收,托伐普坦是V2受体拮抗剂,因而具有促进排水而不排钠的作用特点。EVEREST、TACTIC等[2,3,4]研究发现在急性失代偿性心衰早期使用托伐普坦,可明显减轻体重、增加液体负平衡、缓解瘀血症状。日本QUEST研究[5]初步证实了心原性水肿患者使用托伐普坦的安全性和有效性,本研究旨在中国人群验证常规口服利尿剂治疗后仍有液体潴留(心原性水肿)的心衰患者,无论是否低钠,在常规治疗基础上连续7 d口服托伐普坦15 mg/d的有效性和安全性。
该研究是一项Ⅲ期、随机、双盲、安慰剂平行对照、多中心临床试验,自2012年8月至2013年7月在全国27家医院入选心衰患者,采用中心分层随机方法将受试者进行1∶1随机,在常规治疗基础上联用托伐普坦片(浙江大冢制药有限公司生产)15 mg/d或安慰剂共7 d。每个中心均获得伦理委员会批准,伦理批文号2012-394。每例患者均签署知情同意书。
使用常规利尿剂治疗后仍有心原性水肿的心衰患者具有入选资格,不限制左心室射血分数。患者服药前3 d未改变利尿剂用法用量且服药前2 d体重差在±1.0 kg范围内。
入选标准:使用现有利尿剂治疗后仍有下肢水肿、肺瘀血或颈静脉怒张等液体潴留症状的充血性心衰患者;男女不限,年龄20~85岁;其使用呋塞米(口服)40 mg/d以上或相当于该剂量的襻利尿剂(口服,呋塞米40 mg=托拉塞米10 mg=布美他尼1 mg);襻利尿剂未达到上述剂量,但需要合并使用噻嗪类利尿剂或醛固酮受体拮抗剂。
排除标准:安装循环辅助装置;确诊为活动性心肌炎或淀粉样心肌病;疑有循环血量减少、梗阻性肥厚型心肌病、重度主动脉瓣狭窄;控制不佳的糖尿病,空腹血糖超过12.21 mmol/L;无尿,尿道狭窄、结石、肿瘤等引起的排尿障碍;筛查前30 d内有急性心肌梗死、持续性室性心动过速或心室颤动、脑血管意外;对苯并氮杂卓类药物(莫扎伐普坦盐酸盐、盐酸贝那普利)有过敏史或特异性反应的患者;体重指数超过35 kg/m2的患者;卧位收缩压低于90 mmHg(1 mmHg=0.133 kPa);以下任一实验室检查值异常:总胆红素>正常值上限2.5倍、血清肌酐>正常值上限2.5倍、血清钠>145 mmol/L、血清钾>5.5 mmol/L。
连续7 d每天早饭后口服1片托伐普坦或安慰剂。服药第8天(末次服药次日)进行疗效评价,末次服药后7 d(第14天)进行治疗后观察,末次服药后14 d(第21天)进行结束后调查。试验过程中不限水摄入,不改变常规利尿剂用法用量,避免使用B型利钠肽制剂、静脉正性肌力药和静脉利尿剂。
主要有效性指标为服药第8天体重与基线体重相比的变化量。次要有效性指标是服药后体重变化率及心原性水肿体征变化(下肢水肿、颈静脉怒张、肺瘀血、肝肿大、肺啰音、第三心音)。下肢水肿根据坐位胫骨缘或足背水肿程度分为4级:无压痕;略有压痕;有压痕;水肿明显。改善程度判定:改善1级为改善;消失或改善2级以上为显著改善;严重程度没有变化或试验期间没有症状为不变;恶化1级以上为恶化。通过胸部X线检查评价肺瘀血。
实验室评价指标包括血清钠、钾浓度变化、24 h尿量、24 h摄水量及液体平衡状态。安全性评价指标包括研究中的不良事件、生命体征和心功能分级变化等。
以QUEST结果为依据,给药后体重与基线值的变化量( ±s)安慰剂组为(-0.45±0.93)kg,托伐普坦组为(-1.54±1.61)kg。显著性水平为双侧5%的条件下,确保把握度为90%,样本量为每组32例,结合中国相关法规政策及20%脱落率,最终设定每组为120例。
±s)安慰剂组为(-0.45±0.93)kg,托伐普坦组为(-1.54±1.61)kg。显著性水平为双侧5%的条件下,确保把握度为90%,样本量为每组32例,结合中国相关法规政策及20%脱落率,最终设定每组为120例。
有效性分析以全分析集为对象,采用意向性分析原则。基线时组间比较,分类变量采用χ2检验或Fisher精确检验,连续变量使用t检验或Wilcoxon秩和检验。体重与基线变化值、血清电解质、24 h尿量和摄入量等采用t检验。症状"显著改善"、"改善"和"消除"的百分比用Fisher精确检验。对不良事件以及不良反应,按照组别分析所有事件内容及按严重程度分析发生例数、发生率、发生件数,率比较采用χ2检验或Fisher精确检验。所有统计分析使用软件为Windows版本的SAS V9.2。P值<0.05为差异有统计学意义。
自2012年8月2日至2013年7月29日共在中国27家医院筛选了298例患者,筛选失败54例,随机化入组244例(托伐普坦组124例,安慰剂组120例)(图1)。两组受试者基线的人口学特征、临床特征及心原性水肿分布基本平衡,基线体重、24 h尿量、液体净平衡、肾功能、襻利尿剂用量组间比较差异无统计学意义(表1)。
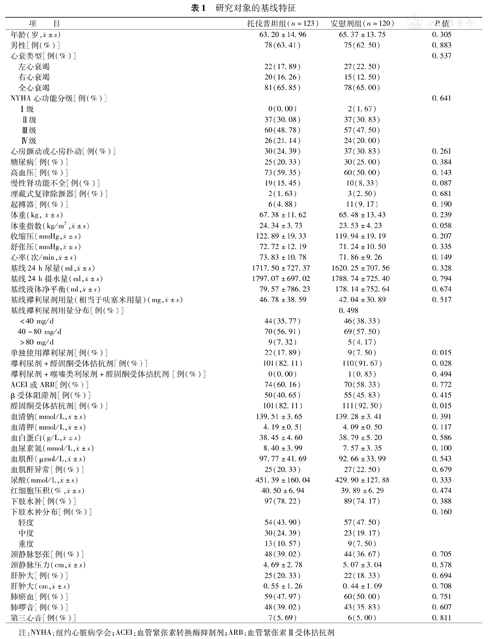
研究对象的基线特征
研究对象的基线特征
| 项 目 | 托伐普坦组(n=123) | 安慰剂组(n=120) | P值 | |
|---|---|---|---|---|
年龄(岁, ±s) ±s) | 63.20±14.96 | 65.37±13.75 | 0.305 | |
| 男性[例(%)] | 78(63.41) | 75(62.50) | 0.883 | |
| 心衰类型[例(%)] | 0.537 | |||
| 左心衰竭 | 22(17.89) | 27(22.50) | ||
| 右心衰竭 | 20(16.26) | 15(12.50) | ||
| 全心衰竭 | 81(65.85) | 78(65.00) | ||
| NYHA心功能分级[例(%)] | 0.641 | |||
| Ⅰ级 | 0(0.00) | 2(1.67) | ||
| Ⅱ级 | 37(30.08) | 37(30.83) | ||
| Ⅲ级 | 60(48.78) | 57(47.50) | ||
| Ⅳ级 | 26(21.14) | 24(20.00) | ||
| 心房颤动或心房扑动[例(%)] | 30(24.39) | 37(30.83) | 0.261 | |
| 糖尿病[例(%)] | 25(20.33) | 30(25.00) | 0.384 | |
| 高血压[例(%)] | 73(59.35) | 60(50.00) | 0.143 | |
| 慢性肾功能不全[例(%)] | 19(15.45) | 10(8.33) | 0.087 | |
| 埋藏式复律除颤器[例(%)] | 2(1.63) | 3(2.50) | 0.681 | |
| 起搏器[例(%)] | 6(4.88) | 11(9.17) | 0.190 | |
体重(kg,  ±s) ±s) | 67.38±11.62 | 65.48±13.43 | 0.239 | |
体重指数(kg/m2, ±s) ±s) | 24.34±3.73 | 23.53±4.23 | 0.058 | |
收缩压(mmHg, ±s) ±s) | 122.89±19.33 | 119.94±19.19 | 0.207 | |
舒张压(mmHg, ±s) ±s) | 72.72±12.19 | 71.24±10.50 | 0.335 | |
心率(次/min, ±s) ±s) | 73.83±10.78 | 71.86±9.26 | 0.149 | |
基线24 h尿量(ml, ±s) ±s) | 1717.50±727.37 | 1620.25±707.56 | 0.328 | |
基线24 h摄水量(ml, ±s) ±s) | 1797.07±697.02 | 1788.74±725.40 | 0.794 | |
基线液体净平衡(ml, ±s) ±s) | 79.57±786.23 | 178.14±752.64 | 0.674 | |
基线襻利尿剂用量(相当于呋塞米用量)(mg, ±s) ±s) | 46.78±38.59 | 42.04±30.89 | 0.517 | |
| 基线襻利尿剂用量分布[例(%)] | 0.498 | |||
| <40 mg/d | 44(35.77) | 46(38.33) | ||
| 40~80 mg/d | 70(56.91) | 69(57.50) | ||
| >80 mg/d | 9(7.32) | 5(4.17) | ||
| 单独使用襻利尿剂[例(%)] | 22(17.89) | 9(7.50) | 0.015 | |
| 襻利尿剂+醛固酮受体拮抗剂[例(%)] | 101(82.11) | 110(91.67) | 0.028 | |
| 襻利尿剂+噻嗪类利尿剂+醛固酮受体拮抗剂[例(%)] | 0(0.00) | 1(0.83) | 0.494 | |
| ACEI或ARB[例(%)] | 74(60.16) | 70(58.33) | 0.772 | |
| β受体阻滞剂[例(%)] | 50(40.65) | 55(45.83) | 0.415 | |
| 醛固酮受体拮抗剂[例(%)] | 101(82.11) | 111(92.50) | 0.015 | |
血清钠(mmol/L, ±s) ±s) | 139.51±3.65 | 139.28±3.41 | 0.391 | |
血清钾(mmol/L, ±s) ±s) | 4.19±0.51 | 4.09±0.50 | 0.117 | |
血白蛋白(g/L, ±s) ±s) | 38.45±4.60 | 38.79±5.20 | 0.586 | |
血尿素氮(mmol/L, ±s) ±s) | 8.40±3.99 | 7.57±3.35 | 0.100 | |
血肌酐(μmol/L, ±s) ±s) | 97.77±41.69 | 92.66±33.99 | 0.543 | |
| 血肌酐异常[例(%)] | 25(20.33) | 27(22.50) | 0.679 | |
尿酸(mmol/L, ±s) ±s) | 451.39±160.04 | 429.90±127.88 | 0.333 | |
红细胞压积(%, ±s) ±s) | 40.50±6.94 | 39.89±6.29 | 0.474 | |
| 下肢水肿[例(%)] | 97(78.22) | 89(74.17) | 0.388 | |
| 下肢水肿分布[例(%)] | 0.160 | |||
| 轻度 | 54(43.90) | 57(47.50) | ||
| 中度 | 30(24.39) | 23(19.17) | ||
| 重度 | 13(10.57) | 9(7.50) | ||
| 颈静脉怒张[例(%)] | 48(39.02) | 44(36.67) | 0.705 | |
颈静脉压力(cm, ±s) ±s) | 4.69±2.78 | 5.07±3.04 | 0.578 | |
| 肝肿大[例(%)] | 25(20.33) | 22(18.33) | 0.694 | |
肝肿大(cm, ±s) ±s) | 0.55±1.26 | 0.44±1.09 | 0.708 | |
| 肺瘀血[例(%)] | 59(47.97) | 60(50.00) | 0.751 | |
| 肺啰音[例(%)] | 48(39.02) | 43(35.83) | 0.607 | |
| 第三心音[例(%)] | 7(5.69) | 6(5.00) | 0.811 | |
注:NYHA:纽约心脏病学会;ACEI:血管紧张素转换酶抑制剂;ARB:血管紧张素Ⅱ受体拮抗剂

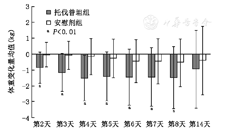
与基线相比,服药第8天托伐普坦组体重下降高于安慰剂组,组间差异有统计学意义[(-1.48±1.95)kg比(-0.54 kg±1.51)kg,-0.94 kg(-1.38,-0.50),P<0.01];体重变化率组间差异有统计学意义[-2.24%比-0.84%,-1.40%(-2.11,-0.70),P<0.01]。治疗第2~7天托伐普坦组体重下降的绝对值及下降率亦均高于安慰剂组,组间差异有统计学意义(P值均<0.01),体重下降组间差值(托伐普坦-安慰剂)为-1.36 kg~-0.82 kg。托伐普坦组体重下降早期显著,第4天达高峰,安慰剂组体重下降平缓。末次服药后7 d两组体重变化仍为负值,组间差异无统计学意义[-0.55 kg(-1.13,0.04),P>0.05](图2)。

亚组分析显示,托伐普坦作用不依赖于性别、年龄、联合使用利尿剂及基线24 h尿量,但纽约心脏病学会(NYHA)心功能Ⅲ级以上的患者服用托伐普坦体重下降更显著(表2)。
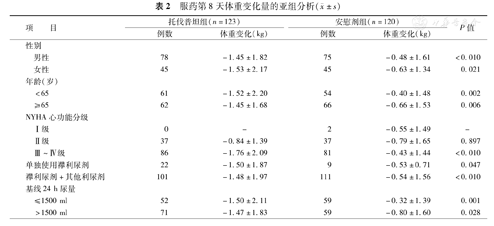
服药第8天体重变化量的亚组分析( ±s)
±s)
服药第8天体重变化量的亚组分析( ±s)
±s)
| 项 目 | 托伐普坦组(n=123) | 安慰剂组(n=120) | P值 | |||
|---|---|---|---|---|---|---|
| 例数 | 体重变化(kg) | 例数 | 体重变化(kg) | |||
| 性别 | ||||||
| 男性 | 78 | -1.45±1.82 | 75 | -0.48±1.61 | <0.010 | |
| 女性 | 45 | -1.53±2.17 | 45 | -0.63±1.34 | 0.021 | |
| 年龄(岁) | ||||||
| <65 | 61 | -1.52±2.20 | 54 | -0.40±1.48 | 0.002 | |
| ≥65 | 62 | -1.45±1.68 | 66 | -0.66±1.53 | 0.006 | |
| NYHA心功能分级 | ||||||
| Ⅰ级 | 0 | - | 2 | -0.55±1.49 | - | |
| Ⅱ级 | 37 | -0.84±1.39 | 37 | -0.79±1.65 | 0.897 | |
| Ⅲ~Ⅳ级 | 86 | -1.76±2.09 | 81 | -0.43±1.44 | <0.010 | |
| 单独使用襻利尿剂 | 22 | -1.50±1.87 | 9 | -0.53±0.71 | 0.047 | |
| 襻利尿剂+其他利尿剂 | 101 | -1.48±1.97 | 111 | -0.54±1.56 | <0.010 | |
| 基线24 h尿量 | ||||||
| ≤1500 ml | 52 | -1.50±2.11 | 59 | -0.32±1.39 | 0.001 | |
| >1500 ml | 71 | -1.47±1.83 | 59 | -0.80±1.60 | 0.028 | |
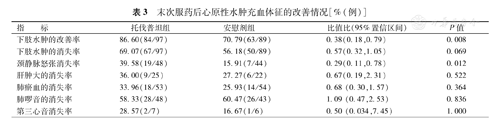
末次服药后心原性水肿充血体征的改善情况[%(例)]
末次服药后心原性水肿充血体征的改善情况[%(例)]
| 指 标 | 托伐普坦组 | 安慰剂组 | 比值比(95%置信区间) | P值 |
|---|---|---|---|---|
| 下肢水肿的改善率 | 86.60(84/97) | 70.79(63/89) | 0.38(0.18,0.79) | 0.008 |
| 下肢水肿的消失率 | 69.07(67/97) | 56.18(50/89) | 0.57(0.32,1.05) | 0.069 |
| 颈静脉怒张消失率 | 39.58(19/48) | 15.91(7/44) | 0.29(0.11,0.78) | 0.012 |
| 肝肿大的消失率 | 36.00(9/25) | 27.27(6/22) | 0.67(0.19,2.31) | 0.522 |
| 肺瘀血的消失率 | 33.96(18/53) | 25.93(14/54) | 0.68 (0.30,1.57) | 0.364 |
| 肺啰音的消失率 | 58.33(28/48) | 60.47(26/43) | 1.09 (0.47,2.53) | 0.836 |
| 第三心音消失率 | 28.57(2/7) | 16.67(1/6) | 0.50 (0.034,7.45) | 1.000 |
与安慰剂相比,服药第8天托伐普坦组下肢水肿的改善率、颈静脉怒张的消失率均显著升高,组间差异有统计学意义(P值均<0.05),下肢水肿、肝肿大、肺瘀血、肺啰音及第三心音消失率两组间比较,差异均无统计学意义(P值均>0.05)。治疗后无充血体征患者比例托伐普坦组(n=31,25.20%)与安慰剂组比较,差异无统计学意义(n=25,20.83%)(P>0.05)。下肢水肿改善和肺瘀血消失的患者托伐普坦组体重下降明显高于安慰剂组,组间差异有统计学意义[-0.97 kg(-1.54,-0.40),P=0.0005;-1.97 kg(-3.31,-0.62),P=0.0056]。
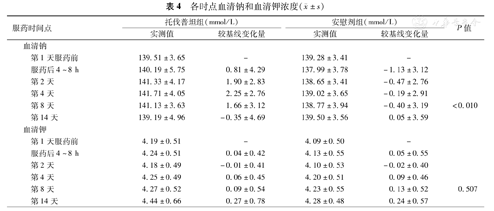
各时点血清钠和血清钾浓度( ±s)
±s)
各时点血清钠和血清钾浓度( ±s)
±s)
| 服药时间点 | 托伐普坦组(mmol/L) | 安慰剂组(mmol/L) | ||||
|---|---|---|---|---|---|---|
| 实测值 | 较基线变化量 | 实测值 | 较基线变化量 | P值 | ||
| 血清钠 | ||||||
| 第1天服药前 | 139.51±3.65 | - | 139.28±3.41 | - | ||
| 服药后4~8 h | 140.19±5.75 | 0.81±4.29 | 137.99±3.78 | -1.13±3.12 | ||
| 第2天 | 141.33±4.17 | 1.90±2.83 | 138.65±3.41 | -0.47±2.76 | ||
| 第4天 | 141.71±4.05 | 2.25±2.76 | 139.02±3.65 | -0.19±2.91 | ||
| 第8天 | 141.13±3.63 | 1.66±3.12 | 138.77±3.94 | -0.40±3.19 | <0.010 | |
| 第14天 | 139.19±4.96 | -0.35±4.69 | 139.50±3.56 | 0.05±3.59 | ||
| 血清钾 | ||||||
| 第1天服药前 | 4.19±0.51 | - | 4.09±0.50 | - | ||
| 服药后4~8 h | 4.24±0.51 | 0.04±0.42 | 4.13±0.55 | 0.05±0.55 | ||
| 第2天 | 4.18±0.49 | -0.01±0.41 | 4.10±0.53 | -0.02±0.40 | ||
| 第4天 | 4.25±0.49 | 0.06±0.45 | 4.20±0.51 | 0.09±0.46 | ||
| 第8天 | 4.27±0.52 | 0.09±0.54 | 4.23±0.55 | 0.13±0.52 | 0.507 | |
| 第14天 | 4.44±0.66 | 0.27±0.78 | 4.28±0.48 | 0.24±0.57 | ||
与基线相比,服药第4~8小时及第2、4、8天托伐普坦组血清钠浓度上升(0.81~2.25 mmol/L),安慰剂组血清钠浓度下降(-1.13 mmol/L~-0.19 mmol/L)。两组服药后4~8 h和第2天均无受试者血清钠浓度升高>12 mmol/L,治疗期间均无受试者血清钠超过155 mmol/L。两组服药后至第8天血清钾浓度无显著变化,组间比较差异无统计学意义。
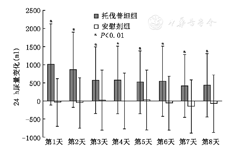

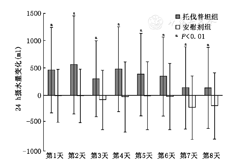

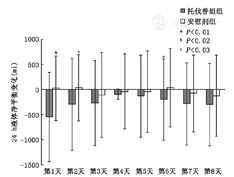

与安慰剂相比,服药第1~8天,托伐普坦组24 h尿量、摄水量较基线的变化量均明显增加,组间比较差异均有统计学意义(P均<0.01),尿量以第1天增加最多(1 013.96 ml),摄水量以第2天增加最多(563.92 ml);服药后第1、2、6天托伐普坦组液体负平衡较基线的变化量显著增加,组间差异均有统计学意义(P均<0.05),其余时点两组液体净平衡较基线变化量差异无统计学意义(P均>0.05)。
本试验记录和分析从取得知情同意到治疗结束后1周内发生的所有不良事件及2周内发生的严重不良事件。
不良事件的发生率托伐普坦组为74.19%(92/124),安慰剂组为66.67%(80/120),组间差异无统计学意义(P=0.19)(表5)。托伐普坦组的主要不良反应为口干(13.71%)。
治疗期间不良事件发生率≥5%的事件[例数(%)]
治疗期间不良事件发生率≥5%的事件[例数(%)]
| 不良事件 | 托伐普坦组(124例) | 安慰剂组(120例) |
|---|---|---|
| 低钾血症 | 8(6.45) | 16(13.33) |
| 低钠血症 | 2(1.61) | 6(5.00) |
| 高尿酸血症 | 12(9.68) | 11(9.17) |
| 上呼吸道感染 | 6(4.84) | 6(5.00) |
| 口渴 | 7(5.65) | 1(0.83) |
| 口干 | 18(14.52) | 3(2.50) |
| 心力衰竭 | 3(2.40) | 9(7.50) |
严重不良事件发生率托伐普坦组为4.03%(5/124),安慰剂组为6.67%(8/120),组间差异无统计学意义(P=0.36)。托伐普坦组心衰发生率更低,组间差异有统计学意义(2.4%比7.5%, P<0.05)。与安慰剂相比,治疗第4天托伐普坦组血肌酐较基线升高更明显,组间差异有统计学意义[(0.58±16.65)μmol/L比(5.72±14.37)μmol/L,P<0.05],第8天和治疗结束后7 d两组间差异均无统计学意义[3.82 μmol/L(-0.69,8.33),P>0.05;-5.67 μmol/L(-13.48,2.13),P>0.05]。
死亡事件托伐普坦组3例(2.42%),死因为急性肾功能衰竭(1例)和猝死(2例);安慰剂组1例(0.83%),死因为猝死。除托伐普坦组1例猝死病例无法判定与试验药物的关系外(未尸检),其余3例均与试验药物无关。
本研究显示,使用常规利尿剂治疗后仍有液体潴留的心衰患者,在常规治疗基础上联用托伐普坦片15 mg/d共7 d可显著降低体重,保持液体负平衡,减轻下肢水肿和颈静脉怒张体征,安全性良好。
SEMI-SEC研究显示,托伐普坦可以提高顽固性心衰合并低钠血症患者的血钠浓度,并增加尿量[6]。目前欧美指南推荐托伐普坦用于容量负荷增加伴顽固性低钠血症的心衰患者。但规模最大的EVEREST研究中,血钠低于135 mmol/L的患者只占11%,托伐普坦仍能显著降低体重,改善下肢水肿和呼吸困难症状[2,3,7,8],提示托伐普坦消除心衰容量负荷的作用并不限于低钠血症患者。
本研究与在日本进行的QUEST研究[5]设计相似,但样本量增加1倍。与QUEST研究结果类似,在主要终点方面7 d口服托伐普坦可显著降低体重。对于充血体征的改善,QUEST研究中托伐普坦可显著改善颈静脉怒张和肝肿大,而本研究则为改善颈静脉怒张及下肢水肿。本研究未发现托伐普坦可改善肺瘀血和肺部啰音,可能是因为细胞外液转移需要一个过程,内脏器官瘀血的改善可能延迟出现[4,9]。
托伐普坦组未限制摄水量,饮水量较对照组增加,但液体净平衡仍持续处于负平衡,总体来说仍然保持了其减轻容量负荷的作用。停用托伐普坦治疗后,未出现体重迅速增长、液体潴留相关症状恶化或尿量减少等情况。此外,托伐普坦的作用不依赖于性别、年龄、合并利尿剂的种类、基线尿量等,但对于心功能Ⅲ级以上的患者托伐普坦效果更佳。
EVEREST研究[2]显示,托伐普坦组高钠血症发生率高于安慰剂组,但该研究中托伐普坦使用剂量为30 mg/d。本研究和QUEST研究托伐普坦使用剂量较低,仅为15 mg/d,均未见严重高钠血症发生。在本研究中,托伐普坦组和安慰剂组基线血钠水平均为139 mmol/L, 92.6%患者血钠水平在正常范围内,托伐普坦组高钠血症发生率仅为3.23%,略高于安慰剂组(1.67%),组间差异无统计学意义,表明15 mg/d托伐普坦在有效降低体重同时,没有增加高钠血症发生风险。另一项研究发现,在正常血钠范围内,患者使用托伐普坦后血钠升高值与基础血钠成反比,基线血钠低的患者使用托伐普坦后血钠升高更显著,基线血钠正常的患者使用托伐普坦后血钠变化不大,本研究显示相似趋势,可能是因为托伐普坦排钠随着基线血钠水平升高而增加[10,11]。
研究显示,托伐普坦能改善肾脏血流,具有肾脏保护作用,因而本研究入选患者血肌酐水平低于正常上限的2.5倍[12,13]。尽管治疗过程中托伐普坦组有一过性血肌酐升高,但治疗结束后观察一周血肌酐较安慰剂组有下降趋势,证实了对于伴有一定程度肾功能损伤的患者托伐普坦是安全的。早期血肌酐升高考虑为利尿剂导致血容量下降,肾小球滤过率可逆性轻度下降所致,也间接反映利尿剂有效。
本研究有一定局限性:(1)本研究未探索对利尿剂反应欠佳的心原性水肿患者,如何预估托伐普坦使用的最佳个体化剂量及如何达到最佳容量状态。(2)本研究未观察托伐普坦对住院期间心衰恶化及出院后长期预后的影响。在将来的研究中有待进一步探索这些问题。
研究组成员(以参与单位入组人数排序,入组人数相同按研究负责人的姓氏笔画排序)哈尔滨医科大学第一临床医院(富路、张翠丽、张瑞英),大庆油田总医院(王丽娜、杨硕),辽宁省人民医院(李占全、刘莹),卫生部北京医院(杨杰孚、佟佳宾、王欣越),中国医学科学院 北京协和医学院 阜外医院(张健、张宇辉、黄燕),中国医学科学院 北京协和医学院 北京协和医院(朱文玲、陈未、朱燕林),徐州医学院附属医院(夏勇、黄炜、徐通达),佛山市第一人民医院(梁茜、梅百强、岑锦明),四川大学华西医院(陈晓平、刘凯、陈静静),海口市人民医院(陆士娟、李小华、黄康),浙江医院(唐礼江、汤益民),江苏大学附属医院(严金川、刘培晶),西安交通大学医学院第一附属医院(袁祖贻、白玲、霍建华),解放军总医院(董蔚、李丹丹、李亚光),中国医科大学附属盛京医院(马淑梅),中山大学附属第一医院(董吁钢、刘晨),武汉大学人民医院(杨波、曹锋),广州军区武汉总医院(丁世芳、蒋桔泉),解放军第二炮兵总医院(胡桃红、胡莉华、崔琳琳),江苏省苏北人民医院(顾翔、沈建华),上海市第一人民医院(刘少稳、史浩颖),天津市第三中心医院(刘迎午、罗洁颖),南昌大学第二附属医院(程晓曙、李菊香、李运德),中国医科大学附属第一医院(孙英贤、张子新),第二军医大学长海医院(赵仙先、马丽萍),成都军区总医院(杨永健),河南省人民医院(徐予)。


























