
免疫检查点抑制剂(ICI)目前已广泛用于多种恶性肿瘤的治疗。但ICI可诱导免疫相关的不良反应(irAEs)。irAEs可累及全身多个器官,其中以胃肠道不良反应为著,病变最常累及结肠和小肠,常伴有腹泻症状,称之为免疫检查点抑制剂导致的小肠结肠炎。本文主要介绍ICI相关肠炎发生机制、风险因素、临床表现及处理方式,以便更好地识别ICI相关胃肠道不良反应并提高其治疗有效性。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肿瘤免疫治疗是肿瘤治疗的又一次突破性进展,免疫检查点抑制剂(immune checkpoint inhibitor,ICI)已广泛用于黑色素瘤、非小细胞肺癌、肝癌、胃癌等恶性肿瘤的治疗。ICI通过抑制负性免疫调控机制,激活T细胞,从而发挥对肿瘤细胞的杀伤作用,但却由此诱导免疫相关的不良反应(immune-related adverse events,irAEs)。irAEs主要见于皮肤、肝脏、胃肠道、内分泌系统,其他少见的还可累及肾脏、神经系统和眼部。ICI作用机理不同于化疗和靶向治疗药物,近年已有多个国际指南关注对于irAEs的管理[1,2,3,4,5]。其中胃肠道不良反应最为常见,以腹泻为主要表现,病变最常累及结肠,亦可累及小肠和上消化道,习惯上称之为ICI相关肠炎(immune checkpoint inhibitor-induced enterocolitis),本文将对其进行介绍与讨论。
ICI能够靶向调控机体免疫系统从而避免恶性肿瘤细胞发生免疫逃逸。ICI药物分为两大类,一类是以程序性死亡蛋白1(programmed cell death protein 1,PD-1)为代表的抑制剂,这类药物主要增强抗肿瘤细胞的适应性免疫、诱导抗肿瘤免疫耐受丢失,靶向抑制细胞毒T淋巴细胞活化、增殖并影响其功能;另一类为激活剂,目前尚处于临床研究阶段[6,7]。
正常人体免疫T细胞通过共刺激和共抑制因子的共同调节,发挥正性和负性调节机制。免疫检查点在免疫负性调节中发挥重要作用,保证免疫调节维持在适当范围内。在肿瘤的发生、发展机制中,共刺激因子使免疫系统识别并攻击肿瘤,但因肿瘤微环境可通过多种机制使免疫活性细胞活性降低甚至失活,从而介导肿瘤的免疫逃逸。其中一个重要机制就是肿瘤微环境中的免疫细胞上调免疫检查点,导致抗肿瘤的T细胞失能。目前研究比较深入的免疫检查点主要有细胞毒T淋巴细胞相关抗原4(cytotoxic T lymphocyte-associated antigen-4,CTLA-4)和PD-1及其配体PD-L1(programmed death-ligand 1)。T细胞表面的CD28受体是主要的共刺激分子,其与抗原递呈细胞(antigen presenting cells,APC)上的CD80和CD86配体结合,放大T细胞受体(T cell receptor,TCR)的信号通道,提高T细胞活性。而CTLA-4和PD-1则进行免疫活性的负性调节。CTLA-4的表达由效应淋巴细胞,特别是CD4+T细胞诱导,其与CD80和CD86的亲和力远高于CD28,因此可竞争性结合CD80和CD86,达到抑制CD28共剌激分子的作用,从而降低T细胞活性。在肿瘤组织中存在的CD4+T细胞具有高度表达CTLA-4能力,从而介导肿瘤的免疫逃逸。PD-1受体表达于T细胞等免疫细胞表面,与PD-L1和PD-L2配体结合,通过募集酪氨酸磷酸酶SHP2等机制,进而导致TCR信号通路上多个关键分子的去磷酸化,从而降低T细胞活性。在肿瘤组织的微环境中,肿瘤细胞高表达PD-L1和PD-L2,与PD-1结合,亦会介导肿瘤的免疫逃逸。因此,ICI的作用就是阻断免疫检查点与其配体的结合,从而打破免疫耐受,增强免疫细胞活性,促进肿瘤细胞的清除。然而,由于肿瘤和正常细胞存在类似的抗原,当T细胞被活化后,正常组织也同时受到攻击,从而有可能导致正常组织的自身免疫相关炎症反应,这便是irAEs发生的基础。由于抗CTLA-4抗体与抗PD-1/PD-L1抗体作用的靶点不同,各自导致的irAEs的发生率、发生部位及严重程度有一定不同[6,8]。
ICI相关胃肠道不良事件发生的高危因素可能包括药物种类(不良反应发生率:联合治疗>抗CTLA-4抗体>抗PD-1抗体)、抗CTLA-4抗体与非甾体类抗炎药合用、单克隆抗体剂量、原有自身免疫性疾病或炎症性肠病(IBD)、肠道菌群等[9,10]。
总体来讲胃肠道不良事件发生率为21%~44%;而抗CTLA-4单抗相关胃肠道不良事件比例高于抗PD-1/PD-L1单抗,腹泻发生率分别为30.2%~35.4%和12.1%~13.7%,两者联合治疗发生率约为32%;结肠炎的发生率分别为5.7%~9.1%和0.7%~1.6%,联合治疗发生率约为13.6%[11,12,13]。该类药物在我国上市较晚,报道尚少,北京协和医学院肿瘤医院报道20例肿瘤患者使用PD-1/PD-L1抗体中有6例(30%)发生irAEs,其中1例为免疫性胃肠损伤[14]。抗CTLA-4单抗(ipilimumab)10 mg/kg治疗的3~4级腹泻(10%比6%)和结肠炎(5%比2%)发生率高于3 mg/kg[15]。研究发现接受抗CTLA-4抗体治疗的肿瘤患者,发生结肠炎者肠道拟杆菌属菌种增加而厚壁菌门菌种减少[16]。年龄并不能预测ICI相关结肠炎的发生情况[17]。与发生高危相关的血清标志物、遗传易感基因尚在研究中。
腹泻是ICI相关肠炎的特征症状,部分患者可表现为腹痛、恶心、呕吐症状,便血和发热发生率相对较低;极少部分患者可出现肠神经元病变和严重便秘[18,19,20]。腹泻可伴或不伴有结肠炎。病情严重程度参考美国国家癌症研究所对不良事件的常用术语标准进行分级(表1)[23]。ICI治疗起始和维持阶段均有可能出现相关肠炎表现,不同种类的ICI临床表现大体相似,但抗CTLA-4单抗与抗PD-1/PD-L1单抗相比,免疫相关胃肠道损伤发生率更高、症状出现更早、症状较重;但也有个别患者在治疗后1年出现肠炎。ICI联合治疗发生免疫性肠炎起始中位时间大约5周。少见病变还有小肠炎、上消化道炎症、显微镜下结肠炎、假性肠梗阻(肠神经病变)。严重的结肠炎可并发肠穿孔(发生率约1%),或同时伴其他组织器官的irAEs。

ICI相关胃肠道不良反应分级[23]
ICI相关胃肠道不良反应分级[23]
| 不良反应 | 1级 | 2级 | 3级 | 4级 |
|---|---|---|---|---|
| 腹泻 | 对比基线期每天增加的大便次数<4次;造口量较基线期轻度增加。 | 对比基线期大便每天增加4 ~ 6次;造口量适度增加 | 对比基线期每天增加的大便次数≥7次;失禁;有住院指征;造口量较基线期显著增加;日常活动受限 | 出现危及生命的临床状况;需要紧急干预(如血流动力学异常) |
| 结肠炎 | 无症状或症状不典型;仅为临床诊断或随访;无需干预 | 腹痛或黏液血便 | 严重或持续的腹痛;排便习惯改变;发热;需要干预治疗的肠梗阻;腹膜炎体征 | 出现危及生命的临床情况;需要紧急干预(如穿孔、出血、缺血、坏死、巨结肠中毒) |
尚未见到在抗PD-1单抗治疗的患者中出现口腔溃疡、肛周病变的情况。此外症状的严重程度可能和ICI剂量相关,标准剂量ICI联合使用如抗CTLA-4单抗3 mg/kg联合抗PD-1/PD-L1 1 mg/kg,每3周注射1次,3~4级腹泻和结肠炎的发生率分别增加至9%~10.7%和8%~17%;低剂量(CTLA-4单抗1 mg/kg + PD-1/PD-L1 1 mg/kg)联合治疗12周后3~4级腹泻和结肠炎的发生率低于5%[21,22]。
全面的实验室检查包括相关的鉴别诊断(肠道微生物感染、艰难梭菌感染、巨细胞病毒感染等)、反映肠道炎症活动指标(全血细胞检查、红细胞沉降率、C-反应蛋白、粪便钙卫蛋白)、判别有无与免疫相关胃肠损伤共存的其他irAEs(如免疫相关肝损伤的肝功能检查)、了解基础病(原发肿瘤)及免疫相关胃肠损伤所造成后果(如血清白蛋白、肌酐等),以及可能要转换英夫利西单抗(IFX)治疗前的筛查(如γ-干扰素释放试验、病毒性肝炎血清标记物)。
约47%的ICI相关肠炎患者影像表现无特殊,约10%的患者出现CT影像下改变但内镜下表现正常,CT或CTE可见肠系膜血管扩张、结肠壁增厚和强化、肠管扩张,这些影像特征可呈现弥漫性或节段性改变,需要进一步鉴别诊断;也有回肠末端增厚的病例报道。CT的阳性预测值可以达到90%,但是阴性预测值仅有40%~60%;CT鉴别ICI相关结肠炎的敏感性和特异性分别为53%和78%[23,24,25]。对严重结肠炎宜行CT检查,尤其是有穿孔或巨结肠者。CT检查有助于鉴别诊断,但CT检查阴性并不能排除本病。出现严重急性肠炎的患者建议行腹部CT检查明确有无穿孔、结肠扩张、腹腔脓肿等情况。
2~4级的腹泻应常规行结肠镜检查。结肠镜检查有助ICI相关肠炎的诊断及病变严重程度评估,同时与肿瘤转移性复发及与其他肠道疾病鉴别。绝大多数病变可以通过直乙结肠镜发现,但少部分病变仅位于近段结肠,甚至在回肠末段,因此有条件者宜行全结肠镜检查。病变的严重程度不一定与腹泻严重程度相关。部分抗PD-1抗体引起的腹泻肠镜下黏膜表现正常,但活检会发现肠黏膜炎症改变[23,26,27]。肠镜下病变严重程度常与便血程度相关,严重病变(Mayo评分2~3分)常提示病情严重且激素疗程欠佳。
ICI相关肠炎的内镜表现多样,可见黏膜下血管纹理模糊或消失、红斑、糜烂、溃疡、自发性出血或深大溃疡等(图1)。病变范围不等,病变可呈弥漫性分布或呈片状散在分布。少部分患者胃镜下可见胃、十二指肠红斑、糜烂或溃疡。
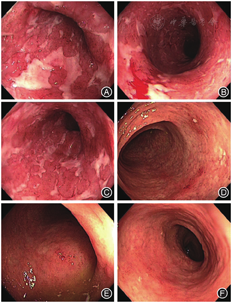

ICI相关肠炎通常表现为黏膜固有层的急性炎症改变,可见中性粒细胞浸润、隐窝炎和隐窝脓肿,亦可见上皮内淋巴细胞浸润;部分患者见隐窝上皮细胞凋亡。炎症分布多为弥漫性,少数为灶性。慢性期(停用ICI数个月后或肠炎复发)可出现类似IBD样改变,表现为黏膜固有层和(或)黏膜下层单核细胞浸润、隐窝结构改变,少数患者可见肉芽肿。免疫组化显示抗CTLA-4单抗相关肠炎的肠黏膜内以CD4+T细胞为主,抗PD-1单抗相关肠炎以CD8+T细胞为主。免疫相关胃肠道损伤亦可只表现为显微镜下结肠炎改变。有上消化道病变者,十二指肠黏膜可见绒毛变纯、萎缩,黏膜固有层急性和慢性炎性细胞浸润,部分病例可见腺体上皮内淋巴细胞浸润[23,28,29,30]。
肿瘤患者接受ICI治疗后(抗CTLA-4抗体1个月后、抗PD-1/PD-L1抗体2~4个月后)出现腹泻,伴或不伴其他胃肠道症状,充分排除其他相似胃肠道疾病后,可予诊断。结肠镜检查及活检有助诊断。CT有助发现并发症。诊断成立后要对腹泻和结肠炎的严重程度进行评估以指导治疗。
需要与各种感染性腹泻,包括艰难梭菌感染和巨细胞病毒感染进行鉴别诊断,大便找虫卵及寄生虫、细菌培养、艰难棱菌毒素检测有助鉴别。恶性肿瘤肠道转移,肠镜检查及活检和腹部CT有助鉴别。通过病史、肠镜及活检、CTE综合分析与IBD进行鉴别,若患者原有IBD基础病,使用ICI后可引起IBD复发。
按照患者的病情严重程度,1级可以继续使用ICI,低纤维清淡饮食和对症治疗,密切监测15 d左右,如症状无好转则按2级治疗;2级暂停用ICI,口服糖皮质激素(泼尼松1 mg·kg-1·d-1或其他制剂相当剂量),监测7 d无效按3级治疗;3级停用ICI,口服糖皮质激素(泼尼松1~2 mg·kg-1·d-1或其他制剂相当剂量),监测3~5 d无效改用或开始即予静脉用糖皮质激素(去甲泼尼松龙1 mg·kg-1·d-1);4级永久停用所有ICI,静脉用糖皮质激素(去甲泼尼松龙1 mg·kg-1·d-1),监测2~3 d无效改用IFX。
腹泻伴显微镜下结肠炎的治疗:IFX和维得利珠单抗的疗效尚未确立,因此激素治疗的疗效可观察较长时间,是否转换治疗视具体情况而定。
约40%~70%患者对糖皮质激素有效,取得临床缓解后激素逐渐减量,约6~8周停用。对静脉用激素3~5 d无反应者、激素减量过程中或激素停用后短期复发者(定义为复发),均应转换到IFX。但激素的使用并不能预防腹泻和结肠炎的发生[2,31,32]。
转换IFX治疗对大多患者有效,3、4级患者宜早期使用或尽早转换IFX,可参考内镜下病变严重程度早期使用IFX。建议剂量为每次5 mg/kg,用药一般不超过3次(第0、2、6周给药),总体应答率约为81%,中位应答时间为2~14 d;开始使用后尽快激素减量[2,33,34]。目前病例报道的维得利珠单抗总体应答率约85%,无激素中位缓解时间为56 d[35],但需要更多研究证实。
对激素和IFX治疗无效者,使用粪菌移植治疗可能有效。研究发现肿瘤患者对ICI原发无应答或应答欠佳与其肠道菌群组成有关,动物模型中也证实肠道菌群可调节个体抗肿瘤免疫反应及药物应答效果;基于该结果,后续病例报道研究发现粪菌移植能够改善难治性ICI相关肠炎患者肠道菌群组成,增加黏膜层中CD4+Foxp3+T淋巴细胞亚群比例降低CD8+细胞毒T淋巴细胞比例,从而改善肠炎[36]。
免疫相关胃肠损伤发生肠穿孔、腹腔脓肿、巨结肠时,应急诊手术治疗,切除病变肠段并行回肠造口术。出现中毒性巨结肠、腹腔脓肿或结肠穿孔的患者须急诊行结肠次全切及回肠造口术治疗。ICI联合治疗导致的免疫性肠炎临床管理与单药管理相同。
对既往已出现过胃肠道不良反应的患者再次使用ICI时需谨慎考虑;相比总体治疗人群,既往使用抗CTLA-4单抗出现过irAEs的患者出现新的3、4级irAEs的频率明显增加[9,37]。ICI导致的免疫相关胃肠损伤经治疗缓解后,再次使用ICI可发生免疫相关胃肠损伤复发,且抗CTLA-4抗体的复发率远高于抗PD-1抗体。因此,在由抗CTLA-4抗体或联合治疗导致的1~3级免疫相关胃肠损伤经治疗后痊愈,如有必要可以权衡利弊考虑使用抗PD-1抗体单药治疗。一般认为使用免疫抑制药物(激素或IFX)并不影响ICI的抗肿瘤疗效[19,37,38,39]。
在随访过程中出现复发的大部分患者需要接受激素再诱导,部分患者需要重复使用IFX治疗。部分初始使用IFX治疗的患者炎症可转为慢性迁延,且与症状不平行,更需要内镜随访,且广泛结肠炎的患者生存期低于病变仅累积左半结肠的患者。
ICI相关的胃肠道不良反应风险因素多样,临床表现常以腹泻为主,需要排除其他相似胃肠道疾病,结肠镜检查及活检有助诊断。诊断成立后需对腹泻和结肠炎的严重程度进行评估以指导治疗,按病情严重程度进行分层治疗的策略。ICI在临床上的成功给予癌症免疫治疗新的革命,不同于目前抗炎抗体的作用机制(抑制促炎介质、信号转导、转运通路),ICI主要作用于共抑制通路,如何更好地理解共抑制通路的相似性、差异以及共抑制通路的协同作用机制可能对肠炎发生机制提供更深入切入点,值得进一步探索。
所有作者均声明无相关利益冲突



























