
极早发型炎症性肠病(VEO-IBD)是炎症性肠病(IBD)的特殊亚群,其病理生理进程与成人或大于6岁的儿童IBD差异较大。其临床症状更重,对传统IBD治疗方案反应差,外科并发症发生率高。外科治疗是VEO-IBD多学科治疗中的重要组成部分,目前对VEO-IBD的外科治疗尚缺乏统一的认识。近年来随着生物制剂、免疫治疗、干细胞移植等新型治疗方式的出现,对VEO-IBD外科治疗的理念和方法也发生了重要的转变。本共识基于循证医学依据,采用Delphi方法制定,在VEO-IBD外科治疗的相关问题上达成共识意见,以期为临床工作提供指导。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
儿童炎症性肠病(pediatric inflammatory bowel disease,PIBD)是指18岁以下发病的炎症性肠病(inflammatory bowel disease,IBD),是一种儿童罕见病,但发病率逐年增高,目前该病在我国儿童三级诊疗中心所占比例越来越高。文献报道PIBD占所有IBD患者的25% ~ 30%,其中起病年龄小于6岁的极早发型炎症性肠病(very early onset inflammatory bowel disease,VEO-IBD)占PIBD的6% ~ 15%[1]。PIBD在发病机制、临床表现、治疗反应及疾病转归等方面和成人炎症性肠病存在较大差异,这些差异在VEO-IBD患儿中尤其明显。VEO-IBD可能以单基因突变为主要致病原因,是以IBD样表现为主要特征的一组疾病。相较于传统的IBD,VEO-IBD的消化道病变主要累及结肠,临床症状更重,常伴有肛周病变及严重的营养不良和生长发育迟缓。传统IBD治疗对VEO-IBD疗效较差,外科并发症发生率高[2,3,4]。随着VEO-IBD内科治疗的长足进展,外科手术干预原则也出现了不同于成人和年长儿童的变化[5,6]。要实现对VEO-IBD患儿更好的诊治管理,外科在多学科团队中发挥着重要的作用,迫切需要制定针对这一特殊群体的外科诊疗方案和临床建议。
本共识由中华医学会消化病学分会炎症性肠病学组儿科协作组发起,已在国际实践指南注册平台(International Practice Guidelines Registry Platform,http://www.guidelines-registry.org)进行了中英文双语注册(注册号为IPGRP-2022CN191)。2022年9月通过向全体共识专家发放问卷的形式,确定本共识需要阐明的22个临床问题。所有工作组成员均声明不存在与本共识相关的经济利益冲突或非经济利益冲突。本共识采用德尔菲法(Delphi method)进行制定。来自内科、外科、护理专业的共识核心组成员通过广泛的文献检索、筛选和评价,将相关临床问题及推荐方案撰写成文。经共识全体专家组成员讨论修改,应用电子系统采用无记名投票表决。表决意见分成5级:a完全赞成(必不可少);b部分赞成,但有一定保留;c部分赞成,但有较大保留;d不赞成,但有一定保留;e完全不赞成。本共识意见中的推荐等级根据投票结果分为A级指标(强烈推荐),即a得票数为80%及以上;B级指标(推荐),即a和b得票数相加为80%及以上;C级指标(建议),即a、b和c得票数相加为80%及以上;未达C级指标则删去。根据证据级别高低及专家投票结果,本共识将推荐分为"强烈推荐"、"推荐"和"建议"3个等级。
1.对发病年龄小于6岁且伴有并发症或合并症的出现黏液血便症状患儿需高度警惕VEO-IBD。推荐等级:强烈推荐
因发病机制不同,VEO-IBD不是6岁以上儿童或成人IBD在婴幼儿期的简单复刻。发病越早基因在发病中的作用就会越强,特别是在2岁前及新生儿期发病的患儿。研究表明20% ~ 30%VEO-IBD由明确的单基因突变致病[7]。2021年欧洲儿童胃肠肝病营养学会的儿科IBD Porto小组就75个单基因IBD的致病基因达成共识[8]。每一种致病基因的表型会有所不同,常以症候群或综合征的形式出现,除了腹泻、黏液血便等基本表现外,其主要特点还包括(1)起病年龄小于6岁,甚至新生儿期即发病;(2)反复感染或不明原因的发热;(3)对传统IBD治疗方案反应较差;(4)常存在免疫缺陷或自身免疫性疾病的表现;(5)常有类似疾病的家族史、近亲婚配史;(6)常伴严重的肛周病变(肛瘘、肛周脓肿);(7)严重的营养不良、生长发育迟缓;(8)内分泌紊乱;(9)会以噬血细胞性淋巴组织细胞增多症/巨噬细胞活化综合征(HLH/MAS)样表现;(10)可能会伴有肠梗阻或肠闭锁;(11)可能有皮肤、毛发、牙齿等外胚层发育不良的表现;(12)会有合并肿瘤等恶性病变的可能[9]。存在上述疾病特点的患儿需要详细询问相关病史,完善相关检查并组织进行多学科讨论,尽早明确诊断以更好地指导治疗。
2.有报警症状的VEO-IBD患儿需尽快进行基因检测、功能验证并给予相应的精准治疗。推荐等级:强烈推荐
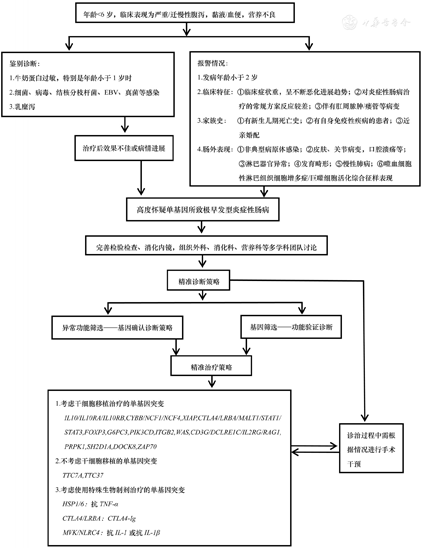
疑诊VEO-IBD的患儿常需要先排除感染、牛奶蛋白过敏、乳糜泻等疾病,若存在以下报警状况时推荐完成基因检测(一代和二代测序技术)和目标基因的功能验证:(1)发病年龄小于2岁;(2)临床特征:①临床症状重,呈不断恶化进展趋势;②对IBD常规治疗方案反应较差;③伴有肛周脓肿/瘘管等病变;(3)家族史:①有新生儿期死亡史;②有自身免疫性疾病的患者;③近亲婚配;(4)肠外表现:①非典型病原体感染;②皮肤、关节病变、口腔溃疡等;③淋巴系统异常;④发育畸形;⑤慢性肺病;⑥噬血细胞性淋巴组织细胞增多症/巨噬细胞活化综合征(HLH/MAS)样表现等[3,9,10]。无论何种基因检测手段都存在一定局限性,故需结合免疫细胞功能、转录水平、蛋白质表达、信号转导通路分析等技术,弥补基因测序存在的不足。除了微观层面,更需要整合临床、遗传、免疫和多组学等多维度数据以提高对疾病诊断和分型的精准度[11,12]。VEO-IBD的诊治流程见图1。

明确发病机制是决定临床分型和精准治疗的关键,已报道的单基因突变主要影响以下功能(表1):(1)肠道上皮细胞屏障功能;(2)T、B细胞数量和功能;(3)免疫调节功能;(4)中性粒细胞吞噬及NADPH氧化酶功能;(5)自身炎症反应调节功能;(6)其他[7,13]。基于发病机制的临床分型或分类有利于精准治疗的实施,近年来也提出基于发病机制的靶向治疗理念[10]。尽管缺乏大型临床试验,但较高的单基因缺陷率使个体化治疗成为VEO-IBD患儿的理想选择。例如基因突变导致的IL-10信号通路异常可通过骨髓造血干细胞或脐血干细胞移植达到治愈的目标。而在没有发现遗传或免疫缺陷的情况下,治疗通常与年长患儿相似。不仅如此,不同基因突变所致VEO-IBD,外科并发症的发生形式和病变累及部位都有其相对独特的特点(表2),对外科实施精准手术治疗有很强的指导意义。

极早发型炎症性肠病基于发病机制的分类及突变基因
极早发型炎症性肠病基于发病机制的分类及突变基因
| 发病机制 | 临床表现 | 相关疾病及综合征 | 突变基因 |
|---|---|---|---|
| 上皮屏障功能 | 多发肠闭锁、重症联合免疫缺陷病、严重的婴儿凋亡性小肠结肠炎 | 遗传性多发性肠闭锁 | TTC7A |
| 障碍 | 感染、缺牙、出汗少、头发稀疏、额头隆起、生长发育不良和腹泻 | NEMO综合征 | IKBKG |
| 葡萄球菌感染、牛皮癣样皮炎、脓疱、断发、指甲异常、腹泻 | ADAM17综合征 | ADAM17 | |
| 回肠梗阻、食管炎、电解质紊乱 | 家族性腹泻病 | GUCY2C | |
| 出生后即出现分泌型腹泻 | 先天性腹泻病 | SLC26A3 | |
| 皮肤复发性水疱或糜烂、食管狭窄、肛裂和肛门狭窄、肠道疾病、头发和指甲异常 | 大疱性表皮松解症 | COL7A1 | |
| 免疫调节功能异常 | 炎症性肠病出生时起病、腹泻、自身免疫性疾病、银屑病样皮炎、脱发、内分泌系统疾病、1型糖尿病 | X连锁多内分泌病肠病伴免疫失调综合征(IPEX) | FOXP3 |
| 毛囊炎、肛周疾病、关节炎、B细胞淋巴瘤风险增加 | 白介素10信号通路功能缺陷 | IL10RA,IL10RB,IL10 | |
| 肉芽肿性结肠炎,严重的肛周疾病 | NOD2信号通路功能缺陷 | TRIM22 | |
| T和(或)B淋巴细胞复合型功能缺陷 | 感染、间质性肺炎、自身免疫性疾病表现(特发性血小板减少症、自身免疫性溶血性贫血、1型糖尿病) | LRBA基因缺陷 | LRBA |
| 自身免疫性疾病、自身免疫性血细胞减少、感染、间质性肺炎 | CTLA4基因缺陷 | CTLA4 | |
| 伴有血小板体积减小的血小板减少症、反复细菌和病毒感染、湿疹、血性腹泻、淋巴瘤、自身免疫性疾病 | Wiskott-Aldrich综合征 | WAS | |
| 反复出现严重细菌感染、小扁桃体、腹泻 | X连锁无丙种球蛋白血症 | BTK | |
| 小头症、小脑发育不全、宫内生长受限、指甲营养不良、再生障碍性贫血和骨髓衰竭 | Hoyeraal-Hreidarsson综合征(先天性角化不良) | DKC1,RTEL1 | |
| 复发性严重感染、慢性腹泻、生长发育迟缓 | 重症联合免疫缺陷(SCID) | ZAP70,IL2RG ADA,CD3ɤ | |
| 复发性细菌和病毒感染、低丙种球蛋白血症、淋巴结病变、脾肿大 | Caspase-8缺乏症 | CASP8 | |
| 皮肤病毒、真菌、葡萄球菌感染、嗜酸性粒细胞增多症、湿疹、腹泻、发育迟缓 | 高IgE综合征 | DOCK8 | |
| 感染性肠炎、小肠疾病突出和胃肠道结节性淋巴增生、脾肿大 | 普通变异型免疫缺陷 | ICOS | |
| 吞噬细胞和NADPH氧化酶复合物缺陷 | 感染、自身免疫、母体盘状狼疮 | 慢性肉芽肿病 | CYBA,CYBB NCF1,NCF2 NCF4,LACC1 |
| 中性粒细胞减少症、心脏发育异常、泌尿生殖缺陷、宫内发育迟缓 | 先天性中性粒细胞减少症 | G6PC3,SLC37A4 | |
| 低血糖发作、中性粒细胞减少症、肝肿大 | 糖原贮积病Ⅰb | ||
| 过度炎症和自身炎症反应缺陷 | 婴儿型炎症性肠病,EBV病毒感染、肝炎、噬血细胞淋巴组织细胞增多症、脾肿大 | X连锁淋巴细胞异常增生征2型 | XIAP |
| 周期性发热、口腔溃疡、关节炎、浆膜炎、皮疹、肠病 | 家族性地中海热 | MEFV | |
| IgD升高、发热、恶心、腹痛、淋巴结肿大、口腔溃疡、关节炎、脾肿大、肠病、肛周疾病 | 甲羟戊酸激酶缺乏症(高IgD)综合征) | MVK | |
| 其他 | 宫内发育迟缓、结节性脱毛、前额凸起、绒毛萎缩 | 发肝肠综合征 | SKIV2L,TTC37 |

不同单基因突变导致的消化道病变及发病机制
不同单基因突变导致的消化道病变及发病机制
| 突变基因 | 累及消化道部位及病变 | 可能的发病机制 |
|---|---|---|
| GUCY2C | 食管炎、回肠梗阻性病变 | 上皮屏障功能障碍 |
| TTC7A | 多发肠闭锁,严重的婴儿凋亡性小肠结肠炎 | |
| COL7A1 | 食管狭窄、肛门狭窄 | |
| FERMT1 | 食管狭窄,结肠病变 | |
| IL-10,IL-10RA,IL-10RB | 肛周脓肿、肛瘘,结肠病变突出 | 获得性免疫功能缺陷 |
| ICOS | 感染性肠炎,小肠病变突出,脾肿大 | |
| PTEN | 结肠多发腺瘤样息肉病 | |
| RAG-1,RAG-2,ZAP70,IL-7R | 肠道受累变异度较大,慢性腹泻 | |
| WASP,ARPC1B | 全结肠炎,黏液血便 | |
| IL-2RB | 小肠结肠病变 | 调节性T细胞功能缺陷 |
| IL-21 | 小肠结肠CD | |
| SKIV2L,TTC37 | 小肠病变,绒毛萎缩 | 自身免疫性/炎性疾病 |
| STXBP2 | 肝脾肿大 | |
| XIAP | 严重的结肠炎及肛周病变,脾肿大 | |
| NLRC4 | 严重的小肠结肠IBD样病变 | |
| MEFV | 小肠结肠均可受累 | |
| MVK | 肛周病变,小肠结肠炎 | |
| HSP1,HSP4 | 结肠炎 | |
| TRIM22 | 肉芽肿性结肠炎,严重肛周病变 | |
| CYBB,CYBA,NCF1,NCF2,NCF4 | 小肠结肠炎,结肠病变突出,肉芽肿性肠炎 | 吞噬细胞功能/NADPH功能缺陷 |
注:CD为克罗恩病;IBD为炎症性肠病
3.VEO-IBD的诊治过程需要外科在内的多学科团队全程参与。推荐等级:强烈推荐
VEO-IBD患儿临床表现多变,部分患儿初诊时可能以外科症状、体征为突出表现(表3)[13,14]。对于小于6岁,尤其是小于2岁的患儿,如果以复杂或严重肛周脓肿、肛瘘,或不明原因的肠穿孔、腹膜炎、腹腔脓肿、肠狭窄或肠梗阻等外科临床表现就诊时,需要警惕VEO-IBD并及时组织多学科团队对其进行全面系统的评估[7,9,15,16]。当外科症状体征隐匿时,常表现为难以控制的感染,需警惕潜在的穿孔、脓肿等外科并发症发生的可能[17,18,19,20,21]。另外,VEO-IBD的疾病特点决定了外科医生可能更倾向于采用回肠末端造口术,术后外科并发症包括与造口相关的感染、出血、伤口裂开等,也需要联合护理和外科的多学科团队进行诊治[6,22,23]。

极早发型炎症性肠病常见的外科临床表现及突变基因
极早发型炎症性肠病常见的外科临床表现及突变基因
| 外科临床表现 | 可能的单基因突变 |
|---|---|
| 肛周病变:肛周脓肿、肛瘘、肛周溃疡、肛裂、肛周皮赘 | IL-10,IL-10RA,IL-10RB,CD40LG,AICDA,ZBTB24,PIK1,CASP8,CYBB,CYBA,NCF1,NCF2,NCF4,SLC37A4,NPC1,XIAP,HPS1,HPS4,MEFV,TRIM22 |
| 肠狭窄、肠梗阻 | DKC1,CASP8,CYBB,CYBA,NCF1,NCF2,NCF4,SLC37A4,G6PC3,ITGB2,MVK,COL7A1,GUCY2C,SLC9A3,CHAPLE |
| 肠穿孔 | CASP8,HPS1,HPS4,MVK, |
| 腹膜炎 | MEFV |
| 肠粘连 | MVK |
| 多发肠闭锁 | TTC7A |
4.造血干细胞移植是部分单基因IBD患儿的治愈方案。推荐等级:推荐
当明确突变基因会导致造血细胞功能缺陷时,推荐异基因骨髓干细胞或脐血干细胞移植作为此类VEO-IBD患儿的治疗方案[24]。Nambu等[3]在2021年总结出有14类单基因位点突变的VEO-IBD是可以通过干细胞移植治疗获得康复。我国研究团队纳入102例进行造血干细胞移植的IL-10信号通路功能缺陷IBD患儿,包括手术和非手术患儿,结果发现与未接受造血干细胞移植的患儿相比,接受移植的患儿总体生存率更高,移植患儿的生存率与移植时机、移植类型及基因型无显著关联;未接受移植的患儿中,合并肠穿孔、肠梗阻患儿生存率显著更低;肠穿孔后急诊肠造口术和保护性肠造口术,不仅改善了生存状况,也大大提高了患儿接受干细胞移植的机会[5]。
5.IBD内科治疗可作为VEO-IBD患儿手术前后及精准治疗方案的桥接或序贯。推荐等级:推荐
目前尚无VEO-IBD患儿全肠内营养治疗的高质量研究,对婴幼儿时期起病的CD样肠道表现的患儿,全肠内营养可以作为一线诱导缓解方案[13,25,26]。虽然很多研究发现5-氨基水杨酸制剂、激素、免疫调节剂等常规IBD治疗方案在VEO-IBD中治疗效果不佳,但与6岁以上的患儿相比,上述药物的使用率并不低[27,28]。在儿童IBD诱导缓解和维持缓解中作用突出的抗肿瘤坏死因子-α单克隆抗体,在VEO-IBD中常因疗效欠佳或不良反应等问题而停用[29]。新型靶向生物制剂有望在治疗某些特定的单基因IBD中获得突破性进展,如阿巴西普(一种CTLA4-IgG1融合药物)和羟氯喹可用于CTLA4和LRBA基因缺陷的患儿[3]。对尚未明确单基因致病的VEO-IBD患儿,在没有其他更好的治疗方案的情况下,内科药物治疗可作为实施手术、精准治疗方案前的桥接治疗[13,23]。沙利度胺是一种特殊的免疫调节剂和血管生成抑制剂,可作为IBD的二线治疗方案,针对VEO-IBD的治疗研究尚不多[13]。研究发现沙利度胺可明显改善VEO-IBD患儿的临床症状,促进黏膜愈合,改善生存状况[5]。结合当前一线治疗方案效果不佳的现状,沙利度胺可考虑作为二线治疗的优选方案,但需密切监测其可能出现的不良反应。
6.如果VEO-IBD患儿病情经过充分的内科治疗仍难以控制,外科手术可能是缓解病情的重要手段。推荐等级:推荐
已有研究表明糖皮质激素、免疫抑制剂、生物制剂等常规治疗方案在VEO-IBD患儿中应答率和缓解率均不高,疾病反复和疾病进展都将严重影响患儿的营养和生长发育[13,29,30]。研究发现,对此类患儿实施积极的保护性回肠造口术可以明显改善其病情及生存状况,提高药物应答率,并为后续治疗(部分单基因VEO-IBD可进行造血干细胞移植治疗)创造机会和提供保障[5,6,14]。
7.急性肠梗阻和肠穿孔是VEO-IBD的绝对急诊手术指征,重度肠道感染的VEO-IBD患儿出现扩张或固定的肠袢,推荐作为相对急诊手术指征。推荐等级:强烈推荐
由于VEO-IBD尤其是其中的单基因IBD患儿发病年龄小,病情重,对药物治疗反应差[31,32]。VEO-IBD较非VEO-IBD患者病程中需手术干预的概率更高,其中1岁前发病的患儿手术率高达50%,1岁后发病的手术率约为29%[33,34]。目前尚无关于VEO-IBD手术指征的专门研究报道。急性肠梗阻和穿孔无疑是明确的手术指征,需要注意的是这类患儿中相当一部分穿孔表现隐匿,部分患儿并无气腹、腹膜炎等典型肠穿孔表现,临床上可能表现为严重的全身感染和与之相关的肠梗阻发作[6]。因此,存在来源于肠道的重度感染的VEO-IBD患儿,若同时在影像学检查上出现扩张或固定的肠袢,需警惕存在穿孔性病变,推荐作为相对的急诊手术指征。
8.药物治疗无效的持续性或复发性严重腹泻和感染、慢性肠梗阻、严重且难以控制的肛周感染、反复感染的直肠尿道瘘和直肠阴道(前庭)瘘,推荐作为择期手术的指征。推荐等级:推荐
VEO-IBD导致的长期或反复腹泻、便血容易引起严重的营养不良和发育障碍,IL-10及其受体基因突变等单基因IBD往往伴有免疫缺陷,极易发生严重的全身感染。由于VEO-IBD病变肠段多局限于结肠或回结肠,通过保护性造口旷置病变肠段能显著减轻肠道炎症和和溃疡,降低感染风险,提高肠内营养的耐受能力[5,6]。因此,对于药物治疗无效的持续性或复发性重度腹泻和全身感染推荐作为择期肠造口术的手术指征。
直肠狭窄或结肠狭窄是VEO-IBD的常见并发症,肠狭窄引起的慢性肠梗阻、反复腹胀感染,持续或间歇性无法耐受肠内营养,影响患儿的生长发育,可通过肠造口术提高肠内营养的耐受性;严重且难以控制的肛周感染、复杂肛瘘、直肠尿道瘘、直肠阴道(前庭)瘘等是VEO-IBD尤其是单基因IBD常见的并发症,容易引起反复发作的局部脓肿或泌尿生殖道感染,甚至诱发脓毒症等全身感染,严重影响患儿的生活质量[5,6,35,36]。肠造口术能显著减少肛周感染的发作,改善局部愈合条件,因此可作为择期肠造口术的手术指征[37,38]。
9.存在潜在高危因素的单基因IBD患儿异基因造血干细胞移植前推荐行预防性肠造口。推荐等级:推荐
异基因造血干细胞移植是治疗单基因IBD的重要手段,肠造口术可作为部分患儿干细胞移植前准备的一部分,以防止干细胞移植期间尤其是骨髓抑制期发生梗阻、穿孔、感染等并发症[5,6,15]。约75% ~ 100%的IL-10及其受体基因突变所致IBD会导致肛周病变[6,18,39]。研究显示异基因造血干细胞移植前行肠造口术能显著改善IL-10及其受体基因突变所致IBD患儿的生活质量,提高移植期间及移植后整体存活率[5]。因此如患儿存在严重的肛周感染、反复感染的直肠尿道瘘和直肠阴道(前庭)瘘、复杂性肛瘘、无法扩张或扩张治疗无效的结直肠或肛门狭窄等高危因素时,建议异基因造血干细胞移植前行保护性肠造口,有利于控制感染并改善营养,提高移植的耐受性[6]。
10.单基因IBD造血干细胞移植后的急慢性胃肠道移植物抗宿主病常表现为肠梗阻、肠穿孔,药物治疗无效时推荐手术干预。推荐等级:推荐
随着异基因干细胞移植越来越多的应用于单基因IBD的治疗,干细胞移植后出现移植物抗宿主病(graft-versus-host disease,GVHD)的患者越来越多。研究显示干细胞移植后约50% ~ 60%患者会发生不同程度的GVHD,其中胃肠道GVHD占20% ~ 30%[40,41,42,43,44]。胃肠道GVHD可导致急性和慢性肠梗阻、肠穿孔、腹膜炎和消化道出血等,对药物治疗反应差。既往认为严重的GVHD患者通常病情危重、病死率高,不适合手术干预,多数患者死于GVHD和感染[45,46]。然而,随着医疗水平和重症监护水平的提高,对于符合手术适应证的患儿,进行积极手术干预显示良好的效果[47,48,49]。Gutierrez等[50]总结既往报道中13例消化道GVHD患儿的治疗经验,认为当继发肠出血、肠穿孔或肠狭窄时,积极的手术干预可改善这些患儿的预后。因此单基因IBD干细胞移植后出现胃肠道GVHD导致的肠梗阻、穿孔等外科并发症时可考虑手术干预,手术方式可根据患儿病情选择肠造口或肠切除吻合术[50,51,52]。
11.术前改善营养、纠正内环境紊乱和控制感染是提高手术耐受性和降低术后并发症的重要因素。推荐等级:强烈推荐
根据VEO-IBD患儿情况选择肠内和(或)肠外途径改善营养状况可有效降低术后并发症的发生,其中白蛋白是衡量营养状况的重要指标,对于低蛋白血症的患儿术前输注白蛋白是必要的[53,54]。无论是急诊手术还是择期手术,术前达到液体、电解质和酸碱平衡、纠正贫血是保障麻醉状况下获得足够组织氧合的基础,可以有效提高患儿手术耐受性[53,54]。反复感染是VEO-IBD患儿的临床特点之一,存在感染的患儿术前推荐使用广谱抗生素,不仅可以对感染或败血症进行治疗,而且可以有效预防围手术期感染并发症的发生[47,55,56,57]。如存在球蛋白缺乏的原发性免疫缺陷病,抗感染的同时应给予人血丙种球蛋白输注的支持治疗[48,49]。
12.符合上述手术指征的活动期VEO-IBD推荐行肠造口术。推荐等级:强烈推荐
由于病理机制和临床表现的差异,成人溃疡性结肠炎常采用的全结肠切除回肠储袋肛管吻合术(ileal pouch-anal anastomosis,IPAA)治疗可能对VEO-IBD不完全适用。研究发现对于活动期VEO-IBD肠造口术能明显缓解大部分患儿的梗阻、腹泻、感染及肛周病变,一期吻合一方面可能无法改善已有症状,另一方面由于肠道炎症、腹腔感染等因素,会显著增加吻合口并发症的发生率,单基因IBD在干细胞移植前行肠造口术可能提高干细胞移植后的存活率[5,6]。因此对于活动期VEO-IBD和干细胞移植前的单基因IBD,在符合上述手术指征的情况下建议采用肠造口术。一期吻合术仅适用于通过药物或干细胞移植治疗后肠道炎症完全控制的缓解期患者,且仅推荐适用于肠狭窄、粘连性梗阻等局限性病变[58,59]。
对于尚未确诊为IBD、因肠梗阻或肠穿孔行手术探查的患儿,即使已进行充分的肠道准备,若存在上述临床警示症状且高度怀疑为VEO-IBD时仍推荐行肠造口术,不建议行一期吻合术。同时需充分探查全消化道,明确病变肠管范围。
13.VEO-IBD患儿肠道病变多局限于结肠和末端回肠,回肠造口可适用于多数患儿。推荐等级:强烈推荐
VEO-IBD包含多种已知病因的单基因IBD及未知原因的IBD,每一种亚型的受累肠道位置及肠管病变程度有很大差别,从靠近屈氏韧带的小肠到直肠肛门均有可能受累,肠道病变可表现为从充血水肿到多发穿孔坏死的不同程度病变[6]。不同的基因异常引起的肠道病变范围不一样,IL-10及其受体基因、PIK3R1和PIK3CD基因、XIAP基因突变所致IBD等多局限于肛周、结肠或回结肠,推荐行病变近端的末端回肠造口;FOXP3等基因突变引起的X连锁多内分泌腺病肠病伴免疫失调综合征(IPEX综合征)、CYBB等基因突变引起的慢性肉芽肿病、BTK等基因突变可广泛累及肛周、结肠、小肠甚至胃和食道,需根据术中探查受累小肠的位置、长度制定个体化的造口方案;对于因直肠或肛周并发症行造口术的患儿,考虑到结肠可能在后续病程中出现新的病变,因此不建议行乙状结肠造口,仍推荐末端回肠造口[6,18,60,61,62,63,64,65]。
14.造口手术过程中除明确的坏死肠段外,不建议以消除炎性病灶为目的行大范围病变结肠切除。推荐等级:强烈推荐
结肠是IBD尤其是溃疡性结肠炎的主要受累器官,结肠切除术是治疗成人溃疡性结肠炎经典的手术方式,切除结肠可去除感染和炎性病灶,控制疾病的活动。但是VEO-IBD的发病机制和疾病进程与成人IBD有较大区别,激进的结肠切除术会对生长发育期的儿童造成不可逆的损伤,甚至影响患儿的生长发育,因此对这些患儿行结肠切除术时应特别谨慎。临时性回肠造口是一种有效的替代治疗策略,回肠造口促进结肠病变愈合的机制尚未完全阐明,可能因为肠造口术避免了粪便中的促炎因子与病变肠管的直接接触[6,10,66,67]。研究发现,单基因IBD在进行干细胞移植免疫重建后多数肠道病变是可逆的,在二期关造口的手术探查中发现,活动期结肠的炎症、水肿、多发穿孔等病变在缓解期多能恢复正常,且关闭造口后并未引起疾病的复发和需要再手术[6]。因此在造口手术过程中除明确的坏死肠段外不建议以消除炎症病灶为目的行大范围的病变肠段切除。尽管大量报道显示全结肠切除和IPAA手术可应用于儿童溃疡性结肠炎的治疗,但多用于大龄儿童且存在较高的并发症发生率[68,69,70,71,72]。根据现有的文献报道暂不推荐在VEO-IBD一期手术中实施大范围结肠切除术和IPAA[5,6,10]。
VEO-IBD患儿经常伴发肛周脓肿、肛瘘、直肠尿道瘘和直肠阴道(前庭)瘘、直肠狭窄等肛周和直肠并发症。VEO-IBD活动期的外科治疗主要包括积极的脓肿引流以控制感染、适时的肠造口以减轻肛门直肠病灶的污染和肠梗阻症状。VEO-IBD缓解期长期不愈的肛瘘、直肠尿道瘘和直肠阴道(前庭)瘘、保守治疗无效的直肠狭窄需手术干预。
15.VEO-IBD活动期出现的肛周脓肿和肛瘘应按照一般的外科原则积极切开引流,缓解期推荐随访观察,长期不愈考虑外科干预。推荐等级:强烈推荐
VEO-IBD尤其是单基因IBD肛周脓肿和肛瘘的发生率高,约一半的单基因IBD患儿伴有肛周脓肿和肛瘘[73]。目前尽管有多种对IBD相关的肛瘘进行分类和评估的方法,多数以瘘管和肛门括约肌的解剖关系为基础,但难以指导临床治疗[74,75,76]。在肠道炎症活动期出现的肛周脓肿和肛瘘应按照一般的外科原则积极切开引流,防止炎症向周围组织及全身扩散。在IBD的缓解期,一半以上的肛瘘可自行愈合,不需要手术治疗[76,77,78,79]。因此VEO-IBD通过药物或干细胞移植治疗充分缓解后应给予半年以上的观察随访期,然后重新对肛瘘进行评估,如肛瘘仍未愈合再考虑挂线、瘘管切开等外科干预治疗措施。
16.反复感染的直肠尿道瘘和直肠阴道(前庭)瘘在VEO-IBD活动期推荐先行保护性肠造口,缓解期则需制定个体化治疗方案。推荐等级:强烈推荐
在克罗恩病导致的直肠瘘中约9%表现为直肠阴道(前庭)瘘[80]。成人IBD导致的直肠阴道(前庭)瘘手术修补后极易复发,据报道手术修补的成功率仅为53%,约22%患者需要行直肠切除术[81]。VEO-IBD导致的直肠阴道(前庭)瘘目前报道较少,缺乏相关的统计数据。Ye等[73]报道的38例婴儿型炎症性肠病(infantile onset inflammatory bowel disease,IO-IBD)患儿中9例存在直肠阴道(前庭)瘘,占女性患儿的52.9%。目前IBD相关直肠阴道(前庭)瘘的治疗仍以手术治疗为主。男性的直肠尿道瘘较女性直肠阴道(前庭)瘘更为少见,目前文献中仅有数例成人的病例报道[82,83,84]。存在直肠阴道(前庭)瘘和直肠尿道瘘的VEO-IBD患儿往往同时伴有严重的直肠周围感染、尿路感染,在IBD活动期行瘘管切除术几乎不可避免的引起感染、复发,因此在IBD活动期推荐先行保护性肠造口,肠造口能够显著减轻肛周区域和尿道的细菌负荷,改善愈合条件,同时能显著提高二期行直肠阴道(前庭)瘘和尿道瘘修补术的手术成功率[35,36,37,38]。VEO-IBD相关的直肠阴道(前庭)瘘和直肠尿道瘘的根治手术应在通过药物或干细胞移植使肠道炎症充分控制的缓解期进行,手术方式需根据位置的高低、直肠炎症及瘢痕、是否伴发其他形式的肛周瘘管等情况制定个体化的手术方案。低位的直肠阴道(前庭)瘘、直肠炎及瘢痕较轻且无直肠狭窄,无其他肛门直肠周围瘘管的患儿可经肛门行瘘管切除,游离近端正常肠壁全层覆盖瘘口,以防止瘘管复发[85,86]。而高位的直肠阴道瘘、直肠炎或瘢痕严重、伴直肠狭窄、合并其他肛门直肠瘘的患儿建议行直肠切除肛门成形术,可采用前矢状入路或后矢状入路的手术方式[6,87]。对于缓解期IBD患儿是否在行直肠阴道瘘修补术的同时行肠造口术目前仍存在争议,推荐行保护性造口。直肠尿道瘘一般位于尿道球部,若无其他伴发的肛周病变可在造口保护的状态下先行经肛门瘘管切除,如瘘管复发或伴有直肠狭窄、其他瘘管等推荐行后矢状入路直肠切除术。
17.VEO-IBD活动期的直肠狭窄建议采用回肠造口来缓解梗阻症状,非手术治疗失败的直肠狭窄可在IBD疾病缓解后行后矢状入路直肠切除术。推荐等级:强烈推荐
直肠肛门狭窄可分为活动期的水肿性狭窄和缓解期的瘢痕性狭窄。在IBD活动期,由于直肠壁的炎症、水肿,单基因IBD患儿经常伴有直肠周围组织的感染、脓肿等,导致直肠腔受压狭窄从而引起低位肠梗阻症状。活动期的直肠狭窄建议采用回肠造口来缓解梗阻症状,同时有利于肠道炎症的控制。通过药物或干细胞移植等内科治疗,进入肠道炎症缓解期的患儿应再次评估直肠狭窄的程度、位置及范围,对于位置较低且不伴有瘘管等其他肛周病变的短段狭窄可首先尝试扩张治疗,扩张治疗失败、长段、位置较高的直肠狭窄可在疾病完全控制后6个月进行直肠切除术。由于这类患儿往往存在直肠周围瘢痕化严重,直肠周围可能存在瘘管、死腔、瘢痕组织和炎性肉芽组织,因此推荐采用后矢状入路直肠切除术[6]。这一术式能充分暴露直肠周围间隙,在切除直肠的同时可处理直肠周围瘘管、死腔等复杂情况,且对肛门括约肌的损伤较小,瘘管复发率低[88]。
18.造口闭合术前进行肠道炎症活动性、继发性肠道病变和肛周病变等全面评估,接受造血干细胞移植的患儿需进行血液学、免疫功能、移植排异等相关评估。推荐等级:强烈推荐
保护性肠造口术在控制感染和缓解炎症方面作用显著,VEO-IBD通过药物或干细胞移植达到缓解或痊愈后需行肠造口闭合术以恢复消化道的连续性[5,33]。造口闭合术后IBD复发是临床上较为关注的问题[89,90,91]。研究显示结肠镜检查和小肠CT或MRI对造口闭合后IBD复发有一定的预测价值,但目前关于VEO-IBD造口关闭的标准可借鉴的经验不多[92,93]。肠造口闭合前应进行多学科团队的评估,包括对肠道炎症活动性、继发性肠管病变、肛周病变的评估。肠道炎症活动性可通过血常规、C-反应蛋白、降钙素原等血液学指标和大便常规、潜血、钙卫蛋白等肠道局部炎症指标进行评估;继发性肠管病变主要通过肠镜和钡剂灌肠检查明确溃疡、狭窄、闭锁、炎性息肉等病变;肛周病变在肠道炎症控制后一部分可自行愈合,直肠尿道瘘和直肠阴道瘘多在肠造瘘后临床症状消失,但多不能自行愈合[76,77,78,79]。需注意瘘管较细时,肠镜、稀钡灌肠造影和排泄性尿路造影可能难以显示瘘管。研究显示内镜超声和MRI是最有价值的术前检查方法[94,95]。然而,对于既往存在明确直肠阴道瘘或尿道瘘的患儿,应在关造口前进行麻醉下经肛门检查[94,96]。另外,接受干细胞移植的患儿需进行相关血液学、免疫功能、排异等移植相关的评估。
19.肠狭窄切除吻合术作为缓解期VEO-IBD相关肠狭窄的首选术式。推荐等级:推荐
肠狭窄是IBD常见的并发症,在肠造口关闭术术中应对远端旷置肠管进行充分探查,尤其是既往存在穿孔、局灶性坏死等病变的患儿。尽管术前的肠镜或钡灌肠造影可排除部分肠狭窄,但仍有部分狭窄在术前难以被发现,因此术中应仔细检查肠壁瘢痕情况。肠狭窄的治疗包括狭窄成形术和切除吻合术,狭窄成形术在成人IBD相关肠狭窄中被广泛应用,但狭窄复发率高达28%[58]。儿童IBD相关肠狭窄的对照研究显示狭窄成形术比狭窄肠段切除吻合手术复发时间更早,复发率更高[59]。因此推荐狭窄肠段切除吻合术作为VEO-IBD相关肠狭窄的首选术式。
20.针对肛周潮湿相关性皮肤损伤,采用"局部清洁"和"保护皮肤"的护理原则。推荐等级:强烈推荐
长期或反复腹泻以及婴幼儿使用纸尿裤可导致患儿肛周较长时间暴露于尿液及粪便中。复杂肛瘘、直肠阴道(前庭)瘘、直肠尿道瘘、肛周脓肿、皮赘等肛周病变的存在可导致肛周皮肤持续接触尿液、粪便及分泌物。VEO-IBD患儿肛周往往并发有较为严重的潮湿相关性皮肤损伤(moisture-associated skin damage,MASD),严重者可表现为皮肤发红、破损、水肿、糜烂、感染等,肛周护理难度较大[97]。对患儿肛周、臀部、骶尾部及会阴部皮肤至少每天评估1次,或根据MASD严重程度及患儿情况进行调整。护理原则包括"局部清洁"和"保护皮肤"[98]。宜采用"免冲洗"的皮肤清洗剂,该类产品使用后皮肤待干速度快,可减少擦拭造成的皮肤损伤,或可使用清水清洁肛周皮肤并轻轻拍干。不宜使用会改变皮肤pH值的肥皂以及纹理结构粗糙易摩擦损伤皮肤的毛巾。清洁之后,喷洒或轻轻涂抹皮肤保护剂以在皮肤角质层与潮湿或刺激物之间形成阻隔层,促进皮肤修复,达到预防和治疗MASD的效果。怀疑有皮肤感染时,应及时向相关领域专家进行咨询。
21.警惕造口皮肤黏膜分离以及刺激性皮炎的发生,采用STOMA流程更换造口袋。推荐等级:强烈推荐
VEO-IBD患儿由于肠道本身的炎症、缝线反应、合并感染、营养不良、依从性差等原因,造口及造口周围皮肤并发症的发生率达27% ~ 54%[22]。皮肤黏膜分离是VEO-IBD患儿最常见的造口并发症,刺激性皮炎是VEO-IBD患儿最常见的造口周围并发症,与成人IBD造口相关并发症研究报道一致[99]。6岁以下的患儿往往配合度低,活动度大,皮肤娇嫩,抗粪便刺激能力弱。加之VEO-IBD患儿多行回肠造口术,而回肠造口由于粪便未经结肠重吸收水分,排泄物稀薄且含丰富的消化酶,对造口周围皮肤刺激大,容易诱发皮肤黏膜分离及刺激性皮炎[100]。术后1周是VEO-IBD患儿发生造口及造口周围皮肤并发症的高峰,刺激性皮炎DET评分(D:颜色改变;E:浸渍/溃疡;T:组织增生)的变化呈现先增后减的趋势,DET评分在第12天左右达到高峰,护理人员对造口及造口周围皮肤并发症应具有预见性并提早进行护理干预。成人研究表明,造口周围瘘管、造口周围肉芽肿以及坏疽性脓皮病可能归因于IBD活动,需要多学科团队共同诊疗[101]。在儿童人群中,VEO-IBD疾病活动导致的肠造口并发症需进一步探索和研究。
术前应重点评估患儿腹部拟开放造口区域的皮肤情况。择期手术时应由外科医生、造口师、达认知年龄的患儿以及家属共同行术前造口定位。向患儿及家属宣教造口相关知识、造口护理产品的作用及使用方法。术后根据STOMA流程更换造口袋,即选择合适的造口产品(set up the equipment)、移除造口袋(take off the pouch)、观察造口及周围皮肤(observe the stoma and skin around it)、测量造口并裁剪底盘开口(measure the stoma)和粘贴造口袋(apply the new pouch)。建议提供儿童造口延续性护理的咨询电话、护理门诊和外科门诊开诊时间,居家照护发生造口并发症时应及时咨询或来院就诊。护理计划需涵盖患儿及家属生活质量、家属照护需求及负担的评估和处理。
22.采用伤口评估三角对伤口进行评估,基于TIME原则行伤口床处理。推荐等级:强烈推荐
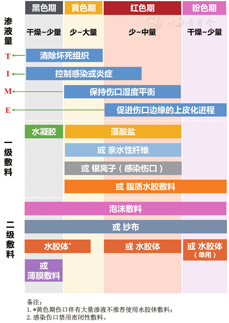
VEO-IBD患儿伤口并发症发生率达34.9%,多发生于术后7 ~ 14 d,以伤口感染和伤口裂开为主。造口的排泄物会污染及刺激伤口,而伤口的存在又会影响造口底盘的粘贴。一旦发生两者其一或共同发生并发症时,会互相影响导致进一步恶化。规律及规范的伤口评估尤为重要。可采用伤口评估三角对伤口进行评估,包括(1)伤口床评估(组织类型、渗出液、感染);(2)伤口边缘评估(浸渍、脱水、潜行、边缘增厚/卷起);(3)伤口周边皮肤评估(浸渍、表皮脱落、皮肤干燥、湿疹等)[102]。伤口并发症应以预防为主,对于存在发生伤口并发症危险因素的患儿,如C-反应蛋白升高(OR:1.40)、wPCDAI评分升高(OR:2.88)以及术前存在肠穿孔(OR:1.72),术后可预防性的使用水胶体敷料覆盖伤口以阻隔造口排泄物,避免排泄物污染伤口造成感染[22]。发生伤口并发症后,应基于TIME原则行伤口床处理,即清除坏死组织(tissue)、控制感染或炎症(infection or inflammation)、保持伤口湿度平衡(moisture)、促进伤口边缘的上皮化进程(edge)[103]。此外,还需根据伤口所处的不同时期合理选择敷料(图2)。伤口并发症需要多学科团队综合管理,应及时转介,共同处理。

共识制定首席专家:黄瑛,董岿然,陈劼
共识制定工作组核心成员:孙松,石杰如,余卓文
评审者(按姓氏汉语拼音排序):白玉作(中国医科大学附属盛京医院),陈功(复旦大学附属儿科医院),陈洁(浙江大学医学院附属儿童医院),陈劼(复旦大学附属儿科医院),陈競芳(复旦大学附属儿科医院厦门医院),陈晓飞(浙江大学医学院附属儿童医院),陈亚军(首都医科大学附属北京儿童医院),陈亚梅(上海市第十人民医院),董岿然(复旦大学附属儿科医院),钭金法(浙江大学医学院附属儿童医院),方莹(西安交通大学附属儿童医院),耿宪杰(河南省儿童医院),龚四堂(广州市妇女儿童医疗中心),黄瑛(复旦大学附属儿科医院),金忠芹(苏州大学附属儿童医院),李丹(上海市儿童医院),李小芹(河南省儿童医院),李中跃(浙江大学附属第四医院),刘志峰(南京医科大学附属儿童医院),马立霜(首都儿科研究所附属儿童医院),马丽丽(复旦大学附属儿科医院),马轶美(上海交通大学医学院附属上海儿童医学中心),梅红(华中科技大学同济医学院附属武汉儿童医院),任红霞(山西省儿童医院),沈淳(复旦大学附属儿科医院),石杰如(复旦大学附属儿科医院),孙梅(中国医科大学附属盛京医院),孙松(复旦大学附属儿科医院),唐维兵(南京医科大学附属儿童医院),汪健(苏州大学附属儿童医院),王朝霞(深圳市儿童医院),王丽波(吉林大学第一医院),吴捷(首都医科大学附属北京儿童医院),徐伟珏(上海市儿童医院),徐樨巍(北京清华长庚医院),许春娣(上海交通大学医学院附属瑞金医院),杨童玲(复旦大学附属儿科医院),游洁玉(湖南省儿童医院),余卓文(复旦大学附属儿科医院),张永红(河南省儿童医院),张中喜(复旦大学附属儿科医院厦门医院),赵新鲜(上海交通大学医学院附属仁济医院),郑珊(复旦大学附属儿科医院),钟微(广州市妇女儿童医疗中心),邹瑜(深圳市儿童医院),左伟(安徽省儿童医院)
所有作者均声明不存在利益冲突


























