
分析胰腺旁Castleman病的临床特点,提高对胰腺旁肿物认识,加强胰腺旁肿物鉴别诊断。
通过1例胰腺旁Castleman病例回顾国内外相关报道,分析发病原因,总结胰腺旁Castleman病的临床表现、术前诊断方法和治疗手段。
患者以左上腹隐痛为主要表现,实验室检查未见明显异常,影像学检查见胰腺上方富血供肿瘤,直径约3.5 cm,术中探查见一椭圆形红色实性包块紧密生长,术中冰冻提示反应性淋巴结增生,术后病理提示透明血管型Castleman病。
胰腺旁Castleman疾病的临床表现无明显特异性,术前诊断较为困难,极易误诊,CT、MRI、血管造影均可见富血供肿物,术前内镜超声引导下的细针抽吸或穿刺组织病理可协助诊断及鉴别诊断,手术切除效果好。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
Castleman病是罕见的淋巴增殖性疾病,可发生于全身,主要表现为无痛性淋巴结肿大。该病发病率低,临床诊断困难,易误诊,需引起重视。我院近期收治1例胰腺旁Castleman病,患者无特异性实验室检查,CT可见胰腺体部肿物,术中探查及术后病理确诊为胰腺旁Castleman病。现在通过分析该病的临床特点及诊疗经过,回顾国内外关于胰腺旁Castleman病的文献报道,提高临床对该病的认识。
患者女性,54岁,因"反复左上腹隐痛1年,发现胰腺占位1月"入院。患者于1年前开始无明显诱因出现左上腹间断性隐痛不适,疼痛无向他处放射,无恶心、呕吐,无长期腹泻、便秘,无长期发热、感冒等病史。入院前1月当地医院腹部彩超提示:胰腺区低回声,MR检查见"胰腺颈体部占位性病变,考虑胰岛细胞瘤可能"。入院后查体未见明显异常。实验室检查肝肾功能、电解质、血淀粉酶、血胰岛素、血糖、肿瘤指标均正常范围,HIV抗体阴性。影像学CT(图1A、图1B)、MRI(图1C)提示腺体部见一直径约3.5 cm肿物,动脉期均匀强化,血供丰富,密度高于胰腺组织。
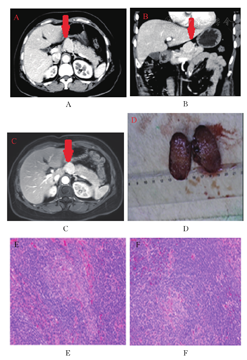

考虑患者无功能胰岛细胞瘤可能性大,行剖腹探查可见胰腺体部上方有一椭圆形红色实性包块紧密生长,肿物直径约3.5 cm,质地硬,有包膜,与胰腺组织界限清晰。手术完整切除包块,术中冰冻提示淋巴结反应性增生。术后标本提示淋巴结1个,镜下淋巴结节结构基本保存,皮质区淋巴滤泡及副皮质区淋巴细胞增生,滤泡生发中心萎缩,伴透明血管穿入现象,套区淋巴细胞同心圆状围绕生发中心呈"洋葱皮"样结构。免疫组化提示CD3及CD5(T细+),CD20(B细胞+),CD21(滤泡树突细胞阳性),CyclinD1(-),Ki-67(滤泡生发中心高表达)(图1D、图1E、图1F)。结合免疫组化,符合透明血管型Castleman病。患者术后恢复良好,1周后出院,术后左上腹隐痛症状未再出现,随访期间无复发。
Castleman病是一种原因不明、介于良恶性之间、以淋巴结肿大为特征的慢性多克隆淋巴组织增生疾病,最先由Castleman于1956年报道,后以Castleman病命名[1]。Castleman病一般好发于纵隔、宫颈、腹膜后、腋窝,近年来胰腺Castleman病偶有报道,但发生于胰腺旁病例极为少见[2]。Castleman病病理学分型可分为透明血管型、浆细胞型、混合型,按发病位置分型可分为局限型、多中心型[3]。Castleman病病因尚不明确,目前有报道证实与HIV、单纯疱疹病毒8型感染有关[4,5]。Musters等[6]证实,Castleman病的发病机制与白细胞介素6刺激T细胞和B细胞增殖密切相关。
本例胰腺旁Castleman病,临床表现及实验室检查无明显特异性,CT、MR可见胰腺体部动脉期明显均匀强化肿物,肿物密度或信号高于胰腺组织,与胰腺组织贴合紧密,但界限清晰。陈耀庭和许林峰[7]曾报道唯一1例行血管造影及栓塞治疗的胰腺旁Castleman病,造影过程提示肿物血供丰富,动脉早期显影,实质期见肿瘤引流静脉粗大,呈"抱球状"环绕肿瘤,造影后行血管栓塞治疗,3 d后行手术切除。我院报道患者CT影像较符合胰岛细胞瘤,但临床无低血糖表现,实验室检查血糖水平及胰岛素水平正常,误诊为无功能性胰岛细胞瘤。术中探查胰腺体部上方有一椭圆形红色实性包块紧密生长,肿物直径约3.5 cm,质地硬有包膜,与胰腺组织界限清晰,行术中冰冻提示淋巴结反应性增生,术后确诊为透明血管型Castleman病。
回顾国内外关于胰腺旁Castleman病的报道,女性患者居多,均为局限型Castleman病。临床表现多不典型,部分无明显症状。1例患者表现发热至39.9℃、乏力等全身症状[2]。部分患者表现为腹痛,甚至可放射至背部[7,8,9,10]。1例患者表现为右髂窝疼痛[11]。另1例患者以压迫症状如黄疸、纳差为主要表现[12]。实验室检查均无明显特异性。术前诊断大多数不明确,仅以腹部CT或MR检查可见局限性胰腺或胰腺旁肿物,极其容易误诊为无功能型胰岛细胞瘤或神经纤维瘤。Rhee等[3]等曾报道1例胰腺旁Castleman病患者行EUS-TCB,镜下见滤泡扩大,取而代之的是密集浸润的小而成熟的淋巴细胞,滤泡中心细胞消失,初步怀疑为低度、结外、边缘区b细胞淋巴瘤,根据对IgH基因重排的PCR研究发现该肿瘤具有多克隆模式。Talarico等[9]曾报道1例胰腺旁Castleman病,术前行EUS-FNA见成束的大小不等的淋巴样细胞及少数核质比例改变的罕见非典型细胞,无法明确诊断Castleman病。Khashab等[13]曾报道1例胰腺旁肿物患者,通过术前行EUS-FNA,细胞学涂片提示存在大小不一的和部分完整的淋巴滤泡,并有毛细血管透过;组织切片提示大量的淋巴滤泡具有典型的同心圆边缘的淋巴细胞,符合透明血管型Castleman病诊断。因此,笔者认为术前行EUS-FNA, EUS-TCB可协助鉴别诊断恶性肿瘤,但多因取材局限、肿物位置等因素较难于术前明确诊断Castleman病。局限型Castleman病的首选治疗仍然是手术切除,肿物多有包膜,完整切除机会大。术后病理分型中透明血管型居多,术后预后良好,随访均无复发。
总之,Castleman病的发病率本身较低,单发于胰腺旁的Castleman病更为少见。术前诊断困难,术前仅凭临床表现、实验室检查、影像学检查容易误诊为胰腺肿物如无功能型胰岛细胞瘤、神经纤维瘤等,临床需提高警惕。术前EUS-FNA、EUS-TCB可协助诊断,但因肿瘤的位置、取材较少等因素,鉴别恶性肿瘤诊断的意义更大。术前血管造影可协助明确肿物血供,介入治疗疗效尚不明确。手术切除是胰腺旁Castleman病的首要治疗方案,结合术中冰冻可明确肿物性质,同时避免行扩大手术。
本人与其他作者宣称没有任何利益冲突,未接受任何不当的职务或财务利益



























