
探讨伴小纤维受损周围神经病表皮内神经纤维密度(IENFD)与临床、神经电生理的关系,评价13项小纤维神经病和症状问卷(SFN-SIQ)、下肢神经症状评分(NSS[LL])对小纤维神经病(SFN)的诊断价值。
选取2012年12月20日至2014年7月14日于解放军总医院神经内科诊治的34例伴小纤维受损的周围神经病(PN)患者,进行SFN-SIQ、NSS[LL]、下肢神经功能评分(NDS[LL]),并行神经电生理检查及皮肤活检。采用相应统计学方法分析IENFD与各量表评分及电生理参数的关系,评价SFN-SIQ、NSS[LL]对小纤维病变的诊断价值。
根据临床特点,分为2组,SFN组16例,混合性PN组18例。根据IENFD国际标准参考值,13例可诊断伴小纤维受损的周围神经病;IENFD与SFN-SIQ中度相关(r=0.437, P=0.012),与NSS[LL]边缘相关(r=0.334, P=0.062),且SFN-SIQ、NSS[LL]对小纤维病变的诊断价值中等,评分为6分时分别对应的正确诊断指数最大;混合性周围神经病组NDS[LL]评分明显高于小纤维病变组(t=–5.605,P<0.001);IENFD异常组NSS[LL]评分明显高于正常组(t=–2.047,P=0.049);IENFD异常组与正常组电生理参数差异无统计学意义。
建立中国人群IENFD正常参考值对于小纤维神经病的诊断至关重要;SFN-SIQ、NSS[LL]有望成为小纤维神经病初筛、病情随访、疗效观察的有效手段。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
周围神经病(PN)常存在小神经纤维受累[1],可表现为单纯的小纤维神经病(SFN)和同时累及大、小纤维的混合性周围神经病[2]。SFN是指主要累及薄髓和无髓纤维而大纤维不受累或很少受累的周围神经病[1]。皮肤活检,可直接观察神经纤维的数目和形态[3],是迄今诊断SFN的金标准[1,2]。小纤维损伤临床表现为疼痛、麻木、感觉异常及自主神经症状等,疼痛性质多为烧灼痛、针刺痛、电击痛等[1]。13项小纤维神经病和症状问卷(SFN-SIQ)可评估SFN感觉和自主神经症状[4]。下肢神经症状评分(neuropathy symptom score [lower limb], NSS[LL])和下肢神经功能评分(neuropathy disability score [lower limb], NDS[LL])可分别评价周围神经病的症状和体征。目前国内尚罕见将皮肤活检和临床问卷及量表相结合进行的研究。本研究对解放军总医院神经内科34例伴小纤维受损周围神经病临床、电生理和表皮内神经纤维密度(IENFD)的关系进行探讨,并评价SFN-SIQ、NSS[LL]对SFN的诊断价值。
选取2012年12月20日至2014年7月14日于解放军总医院神经内科诊治的34例周围神经病患者,均有小纤维受损的感觉和(或)自主神经症状。其中男20例,女14例,年龄22~77岁,平均(54±16)岁。所有患者进行详细的病史采集、神经系统查体及辅助检查以查询病因。实验室检查包括血、尿、便常规,红细胞沉降率,C反应蛋白,血脂,空腹血糖,糖化血红蛋白,糖耐量试验(OGTT),肝、肾功能,甲状腺功能,叶酸、维生素B12,肿瘤标志物,类风湿三项,抗ENA六项,抗核抗体五项。
根据患者临床症状及体征分为SFN组和混合性周围神经病组。分类标准:(1)SFN:感觉症状包括疼痛、麻木、烧灼感、针刺感、冰冷感、电击感、紧箍感、触诱发痛等;自主神经症状如多汗、少汗、眼干、口干、心悸、面部潮红、皮温改变、性功能障碍、体位性低血压、胃肠动力障碍等;体检伴或不伴痛温觉及轻触觉减退。(2)大纤维病:足趾本体感觉减退,踝及以上振动觉减退,远端肌无力伴肌萎缩,普遍的腱反射减低。(3)若同时累及大小纤维则归为混合性周围神经病[2]。本研究获解放军总医院伦理委员会批准,所有患者均签署知情同意书。
(1)对所有患者进行SFN-SIQ评估,评价SFN的感觉和自主神经症状[4,5]。包括:①泌汗功能改变;②腹泻;③便秘;④泌尿系统症状如尿急、尿失禁等;⑤眼干;⑥口干;⑦体位性低血压;⑧心悸;⑨潮热、潮红;⑩触诱发痛;⑪足烧灼感;⑫接触床单后感觉异常;⑬不宁腿。每项症状评分标准:从未出现=0分,有时出现=1分,经常出现=2分,总是出现=3分。评分越高,表明小纤维病变的症状越重。(2)对所有患者行NSS[LL]评分[6,7],包括:麻木、冷热觉、针刺觉、接触床单后感觉异常、烧灼痛、刺痛、钝痛。每项评分标准:无=0分,有时=1分,经常=2分,夜间好发=3分,总共21分。评分越高,表明下肢神经症状越重。(3)对所有患者行NDS[LL]评分[6,8],包括:踇趾、足背、外踝、胫骨前部、膝5个部位轻触觉(棉签)、针刺觉(针)、振动觉(128 Hz音叉)、冷觉(音叉)以及双侧踝反射、膝反射。总共28分,1~5分为轻度,6~16分为中度,17~28分为重度。(4)对所有患者行10分制视觉模拟评分(VAS)。
使用Medtronic公司Keypoint肌电图仪,肢体复温至34 ℃以上,对所有患者进行神经传导检查。选病变较重侧检查,若两侧严重程度大致相当,则选择右侧进行检查。
所有患者于病变较重侧(若两侧病变程度相当,则选取右侧)外踝上方10 cm处,利多卡因局部麻醉下使用直径为3 mm皮肤活检环钻(Acu-punch, Acuderm)钻取小块皮肤。皮肤标本于2%福尔马林-赖氨酸高碘酸钠溶液中进行固定,使用多克隆兔抗人蛋白基因产物9.5(protein gene product 9.5, PGP9.5)(Chemicon, Temecula, CA, USA; 1∶1 300)进行免疫组织化学染色标记皮肤神经纤维[9]。
计数表皮内神经纤维时,以每根从真皮神经丛发出穿过基底膜进入表皮的神经计数为1根[2]。表皮层长度使用Image Pro Plus 6.0测量(Media Cybernetics, Silver Spring, MD),由此可计算出表皮内神经纤维密度(根/mm)。IENFD低于国际标准参考值第5百分位数时被认为异常[10]。所有标本由对患者临床资料不知情的同一人计数和测量。
使用SPSS 19.0统计软件进行数据分析。采用偏相关分析IENFD与其他指标的相关性,对年龄、性别进行控制;采用ROC分析评价SFN-SIQ、NSS[LL]对小纤维病变的诊断价值;两组均数间的比较采用独立样本t检验,数据采用 ±s的形式表示;P<0.05差异有统计学意义。
±s的形式表示;P<0.05差异有统计学意义。
34例中16例仅有小纤维病变的症状/体征(SFN组),18例为混合性PN。其中糖耐量异常11例,特发性PN 10例,2型糖尿病3例,酒精中毒2例,副肿瘤综合征2例,吉兰巴雷综合征1例,未分化结缔组织病1例,慢性炎症性脱髓鞘性多发性神经根神经病1例,脂质沉积性肌病1例,腓骨肌萎缩症1例,多发性骨髓瘤1例。34例患者VAS评分(3.7±3.8)分,SFN-SIQ评分(6.2±3.5)分,NSS[LL]评分(6.2±2.7)分,NDS[LL]评分(5.4±3.6)分。
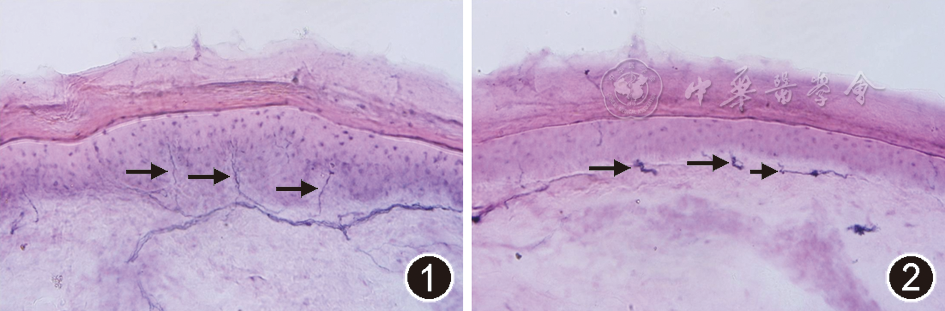

34例中13例神经传导检查正常,21例异常;SFN组12例正常,4例异常。与国际标准参考值相比,13例IENFD异常,其中糖耐量异常5例,酒精中毒2例,特发性SFN 2例,2型糖尿病1例,吉兰-巴雷综合征1例,遗传性感觉运动性周围神经病1例,脂质沉积性肌病1例;21例正常;单纯的SFN共5例。SFN组6例异常,10例正常,该组单纯的SFN共4例,包括糖耐量异常2例,酒精中毒1例,特发性SFN 1例。
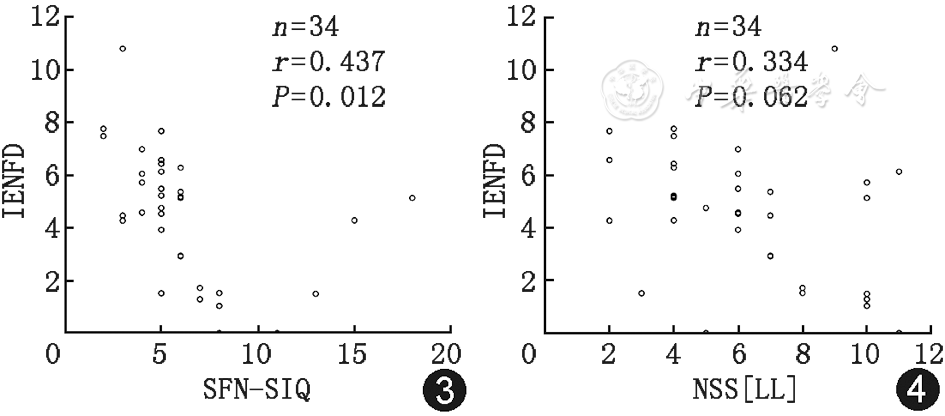
其中IENFD与SFN-SIQ偏相关系数r=0.437,P=0.012,差异有统计学意义,两者呈中度相关(图3);IENFD与NSS[LL]偏相关系数r=0.334,P=0.062,两者呈边缘相关(图4);IENFD与其他量表评分无相关性。

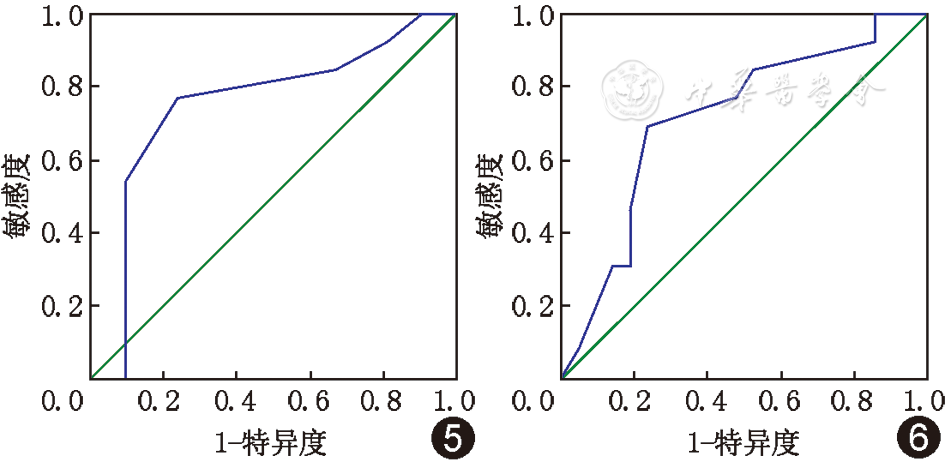
SFN-SIQ诊断小纤维病变的ROC曲线下面积为0.753,P=0.014,差异有统计学意义,利用SFN-SIQ诊断小纤维病变的准确性中等(图5),分界点6对应的正确诊断指数最大;NSS[LL]诊断小纤维病变的ROC曲线下面积为0.712,P=0.04,差异有统计学意义,利用NSS[LL]诊断小纤维病变的准确性中等(图6),分界点6对应的正确诊断指数最大。

混合性PN组IENFD略低于SFN组,差异无统计学意义;混合性PN组NDS[LL]评分明显高于SFN组,P<0.001差异有统计学意义(表1)。
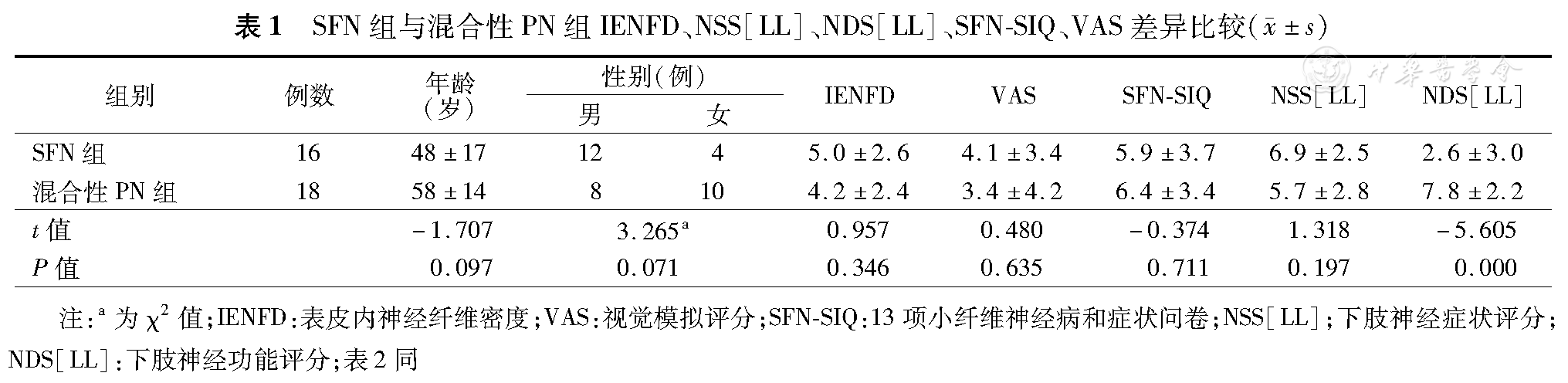
SFN组与混合性PN组IENFD、NSS[LL]、NDS[LL]、SFN-SIQ、VAS差异比较( ±s)
±s)
SFN组与混合性PN组IENFD、NSS[LL]、NDS[LL]、SFN-SIQ、VAS差异比较( ±s)
±s)
| 组别 | 例数 | 年龄(岁) | 性别(例) | IENFD | VAS | SFN-SIQ | NSS[LL] | NDS[LL] | ||
|---|---|---|---|---|---|---|---|---|---|---|
| 男 | 女 | |||||||||
| SFN组 | 16 | 48±17 | 12 | 4 | 5.0±2.6 | 4.1±3.4 | 5.9±3.7 | 6.9±2.5 | 2.6±3.0 | |
| 混合性PN组 | 18 | 58±14 | 8 | 10 | 4.2±2.4 | 3.4±4.2 | 6.4±3.4 | 5.7±2.8 | 7.8±2.2 | |
| t值 | –1.707 | 3.265a | 0.957 | 0.480 | –0.374 | 1.318 | –5.605 | |||
| P值 | 0.097 | 0.071 | 0.346 | 0.635 | 0.711 | 0.197 | 0.000 | |||
注:a为χ2值;IENFD:表皮内神经纤维密度;VAS:视觉模拟评分;SFN-SIQ:13项小纤维神经病和症状问卷;NSS[LL];下肢神经症状评分;NDS[LL]:下肢神经功能评分;表2同
IENFD正常组中,10例仅有小纤维症状,11例(52.4%)有大纤维症状;IENFD异常组中,6例仅有小纤维症状;7例(53.8%)有大纤维症状。IENFD异常组NSS[LL]评分明显高于正常组,P=0.049差异有统计学意义(表2)。IENFD与各项电生理参数差异均无统计学意义(表3)。
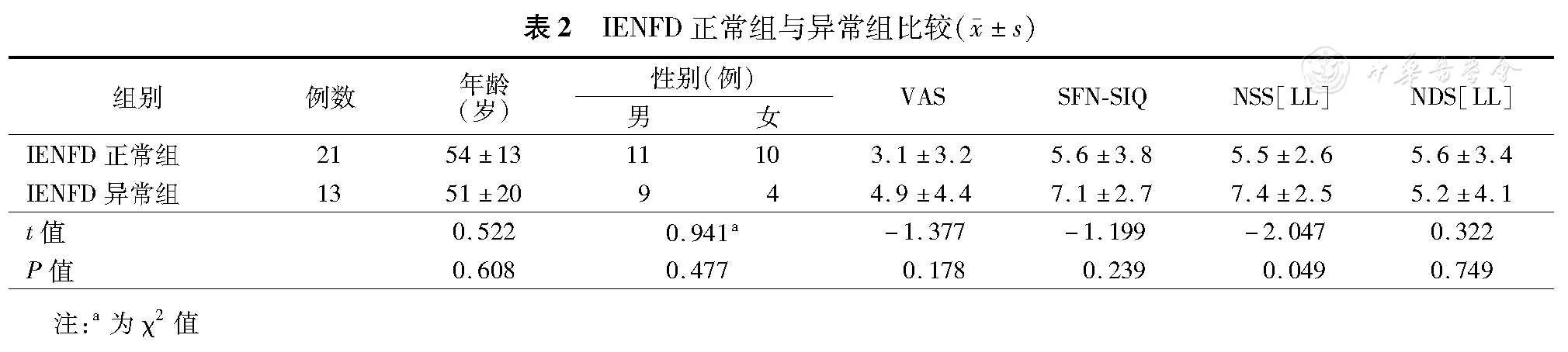
IENFD正常组与异常组比较( ±s)
±s)
IENFD正常组与异常组比较( ±s)
±s)
| 组别 | 例数 | 年龄(岁) | 性别(例) | VAS | SFN-SIQ | NSS[LL] | NDS[LL] | ||
|---|---|---|---|---|---|---|---|---|---|
| 男 | 女 | ||||||||
| IENFD正常组 | 21 | 54±13 | 11 | 10 | 3.1±3.2 | 5.6±3.8 | 5.5±2.6 | 5.6±3.4 | |
| IENFD异常组 | 13 | 51±20 | 9 | 4 | 4.9±4.4 | 7.1±2.7 | 7.4±2.5 | 5.2±4.1 | |
| t值 | 0.522 | 0.941a | –1.377 | –1.199 | –2.047 | 0.322 | |||
| P值 | 0.608 | 0.477 | 0.178 | 0.239 | 0.049 | 0.749 | |||
注:a为χ2值
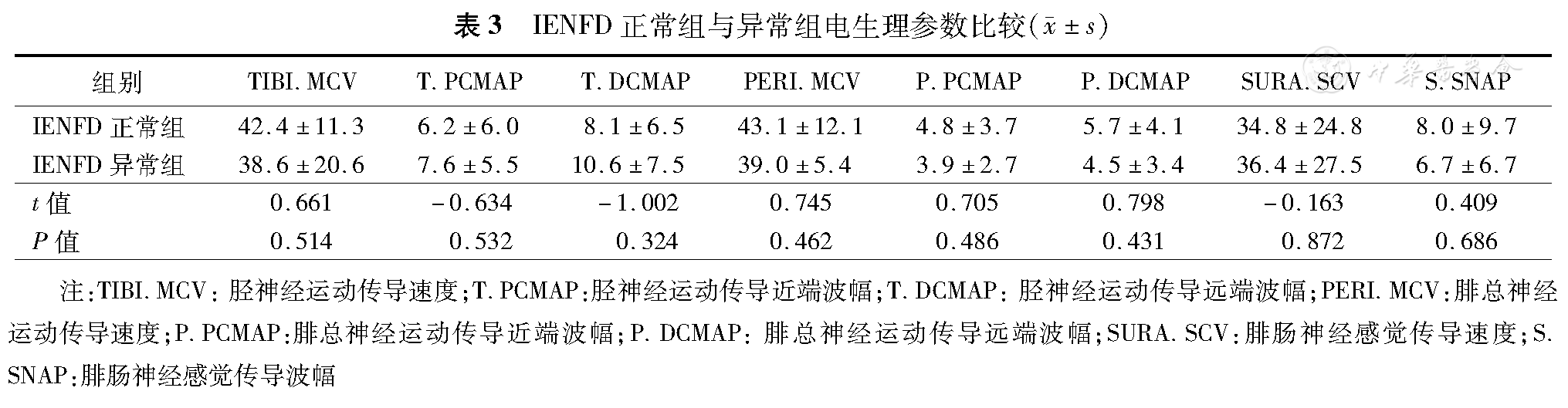
IENFD正常组与异常组电生理参数比较( ±s)
±s)
IENFD正常组与异常组电生理参数比较( ±s)
±s)
| 组别 | TIBI.MCV | T.PCMAP | T.DCMAP | PERI.MCV | P.PCMAP | P.DCMAP | SURA.SCV | S.SNAP |
|---|---|---|---|---|---|---|---|---|
| IENFD正常组 | 42.4±11.3 | 6.2±6.0 | 8.1±6.5 | 43.1±12.1 | 4.8±3.7 | 5.7±4.1 | 34.8±24.8 | 8.0±9.7 |
| IENFD异常组 | 38.6±20.6 | 7.6±5.5 | 10.6±7.5 | 39.0±5.4 | 3.9±2.7 | 4.5±3.4 | 36.4±27.5 | 6.7±6.7 |
| t值 | 0.661 | –0.634 | –1.002 | 0.745 | 0.705 | 0.798 | –0.163 | 0.409 |
| P值 | 0.514 | 0.532 | 0.324 | 0.462 | 0.486 | 0.431 | 0.872 | 0.686 |
注:TIBI.MCV:胫神经运动传导速度;T.PCMAP:胫神经运动传导近端波幅;T.DCMAP:胫神经运动传导远端波幅;PERI.MCV:腓总神经运动传导速度;P.PCMAP:腓总神经运动传导近端波幅;P.DCMAP:腓总神经运动传导远端波幅;SURA.SCV:腓肠神经感觉传导速度;S.SNAP:腓肠神经感觉传导波幅
皮肤活检是诊断SFN的金标准[1,2],本研究中,与国际标准参考值[10]比较,13例患者可明确诊断为伴有小纤维受损的周围神经病,其中糖耐量异常占38.5%,所占比例最大,与其他研究相符合[11]。本研究中有一例脂质沉积性肌病,分组标准符合混合性PN组,但神经传导检查正常,提示无大纤维受累,考虑肌无力、腱反射减退等临床特点为肌肉疾病所致;其临床表现有痛觉过敏,该患者同时伴有高脂血症;有研究表明,除糖耐量异常外,代谢综合征的其他组分,如血脂异常、肥胖,均为SFN的危险因素[12]。血脂异常在特发性周围神经病中的比例升高[12],考虑该例SFN病因可能为血脂异常或存在其他导致小纤维损伤的潜在病因。本研究进行了严格的病因筛查,但在4例单纯SFN中,有1例未找到明确病因。既往文献报道,SFN可能在原发病明确之前出现,40%~50%特发性SFN被证实为糖耐量异常相关SFN[11],因此,对该类病例应定期随访,如复查OGTT,观察其是否有糖耐量异常。此外,由于SFN可能是晚发型Fabry病的唯一表现,对于特发性SFN,应考虑Fabry病的可能[13]。特发性SFN还与编码电压门控钠通道的SCN9A、SCN10A突变有关[14]。
本研究所纳入研究对象均有小纤维病变的临床表现,但仅13例IENFD异常,可能是由于以国际标准参考值第5百分位数作为诊断标准有较高的特异性(95%~97%),但敏感度较低(35%~45%)[15]。此外,泰国人群IENFD是美国人群的2~3倍[16]。由此可推断,IENFD不但与年龄、性别密切相关[10],还可能与种族、地域等有关,同样作为黄种人的中国人群IENFD可能比西方人群高;因此,在中国人群中募集健康志愿者,建立我国IENFD正常参考值范围对于明确诊断至关重要。
SFN-SIQ包括多种小纤维病变的感觉和自主神经症状[4,5]。SFN-SIQ曾用于IENFD与生活质量相关性的研究,作为评价小纤维病变症状的一个手段[4];相似问卷还曾用于一项关于结节病的研究,在伴和不伴SFN的结节病患者中,其SFN-SIQ差异有统计学意义[5],从而说明SFN-SIQ在评价是否存在小纤维受损方面有一定价值。皮肤神经活检计算IENFD过程复杂,耗时较长,国内外仅少数实验室可进行皮肤活检免疫组化染色,而SFN-SIQ无创,实施方便,可以有效解决不能将小纤维病变症状量化评估这一问题,可以作为SFN初筛、病情随访、疗效观察的有效方法,且国内尚未有将两者相结合进行的研究。此外,我们采用ROC曲线分析SFN-SIQ对小纤维病变的诊断价值,寻找最佳诊断分界点。本研究发现,IENFD与SFN-SIQ中度相关,ROC曲线分析表明SFN-SIQ诊断SFN的准确性中等,其诊断最佳分界点为6分。NSS[LL]用于评价周围神经病,如糖尿病周围神经病[6,7],IENFD与NSS[LL]边缘相关,ROC曲线分析表明NSS[LL]诊断SFN的准确性中等,其诊断最佳分界点为6分。本研究发现SFN-SIQ与NSS[LL]对SFN的诊断有一定价值,并明确了其诊断最佳分界点,这在国内外尚属首次。SFN-SIQ与NSS[LL]有潜质作为SFN的初筛手段,但尚需大样本研究验证。
IENFD正常组与异常组各项电生理参数均无差异。其原因为合并大纤维症状者在两组中比例相当:IENFD正常组中,52.4%有大纤维症状;IENFD异常组中,53.8%有大纤维症状。这一结果表明小纤维与大纤维损伤的严重程度并不平行。日本一项研究表明IENFD与神经传导速度相关[17],而另一项研究表明IENFD与神经传导速度无相关关系[18]。国内外研究结果不统一可能与疾病诊断水平、纳入对象病情轻重、不同病因以及不同样本量有关。同时,本研究也说明以IENFD作为小纤维损伤的标志、神经传导检查作为大纤维损伤的标志时,两者之间并不一定存在严重程度或时间上的相关性。这提示在全面评价周围神经功能时,两种针对不同类型纤维的检查方法缺一不可。
本研究可进一步扩大样本量,将研究对象按病因分类,研究单一病种IENFD与临床特点及神经电生理的关系。此外,通过结合接触性热痛诱发电位(CHEPs)[1,19]、皮肤交感反应(SSR)以及定量发汗轴索反射(QSART)[1]等检查方法,研究与SFN-SIQ、NSS[LL]等临床量表相关性,以期寻找小纤维受损更直观、敏感、特异的临床筛查手段,早期诊断,早期干预。



























