
用MDA-MB-231人乳腺癌细胞悬液及移植瘤组织块分别建立裸鼠乳腺癌淋巴转移模型。
雌性BALB/C裸鼠12只,5周龄,随机分成A、B两组,A组为细胞悬液组,共7只裸鼠,B组为移植瘤组织块组,共5只裸鼠。将MDA-MB-231细胞悬液各0.1 ml分别注射于A组裸鼠的右侧第2对乳腺脂肪垫下,成瘤2周后,切取2只裸鼠的原位肿瘤种植于B组裸鼠的右侧第2对乳腺脂肪垫下,A组其余5只裸鼠继续饲养。A、B两组均于接种后第6周处死,解剖裸鼠后切取原位肿瘤及腋窝肿大淋巴结进行病理检查。
①A组裸鼠种植后第7天,成瘤率为7/7只,B组裸鼠种植后第5天,成瘤率为5/5只;②两组裸鼠原位肿瘤的体积差异有统计学意义(P=0.023),移植瘤组织块组的肿瘤体积>细胞悬液组;③解剖后,A组有3只裸鼠右侧腋窝各检出1枚肿大淋巴结,淋巴结肿大率为3/5只,B组有1只裸鼠右侧腋窝检出1枚肿大淋巴结,淋巴结肿大率为1/5只,两组裸鼠腋窝淋巴结肿大率差异无统计学意义(P=0.524);④病理学检查,两组裸鼠原位肿瘤均为浸润性导管癌,A组肿大淋巴结均为反应增生性,B组为转移性。
原位种植MDA-MB-231移植瘤组织块建立裸鼠乳腺癌淋巴转移模型,为研究乳腺癌淋巴转移机制提供可行工具。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
乳腺癌是恶性肿瘤,随着医疗水平的发展,乳腺癌的诊断和治疗技术有所提高,但乳腺癌的病死率仍较高[1],主要是由于转移的发生。据统计,仅患有乳腺癌局部病灶的患者,5年生存率达85%,而伴有转移的乳腺癌患者,5年生存率为23%[2]。乳腺癌常转移至淋巴结,决定乳腺癌患者预后的主要相关因素是有无腋窝淋巴结转移[3],但目前淋巴结转移机制尚不十分清楚,而且乳腺癌患者是否有腋窝淋巴结转移决定其手术方式和预后判断,为了更好的研究乳腺癌淋巴转移机制,建立乳腺癌淋巴结转移模型是必要的。本研究将用MDA-MB-231乳腺癌细胞悬液及移植瘤组织块分别种植于裸鼠乳腺脂肪垫建立乳腺癌淋巴转移模型,旨在探讨一种合适有效的乳腺癌淋巴转移模型,为研究乳腺癌淋巴转移机制提供重要工具。
雌性BALB/C裸鼠12只,4周龄,体重17~20 g,购于宁夏医科大学动物实验中心,动物许可证编号:SCXK(宁)2011-0001,裸鼠适应性饲养于无特定病原体(SPF)环境1周,实验前按体重从小到大、顺序分成A、B两组并进行编号,A组为细胞悬液组,共7只裸鼠,B组为移植瘤组织块组,共5只裸鼠。
(1)试剂:RPMI-1640培养液(美国HyClone公司,批号NZC1097)、胎牛血清(澳大利亚Gibco公司,批号NY14072)、磷酸盐缓冲液PBS(美国HyClone公司,批号NZD1123)、0.25%胰蛋白酶(美国HyClone公司,批号SH40003-12)、异氟烷、碘酒。(2)器材:离心机(北京医用离心机厂,型号LD4-2)、HF90/HF240CO2培养箱(德国Heal Force公司,型号HF-90)、倒置显微镜(日本OLYMPUS公司,型号CX51)、无菌超净台(德国Heal Force公司,型号HFSAFE-1200)、吸管、离心管、分装瓶、1 ml注射器、手术切开包、缝合线、冰袋、卡尺。
(1)A组裸鼠进行异氟烷吸入麻醉,四肢固定,选择裸鼠右侧第2对乳腺进行接种,手术区域用碘酒消毒,乳头旁切开一个4~5 mm切口,暴露乳腺脂肪垫,分别注射0.1 ml传代培养的MDA-MB-231细胞悬液(宁夏医科大学总医院医学实验中心提供)后缝合切口,细胞浓度为1×107个/0.1 ml。(2)A组裸鼠成瘤2周后,切取2只裸鼠的原位肿瘤,选择移植瘤新鲜鱼肉样组织,剪成直径2~3 mm的碎块,置于盛有PBS的器皿中,冰上放置,准备接种于B组裸鼠,其余5只A组裸鼠继续饲养。(3)B组裸鼠同样暴露乳腺脂肪垫,将准备好的移植瘤组织块分别种植于乳腺脂肪垫下,缝合切口,术后继续无菌饲养。(4)大体观察:观察接种区是否形成肿瘤,腋窝是否能触及肿大淋巴结,皮肤有无溃烂,裸鼠的活动状态及生长情况有无异常。(5)病理检查:两组裸鼠均于接种后第6周,解剖取得原位肿瘤和肿大淋巴结进行HE染色病理检查。
采用SPSS 17.0统计软件进行数据分析,所有数据以 ±s表示,比较A、B两组的原位肿瘤块体积差异采用配对设计t检验,比较两组裸鼠腋窝淋巴结肿大率采用四格表资料的Fisher确切概率法,均以P<0.05为差异有统计学意义。
±s表示,比较A、B两组的原位肿瘤块体积差异采用配对设计t检验,比较两组裸鼠腋窝淋巴结肿大率采用四格表资料的Fisher确切概率法,均以P<0.05为差异有统计学意义。
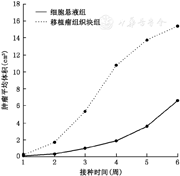
A组裸鼠种植后第7天,成瘤率7/7只,B组裸鼠种植后第5天,成瘤率5/5只;两组裸鼠成瘤后于接种部位均可见一个白色小结节,质略硬,随着种植时间的延长,肿瘤体积逐渐增大,肿瘤表面出现溃烂,以移植瘤组织块组为明显;两组裸鼠右侧腋窝均未触及肿大淋巴结。实验结束前所有裸鼠无死亡、生长状态良好。用卡尺每周测量两组裸鼠肿瘤块的长径a、短径b,按公式V=4/3πab2统计肿瘤体积,两组原位肿瘤块体积差异有统计学意义(P=0.023),移植瘤组织块组肿瘤体积>细胞悬液组。第1~6周,细胞悬液组肿瘤体积每周分别为(0.010±0.003)、(0.254±0.020)、(0.962±0.032)、(1.848±0.290)、(3.561±0.942)、(6.578±1.341) cm3;移植瘤组织块组肿瘤体积每周分别为(0.141±0.038)、(1.663±0.813)、(5.379±2.490)、(10.795±4.994)、(13.751±5.541)、(15.442±6.927) cm3(图1)。

两组原位肿瘤解剖大体观均为结节状,边界不整,同周围组织无粘连,移植瘤组织块组肿瘤内部坏死范围>细胞悬液组;A组有3只裸鼠右侧腋窝各检出1枚肿大淋巴结,淋巴结肿大率为3/5,B组有1只裸鼠右侧腋窝检出1枚肿大淋巴结,淋巴结肿大率为1/5,两组裸鼠腋窝淋巴结肿大率差异无统计学意义(P=0.524)。镜下检查,两组肿瘤细胞多呈卵圆形,弥漫分布,细胞核大、深染,胞质丰富、淡染,核质比约1∶2,核异型性显著,癌细胞周围可见散在淋巴细胞浸润,诊断为浸润性导管癌;A组肿大淋巴结均为反应增生性,淋巴结正常形态存在,可见生发中心,无肿瘤细胞侵袭,B组肿大淋巴结为转移性,淋巴结正常形态消失,淋巴细胞减少,由大量肿瘤细胞取代,肿瘤细胞类型与原始肿瘤细胞一致(图2)。


肿瘤转移模型建立有2种方法:(1)实验性转移模型:将癌细胞直接注射于体循环,这些模型转移发生快;(2)自发性转移模型:将肿瘤组织或肿瘤细胞原位或异位种植[4]。实验性转移模型的主要缺点是它不能表明转移过程的早期阶段,而只有器官浸润,所以不能代表真实的转移过程[5]。而且对于裸鼠乳腺癌转移模型,通过鼠尾静脉注射肿瘤细胞主要出现肺转移[6],通过心腔注射主要出现骨转移[7],不是非常适用于裸鼠乳腺癌淋巴转移的研究。自发性转移模型中,异位种植不能模拟原始肿瘤的微环境和相应的器官转移[5]。原位种植则可以较好模拟肿瘤血管分布、组织学、基因表达谱、化疗反应、转移情况等[8]。
原位种植模型中种植方法主要有细胞悬液、新鲜组织块、组织块悬液、移植瘤。目前关于肿瘤转移模型建立的实验研究报道较多,而专门报道乳腺癌淋巴转移模型建立的文章并不多见。Lee等[9]将MDA-MB-435乳腺癌细胞悬液注射于5~6周雌性SCID鼠的第2对乳腺脂肪垫内,12~13周后从淋巴结转移结节中培养得到细胞亚系LN435后再次原位种植,结果腋窝淋巴结转移率达100%。Vantyghem等[10]将转移能力低的MDA-MB-468乳腺癌细胞原位种植于8只7~8周雌性裸鼠第2对乳腺脂肪垫下,接种16周后,8只裸鼠中有1只出现肺转移,将转移结节重新培养得到细胞468LN再次原位种植后,原始肿瘤生长增快、淋巴结转移率显著提高。上述两位学者的研究均是用乳腺癌细胞接种成瘤后的转移结节培养新的细胞系再原位种植,观察乳腺癌淋巴结转移情况。本研究用MDA-MB-231乳腺癌细胞悬液及移植瘤组织块分别原位种植于裸鼠乳腺脂肪垫,结果表明注射细胞悬液比种植移植瘤组织块的成瘤时间晚,肿瘤体积小,中心坏死少,表面溃疡出现晚,腋窝淋巴结肿大率较高,但无转移性淋巴结发生,而种植移植瘤组织块后检出转移性淋巴结,说明在研究乳腺癌淋巴结转移方面,移植瘤组织块法优于细胞悬液法。
有研究表明,将人乳腺癌细胞注射于NSG(NOD scid gamma)小鼠体内比注射于裸鼠和NOD/SCID鼠(杂交双突变小鼠)体内后的转移率高,可能是由于NSG鼠为B细胞、T细胞、NK细胞同时缺陷,而裸鼠仅有T细胞缺陷,NOD/SCID鼠保持NK细胞活性,说明宿主的免疫环境在一定程度上决定人乳腺癌细胞的转移能力[11]。本研究选择裸鼠,裸鼠无胸腺,缺乏成熟T细胞的功能,淋巴细胞减少,可有发育不全的初级淋巴滤泡和不成熟的浆细胞,而研究表明人类肿瘤异种种植于裸鼠后,可部分激活裸鼠的免疫反应系统,大部分裸鼠会出现发育好的初级淋巴滤泡、浆细胞增生[12]。本研究中虽然种植移植瘤组织块后,裸鼠腋窝出现转移性淋巴结,但转移率低,仅有1/5,可能与裸鼠自身的免疫缺陷程度低或肿瘤促使其免疫反应系统部分激活有关;注射乳腺癌细胞悬液后,出现腋窝淋巴结反应增生性现象,可能是肿瘤刺激的结果,如果延长接种时间,也许会出现转移性淋巴结。
裸鼠乳腺癌淋巴结转移不易发生,而且裸鼠淋巴结较小,即使有肿大淋巴结的出现,肉眼很难发现,需要解剖才能检出,近年来,有学者采用辅助技术来观察裸鼠的淋巴结,如Wu等[13]用绿色荧光蛋白转染乳腺癌细胞4T1后接种于裸鼠侧腹皮下,有助于淋巴结的定位和检出。在研究一些物质对乳腺癌淋巴结转移的影响时,有学者将人乳腺癌细胞BT-474注射于5~6周雌性裸鼠侧腹皮下,淋巴结转移率为1/11,而如果在种植肿瘤细胞前48 h于裸鼠体内注射合成孕激素后,淋巴结转移率提高到8/11[14],或许我们可以利用诸如此类促进乳腺癌淋巴结转移的物质建立乳腺癌淋巴转移模型。
原位种植MDA-MB-231移植瘤组织块可以成功建立裸鼠乳腺癌淋巴转移模型,同时,我们可以继续探讨新的辅助方法来建立高效的乳腺癌淋巴转移模型,为研究乳腺癌淋巴转移机制提供重要工具。



























