
探讨血清游离三碘甲状腺原氨酸(FT3)对接受心脏再同步化治疗(CRT)的心力衰竭(心衰)患者预后的评估价值。
回顾性分析阜外医院2010年1月至2014年12月首次行CRT植入的202例心衰患者临床资料和电话随访资料。定义随访终点为全因死亡(包括心脏移植)和心衰再住院。根据入院FT3三分位水平将患者分为FT3≤4.08 pmol/L(67例)、4.09~4.71 pmol/L(68例)和> 4.71 pmol/L(67例)3组。Kaplan-Meier法比较各组临床终点情况,单因素和多因素cox回归分析评价FT3水平对临床终点的预测作用。
基线数据显示FT3≤4.08 pmol/L组年龄较大,女性患者比例较高,估计肾小球滤过率(eGFR)、血红蛋白、血钠、吸烟史、饮酒史、服用肾素-血管紧张素系统抑制剂比例低,纽约心脏病学会(NYHA)心功能Ⅳ级患者所占比例更高(均P<0.05)。Kaplan-Meier生存曲线显示FT3 4.09~4.71 pmol/L组全因死亡和心衰再住院发生率最低(P=0.022、0.020);多因素cox回归分析显示,以FT3≤4.08 pmol/L组为参照,FT3 4.09~4.71 pmol/L是全因死亡(HR=0.220,95%CI:0.069~0.700,P=0.011)和心衰再住院(HR=0.490,95%CI:0.241~0.996,P=0.049)的独立保护因素;左室舒张末内径(HR=1.043,95%CI:1.004~1.083,P=0.031)是全因死亡的独立危险因素。
FT3 4.09~4.71 pmol/L的CRT患者全因死亡和心衰再住院风险最低。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
心力衰竭(心衰)是多种心脏疾病发展的晚期阶段。心脏再同步化治疗(CRT)已成为改善心衰患者预后的重要措施之一。然而目前仍有30%经过严格筛选的CRT患者未能从中获益。临床实践发现,心衰患者常合并甲状腺功能异常[1];低T3综合征被认为是引起心功能恶化的重要因素,是预测心衰死亡的强力因子[2]。近年来,有关CRT的临床研究集中在影响CRT疗效的预测因素方面,而甲状腺功能与CRT患者远期预后的关系目前还不清楚。本研究主要探讨不同FT3水平的CRT患者全因死亡和心衰再住院情况,评估FT3对CRT患者远期预后的预测作用。
回顾性收集2010年1月至2014年12月在阜外医院心律失常中心行首次CRT植入术的264例患者病历资料,排除近3个月有特殊药物(胺碘酮、甲状腺激素、抗甲状腺功能药物、肝素、苯妥英钠、利福平)服用史和1个月内行碘造影检查的患者,最终符合条件者共202例,所有患者均符合2013年ESC指南推荐的CRT植入适应证,并签署知情同意书。根据入院FT3三分位水平将患者分为FT3≤4.08 pmol/L(67例)、4.09~4.71 pmol/L(68例)和>4.71 pmol/L(67例)3组。
收集患者的人口学资料、基础心脏病、伴随疾病、纽约心功能(NYHA)分级、术后用药、实验室检查、甲状腺功能、超声心动图指标和CRT术前术后心电图和电话随访资料。定义随访终点为全因死亡(包括心脏移植)和心衰再住院(多次住院只算1次)。
采集患者入院第2天清晨空腹血,完善血常规、生化全套、高敏C反应蛋白(hsCRP)、N末端B型脑钠肽原(NT-proBNP)等。采用免疫化学发光法(德国Siemens公司)检测血清中促甲状腺激素(TSH)、游离三碘甲状腺原氨酸(FT3)、游离甲状腺素(FT4)、总三碘甲状腺原氨酸(TT3)和总甲状腺素(TT4)水平;甲状腺功能正常值范围:TSH:0.55~4.78 mU/L;FT4:1.23~2.90 pmol/L;FT3:2.76~6.30 pmol/L;TT4:55.34~160.86 nmol/L;TT3:1.00~2.94 nmol/L。使用GE公司Vivid7型彩色多普勒超声心动仪采集CRT植入术前左房大小(LAd)、左室舒张末期内径(LVEDd)和左室射血分数(LVEF)等指标;LVEF采用Simpson双平面法。术前术后QRS波宽度为Ⅰ、aVF、V1导联QRS波宽度的平均值。
采用SPSS 19.0统计软件进行数据分析。计量资料呈正态分布用 ±s表示,组间比较使用单因素方差分析(ANOVA),两两比较采用Bonferroni法;呈非正态分布用M[四分位数间距(QR)]表示,组间比较使用非参数检验(Kruskal-Wallis法),两两比较采用Pairwise法;计数资料用百分率表示,组间比较采用χ2检验;生存分析采用Kaplan-Meier方法和log-rank检验;采用cox比例风险回归模型分析FT3水平对各临床终点的风险预测价值。双侧P<0.05为差异有统计学意义。
±s表示,组间比较使用单因素方差分析(ANOVA),两两比较采用Bonferroni法;呈非正态分布用M[四分位数间距(QR)]表示,组间比较使用非参数检验(Kruskal-Wallis法),两两比较采用Pairwise法;计数资料用百分率表示,组间比较采用χ2检验;生存分析采用Kaplan-Meier方法和log-rank检验;采用cox比例风险回归模型分析FT3水平对各临床终点的风险预测价值。双侧P<0.05为差异有统计学意义。
患者年龄(59±11)岁,男134例,女68例。扩张性心肌病150例(74.3%),缺血性心脏病38例(18.8%),酒精性心肌病6例(3.0%),心脏瓣膜病5例(2.4%),高血压心肌病1例(0.5%),肥厚性心肌病1例(0.5%),围产期心肌病1例(0.5%)。NYHA Ⅱ级70例(34.6%),Ⅲ级103例(51.0%),Ⅳ级29例(14.4%)。死亡23例(11.4%),心脏移植5例(2.4%),心衰再住院53例(26.2%)。中位随访时间22个月。
FT3≤4.08 pmol/L组患者年龄较大,女性比例较高,估计肾小球滤过率(eGFR)、血红蛋白、血钠、左房内径(LAd)、血管紧张素系统抑制剂使用比例较低(均P<0.05)。FT3 >4.71 pmol/L组NYHA Ⅱ级比例最高,FT 3≤4.08 pmol/L组NYHA Ⅳ级比例最高(均P<0.05,表1)。
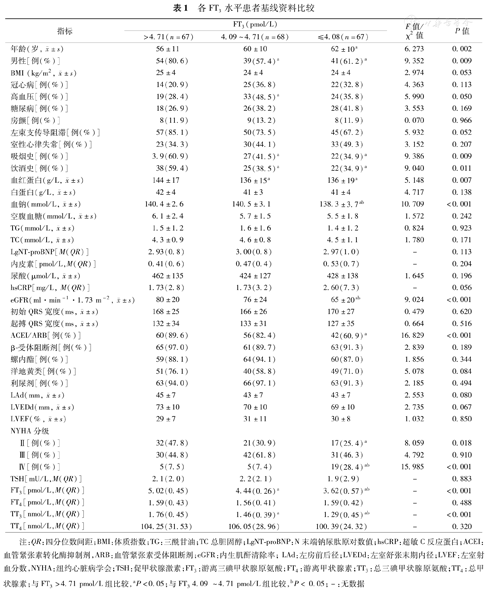
各FT3水平患者基线资料比较
各FT3水平患者基线资料比较
| 指标 | FT3 (pmol/L) | F值/χ2值 | P值 | |||
|---|---|---|---|---|---|---|
| >4.71(n=67) | 4.09~4.71(n=68) | ≤4.08(n=67) | ||||
年龄(岁, ±s) ±s) | 56±11 | 60±10 | 62±10a | 6.273 | 0.002 | |
| 男性[例(%)] | 54(80.6) | 39(57.4)a | 41(61.2)a | 9.352 | 0.009 | |
BMI (kg/m2, ±s) ±s) | 25±4 | 24±4 | 24±4 | 2.974 | 0.053 | |
| 冠心病[例(%)] | 14(20.9) | 25(36.8) | 22(32.8) | 4.363 | 0.113 | |
| 高血压[例(%)] | 19(28.4) | 33(48.5)a | 24(35.8) | 5.990 | 0.050 | |
| 糖尿病[例(%)] | 18(26.9) | 26(38.2) | 28(41.8) | 3.553 | 0.169 | |
| 房颤[例(%)] | 8(11.9) | 9(13.2) | 8(11.9) | 0.070 | 0.966 | |
| 左束支传导阻滞[例(%)] | 57(85.1) | 50(73.5) | 45(67.2) | 5.932 | 0.052 | |
| 室性心律失常[例(%)] | 23(34.3) | 30(44.1) | 33(49.3) | 3.152 | 0.207 | |
| 吸烟史[例(%)] | 3.9(60.9) | 27(41.5)a | 22(34.9)a | 9.386 | 0.009 | |
| 饮酒史[例(%)] | 38(59.4) | 25(38.5)a | 22(34.9)a | 9.040 | 0.011 | |
血红蛋白(g/L,  ±s) ±s) | 144±17 | 136±15a | 136±19a | 5.148 | 0.007 | |
白蛋白(g/L,  ±s) ±s) | 42±4 | 41±3 | 41±4 | 4.717 | 0.138 | |
血钠(mmol/L,  ±s) ±s) | 140.4±2.6 | 140.5±3.1 | 138.3±3.7ab | 10.709 | <0.001 | |
空腹血糖(mmol/L,  ±s) ±s) | 6.1±2.4 | 5.7±1.5 | 5.5±1.8 | 1.572 | 0.242 | |
TG(mmol/L,  ±s) ±s) | 1.5±1.2 | 1.6±1.6 | 1.4±1.2 | 0.824 | 0.923 | |
TC(mmol/L,  ±s) ±s) | 4.3±0.9 | 4.6±0.8 | 4.5±1.1 | 1.780 | 0.171 | |
| LgNT-proBNP[M(QR)] | 2.93(0.8) | 3.00(0.8) | 2.97(1.0) | - | 0.113 | |
| 内皮素[pmol/L,M(QR)] | 0.41(0.6) | 0.47(0.4) | 0.53(0.7) | - | 0.204 | |
尿酸(μmol/L,  ±s) ±s) | 462±135 | 424±127 | 428±138 | 1.645 | 0.196 | |
| hsCRP[mg/L, M(QR)] | 1.73(2.8) | 1.73(3.2) | 2.60(7.3) | - | 0.056 | |
eGFR(ml·min-1·1.73 m-2, ±s) ±s) | 80±20 | 76±24 | 65±20ab | 9.024 | <0.001 | |
初始QRS宽度(ms,  ±s) ±s) | 168±25 | 166±26 | 170±27 | 0.479 | 0.620 | |
起搏QRS宽度(ms,  ±s) ±s) | 132±34 | 133±31 | 127±35 | 0.664 | 0.516 | |
| ACEI/ARB[例(%)] | 60(89.6) | 56(82.4) | 42(60.9)a | 16.829 | <0.001 | |
| β-受体阻断剂[例(%)] | 65(97.0) | 61(89.7) | 63(91.3) | 2.839 | 0.189 | |
| 螺内酯[例(%)] | 59(88.1) | 64(94.1) | 60(87.0) | 1.856 | 0.344 | |
| 洋地黄类[例(%)] | 51(76.1) | 40(58.8) | 49(71.0) | 5.078 | 0.084 | |
| 利尿剂[例(%)] | 63(94.0) | 66(97.1) | 63(91.3) | 2.185 | 0.494 | |
LAd(mm,  ±s) ±s) | 45±7 | 43±7 | 43±7 | 2.553 | 0.080 | |
LVEDd(mm,  ±s) ±s) | 73±10 | 70±10 | 69±10 | 2.735 | 0.067 | |
LVEF(%,  ±s) ±s) | 29±7 | 31±11 | 30±8 | 1.032 | 0.850 | |
| NYHA分级 | ||||||
| Ⅱ[例(%)] | 32(47.8) | 21(30.9) | 17(25.4)a | 8.059 | 0.018 | |
| Ⅲ[例(%)] | 30(44.8) | 42(61.8) | 31(46.3) | 4.792 | 0.910 | |
| Ⅳ[例(%)] | 5(7.5) | 5(7.4) | 19(28.4)ab | 15.985 | <0.001 | |
| TSH[mU/L,M(QR)] | 2.1(2.0) | 2.2(2.1) | 1.9(2.9) | - | 0.883 | |
| FT3[pmol/L,M(QR)] | 5.02(0.45) | 4.44(0.26)a | 3.62(0.57)ab | - | <0.001 | |
| FT4[pmol/L,M(QR)] | 1.59(0.43) | 1.56(0.41) | 1.59(0.42) | - | 0.488 | |
| TT3[nmol/L,M(QR)] | 1.76(0.45) | 1.46(0.39)a | 1.29(0.45)ab | - | <0.001 | |
| TT4[nmol/L,M(QR)] | 104.25(31.53) | 106.05(28.96) | 100.39(24.32) | - | 0.320 | |
注:QR:四分位数间距;BMI:体质指数;TG:三酰甘油;TC总胆固醇;LgNT-proBNP:N末端钠尿肽原对数值;hsCRP:超敏C反应蛋白;ACEI:血管紧张素转化酶抑制剂,ARB:血管紧张素受体阻断剂;eGFR:内生肌酐清除率;LAd:左房前后径;LVEDd:左室舒张末期内径;LVEF:左室射血分数,NYHA:纽约心脏病学会;TSH:促甲状腺激素;FT3:游离三碘甲状腺原氨酸;FT4:游离甲状腺素;TT3:总三碘甲状腺原氨酸;TT4:总甲状腺素;与FT3>4.71 pmol/L组比较,aP<0.05;与FT3 4.09~4.71 pmol/L组比较,bP< 0.05;-:无数据
FT3 4.09~4.71 pmol/L组全因死亡(χ2=10.055,P=0.022)和心衰再住院率(χ2=15.300,P=0.020)显著低于FT3 ≤4.08 pmol/L组和FT3>4.71 pmol/L组。
将FT3作为三分类自变量,以全因死亡和心衰再住院分别作为因变量,分别行单因素和多因素cox回归分析。单因素分析显示,年龄、性别、高血压、吸烟史、饮酒史、血红蛋白、血钠、eGFR和使用血管紧张素转化酶抑制剂/血管紧张素受体阻断剂(ACEI/ARB)类药物对全因死亡和心衰再住院均无显著影响。多因素分析结果显示,以FT3≤4.08 pmol/L组作参照,FT3 4.09~4.71 pmol/L组分别是全因死亡(HR=0.220,95%CI:0.069~0.700,P=0.011)和心衰再住院(HR=0.490,95%CI:0.241~0.996,P=0.049)的独立保护因素;同时LVEDd(HR=1.043,95%CI:1.004~1.083,P=0.031)是全因死亡的独立危险因素(表2)。
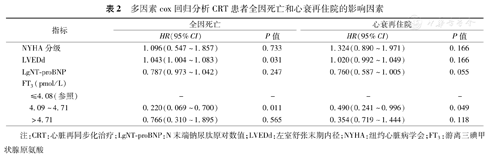
多因素cox回归分析CRT患者全因死亡和心衰再住院的影响因素
多因素cox回归分析CRT患者全因死亡和心衰再住院的影响因素
| 指标 | 全因死亡 | 心衰再住院 | |||
|---|---|---|---|---|---|
| HR(95%CI) | P值 | HR(95%CI) | P值 | ||
| NYHA分级 | 1.096(0.547~1.857) | 0.733 | 1.324(0.890~1.971) | 0.166 | |
| LVEDd | 1.043(1.004~1.083) | 0.031 | 1.020(0.992~1.049) | 0.166 | |
| LgNT-proBNP | 0.787(0.973~1.042) | 0.247 | 0.760(0.587~1.005) | 0.055 | |
| FT3(pmol/L) | |||||
| ≤4.08(参照) | - | - | - | - | |
| 4.09~4.71 | 0.220(0.069~0.700) | 0.011 | 0.490(0.241~0.996) | 0.049 | |
| >4.71 | 0.766(0.310~1.895) | 0.565 | 0.354(0.719~1.444) | 0.118 | |
注:CRT:心脏再同步化治疗;LgNT-proBNP:N末端钠尿肽原对数值;LVEDd:左室舒张末期内径;NYHA:纽约心脏病学会;FT3:游离三碘甲状腺原氨酸
神经内分泌系统的异常激活是心衰恶化的主要原因。除肾素-血管紧张素-醛固酮系统和交感-肾上腺髓质系统外,甲状腺功能异常也参与心衰的发生和发展[3,4,5]。血清中非蛋白结合形式的FT4,经过循环或组织的脱碘,最终转化为具有生理功能的FT3。心衰患者除存在原发的甲状腺功能异常外,因局部组织将FT4转化为FT3的能力减弱,更容易出现低T3状态。动物研究证实,低FT3通过减少心脏α-肌球蛋白重链(α-MHC)、肌浆网钙调控基因Ca2+-ATP酶(SERCA)等兴奋收缩偶联相关基因的表达[6]引起心肌舒缩功能减弱;通过影响细胞骨架蛋白的合成[7],促进心肌间质纤维化和基质重构;通过抑制内源性一氧化氮合酶(NOS)[8]的合成和释放,导致微循环紊乱,最终造成心肌缺血。人群研究证实,低FT3的心衰患者常伴随NT-proBNP和脂联素水平升高[9],血清白细胞介素6、肿瘤坏死因子-α[10]等炎症因子水平也相应增加;Chuang等[11]发现低FT3水平是急性失代偿性心衰患者全因死亡的独立危险因素。
本研究发现,FT3> 4.71 pmol/L组年龄最小,男性比例最高,提示FT3水平在老年人和妇女人群中相对较低[12],与既往队列研究结论一致。FT3≤4.08 pmol/L组血钠、血红蛋白、白蛋白水平最低,这与生理剂量下FT3具有维持细胞膜Na+-K+-ATP酶活性和促进蛋白质合成的生理功能相关。心功能方面,FT3≤4.08 pmol/L组NYHA Ⅱ级患者构成比最低,NYHA Ⅳ级患者构成比最高,提示FT3水平在一定范围内与患者心功能呈正相关[13,14]。
既往研究[15]发现甲状腺功能亢进和甲状腺功能低下均增加心衰患者的死亡率;而甲状腺素替代治疗恢复正常FT3、FT4水平可改善心衰患者预后。值得注意的是,国外心衰患者以缺血性心肌病为主;而本研究中扩张性心肌病等非缺血性心肌病占多数。Li等[16]回顾性分析了我国963例扩张性心肌病患者,发现亚临床甲状腺功能异常增加患者死亡率,亚临床甲状腺功能亢进也是全因死亡的独立危险因素。本研究发现FT3 4.09~4.71 pmol/L组患者的全因死亡和心衰再住院的风险最低,提示过高或过低的FT3水平均不利于CRT患者的远期预后;此外本研究也证实,植入术前较大的左心室不仅与CRT反应性较低相关[17],也增加CRT患者远期全因死亡风险。
本研究为单中心回顾性队列研究,样本量有限,随访时间较短。但本研究首次提出了FT3在CRT患者临床预后的评估作用。作为一个能真实反映甲状腺功能的实验室指标,FT3理论上具有广阔的临床应用前景。本研究结论有待于更大样本的前瞻性长期随访研究证实。



























