
探讨奥司他韦雾化吸入治疗人感染H7N9禽流感病例的临床疗效。
分析我院2017年3月6日至4月12日收治的4例H7N9禽流感患者诊疗过程,在常规抗病毒治疗(奥司他韦150 mg,口服,2次/d)基础上尝试联用奥司他韦(奥司他韦75 mg,胶囊内粉末融入20 ml生理盐水,2次/d)雾化吸入,并同时予以抗菌、血液净化及免疫调节治疗,并观察其疗效。
经治疗4例患者分别于治疗后第3、3、4、1天病毒核酸转阴;4例病例均治愈出院,无后遗症。
奥司他韦雾化吸入联合口服治疗能明显缩短病毒核酸转阴时间,可提高抗H7N9禽流感病毒疗效,提高人感染H7N9禽流感患者治愈率。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
我国为人感染H7N9禽流感病例全球首发[1],2016年9月开始出现第五波散发病例,12月份以来确诊病例明显增多,病死率高,贵州省是第一次出现疫情,先发病的6例仅1例成活,如何降低死亡率,是我们面临的巨大挑战。众所周知,在综合治疗的基础上,及时有效的抗病毒治疗是救治成功的关键。奥司他韦是治疗人感染H7N9禽流感病毒感染的首选药物[2,3],目前仅有口服制剂,其口服后经肝脏和(或)肠壁酯酶转化为活性代谢产物(奥司他韦羧酸盐)而发挥抗病毒作用[4]。有研究报道奥司他韦在体外可直接杀伤H5N1病毒,也可作用于正常细胞,阻断该细胞被H5N1病毒感染[5]。故我们分析奥司他韦也许存在通过口服之外的途径去杀伤H7N9禽流感病毒或阻断该病毒感染正常细胞的可能。因此,我们对本院2017年3—4月收治的4例H7N9禽流感患者,在常规治疗的基础上尝试性加用奥司他韦雾化吸入,以期阻断病毒在肺内的播散,避免肺内新病灶的出现,经观察取得了很好的疗效,患者全部治愈,现将诊治经过报道如下。
本研究对象均来自黔东南苗族侗族自治州人民医院2017年3月6日至4月12日期间住院患者,治疗前报请院相关部门批准并征得患者知情同意。4例患者均为男性,平均年龄49岁,诊断均符合国家卫计委《人感染H7N9禽流感诊疗方案2017年第一版》标准[6],发病前均有禽类接触史,采集其呼吸道分泌物H7N9病毒核酸检测结果为阳性,并由省疾控中心复核确诊,起病时均伴发热、咳嗽、咳痰、畏寒、全身乏力等症状,其中3例患者合并低钾周期性麻痹、陈旧性肺结核、高血压、肾结石等基础疾病,胸部影像学检查提示均合并肺部炎症性病变,其中病例1为重症患者。
4例患者在口服奥司他韦及常规综合治疗的基础上,加用奥司他韦75 mg(将胶囊内粉剂溶解于20 ml生理盐水中)雾化吸入治疗,2次/d,详见表1。奥司他韦胶囊为罗氏制药有限公司生产,产品批号M1025,分装批号SH0063。雾化器为其乐康成人型一次性使用雾化器。病毒核酸检测采用RT-PCR技术。4例患者给予鼻导管持续吸氧、吸痰护理,均未使用机械通气或正压通气治疗。针对性地给予血液净化清除炎症介质及减轻肺水肿、输注人血白蛋白和(或)同型血浆提高胶体渗透压,使用人免疫球蛋白及注射用胸腺法新提高患者免疫功能,皮下注射重组人粒细胞刺激因子以促进粒细胞生长,使用抗生素防治继发感染,用乌司他丁清除氧自由基及抑制炎症介质释放。
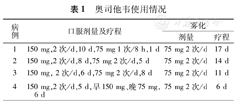
奥司他韦使用情况
奥司他韦使用情况
| 病例 | 口服剂量及疗程 | 雾化 | |
|---|---|---|---|
| 剂量 | 疗程 | ||
| 1 | 150 mg,2次/d,10 d,75 mg 1次/8 h,1 d | 75 mg 2次/d | 17 d |
| 2 | 150 mg,2次/d,8 d,75 mg 2次/d,5 d | 75 mg 2次/d | 14 d |
| 3 | 150 mg, 2次/d,6 d,75 mg 2次/d,8 d | 75 mg 2次/d | 11 d |
| 4 | 150 mg,2次/d,5 d,早150 mg、晚75 mg,6 d | 75 mg 2次/d | 6 d |
观察4例病例治疗前后疾病转归,包括:临床表现,呼吸道标本病毒核酸检测情况,实验室及影像学X线检查结果,肺部病灶变化。
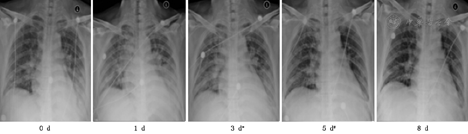
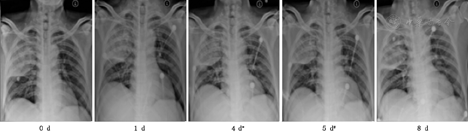
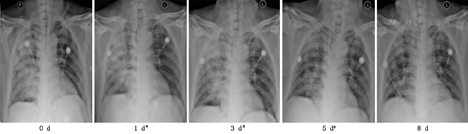
由疾控中心专业人员采样留取两份呼吸道标本(鼻咽分泌物及深部痰)作病毒核酸检测,雾化治疗后1~4 d,4例患者第1次病毒核酸检测转阴,分别间隔24 h以上再次阴性后解除隔离,详见表2。治疗后患者咳嗽、咳痰、胸闷等呼吸道症状及发热等症状逐渐好转,详见表3。呼吸频率、血常规及血气分析均恢复正常,详见表4。复查胸部影像X线检查,肺部原发病灶均逐渐吸收好转,均无新发病灶,详见图1,图2,图3,图4。


注:*表示第一次咽试子及深部痰病毒核酸检测转阴,#表示第二次咽试子及深部痰病毒核酸检测转阴(以下相同)



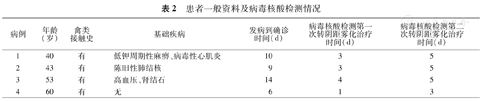
患者一般资料及病毒核酸检测情况
患者一般资料及病毒核酸检测情况
| 病例 | 年龄(岁) | 禽类接触史 | 基础疾病 | 发病到确诊时间(d) | 病毒核酸检测第一次转阴距雾化治疗时间(d) | 病毒核酸检测第二次转阴距雾化治疗时间(d) |
|---|---|---|---|---|---|---|
| 1 | 40 | 有 | 低钾周期性麻痹、病毒性心肌炎 | 10 | 3 | 5 |
| 2 | 43 | 有 | 陈旧性肺结核 | 9 | 3 | 5 |
| 3 | 53 | 有 | 高血压、肾结石 | 14 | 4 | 5 |
| 4 | 60 | 有 | 无 | 6 | 1 | 3 |
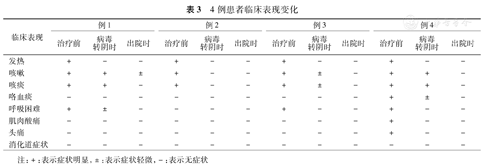
4例患者临床表现变化
4例患者临床表现变化
| 临床表现 | 例1 | 例2 | 例3 | 例4 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | |
| 发热 | + | - | - | + | - | - | + | - | - | + | - | - |
| 咳嗽 | + | + | ± | + | - | - | + | ± | - | + | + | - |
| 咳痰 | + | + | - | + | - | - | + | ± | - | + | + | - |
| 咯血痰 | - | - | - | - | - | - | - | - | - | + | ± | - |
| 呼吸困难 | + | ± | - | - | - | - | + | - | - | + | - | - |
| 肌肉酸痛 | - | - | - | - | - | - | - | - | - | + | - | - |
| 头痛 | - | - | - | - | - | - | - | - | - | + | - | - |
| 消化道症状 | - | - | - | - | - | - | - | - | - | - | - | - |
注:+:表示症状明显,±:表示症状轻微,-:表示无症状
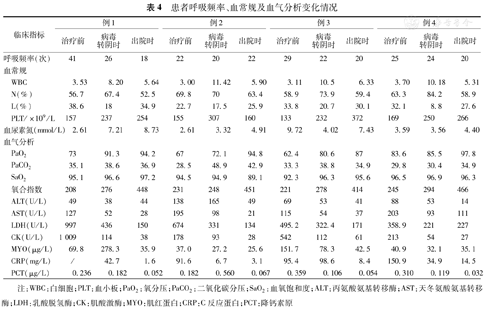
患者呼吸频率、血常规及血气分析变化情况
患者呼吸频率、血常规及血气分析变化情况
| 临床指标 | 例1 | 例2 | 例3 | 例4 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | 治疗前 | 病毒转阴时 | 出院时 | ||
| 呼吸频率(次) | 41 | 26 | 18 | 22 | 20 | 22 | 29 | 22 | 20 | 25 | 24 | 20 | |
| 血常规 | |||||||||||||
| WBC | 3.53 | 8.20 | 5.64 | 3.00 | 11.42 | 5.90 | 3.11 | 10.5 | 6.33 | 3.70 | 10.18 | 5.31 | |
| N(%) | 56.7 | 67.4 | 52.5 | 69.8 | 70 | 63.4 | 58.9 | 73.9 | 59.4 | 63.3 | 84.2 | 58.9 | |
| L(%) | 38.6 | 18 | 34.9 | 22.7 | 17.5 | 25.9 | 33.8 | 20.7 | 30.1 | 32.1 | 8.8 | 27.6 | |
| PLT/×109/L | 157 | 237 | 254 | 155 | 307 | 160 | 133 | 232 | 372 | 169 | 250 | 266 | |
| 血尿素氮(mmol/L) | 2.61 | 7.21 | 8.73 | 2.61 | 3.32 | 4.91 | 9.72 | 4.02 | 7.43 | 3.59 | 3.56 | 4.40 | |
| 血气分析 | |||||||||||||
| PaO2 | 73 | 91.3 | 94.2 | 67 | 72.1 | 94.8 | 62.4 | 80.6 | 87 | 83.6 | 85.5 | 97.8 | |
| PaCO2 | 35.1 | 38.6 | 36.9 | 28.5 | 48.9 | 42.9 | 33.3 | 38.8 | 34.9 | 29.8 | 30.4 | 34.9 | |
| SaO2 | 95.1 | 96.6 | 97.2 | 94.5 | 94.9 | 89.1 | 92.3 | 96.3 | 95.6 | 96.5 | 96.9 | 96.3 | |
| 氧合指数 | 208 | 276 | 448 | 231 | 248 | 451 | 221 | 278 | 414 | 245 | 294 | 466 | |
| ALT(U/L) | 49 | 38 | 44 | 138 | 165 | 49 | 69 | 53 | 41 | 88 | 53 | 14 | |
| AST(U/L) | 127 | 52 | 28 | 195 | 98 | 21 | 115 | 54 | 37 | 203 | 93 | 111 | |
| LDH(U/L) | 997 | 436 | 150 | 674 | 331 | 134 | 495.2 | 322.4 | 171 | 358.9 | 221 | 227 | |
| CK(U/L) | 1 009 | 114 | 38 | 178 | 93 | 28 | 542 | 112 | 61 | 213 | 54 | 27 | |
| MYO(μg/L) | 69.8 | 278.3 | 35.9 | 37.0 | 27.2 | 25.6 | 151.7 | 78.3 | 42.5 | 40.9 | 32.1 | 35.1 | |
| CRP(mg/L) | / | 42.7 | 1.6 | 91.6 | 6.7 | 3.1 | 95.4 | 98.6 | 8.4 | 150.9 | 34.9 | 14.5 | |
| PCT(μg/L) | 0.236 | 0.182 | 0.052 | 0.182 | 0.560 | 0.067 | 0.359 | 0.106 | 0.054 | 0.310 | 0.119 | 0.032 | |
注:WBC:白细胞;PLT:血小板;PaO2:氧分压;PaCO2:二氧化碳分压;SaO2:血氧饱和度;ALT:丙氨酸氨基转移酶;AST:天冬氨酸氨基转移酶;LDH:乳酸脱氢酶;CK:肌酸激酶;MYO:肌红蛋白;CRP:C反应蛋白;PCT:降钙素原
治疗期间患者无恶心、呕吐、失眠、头晕等不良反应,无气促、哮鸣音加重等情况,仅病例3稍感口腔干燥。所有病例经省、州专家组会诊后宣布人感染H7N9禽流感治愈并出院。
人感染H7N9禽流感是由甲型H7N9禽流感病毒感染引起的一种急性呼吸道传染病。H7N9禽流感病毒可同时结合分布在人类上呼吸道及气管上的唾液酸α-2,6型受体(人流感病毒受体)和肺组织中的唾液酸α-2,3型受体(禽流感病毒受体),但H7血凝素与唾液酸α-2,3型受体亲和力更高,容易感染人类的下呼吸道上皮细胞,且病毒可持续复制[6]。奥司他韦口服后转化为奥司他韦羧酸盐,通过特异性抑制流感病毒表面的神经氨酸酶活性,阻止其在宿主细胞内复制、表达以及释放[4]。
本组病例,分别在奥司他韦雾化吸入治疗第3、3、4、1天后第一次尝试检测就发现病毒核酸转阴,平均2.75 d,间隔24 h再次检测仍阴性,明显优于相关报道中单用奥司他韦口服抗病毒治疗到病毒核酸转阴的平均时间6.5 d[7]。4例患者接受奥司他韦雾化吸入治疗的时间分别为发病后10、9、14、6 d,平均9.75 d,虽然较晚,但仍取得较好疗效。
人感染H7N9禽流感患者容易发展为重症[8],本次观察的病例2、3、4在入院时均有两项达到了诊断重症的次要标准,病例1入院时为重症患者,所有病例经积极治疗,病情均未进一步加重,肺部未出现新发病灶,呼吸道症状渐缓解,肺部病灶逐渐吸收,各项实验室检查指标逐渐恢复正常,避免了气管插管等机械通气。
奥司他韦雾化吸入治疗人感染H7N9禽流感国内外尚未见报道。近期有研究[9]发现,奥司他韦雾化吸入可提高小鼠感染H7N9禽流感的抗病毒疗效,为该治疗提供了一定的动物实验依据。
单纯口服奥司他韦抗病毒治疗人感染H7N9禽流感病例的死亡率很高[10,11],而我院奥司他韦雾化吸入联合口服治疗的4例患者全部救治成功,疗效显著,初步总结治疗经验如下:奥司他韦雾化吸入联合口服治疗能使呼吸道H7N9病毒核酸快速转阴,阻止病毒肺内播散,及时控制病情发展。该治疗方法简易可行,在基层医院也能开展,可在人感染H7N9禽流感病例以及其他流感病例的救治中试用。但由于该病的特殊性,该方法与报道中单纯口服奥司他韦的疗效的巨大差别,以及从医学伦理学方面考虑而未能设置对照组。我们初步观察的病例数较少,有待更多的基础及临床试验进一步深入研究。



























