
寻找合适的方法对结石患者尿中草酸的含量进行测定,以期为开展结石预防及治疗的研究提供方法和依据。
采用液相色谱-质谱串联技术对尿中草酸含量进行直接分析。并对检测结果的准确性、稳定性、可重复性等指标进行检测。
检测结果与尿中草酸含量呈良好的线性关系,y=58.524x-15.246(R2=0.979 02)。结果稳定,具有很好的可重复性。日内、日间变异系数分别小于10%和15%。其准确性与酶法相当(N=20,R=0.93)。
采用本研究方法对尿中草酸含量进行检测,具有操作简便、重复性好、结果准确等优点,值得在临床中推广和应用。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
泌尿系结石的发病率近来逐渐增加[1,2],且治疗后复发率高[3],其病因学诊断和预防正在受到高度的关注。作为结石代谢评估的重要组成部分,24 h尿结石危险因素分析对结石的预防和药物治疗及饮食调节是必不可少的。由于泌尿系结石中70%~80%为草酸钙结石[4]。尿液中草酸的含量的测定是临床开展完整的代谢评估的必备条件。目前国内外常用方法为离子色谱法和酶法。本研究采用液相色谱-质谱串联(LC-MS/MS)技术,对尿液中草酸进行直接检测,分析结石患者尿中草酸的含量,探讨该方法在尿路结石治疗和预防中的应用价值,以期为开展结石预防及治疗的研究提供方法和依据。
(1)质谱仪:Waters quanttro micro三重四级杆质谱。色谱柱:Waters OASIS WAX 2.1 50 mm, 30 μm column。10 KD滤膜购自Pall过滤器(北京)有限公司。(2)试剂:草酸标准品购自美国Sigma公司,配制成母液500 μmol/L;1,2 C13 oxalate购自Cambridge Isotope Laboratories(Cambridge Isotope Laboratories,MA,美国,CLM-2002),配制成母液500 μmol/L;草酸内标(商品)50 μmol/L;草酸标准品(商品)500 μmol/L;试剂盒:草酸纯化试剂盒(R-biopharm AG,德国,RBC004)和草酸酶标定量试剂盒(R-biopharm AG,德国,RBC005)购自R-biopharm AG;其他试剂包括甲醇(Fisher Scientific,美国,A456),氨水(Sigma公司)均为质谱级。Sample solution缓冲液(1 mmol/L phophotase, pH=2.0)
(1)质谱方法:负离子模式;(2)草酸:trasition:88.6-60.5;88.6-44.5;1,2 C13 oxalate:trasition:90.6-61.5;90.6-45.5; cone voltage 20V;collison energy: 8;(3)液相方法:WAX LC-MS A液:2 mmol/L醋酸铵0.1%FA; B液:75%甲醇60 mmol/L NH3H2O。时间表0~1 min切换阀至废液,以防止尿液样品污染。每个样品做3次重复,两个样品中间洗2次。
入组协和医院泌尿科门诊的泌尿系结石患者20例,收集其24 h尿液进行检测。
按倍比浓度稀释草酸标准品,浓度如表1所示。每种浓度取170 μl,加入20 μl草酸内标和10 μl Sample solution缓冲液,制成倍比浓度的草酸标准溶液。浓度分别为500、250、125、62、31、16、8 μmol/L。
草酸检测的可重复性及稳定性
草酸检测的可重复性及稳定性
| 草酸及尿液样本 | 变异系数 | ||
|---|---|---|---|
| 对照 | 日内 | 日间(连续7 d) | |
| 高浓度草酸标准溶液 | 2.2 | 3.3 | 7.8 |
| 低浓度草酸标准溶液 | 2.7 | 2.0 | 5.1 |
| 尿样1(4 ℃保存) | 9.4 | 6.6 | 14.2 |
| 尿样1(-20 ℃保存) | 9.7 | na | 10.2 |
| 尿样2(4 ℃保存) | 5.5 | 4.3 | 11.6 |
| 尿样2(-20 ℃保存) | 7.4 | na | 13.3 |
将标准溶液分别上样,以各自的标准溶液草酸峰面积/内标溶液草酸峰面积得到校正后的草酸峰面积,对标准溶液浓度进行线性回归,得到草酸的标准曲线。
取40 μl尿液,加入20 μl草酸内标溶液,构成60 μl原液。将原液倒入含滤膜的离心管进行14 000 g,离心5 min,去除大分子蛋白,形成过滤液。取30 μl过滤液,加入170 μl Sample solution缓冲液,构成200 μl的尿液样品。
将样品溶液上样,单次进样20 μl,以样品草酸峰面积/内标溶液草酸峰面积得到校正后的样品草酸峰面积,根据标准曲线计算得出样品的草酸浓度。27.5~250 μmol/L的草酸标准溶液放置4 ℃保存,样品(尿液)分别放置4 ℃和-20 ℃保存。第1天样品做3次日内重复,从第1~7天每天做1次日间重复,每天做1次标准曲线,用该天标准曲线为该天样品定量。每个点做3次重复。用于质谱分析的尿液样品先用草酸纯化试剂盒处理,再用草酸酶标定量试剂盒定量。
标准曲线用线性回归方法获得,计算R2值。技术重复和日内日间重复计算CV值。
草酸和1,2 C13-草酸的保留时间约2.5 min,草酸的88.8>60.8,88.8>44.8离子对和1,2 C13-草酸90.8>61.8、90.8>45.8离子对的色谱图(图1)。可见没有明显的干扰峰。整个测定程序时间需要7 min。
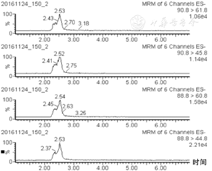

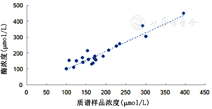
草酸的标准曲线为y=58.524x-15.246 (R2=0.979 02)。其中y为草酸浓度,x为校正后的样品草酸峰面积。通过动态范围分析,样品在8~500 μmol/L范围内有良好的线性关系,对应原始尿液浓度(80~5 000 μmol/L),正常人和患者尿液草酸浓度处于该范围内(图2)。
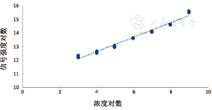

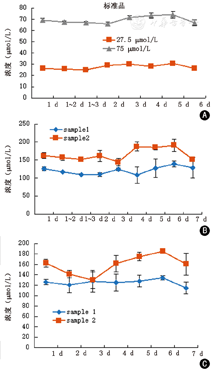

我们对高浓度草酸标准溶液(75 μmol/L)、低浓度草酸标准溶液(27.5 μmol/L)以及两个尿液样品进行了日内、日间(连续7 d)以及不同温度(4 ℃和-20 ℃)下的检测,以了解检测结果的可重复性以及草酸的稳定性。结果如图3、表2所示。研究证实,本检测发现准确可靠,可重复性好,且草酸样本稳定性佳。
我们将同一份尿样分成两份,对20例尿液标本分别使用LC-MS/MS方法和酶法进行检测,并对检测结果进行比较。结果(图4)显示,LC-MS/MS方法和酶法对同一份样本进行检测所得的结果基本一致(N=20,R=0.93)。由此证明,LC-MS/MS方法准确性与酶法相当。

泌尿系结石是泌尿外科的常见病之一,在泌尿外科住院患者中占居首位。发病率日益增加。文献显示美国的患病率从1976—1980年间的3.8%上升到2007—2010年间的8.4%[1,2]。同时泌尿系结石的复发率较高,根据国外的研究:结石患者治疗后如未进行预防性干预,其5年的复发率为10%,10年的复发率为50%[3]。
只有通过对结石病患者的尿液成分进行分析,才能更有针对性的调整其代谢状态,达到降低结石复发风险的目的。因此,在欧洲泌尿协会和美国泌尿协会的指南均推荐,将24 h尿液成分分析作为结石预防的首要工作。
有研究表明[4],泌尿系结石中70%~80%为草酸钙结石。尿液中草酸浓度的增加对泌尿系结石的形成具有重要意义[5]。Robertson等[6]指出,在各种因素中,草酸是最关键的因素,其促进结石形成的作用超过了尿钙、尿pH值等其他所有因素。高草酸尿症与泌尿系结石之间的关系已经得到了众多研究的证实[7,8,9]。
研究一种能够准确并简便的测定尿中草酸含量的方法,对泌尿系结石的病因学诊断和预防就显得尤为重要。但草酸为有机酸,含量低,检查难度较大。目前认为,影响尿草酸测定准确与否的因素,包括检测方法、保存条件、收集及运送方法。
检测方法方面,目前国内常用的方法主要有滴定法、比色法、高压液相色谱法(HPLC)、离子色谱法和毛细管电泳法等[10]。滴定法建立最早,但发展不大,灵敏度低,操作繁琐、耗时。比色法廉价、灵敏度高,但预沉淀操作难于完全将草酸提取出来,操作繁琐且重复性差。高压液相色谱法灵敏度高、重复性好、操作简便、快捷,但分离过程中无机酸的干扰严重,且仪器昂贵,对操作人员要求高,普及困难。离子色谱法重复性不高,难以对尿液样品中微量的草酸进行直接定量分析。毛细管电泳灵敏度高,操作也简便,但仪器尚未普及。国外应用较多的是用酶法测定尿中草酸[11]。这种方法准确,但步骤复杂,成本较高,难以在国内临床中广泛开展。本研究中应用的LC-MS/MS技术是小分子定量的较好的检测方法,具有操作简便,重复性好,受干扰少等优势,且准确度与酶法相当。
由于24 h尿标本收集周期较长,尿中成分真实水平易受其他因素影响。因此有效的保存方法是分析的前提。既往文献常用的保存剂包括麝香草酚、浓盐酸、甲苯、硼酸等,亦有低温长时间保存的报道。2015年,Wu等[12]就24 h尿样保存方法进行了研究,指出尿中草酸无需保存剂,在常规或4 ℃条件下保存48 h,浓度无明显变化。
同时,我国幅员辽阔,人口众多,地区医疗水平发展不平衡。24 h尿液标本收集和运送过程繁琐,对患者依从性有较高要求。在收集和运送过程中,不正规的操作可能影响测定结果。如何使患者更加简单、便捷的收集和运送24 h尿样,还有待探讨。
综上所述采用本研究方法对尿中草酸含量进行检测,具有操作简便、重复性好、结果准确等优点,且较酶法价格低廉,值得在临床中推广和应用。



























