
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者男,1995年2月出生。因"烦渴、多饮、多尿9个月,加重1个月余"于2014年7月29日入住复旦大学附属华山医院内分泌科。2013年10月(18岁)无明显诱因下出现烦渴、多饮、多尿,每日饮水量6 000~8 000 ml,排尿10余次,夜尿4~5次,每次约250 ml,尿色淡,一周后出现左侧胸部阵发性疼痛,偶有头痛,但无复视、视物模糊、皮疹、淋巴结肿大等其他症状。患者于当地医院胸X线片检查提示左侧肋骨病变。2014年2月外院行单光子发射计算机断层显像(SPECT)检查提示左侧第5肋骨病变,考虑为恶性骨肿瘤,行"左第5肋骨肿瘤切除+左肺上叶楔形切除术",病理考虑左第5肋骨"嗜酸性肉芽肿",累及周围软组织(图1)。术后患者自觉多尿症状缓解(自觉口干好转,尿量减少,夜尿减少至0~1次),未就嗜酸性肉芽肿和多尿进一步诊治。2014年6月多饮多尿症状再现并加重,伴乏力、双下肢酸痛和失眠。2014年7月外院垂体磁共振成像(MRI)增强提示垂体柄增粗(图2),结合多尿症状诊断为中枢性尿崩症,予弥凝(醋酸去氨加压素)0.1 mg/次,2次/d治疗,多饮多尿症状明显好转。为进一步明确诊断和后续治疗方案,患者于2014年7月入住我科。
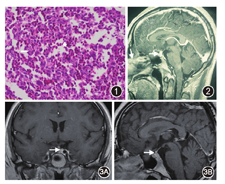

体格检查:体温37.7 ℃,脉搏80次/min,呼吸14次/min,血压:115/67 mmHg(1 mmHg=0.133 kPa),颜面部及胸背部可及痤疮,无紫纹,未见皮下出血点,瘀点瘀斑;左侧肋下可见长约15 cm的陈旧性手术瘢痕;全身浅表淋巴结无肿大;腹部平坦,肝脾肋下未触及;双下肢无水肿。入院后辅助检查:血、尿和大便常规及肝肾功能正常,血糖正常,胸片和心电图未见异常。血钠146 mmol/L,血钾3.8 mmol/L,游离三碘甲状腺原氨酸4.88 pmol/L,游离甲状腺素12.85 pmol/L,促甲状腺激素3.36 mU/L,三碘甲状腺原氨酸1.76 nmol/L,甲状腺素113.30 nmol/L,晨血皮质醇417.36 nmol/L,促肾上腺皮质激素(ACTH)113.5 pmol/L,卵泡刺激素1.55 U/L,黄体生成素4.04 U/L,催乳素64.02 mU/L,睾酮12.80 nmol/L。血渗透压303 mOsm/kg·H2O(1 mOsm/kg·H2O=2.575 kPa),尿渗透压108 mOsm/kg·H2O。肿瘤标志物:正常范围。腹部B超未见肝脾肿大,浅表淋巴结B超检查发现双侧腋下少量肿大淋巴结。全身扁骨及长骨摄片未见异常。鞍区MRI增强:垂体高度正常,信号较均匀,增强后均匀强化,垂体柄下方结节状增粗,增强后结节状强化(图3)。正电子发射计算机断层成像(PET/CT):左侧第5肋骨病变治疗后,垂体柄稍饱满,未见脱氧葡萄糖(FDG)代谢异常增高,脑干FDG代谢欠均匀(未见异常增高灶);余PET显像未见FDG代谢异常增高灶。特殊检查:骨穿未见造血系统累及。
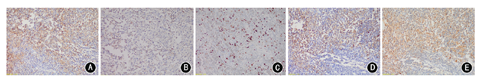
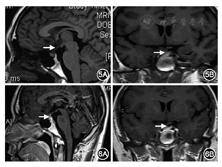
诊疗经过和预后:根据临床表现、实验室检查、影像学检查以及外院诊疗经过,弥凝治疗有效,功能诊断考虑中枢性尿崩症,垂体前叶各轴功能均正常。外院肋骨手术标本病理会诊:S-100(+),CD1α(+),langerin(+),CD68(-),LCA(-),Ki-67(+)(约30%),符合朗格汉斯组织细胞增生症(LCH)(图4)。病因诊断考虑为多系统LCH(累及垂体和肋骨)。治疗:继续弥凝片0.1 mg/次,2次/d控制尿量;原发病由血液科制定化疗方案。2014年8月11日起予以LCH-Ⅲ方案化疗1次[长春地辛4 mg(第1、8天)+地塞米松10 mg,1次/d(第1~8天)];2014年9月3日至10月17日给予长春地辛4 mg+醋酸泼尼松50 mg,1次/周,共5次;2014年10月29日至12月8日给予长春地辛4 mg(第1天)+醋酸泼尼松25 mg/次,2次/d(第1~3天),1次/周,共5次。患者减少并停用弥凝片,监测尿量维持2 000~3 000 ml/d。复查全身扁骨及长骨摄片未见明显异常,双侧颈部、锁骨上、腋下、腹股沟未见明显异常淋巴结肿大。垂体MRI平扫:垂体柄下方小结节,较前相仿,视交叉清晰(图5)。2014年12月11日至2015年9月25日继续给予长春地辛(第1天)+醋酸泼尼松25 mg/次,2次/d(第1~5天),每3周1次,共12次。治疗期间监测血糖、血脂、血压,未见异常,但体重增加15 kg。于2015年9月25日再次评估全身病情并未有复发情况。2016年1月行全身评估,三大常规、电解质、肝肾功能均在正常范围;垂体-甲状腺轴、肾上腺皮质轴、性腺轴评估均在正常范围;尿渗透压:557 mOsm/kg·H2O,尿量1 900 ml/d,腹部B超未见异常,全身扁骨及长骨X线片未见明显异常;查垂体MRI增强提示垂体柄结节状强化,病灶较前略有缩小(图6)。


青年男性,多饮、多尿起病伴左肋疼痛,影像学示垂体柄增粗。垂体柄增粗的病因包括炎症、肿瘤、先天性疾病等,病因诊断是临床难题。
垂体柄增粗病因多样,同时累及骨骼时,需要考虑LCH。
由专科系统评估后个体化制定LCH治疗和随访方案,重新评估腺垂体和神经垂体功能,调整治疗方案。治疗有效者尿崩症状有完全缓解可能。
患者有典型多饮多尿症状,弥凝治疗有效,结合实验室检查高血渗透压、低尿渗透压,影像学提示垂体柄增粗,虽未行禁水加压试验,功能诊断中枢性尿崩症明确,病变部位在垂体柄。而垂体柄增粗的病因诊断一直是个临床难题。目前已有的病例报道中,垂体柄增粗病因主要包括肿瘤(生殖细胞瘤、转移性肿瘤、原发垂体瘤、血液系统肿瘤、组织增生症等)和炎症(淋巴细胞性垂体炎、结节病、肉芽肿等),其次是感染(如结核)和先天性病变(垂体柄中断、视隔发育不全等),病因多样,而病灶常常很小,活检创伤大,病灶位置特殊,导致病因诊断困难[1,2]。不同病因有一定的性别和年龄差异,如生殖细胞瘤多见于男性青少年,LCH(2016年世界卫生组织中枢系统肿瘤分类将其归为组织增生症的一种)多见于儿童与青少年,而转移性肿瘤见于老年患者;近期妊娠女性患者提示淋巴细胞性垂体炎可能。除了详细的病史记录、全面体格检查以外,垂体增强MRI虽然没有特异性,但是其影像学特征有助于缩小病因范围[3]。需同时行全身多系统评估,除垂体及靶腺相关功能外,需查颈胸腰腹CT、肿瘤标志物、血管紧张素转化酶、人绒毛膜促性腺激素(hCG)、甲胎蛋白(AFP)、IgG4、乳酸脱氢酶(LDH)、自身免疫指标甚至PET/CT等,具体检查内容和顺序应结合患者综合情况而有所侧重[4]。当系统检查发现异常时,部分情况可直接按一元论病因得出结论,如血清hCG显著升高,特别是男性青少年患者,可临床诊断生殖细胞肿瘤;当影像学检查发现颅外病灶,可活检进一步帮助明确病因。如全面评估均无异常发现,可行垂体柄病变活检以明确病因。Catford等[4]建议孤立性垂体柄病灶>6.5 mm、中枢性尿崩和(或)腺垂体功能减退、影像学病变进展时,可由经验丰富的医师进行活检[5]。不符合上述条件而在对症治疗垂体功能减退时,建议3~6个月复查MRI观察病灶变化趋势[1,2]。临床中发现一部分患者,病灶可自行缩小甚至消失。我院随访18例垂体柄增粗患者自然病程,7例患者病灶自行消失(未发表数据)。
本例患者因烦渴、多尿,同时伴有胸痛,切除左侧第5肋骨病变,病理会诊免疫组化S-100(+),CD1α(+),langerin(+),LCH诊断明确。LCH由朗格汉斯细胞克隆增殖形成(除了肺部原发性LCH),具体机制不明。既往将其归在炎症性病变中,由于半数研究样本中发现BRAFV600E基因突变,目前倾向于将其归为肿瘤增生性病变[6]。LCH常多器官累及,临床表现因累及器官的不同而不同[7]。最常累及骨骼(80%),其次是皮肤(33%)及垂体(25%),然后是血液系统(15%)、肺(15%)及淋巴结(5%~10%)[7]。25%的患者出现中枢性尿崩症,多系统累及患者中高达50%[8]。累及鞍区者MRI可表现为垂体柄增粗(>3 mm)、下丘脑占位等,根据影像学特点无法确诊,确诊依赖病理[9],膜表面S-100蛋白、Ki-67抗原、CD1α抗原、langerin抗原及膜结合的ATP酶等为确诊依据。本例患者尿崩症状同时鞍区MRI增强结果发现垂体柄下方结节状增粗,根据临床特点综合考虑垂体柄病灶为LCH。
LCH患者治疗方案的制定与随访也是临床一大挑战。由于LCH可累及全身多系统多病灶,在制定治疗方案前需对患者进行全身病情的评估。2013年关于青少年和成人LCH共识[5,6]推荐所有患者治疗前需要完成血常规、血生化(肝肾功能、电解质)、红细胞沉降率、C反应蛋白、凝血功能、腹部B超(肝、脾和淋巴结)、甲状腺B超及甲状腺功能、胸部X线片、全身骨X线片等常规检查,结合患者临床表现选择性行头颅或鞍区MRI检查,病变部位的活检等,PET-CT可替代B超、CT/MRI,更能发现病灶所在。进一步检查方案根据患者症状及基础评估结果而定[5]。本病例在肋骨病灶病理确诊LCH后,入院后查血、尿常规及电解质、肝肾功能正常、尿渗透压偏低,垂体-甲状腺轴、肾上腺皮质轴、性腺轴评估均在正常范围;肿瘤标志物在正常范围;腹部B超未及肝脾和腹腔淋巴结肿大,浅表淋巴结B超检查发现双侧腋下少量肿大淋巴结,骨穿检查未见造血系统累及;胸片未见异常;全身扁骨及长骨X线片未见异常。鞍区MRI增强:垂体柄下方结节状增粗;PET/CT示左侧第5肋骨病变治疗后,垂体柄稍饱满,余PET显像未见FDG代谢异常增高灶。结合烦渴、多尿、胸痛症状,考虑患者目前LCH累及骨骼和垂体柄。LCH的治疗依据其累及器官/系统的部位及多少[6,7]。2013年关于成人LCH诊治的欧洲共识[6]建议LCH累及单个系统时,主要是针对局部病灶的治疗,有两个以上系统累及或者一个系统多部位、危险器官(骨髓、肝、脾或中枢)累及者需行系统治疗;对于症状明显的多系统累及患者,建议阿糖胞苷(cytarabine)100 mg/m2(第1~5天),每4周1次静脉滴注,或者依托泊苷(etoposide)100 mg/m2(第1~5天),每4周1次静脉滴注,长春地辛和泼尼松龙的治疗类似儿科中的使用。2~3个疗程后需要评估患者病情,如果病情有进展或活动,需要进行类似治疗前的全面评估。本病例中,患者19岁,病灶累及骨骼及垂体柄两个系统,根据目前LCH治疗共识[6,7]给予长春地辛联合醋酸泼尼松的治疗方案。治疗后随访患者尿崩症状有明显改善,包括骨骼系统在内全身各系统检查并未发现新发病灶,最后一次随访中其垂体MRI提示垂体柄区域病灶明显缩小,尿崩逆转,提示治疗效果好。该患者垂体病变仅累及垂体柄,且病灶较小,临床上仅表现为尿崩,治疗前后无其他下丘脑功能障碍如贪吃、嗜睡等,但体重增加15 kg,考虑为治疗方案中糖皮质激素的不良反应。如LCH累及下丘脑者应注意下丘脑功能障碍伴随的摄食障碍和代谢异常,在选择治疗方案时尽可能避免糖皮质激素。
对于垂体柄增粗需进行全面系统地评估,有条件时手术活检尽可能明确病因诊断;当合并其他系统临床表现尤其是骨骼系统损害时,LCH是可能病因;外周病灶活检病理报告可明确诊断;明确LCH诊断后,需全面评估LCH累及情况,个体化制定治疗和随访方案。


























