
分析原发性干燥综合征(pSS)合并静脉血栓病例的临床特点,提高对该病的认识。
北京朝阳医院2013年1月至2017年10月资料完整的pSS合并静脉血栓病例的临床和实验室特点。16例中女14例,男2例,年龄45~71岁。
单侧小腿肌间静脉血栓6例,双侧肌间静脉血栓1例,右侧胫后静脉血栓1例,单侧腘静脉血栓2例,双下肢静脉血栓合并肺栓塞2例,颈静脉血栓2例,单大隐静脉血栓2例。12例患者以干燥症状起病,4例患者以肺部症状起病。16例患者抗心磷脂抗体、狼疮抗凝物均为阴性。抗SSA 52 000抗体、抗SSA 60 000抗体阳性例数分别12例。16例患者均伴有间质肺疾病。
pSS患者具有潜在静脉血栓高风险,尤其是合并间质肺疾病和抗SSA抗体阳性患者,更应提高对pSS患者静脉血栓的警惕。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
原发性干燥综合征(pSS)是一种自身免疫性外分泌腺体慢性炎症性疾病,主要侵犯唾液腺和泪腺。同时,该病也可累及其他器官造成多脏器受损,导致其功能衰竭,严重影响患者生活质量,甚至缩短患者生存时间。自身免疫性疾病中,血栓事件多见于系统性红斑狼疮(SLE),抗磷脂综合征(APS)。
但是,pSS血栓发生率低。目前,国内外关于pSS合并静脉血栓的临床报道甚少。本研究总结16例pSS合并静脉血栓的临床和实验室特点,希望有益于提高临床医师对静脉血栓的认识有所裨益。
北京朝阳医院2013年1月至2017年10月资料完整pSS合并静脉血栓病例16例,年龄45~71岁。单侧肌间静脉血栓6例,双侧肌间静脉血栓1例,右侧胫后静脉血栓1例,单侧腘静脉血栓2例,双下肢静脉血栓合并肺栓塞2例,颈静脉血栓2例,单大隐静脉血栓2例。16例中女14例,男2例。
pSS符合1992年欧洲分类标准或者2016年美国/欧洲分类标准。研究对象均无血栓高危因素:吸烟史,长期服用激素类避孕药物史,长期静坐史等。研究资料包括:血常规,血脂系列,自身抗体,类风湿因子(RF),红细胞沉降率(ESR),C反应蛋白(CRP),免疫球蛋白,补体C3,补体C4,抗心磷脂抗体(ACL),抗β2糖蛋白1抗体(β2GPI),狼疮抗凝物(LA),抗中性粒细胞胞质抗体(ANCA),D-二聚体(D-Dimer),活化部分凝血酶原时间(APTT),纤维蛋白原(Fbg),肺HRCT。肺脏进行欧洲干燥综合征疾病活动度分级(ESSDAI)。
12例以干燥症状起病,病史3个月~5年;4例无干燥综合征症状仅以肺部受累症状起病。1例伴随周围神经病变。1例有尘肺病史。2例高血压病史,血压控制稳定。6例初诊时发现新鲜静脉血栓。10例初诊时发现陈旧静脉血栓或血栓病史。
15例胆固醇、三酰甘油均正常,1例胆固醇轻度升高,1例三酰甘油轻度升高。4例血常规白细胞降低,12例白细胞正常。2例贫血。4例血小板低于50×109/L。16例ANCA-PR3及ANCA-MPO均为阴性。8例患者ESR升高,8例ESR正常。15例CRP均正常,1例CRP轻度升高。免疫学指标ESSDAI:2分6例,1分2例,0分8例。血液系统ESSDAI:1分2例,2分4例,0分10例。LA、ACL均为阴性,抗β2GPI抗体阳性1例。D-Dimer升高2例。APTT 1例延长。Fbg均在正常范围。其他免疫指标见表1。
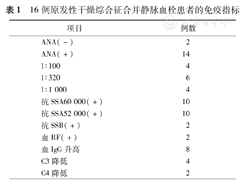
16例原发性干燥综合征合并静脉血栓患者的免疫指标
16例原发性干燥综合征合并静脉血栓患者的免疫指标
| 项目 | 例数 |
|---|---|
| ANA(-) | 2 |
| ANA(+) | 14 |
| 1∶100 | 4 |
| 1∶320 | 6 |
| 1∶1 000 | 4 |
| 抗SSA60 000(+) | 10 |
| 抗SSA52 000(+) | 10 |
| 抗SSB(+) | 2 |
| 血RF(+) | 2 |
| 血IgG升高 | 8 |
| C3降低 | 4 |
| C4降低 | 2 |
4例积化性肺炎,6例以肺大泡性病变为主,6例以非特性间质性肺炎为主。肺脏ESSDAI,5分(轻度肺脏受累)6例,10分(中度肺脏受累)10例。1例出现周围神经受累,ESSDAI,5分。2例心脏超声正常,4例左侧心房轻度增大,6例轻度肺动脉高压,2例双侧心房增大,2例右心增大。16例均通过静脉超声检查证实静脉血栓(表2)。
6例应用纷乐+帕夫林治疗。2例仅加用帕夫林治疗。2例仅加用纷乐治疗。6例肺内新发病变,加用糖皮质激素+静脉环磷酰胺治疗。4例新发静脉血栓(其中2例考虑合并肺栓塞)应用华法林抗凝。8例陈旧静脉血栓及4例肌间静脉血栓未抗凝治疗。上述治疗后,16例病稳定,1例后因合肺部感染死亡。
某些自身免疫性疾病,特别是存在APS,容易合并静脉血栓事件。目前,关于pSS合并静脉血栓的文献报道有限。国内仅有3例pSS合并下肢静脉血栓的病例报道[1]。Haga等[2]对90例pSS随访4.6年后有7例发生静脉血栓。pSS合并静脉血栓发病率低,北京朝阳医院近4年仅7例。但是,静脉血栓是致命的并发症,严重影响患者生活质量,甚至因肺栓塞而猝死。pSS发生静脉血栓的原因并不十分清楚。本研究希望有助于提高临床医师对pSS合并静脉血栓的警惕和认识,并为进一步深入研究提供借鉴。
传统静脉血栓的高危因素包括妊娠、口服避孕药物、激素替代治疗、肿瘤、长期制动等。其他有关因素包括高血压、糖尿病、血脂异常等。这些高危因素可以促进pSS患者静脉血栓的形成。本研究中16例患者中无长期高血压状及高血脂,无长期服用糖皮质激素史等静脉血栓高危因素。因而,本组患者静脉血栓形成与可能与上述传统高危因素无关。
抗磷脂抗体(aPL)或者APS是静脉血栓的高危因素。pSS可以伴有aPL或者APS。Pasoto等[3]对100例pSS患者流调显示,aPL阳性率16%。LA(9%)是最常见,其次是抗β2GPI (5%)和ACL (4%)。仅5例患者发生静脉血栓,其中3例静脉血栓APS和LA阳性。在aPL阳性患者中深静脉血栓发生显著增高。但是,关于aPL阳性及APS与静脉血栓关系存在争议。本组16例患者的ACL(IgG/IgM/IgA)和LA(IgG/IgM/IgA)均为阴性,其中仅2例抗β2GPI阳性,2例APTT轻度升高,4例血小板(40~50)×109,未提示与aPL有关。Haga等[2]对90例pSS患者随访4.6年,7例出现静脉血栓。1例患者ACL-IgG阳性,但抗β2GPI和LA均为阴性。该队列研究显示,静脉血栓似乎与aPL无关。Mercurio等[4]报道2例中枢神经系统静脉血栓患者,3种aPL抗体均为阴性。学者们认为3种可能的机制解释aPL阴性患者发生静脉血栓。首先,既往aPL阳性;其次,患者血清中存在传统的实验室检测方法不能检测的磷脂类抗体或蛋白辅助因子,如磷酸酰丝氨酸,磷脂酸,磷脂酰肌醇等。第三,患者存在凝血异常。因此,pSS发生静脉血栓与aPL的关系尚不明确,可能涉及多种危险因素。
ANCA是否与pSS的血管病变相关呢? Font等[5,6]报道82例pSS患者,ANCA阳性9例(11%),其中p-ANCA 7例,血管受累8例(89%)。对于ANCA阳性与pSS血管病变尚存在争议。Nishiya等[7]报道60例pSS患者,ANCA阳性率16.7%。但是,与pSS临床表现之间没有相关性。他们认为,ANCA仅是一种多克隆B细胞激活的附带现象,无特殊临床意义。本组16例患者ANCA-PR3及ANCA-MPO均为阴性。因此,ANCA与静脉血栓关系尚需进一步研究。
流行病学结果表明,特发性肺纤维化(IPF)患者合并静脉血栓的风险增加,是间质肺疾病(ILD)肺外并发症。我院IPF患者的静脉血栓发病率是9.9%。Park[8]的研究显示,ILD患者发病率是2.79%。既往多项研究提出,ILD是静脉血栓的高危因素,发生静脉血栓的风险提高4~6倍[8]。本组16例患者均表现为ILD。其中,10例肺CT提示新进展的肺脏病变,肺脏ESSDAI评分显示肺脏轻中度受累。研究证实,ILD合并静脉血栓的机制包括纤维化导致肺血流速度减低,产生的淤血加大静脉血栓发生的风险;纤维化后凝血纤溶异常。因此,pSS合并ILD的患者,应警惕静脉血栓。
对于自身抗体与静脉血栓关系尚无大队列究的相关报道。西班牙学者对1 010例pSS患者队列研究显示,抗SSB抗体阳性、低补体、高球蛋白血症的患者更易出现血管病变[9]。本组病例抗SSA 52 000阳性率、抗SSA 60 000阳率及抗SSB抗体阳性率分别是66.7%、66.7%及11.1%,高球蛋白血症患者比例44.5%。本研究结果提示,抗SSA抗体、高球蛋白血症可能与静脉血栓形成有关。关于pSS与静脉血栓的发病率低,本研究所涉及样本量少,后续将增加样本量,进行深入研究。
pSS患者具有潜在静脉血栓高风险,特别是pSS诊断后第1年内[9]。pSS免疫炎症异常可能出现凝血级联反应的异常活化,显示炎症紊乱状态下静脉血栓事件的可能机制。本组10例患者ILD显示急性进展,6例静脉血栓形成在半年之内,1例急性肺栓塞。提示,急性炎症紊乱促进高凝状态。因此,pSS早期诊断,早期治疗,尽快控制免疫紊乱,可以预防静脉血栓发生。
自身免疫性疾病是静脉血栓的高危因素。但是,pSS患者中静脉血栓罕见。关于静脉血栓机制,除了静脉瘀滞,高凝外,免疫性炎症通过改变选择素和细胞黏附因子导致动脉和静脉内皮功能异常是主要因素[10]。临床实践中,pSS患者静脉血栓发生时通常缺乏系统性炎症。本组病例与系统性炎症及高凝状态相关的指标如CRP、ESR、Fbg、D-Dimer等均无显著升高。是否存在内皮细胞功能紊乱导致对静脉血栓的影响?本团队将进一步深入研究内皮细胞功能异常与静脉血栓间的关系,及相应的靶向治疗。
鉴于静脉血栓的高致残率和死亡率,临床医生必须意识到pSS是一种血栓前状态,尤其诊断后早期风险最高。因此,提高对pSS患者静脉血栓的警惕。即使患者aPL均为阴性,临床医生也不应该忽视静脉血栓。同时,在pSS合并ILD和抗SSA抗体阳性的患者,更应该重视静脉血栓的风险,预防静脉血栓事件发生至关重要。



























