
探讨Modic改变对于经椎间孔腰椎椎间融合术(TLIF)术后椎间融合效果和融合器沉降的影响。
回顾性分析186例于2015年1月至2018年1月在南京鼓楼医院放置单枚高分子聚醚醚酮(PEEK)融合器行单节段TLIF手术患者的临床资料,根据术前MRI影像放置融合器节段是否存在Modic改变,将患者分为Modic改变组和无Modic改变组,于X线片上测量术前、术后及末次随访时行TLIF节段的椎间隙高度、腰椎前凸角和融合器节段前凸角,于末次随访的CT上观察融合情况和融合器沉降。使用Oswestry功能障碍指数(ODI)、腰腿痛视觉模拟评分(VAS)评价临床疗效。各组不同时间数据比较采用配对t检验。
全组患者中男70例,女116例,平均年龄(55±13)岁。Modic改变组99例,Ⅰ型25例,Ⅱ型66例,Ⅲ型8例;无Modic改变组87例。两组患者在年龄、性别、诊断、手术时间、手术出血量、融合节段数、随访时间及术后影像学参数等差异均无统计学意义。术后平均随访(19±4)个月(13~48个月),两组所有放置融合器节段均达到1级或2级融合。34例(18.3%,34/186)观察到融合器沉降。Modic改变组融合器沉降发生率(24.2%,24/99)高于无Modic改变组(11.5%,10/87),差异有统计学意义(χ2=5.038,P<0.05),其中Ⅰ型(28.0%,7/25)和Ⅱ型(24.2%,16/66)明显高于无Modic改变组(11.5%,10/87)。术前、术后及末次随访时Modic改变组与无Modic改变组VAS评分及ODI的差异均无统计学意义(t=0.397~1.568,均P>0.05)。
术前Modic改变对于TLIF术后椎间融合效果没有明显影响,但可显著增加融合器沉降风险,尤以Modic Ⅰ型和Ⅱ型为著。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
Modic改变是MRI上终板及终板下骨质的信号改变,分为三型[1,2]。研究表明,Modic改变与腰椎退行性变密切相关,是引起腰痛的原因之一[2,3],因此Modic改变对手术疗效的影响受到广泛关注。不过,这些关注多集中于生活质量方面,对融合效果关注甚少。Modic改变是否影响融合效果目前尚存争议。Kim等[4]指出Modic改变抑制融合过程,伴Modic改变的患者行后路椎间融合术后融合率较低。而也有研究提示伴Modic改变患者融合效果良好[5]。在椎间融合术中,植入椎间融合器可恢复椎间隙高度与腰椎曲度,促进融合。然而,融合器沉降并不罕见。融合器下沉可致椎间隙高度、局部前凸角度丢失,影响融合效果[6]。既往研究认为,融合器沉降与骨质疏松、椎间隙过度撑开及终板损伤等有关[6,7]。目前,Modic改变是否会影响椎间融合效果及增加融合器沉降的风险,尚缺乏详细分析。本研究回顾性分析在我院接受经椎间孔椎间融合术(TLIF)治疗的腰椎退变性疾病患者的临床资料,探讨Modic改变对椎间融合效果和融合器沉降的影响。
回顾性分析于2015年1月至2018年1月在南京鼓楼医院接受TLIF手术治疗的腰椎退行性疾病患者的临床资料。患者纳入标准:(1)术前行腰椎MRI检查;(2)仅行单节段TLIF,且放置单枚高分子聚醚醚酮(PEEK)融合器;(3)术后随访>1年;(4)末次随访时有完整的临床及影像学资料,包括立位全脊柱正侧位X线片和腰椎CT。排除标准:(1)术中终板损伤或术后即刻摄片发现融合器沉降者;(2)既往有腰椎手术或外伤病史者;(3)合并有腰椎先天性或发育性畸形者;(4)骨质疏松者(骨密度T值≤-2.5);(5)手术节段有许莫氏结节;(6)术后并发急性或迟发型深部感染者。
最终本研究共纳入186例患者,其中男70例,女116例,平均年龄(55±13)岁(23~78岁),腰椎间盘突出65例(合并腰椎管狭窄59例),崩裂性滑脱38例(合并腰椎间盘突出4例,腰椎管狭窄15例),退变性滑脱42例(合并腰椎间盘突出16例,腰椎管狭窄29例),腰椎管狭窄41例(合并腰椎间盘突出37例)。所有患者术前行立位全脊柱正侧位和腰椎动力位X线片、腰椎CT平扫、腰椎MRI检查及骨密度测量。根据术前MRI影像放置融合器的节段终板是否存在Modic改变,将患者分为Modic改变组和无Modic改变组。本研究获南京鼓楼医院伦理委员会批准。
参照陈曦等[8]的手术方法,采用开放后正中入路,显露手术节段椎体及小关节突等解剖结构,确定进钉点,准确置入椎弓根螺钉。先行全椎板减压,再针对明显椎间盘突出或滑脱节段行单一节段TLIF术,采用症状较重一侧作为TLIF入路侧。切除该侧下关节突及上关节突上部内侧,切除深面的黄韧带,暴露椎间孔,显露椎间盘的后外侧,保护椎管内硬膜、下位神经根及椎间孔内神经根。切开椎间盘,运用髓核钳清除髓核,并用刮匙清理上下终板,刮除病变的软骨终板,使骨性终板少量渗血。置棒连接椎弓根螺钉后并撑开椎间隙,再次保护好神经。使用特殊角度终板绞刀和铲刀尽量去除前侧的纤维环组织,椎间隙内预先植入自体骨颗粒,选择适当尺寸的PEEK融合器(Capstone,美国美敦力公司)1枚放入椎间隙,安装连接棒加压抱紧。多节段融合固定中未做椎间融合节段行横突间植骨融合。
术前及术后48 h应用抗生素预防感染。引流量小于50 ml/24 h后拔除引流管,术后1周复查腰椎正侧位片。卧床期间行直腿抬高功能锻炼,支具保护下地活动。术后3、6个月复查立位全脊柱正侧位片,术后1年以上每年复查立位全脊柱正侧位X线片和腰椎CT平扫。
观察术前腰椎MRI矢状面影像,判断终板是否存在Modic改变。所有MRI影像资料均由1位放射科医师与1位脊柱外科医师进行观察,对有异议的影像进行讨论分析后确定。Modic改变的分型:无信号改变;Ⅰ型:T1加权像(T1WI)上终板及终板下骨质为低信号,T2加权像(T2WI)上为高信号;Ⅱ型:T1WI上为高信号,T2WI为等信号或轻度升高;Ⅲ型,T1WI、T2WI上信号均降低。
采用SurgimapSpine软件测量所有患者术前、术后1周和末次随访时站立位全脊柱侧位X线片,记录放置融合器节段及腰椎矢状面参数。所有参数均由1名脊柱外科医师独立测量,连续测量2次后计算平均值。矢状面参数:(1)腰椎前凸角(LL),L1椎体上终板与S1椎体上终板间成角,定义前凸为正值;(2)融合器节段前凸角(SL):放置融合器节段的上下椎体的上终板间成角,定义前凸为正值;(3)TLIF节段椎间隙高度(DH):分别测量椎间隙前中后缘的高度,取其平均值。
术前、术后3个月和末次随访时对患者进行问卷调查以评价生活质量,采用Oswestry功能障碍指数(ODI)量表进行临床疗效评价,腰腿痛采用视觉模拟评分(VAS)进行评估。由2名脊柱外科医师对以上问卷独立进行计算,对有异议的问卷进行再次统计。
采用SPSS 22.0软件进行统计学处理。计量资料采用 ±s表示。运用χ2检验及Fisher精确检验比较两组节段差异、融合率和融合器沉降的发生率,对两组患者的一般资料、影像学参数及临床量表评分采用独立样本t检验,各组不同时间数据比较采用配对t检验。检验水准均取双侧0.05。
±s表示。运用χ2检验及Fisher精确检验比较两组节段差异、融合率和融合器沉降的发生率,对两组患者的一般资料、影像学参数及临床量表评分采用独立样本t检验,各组不同时间数据比较采用配对t检验。检验水准均取双侧0.05。
所有患者均于一期顺利完成手术。手术时间(210±41)min,出血量(416±127)ml。单节段固定101例,双节段54例,三节段及以上31例。4例术后出现TLIF侧下肢麻木、感觉减退,但无运动及大小便功能障碍,给予营养神经治疗,6~14 d后感觉恢复;2例出现术中硬膜撕裂,予以修补,其中1例术后有脑脊液漏,拔出引流加压包扎后伤口Ⅰ期愈合;1例术后浅表性伤口感染,予以敏感抗生素及时换药后延迟愈合。平均随访(19±4)个月(13~48个月),其间均无内固定松动、断裂发生。
Modic改变组99例,其中Ⅰ型25例,Ⅱ型66例,Ⅲ型8例。无Modic改变组87例。两组患者的年龄、随访时间、融合节段、融合器放置节段及术后局部形态学参数等差异均无统计学意义(表1、表2)。术前及末次随访时,Modic改变组DH均低于无Modic改变组,差异有统计学意义(t=2.491、2.530,均P<0.05)。
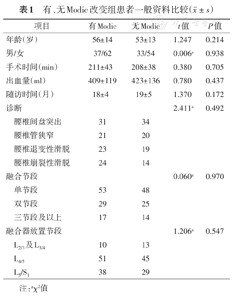
有、无Modic改变组患者一般资料比较( ±s)
±s)
有、无Modic改变组患者一般资料比较( ±s)
±s)
| 项目 | 有Modic | 无Modic | t值 | P值 | |
|---|---|---|---|---|---|
| 年龄(岁) | 56±14 | 53±13 | 1.247 | 0.214 | |
| 男/女 | 37/62 | 33/54 | 0.006a | 0.938 | |
| 手术时间(min) | 211±43 | 208±38 | 0.380 | 0.705 | |
| 出血量(ml) | 409±119 | 423±136 | 0.780 | 0.437 | |
| 随访时间(月) | 18±4 | 19±5 | 1.370 | 0.172 | |
| 诊断 | 2.411a | 0.492 | |||
| 腰椎间盘突出 | 31 | 34 | |||
| 腰椎管狭窄 | 21 | 20 | |||
| 腰椎退变性滑脱 | 23 | 19 | |||
| 腰椎崩裂性滑脱 | 24 | 14 | |||
| 融合节段 | 0.060a | 0.970 | |||
| 单节段 | 53 | 48 | |||
| 双节段 | 29 | 25 | |||
| 三节段及以上 | 17 | 14 | |||
| 融合器放置节段 | 1.206a | 0.547 | |||
| L2/3及L3/4 | 10 | 13 | |||
| L4/5 | 51 | 45 | |||
| L5/S1 | 38 | 29 | |||
注:aχ2值
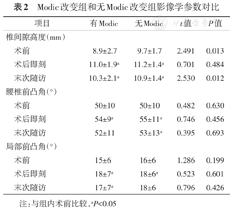
Modic改变组和无Modic改变组影像学参数对比
Modic改变组和无Modic改变组影像学参数对比
| 项目 | 有Modic | 无Modic | t值 | P值 | |
|---|---|---|---|---|---|
| 椎间隙高度(mm) | |||||
| 术前 | 8.9±2.7 | 9.7±1.7 | 2.491 | 0.013 | |
| 术后即刻 | 11.0±1.9a | 11.2±1.4a | 0.701 | 0.484 | |
| 末次随访 | 10.3±2.1a | 10.9±1.4a | 2.530 | 0.012 | |
| 腰椎前凸角(°) | |||||
| 术前 | 50±10 | 50±10 | 0.482 | 0.630 | |
| 术后即刻 | 54±9a | 55±11a | 0.746 | 0.456 | |
| 末次随访 | 52±11 | 53±13a | 0.395 | 0.693 | |
| 局部前凸角(°) | |||||
| 术前 | 15±6 | 16±6 | 1.286 | 0.199 | |
| 术后即刻 | 18±7a | 18±6a | 0.523 | 0.601 | |
| 末次随访 | 17±7a | 18±6 | 0.796 | 0.426 | |
注:与组内术前比较,aP<0.05
在末次随访时,Modic改变组1级融合76例,2级融合23例。其中Ⅰ型1级融合17例,2级融合8例;Ⅱ型1级融合54例,2级融合12例;Ⅲ型1级融合5例,2级融合3例。无Modic改变组1级融合72例,2级融合15例,两组患者均未见3级或4级融合。各组间融合等级分布差异虽无统计学意义,但Modic Ⅰ型和Ⅱ型融合2级发生率要明显高于无Modic改变组。
全部患者中有34例(18.3%)观察到沉降,沉降2~4 mm者25例(13.4%),>4 mm者9例(4.8%);L5/S1节段发生率最高,为23.9%(16/67)。单节段、双节段和三节段及以上融合沉降的发生率分别为14.8%(15/101),20.3%(11/54),25.8%(8/31),差异无统计学意义(χ2=2.128,P>0.05)(表3)。Modic改变组24例(24.2%)发生沉降,沉降侧的终板均存在Modic改变;无Modic改变组中10例(11.5%)观察到沉降。Modic改变组沉降率高于无Modic改变组,差异有统计学意义(χ2=5.038,P<0.05)。Modic Ⅰ、Ⅱ和Ⅲ型沉降发生率分别为28.0%(7/25)、24.2%(16/66)和12.5%(1/8),Modic Ⅰ和Ⅱ型融合器沉降率明显高于无Modic改变组(11.5%,10/87),尽管差异无统计学意义,但接近临界值(χ2=5.762,P=0.056)。
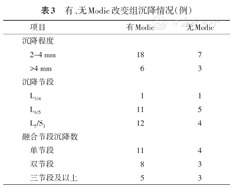
有、无Modic改变组沉降情况(例)
有、无Modic改变组沉降情况(例)
| 项目 | 有Modic | 无Modic | |
|---|---|---|---|
| 沉降程度 | |||
| 2~4 mm | 18 | 7 | |
| >4 mm | 6 | 3 | |
| 沉降节段 | |||
| L3/4 | 1 | 1 | |
| L4/5 | 11 | 5 | |
| L5/S1 | 12 | 4 | |
| 融合节段沉降数 | |||
| 单节段 | 11 | 4 | |
| 双节段 | 8 | 3 | |
| 三节段及以上 | 5 | 3 | |
1级和2级融合患者、沉降和未沉降患者以及Modic改变组和无Modic改变组间的ODI和VAS评分,无论是术前、术后,还是末次随访时对比差异均无统计学意义。所有患者术后3个月及末次随访时ODI和VAS评分均较术前明显改善(均P<0.05)(表4)。
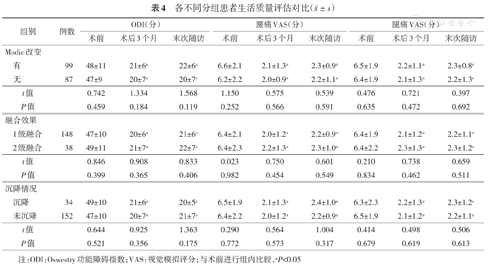
各不同分组患者生活质量评估对比( ±s)
±s)
各不同分组患者生活质量评估对比( ±s)
±s)
| 组别 | 例数 | ODI(分) | 腰痛VAS(分) | 腿痛VAS(分) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 术前 | 术后3个月 | 末次随访 | 术前 | 术后3个月 | 末次随访 | 术前 | 术后3个月 | 末次随访 | ||||
| Modic改变 | ||||||||||||
| 有 | 99 | 48±11 | 21±6a | 22±6a | 6.6±2.1 | 2.1±1.3a | 2.3±0.9a | 6.5±1.9 | 2.2±1.1a | 2.3±0.8a | ||
| 无 | 87 | 47±9 | 20±7a | 20±7a | 6.2±2.2 | 2.0±0.9a | 2.2±1.1a | 6.4±1.9 | 2.1±1.3a | 2.2±1.3a | ||
| t值 | 0.742 | 1.334 | 1.568 | 1.150 | 0.575 | 0.539 | 0.476 | 0.721 | 0.397 | |||
| P值 | 0.459 | 0.184 | 0.119 | 0.252 | 0.566 | 0.591 | 0.635 | 0.472 | 0.692 | |||
| 融合效果 | ||||||||||||
| 1级融合 | 148 | 47±10 | 20±6a | 21±6a | 6.4±2.1 | 2.0±1.2a | 2.2±0.9a | 6.4±1.9 | 2.1±1.2a | 2.2±1.1a | ||
| 2级融合 | 38 | 49±11 | 21±7a | 22±7a | 6.4±2.3 | 2.2±1.3a | 2.3±1.0a | 6.4±2.2 | 2.3±1.3a | 2.3±1.2a | ||
| t值 | 0.846 | 0.908 | 0.833 | 0.023 | 0.750 | 0.601 | 0.210 | 0.738 | 0.659 | |||
| P值 | 0.399 | 0.365 | 0.406 | 0.982 | 0.454 | 0.549 | 0.834 | 0.462 | 0.511 | |||
| 沉降情况 | ||||||||||||
| 沉降 | 34 | 49±10 | 21±6a | 20±5a | 6.5±1.9 | 2.1±1.3a | 2.4±1.0a | 6.3±2.3 | 2.2±1.3a | 2.3±1.2a | ||
| 未沉降 | 152 | 47±10 | 20±7a | 21±7a | 6.4±2.2 | 2.0±1.2a | 2.2±0.9a | 6.5±1.9 | 2.1±1.2a | 2.2±1.1a | ||
| t值 | 0.644 | 0.925 | 1.363 | 0.290 | 0.564 | 1.004 | 0.414 | 0.498 | 0.506 | |||
| P值 | 0.521 | 0.356 | 0.175 | 0.772 | 0.573 | 0.317 | 0.679 | 0.619 | 0.613 | |||
注:ODI:Oswestry功能障碍指数;VAS:视觉模拟评分;与术前进行组内比较,aP<0.05


Modic改变与椎间盘退变关系密切[1,2,3,11]。杜长志等[12]发现青少年椎间盘突出中未见Modic改变,可为其证。生物力学研究认为,椎间盘退变使其缓冲作用减弱,终板承受剪切应力增大,引发微骨折,出现炎症反应[2,3,13]。而椎间盘营养来源于软骨终板的弥散作用,终板的损伤将加重椎间盘退变[14,15]。Modic Ⅰ型的组织学特点是终板破坏伴骨小梁增厚,血管肉芽组织、纤维组织填充;Ⅱ型是慢性重复损伤导致的终板破坏,脂肪组织取代骨髓中的造血组织;Ⅲ型则是骨质硬化形成[1,2],印证了上述假说。Modic Ⅰ型常是损伤急性期的表现,Ⅱ型则趋于稳定,可能继发于Ⅰ型中纤维血管组织的瘢痕化,在炎症因子、局部微环境及生物力学改变刺激下引起脂肪细胞增多,红黄骨髓转化[1,2,11]。本研究Modic改变以Ⅱ型为主,这与终板退变的进程有关;术前Modic改变组的椎间隙高度低于无Modic改变组,表明伴Modic改变的椎间盘退变程度较高。
在Modic改变中,局部微环境的变化可能会影响融合[1,2,16]。Toyone等[17]研究结果显示Modic Ⅰ型患者节段稳定性较差。Ⅲ型Modic改变的骨质硬化使得终板不能为植骨区提供营养和血供会影响融合效果[1,2,18]。Modic改变对于椎间融合效果的影响尚存争议。Lang等[19]评估14例融合不佳的患者,发现10例伴有Modic Ⅰ型改变。Kwon等[16]发现伴Modic改变患者的融合率低于正常患者,且Ⅲ型的融合率明显低于Ⅰ型和Ⅱ型。而Ohtori等[20]报道33例伴Modic改变行椎间融合的患者均成功融合。上述各研究中纳入病例、手术方式及随访时间等因素可能是造成融合效果差异的原因。本组患者均行TLIF,术中刮除终板,椎间隙置入自体骨及融合器,椎弓根螺钉固定,末次随访时,两组均达到融合1级或2级,效果满意。虽然Modic Ⅰ型和Ⅲ型的融合效果要稍逊于Modic Ⅱ型和无Modic改变组,但无统计学差异,且并未对生活质量造成影响,因此Modic改变对椎间融合的影响还需进一步探讨。
融合器沉降的危险因素包括融合节段L5/S1、融合节段数和椎间隙撑开高度等[10,21,22]。在本研究中,沉降的发生率为18.3%,L5/S1节段发生率最高。不同融合节段数的沉降率虽无统计学差异,但存在一种趋势:融合节段数越多,沉降率越高,与既往研究一致。终板与融合器沉降密切相关。多数研究结果表明终板损伤和骨质疏松可使终板承载能力降低,为沉降的危险因素[7,23,24]。而Modic改变中的终板损伤可能削弱了终板强度,微环境改变影响了终板的营养供给,损伤无法及时修复[1,2,15]。大量破骨和成骨细胞活跃导致编织骨增多,骨小梁增厚,微结构改变,影响了对融合器的支撑作用。本研究中,Modic改变组沉降率显著高于无Modic改变组,其中Modic Ⅰ型和Ⅱ型的沉降率均高于无Modic改变组,表明Modic改变对融合器沉降存在影响。而Modic Ⅲ型的沉降率较低,这可能与其骨质硬化有关[1]。虽然末次随访时椎间隙高度有所丢失,但是仍高于术前水平,且未影响生活质量,这可能是沉降程度较轻。
通过文献和本研究结果,我们总结应对融合失败和融合器下沉的策略:(1)牢靠的内固定可在术后加强手术节段的稳定性,促进融合;(2)刮除软骨终板去除部分病变,清理终板时使其少量渗血,可促进植骨区的营养和血供,有助于融合[18];(3)保留完整的骨性终板,防止终板受损,可预防融合器沉降[7];(4)选择合适的融合器,避免椎间隙过度撑开,以免损伤终板[6,21];(5)联合使用横突间植骨确保手术节段实现骨性融合。
本研究的局限如下:(1)本研究中Modic Ⅰ型和Ⅲ型患者较少,这与Modic改变分布特点有关,需进一步扩大样本量;(2)随访时间较短,Modic改变的发展及远期疗效尚不明确;(3)本研究着重分析Modic改变对融合效果及融合器沉降的影响,未纳入融合器位置和终板形态等参数,对影响下沉因素的分析不全面。
综上所述,行TLIF手术的腰椎退变性疾病患者均获得良好的融合效果,手术节段存在的Modic改变对于椎间融合效果没有明显影响,但可增加融合器沉降的风险,尤以Ⅰ型和Ⅱ型为著。
所有作者均声明不存在利益冲突



























