
患者为18岁女性,主因"原发性闭经,发现肾上腺占位1个月"入院。患者11岁出现乳房发育,13岁出现阴毛及腋毛生长,但无月经来潮,外院曾给予人工周期治疗无效;16岁时自觉脸变圆,毛发增多。辅助检查提示血孕酮、硫酸脱氢表雄酮、睾酮、皮质醇升高,促肾上腺皮质激素减低,中剂量地塞米松抑制试验不被抑制,肾上腺影像学检查提示左肾上腺区占位。考虑肾上腺多功能内分泌腺瘤可能性大,于全麻下行左肾上腺肿瘤切除,术后病理提示肾上腺皮质腺瘤。术后患者食欲减退、皮肤蜕皮,术后1个月出现月经初潮,复查血孕酮、硫酸脱氢表雄酮、睾酮、皮质醇水平下降。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
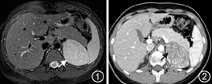
患者女,18岁,主因"原发性闭经,发现肾上腺占位1个月"于2018年7月12日收入北京协和医院内分泌科。患者为第2胎第1产,母孕期平顺,足月顺产,无窒息,出生体重3.0 kg,身长不详,无生殖器畸形。自幼身高增速与同年龄、同性别者相似,身高位于全班女生中游,13岁身高148 cm,16岁身高158 cm,18岁身高160.5 cm。学习成绩中上水平。11岁出现乳房发育,13岁出现阴毛及腋毛生长,但无月经初潮。2015年8月(15岁)时就诊外院,查性激素:卵泡刺激素(FSH)7.29 U/L,黄体生成素(LH)9.24 U/L,孕酮13.25 nmol/L,雌二醇187.39 pmol/L,睾酮2.79 nmol/L,催乳素0.44 nmol/L;染色体核型分析:46,XX;超声:考虑幼稚子宫(具体不详)。予以戊酸雌二醇环丙孕酮片(含戊酸雌二醇2 mg及醋酸环丙孕酮1 mg)(1次/d×21 d,停药7 d为1个周期)人工周期治疗,并联合中成药治疗(具体不详),服药期间无月经来潮,2个月后患者出现右乳房胀痛自行停用。2016年起自觉脸略变圆,毛发略增多,面部及背部痤疮增多,否认腹围增加、皮肤紫纹等。2016年1月再次因闭经于外院就诊,查24 h尿游离皮质醇(24 h UFC)75.83 μg(正常参考值:30~110 μg);促甲状腺激素(TSH)4.3 mU/L(正常参考值:0.3~5.0 mU/L),游离甲状腺素(FT4)16.30 pmol/L(正常参考值:11.5~23.5 pmol/L),游离三碘甲状腺原氨酸(FT3)9.12 pmol/L(正常参考值:3.5~6.5 pmol/L)。给予口服戊酸雌二醇片1 mg/次,1次/d×21 d联合黄体酮200 mg/次,1次/d×10 d,停药10 d为1个周期,仍无月经来潮,5个周期后停用。2018年6月20日为进一步诊治就诊我院门诊,完善相关检查:LH 8.24 U/L,FSH 7.99 U/L,孕酮15.72 nmol/L,雌二醇196.51 pmol/L,睾酮5.97 nmol/L(正常参考值:0.35~2.60 nmol/L),催乳素0.77 nmol/L,硫酸脱氢表雄酮(DHEAS)8.17 μmol/L(正常参考值:0.47~10.17 μmol/L),17α羟孕酮(17α-OHP)7.51 nmol/L(正常参考值:0.30~8.79 nmol/L);促肾上腺皮质激素(ACTH)8∶00<1.1 pmol/L,血皮质醇8∶00 239.84 nmol/L(正常参考值:110.4~615.5 nmol/L),24 h UFC 158.38 μg(正常参考值:12.3~103.5 μg);甲状腺功能正常。盆腔常规磁共振成像(MRI):幼稚型子宫;双侧卵巢体积小。肾上腺超声:左肾上腺区可见一5.9 cm×5.8 cm×4.4 cm低回声占位,形态尚规则,边界尚清,内见点状强回声,彩色多普勒血流显像:周边见条状血流信号。肾上腺薄层扫描+增强MRI(图1):左肾上腺区类椭圆形等T1、略长T2信号肿块,信号均匀,大小约49.4 mm×69.7 mm;增强扫描病灶呈明显延迟强化;周围组织未见明显浸润影。为进一步诊治以"高雄激素血症、左肾上腺区肿瘤"收入病房。病程中否认脸变圆红、腹围增加,否认特殊药物、保健品服用史,起病以来一般情况好,体重近1年稳定。

体格检查:血压120/59 mmHg(1 mmHg=0.133 kPa),心率92次/min,轻度锁骨上脂肪垫,未见水牛背,全身皮肤未见瘀斑、紫纹,面部及背部可见多发痤疮,面部毛发增多,唇上可见小须,双乳对称Ⅱ期,无触发泌乳,双侧乳晕可见细毛,心肺无殊,腹软无压痛,未触及包块,阴毛Ⅵ期,女性外阴,阴蒂增大,长约1 cm,肛周未见长毛。
辅助检查:血、尿、便常规及肝肾功能未见异常,电解质:血钠139 mmol/L,血钾3.9 mmol/L,血氯103 mmol/L,二氧化碳结合力(TCO2)24.5 mmol/L,空腹血糖4.6 mmol/L。肾上腺占位功能评估:肾上腺皮质轴:皮质醇节律消失(血皮质醇0∶00 249.23 nmol/L,血皮质醇8∶00 269.38 nmol/L);24 h UFC 149.64 μg,过夜小剂量地塞米松抑制试验不被抑制(服药后血皮质醇280.14 nmol/L);多次查ACTH8∶00<1.1 pmol/L。FSH 4.64 U/L,LH 7.14 U/L,雌二醇251.08 pmol/L,孕酮20.51 nmol/L,睾酮5.59 nmol/L,DHEAS 7.36 μmol/L,17α-OHP 15.24 nmol/L;中剂量地塞米松抑制试验,睾酮、DHEAS、孕酮均不被抑制(具体见表1)。盐皮质激素:肾素活性(PRA)1.85 ng·ml-1·h-1,血管紧张素Ⅱ 80.15 ng/L,醛固酮560.37 pmol/L(180.0~820.0 pmol/L);肾上腺髓质激素:24 h尿儿茶酚胺:去甲肾上腺素15.54 μg(正常参考值:16.69~40.65 μg),肾上腺素2.27 μg(正常参考值:1.74~6.42 μg),多巴胺163.02 μg(正常参考值:120.93~330.59 μg);骨龄相:骨龄18~20岁。子宫双附件超声检查:未见子宫内膜回声,肌层回声均;子宫小(2.6 cm×2.9 cm×1.0 cm),幼稚子宫,左卵巢3.1 cm×1.5 cm,右卵巢2.1 cm×1.1 cm。肾上腺增强CT(图2):左侧肾上腺可见一软组织密度影,大小约50 mm×70 mm,增强扫描可见明显强化,边缘光滑。生长抑素受体显像+腹部CT:左肾上腺软组织占位,生长抑素受体表达轻度不均匀增高。全身骨显像:未见明显异常。正电子发射计算机断层显像(PET/CT):左肾上腺区见一巨大软组织团块,大小5.1 cm×5.3 cm×5.3 cm,平均标准摄取值(SUV)3.5,最高SUV 6.0;左肾上腺区代谢异常增高软组织团块,不能完全除外恶性病变。
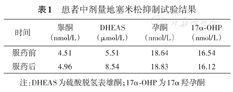
患者中剂量地塞米松抑制试验结果
患者中剂量地塞米松抑制试验结果
| 时间 | 睾酮(nmol/L) | DHEAS(μmol/L) | 孕酮(nmol/L) | 17α-OHP(nmol/L) |
|---|---|---|---|---|
| 服药前 | 4.51 | 5.51 | 18.64 | 16.54 |
| 服药后 | 4.96 | 8.54 | 18.83 | 16.12 |
注:DHEAS为硫酸脱氢表雄酮;17α-OHP为17α羟孕酮
诊疗经过:考虑左侧肾上腺占位,高孕酮血症、高雄激素血症、非ACTH依赖性亚临床库欣综合征诊断明确,患者于2018年8月24日全麻下行左肾上腺肿瘤探查切除术。术中见左肾上腺来源肿瘤,大小约7 cm×6 cm×6 cm,表面光滑,包膜完整,术中完整切除肿瘤。病理回报:肾上腺皮质腺瘤;免疫组化结果:Melan-A(+),AE1/AE3(局灶+),嗜铬粒蛋白A(-),Ki-67(index 3%),S-100(-),抑制素α(α-inhibin)(局灶+),钙网膜蛋白(Calretinin)(-),突触素(Syn)(部分+),波形蛋白(Vimentin)(+)。术后1个月内患者多毛逐渐减轻,唇上小须、面部痤疮逐渐消失。脸圆减轻,体重基本同前,食欲较前稍差,面部、手脚皮肤出现蜕皮。术后1个月复查血皮质醇8∶00 221.63 nmol/L,ACTH8∶00 13.68 pmol/L,24 h UFC 23.57 μg;FSH 7.48 U/L,LH 7.79 U/L,雌二醇69.54 pmol/L,孕酮1.46 nmol/L,睾酮0.90 nmol/L(月经1~3 d);17α-OHP 4.24 nmol/L,DHEAS 0.59 μmol/L。目前仍在规律随访中。术后34 d患者出现月经初潮,此后月经规律。
患者青少年女性,慢性病程,临床主要表现为原发性闭经及肾上腺占位,从一元论角度,考虑原发性闭经的原因与肾上腺占位相关可能性大。女性年龄超过14岁,第二性征未发育,或年龄超过16岁,第二性征已发育,月经还未来潮,称为原发性闭经[1]。根据我国闭经诊断与治疗指南[2],原发性闭经的原因按照部位来分,主要分为下丘脑性闭经、垂体性闭经、卵巢性闭经、子宫性闭经及下生殖道发育异常及其他内分泌疾病。该患者FSH、LH不低,病程中多次雌孕激素替代后无阴道出血,盆腔超声未见子宫发育异常,故考虑上述主要病因可能性小。该患者雄激素、孕激素持续升高,且合并亚临床库欣综合征,行肾上腺占位切除术后有自然月经来潮,因此我们推测,由肾上腺肿瘤导致的高雄激素血症及高孕酮血症是该患者原发性闭经的主要原因。
首诊时原发性闭经的病因,除了下丘脑性闭经、垂体性闭经、卵巢性闭经、子宫性闭经及下生殖道发育异常外,容易遗漏其他内分泌疾病,特别是肾上腺疾病的诊断。
肾上腺腺瘤与肾上腺皮质癌有时难以鉴别,肿瘤分泌的激素类型、肿瘤大小、影像学特征及病理表现均可帮助判断其良恶性,肿瘤是否复发和转移为诊断的金标准。
高孕酮血症、高雄激素血症均为导致闭经的原因之一,且高孕激素血症在雌孕激素人工周期后可无撤退性出血。
中剂量地塞米松抑制试验可帮助鉴别孕酮、睾酮是否受ACTH调控。
对于肾上腺肿物,可根据其分泌的激素类型、肿瘤体积、影像学表现鉴别其良恶性。
该患者病程中多次查孕激素明显升高,持续的高孕激素对子宫内膜可发挥类似"含孕激素避孕药"的作用[3]。患者血清孕酮水平持续高于卵泡期的正常范围,导致FSH和LH虽没有被完全抑制,但它们的水平低于或接近正常范围的下限,这可能是导致其闭经的原因之一。此外,患者多次在雌孕激素人工周期后无撤退性出血,考虑也与持续性高孕激素血症相关。患者同时合并高雄激素血症,伴有DHEAS水平明显升高,所以考虑肾上腺来源雄激素可能性大。高雄激素可作用于卵巢,抑制卵泡成熟,引起发育中卵泡闭锁,不能形成优势卵泡,导致持续无排卵。因此,推测肾上腺来源的高雄激素血症也是导致患者原发性闭经的原因之一。此外,入院后查血、尿皮质醇水平升高,皮质醇节律消失,小剂量地塞米松抑制试验不被抑制,考虑库欣综合征诊断明确。患者ACTH水平明显减低,考虑为非ACTH依赖性的库欣综合征,皮质醇为肾上腺来源,左肾上腺占位来源可能性大。患者库欣综合征相关临床表现不突出,考虑为亚临床库欣综合征。高皮质醇血症也可抑制下丘脑-垂体性腺轴功能,引起月经稀发或闭经。
患者肾上腺皮质肿瘤切除后出现月经来潮,脸圆、多毛、痤疮等临床表现消失,复查血孕激素、睾酮、皮质醇、DHEAS均较前下降,支持上述激素为肾上腺皮质肿瘤来源。
肾上腺皮质肿瘤的病理分型包括肾上腺皮质腺瘤与肾上腺皮质癌,其良恶性判断,临床以是否复发和转移作为金标准,其分泌的激素类型、影像学特点、病理特征可帮助鉴别。肾上腺皮质腺瘤多分泌单一类型类固醇激素,而肾上腺皮质癌可分泌多种类固醇激素(皮质醇、醛固酮、雄激素)及其前体,DHEAS水平增加多提示肾上腺皮质癌[4]。影像学可帮助进一步鉴别,体积巨大被看作是肾上腺皮质癌重要特征之一[5]。病理学检查是确诊肾上腺皮质癌的关键,其结合镜检及免疫组化综合判断,Weiss评分镜下诊断是目前肾上腺皮质癌最优的评估系统[6]。
治疗方面,对于肾上腺功能性皮质腺瘤,首选手术治疗,但需注意术后可出现肾上腺皮质功能不全。因此,术后需密切观察患者精神、食欲、体力情况,给予短期糖皮质激素替代治疗,并根据体力、食欲等逐渐减停。
所有作者均声明不存在利益冲突



























