
探讨类风湿关节炎(RA)滑膜过氧化物酶体增殖物激活受体γ辅激活因子(PGC)1β表达与病理滑膜炎的相关性及其临床意义。
横断面研究纳入2010年5月至2016年10月在中山大学孙逸仙纪念医院住院的确诊RA患者并收集临床资料,采用改良Sharp评分(mTSS)评估双手正位X线片关节破坏程度。膝关节滑膜活检获取滑膜组织并连续切片,苏木精伊红染色评估滑膜病理改变,免疫组化染色检测PGC-1β表达及炎症细胞和血管内皮细胞数量。相关及多重线性回归分析RA滑膜PGC-1β表达与病理滑膜炎、临床病情活动及影像学关节破坏程度的关系。
共纳入83例RA患者,男20例(24.1%),女63例(75.9%),年龄(54±14)岁。PGC-1β在RA滑膜衬里层及衬里下层多种细胞胞核中表达,滑膜PGC-1β+细胞比例与病理滑膜炎评分及衬里下层CD3+T细胞、CD20+B细胞、CD38+浆细胞、CD68+巨噬细胞数量呈正相关(r=0.333、0.259、0.320、0.342、0.309,均P<0.05)。滑膜PGC-1β表达与红细胞沉降率、C反应蛋白及mTSS显著正相关(r=0.219~0.301,均P<0.05)。多重线性回归分析示滑膜PGC-1β表达与mTSS显著正相关(β=0.312,P=0.004)。
RA滑膜PGC-1β表达与滑膜局部及全身炎症水平、关节破坏程度呈正相关,提示可能参与RA滑膜炎症及关节破坏过程。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
类风湿关节炎(RA)是一种常见的以进行性关节破坏为特征的慢性自身免疫性疾病,慢性增生性滑膜炎是RA的基本病理改变,是导致患者出现关节软骨及骨破坏的重要原因[1]。过氧化物酶体增殖物激活受体γ辅激活因子(PGC)1β是重要的转录调控因子,在心脏、棕色脂肪组织、脑、骨骼肌等富含线粒体的组织中高表达,广泛参与机体多种生物学过程,包括调控线粒体生物合成、脂肪酸代谢、糖异生、三羧酸循环、血管生成、炎症及细胞分化等[2, 3]。笔者前期研究发现,PGC-1β在RA滑膜组织中表达显著高于骨关节炎和关节外伤的患者[4]。体外培养的RA滑膜成纤维样滑膜细胞中PGC-1β表达上调,并促进其分泌炎症因子肿瘤坏死因子(TNF)-α、白细胞介素(IL)-6和IL-8,发挥促炎效应。然而,PGC-1β在RA滑膜高表达的临床意义少见报道。为此,本文拟进一步探讨RA滑膜PGC-1β表达与病理滑膜炎、临床病情活动及关节破坏的关系。
本研究为横断面研究,纳入2010年5月至2016年10月在中山大学孙逸仙纪念医院风湿免疫科住院的确诊RA患者。入选标准:诊断符合1987年美国风湿病学会(ACR)关于RA的分类标准[5]或2010年ACR与欧洲抗风湿病联盟(EULAR)联合修订的RA分类标准[6],伴有膝关节肿痛并行Parker-Pearson细针滑膜活检术者[7]。排除标准:合并肝脏疾病[丙氨酸转氨酶(ALT)>100 U/L或天冬氨酸转氨酶(AST)>88 U/L]、肾脏疾病(血肌酐>133 μmol/L)、血液系统疾病(白细胞计数<4×109/L或血小板计数<100×109/L)、严重呼吸系统疾病、恶性肿瘤、精神疾病及妊娠。所有患者均签署知情同意书,并经本院伦理委员会批准(伦理号:SYSEC-2009-06,SYSEC-2014-LSY-89)。
临床指标包括患者年龄、性别、病程、既往用药情况、28个关节压痛数和肿胀数、患者和医生总体病情活动度评估(0~10分)、疼痛视觉模拟评分(VAS,0~10分)、红细胞沉降率(ESR,女:0~20 mm/1h,男:0~15 mm/1h)、C反应蛋白(CRP,0~5 mg/L)、类风湿因子(RF,0~20 U/ml)、抗环瓜氨酸肽抗体(抗CCP抗体,0~18 U/ml),并计算病情活动性评分,包括28个关节疾病活动度评分(DAS28-CRP)、简化的疾病活动指数(SDAI)和临床疾病活动指数(CDAI)。
所有患者行双手正位X线检查(包括腕关节),由经过阅片培训的两名研究者在不了解患者信息的情况下采用改良Sharp评分评估双手关节破坏程度[8]。具体评分指标包括改良Sharp评分总分(mTSS)、关节间隙狭窄评分和关节侵蚀评分。两名研究者评分一致性评价的组内相关系数(ICC)平均值为0.93。
膝关节滑膜组织经固定、脱水和包埋后连续切片,分别行HE染色及免疫组化染色。在HE染色下采用Krenn评分评估病理滑膜炎程度[9],包括衬里层增生、衬里下层炎症细胞浸润和基质活化3个亚分,每个亚分根据相应病理改变的轻重程度进行半定量评分(0~3分),相加为Krenn总分(0~9分)。根据Krenn总分,0~4分为轻度滑膜炎,5~9分为重度滑膜炎。
免疫组化染色一抗包括PGC-1β(北京Bioss公司)和CD3(标记T细胞)、CD20(标记B细胞)、CD38(标记浆细胞)、CD68(标记巨噬细胞)、CD15(标记中性粒细胞)、CD34(标记血管内皮细胞),均购自美国Invitrogen公司。二抗试剂盒购自上海基因科技有限公司。计算PGC-1β阳性细胞占RA滑膜总细胞数的比例。定量计算滑膜衬里下层CD3+T细胞、CD20+B细胞、CD38+浆细胞、CD68+巨噬细胞、CD15+中性粒细胞的数量[10]。Krenn评分及免疫组化阳性细胞计数由两名研究者双盲进行,平均ICC为0.91。
数据采用SPSS 25.0软件进行统计分析。定量资料以或M(Q1, Q3)表示,定性资料数据以例(%)表示。采用Kruskal-Wallis非参数检验比较两组样本间的差异,两组二分类资料的比较采用χ²检验,两变量间相关性分析采用Spearman秩相关检验。采用多重线性回归模型分析滑膜PGC-1β表达、衬里下层CD68+巨噬细胞数与mTSS的相关性,以mTSS为因变量,纳入滑膜PGC-1β+细胞比例和衬里下层CD68+巨噬细胞数为自变量进行逐步回归分析。检验水准值取双侧α=0.05。
共纳入83例RA患者,年龄为(54±14)岁,男20例(24.1%),女63例(75.9%)。中位病程为24(10,120)个月,中位DAS28-CRP为5.8(4.8, 7.0)。RF阳性率为86.8%,抗CCP抗体阳性率为81.9%,影像学评估mTSS为15(6, 37),25.3%的患者就诊前未接受糖皮质激素或改善病情抗风湿药(DMARDs)治疗。
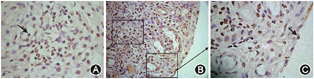
PGC-1β在RA滑膜衬里层细胞(巨噬细胞样滑膜细胞和成纤维样滑膜细胞)、衬里下层炎症细胞(主要为淋巴细胞、浆细胞、巨噬细胞)及血管内皮细胞胞核中均有表达。RA滑膜PGC-1β+细胞比例为82.0%(71.2%,88.2%),其中衬里层PGC-1β+细胞比例为78.5%(70.7%,87.0%),衬里下层PGC-1β+细胞比例为85.4%(74.8,89.3%)(图1)。

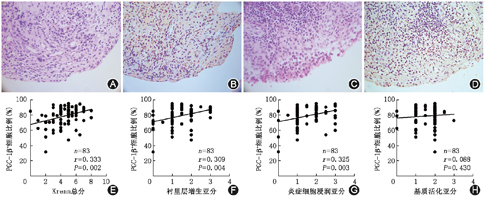
83例RA滑膜中,重度滑膜炎占51.8%(43/83),其滑膜PGC-1β+细胞比例高于轻度滑膜炎组[85.0%(78.0%,88.4%)比79.2%(68.8%,85.2%),Z=-2.538,P=0.011]。采用Spearman秩相关检验分析发现RA滑膜PGC-1β+细胞比例与滑膜病理Krenn总分、衬里层增生亚分、衬里下层炎症细胞浸润亚分呈显著正相关(r=0.333、0.309、0.325,均P<0.05)(图2)。

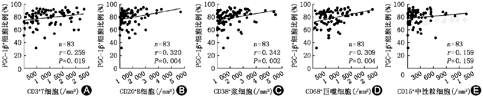
进一步采用Spearman秩相关检验分析RA滑膜PGC-1β表达与浸润的不同炎症细胞的相关性,结果显示滑膜PGC-1β+细胞比例与衬里下层CD3+T细胞、CD20+B细胞、CD38+浆细胞、CD68+巨噬细胞数量呈显著正相关(r=0.259、0.320、0.342、0.309, 均P<0.05),而与CD15+中性粒细胞数无相关性(r=0.159,P=0.159)(图3)。

Spearman相关分析RA滑膜PGC-1β表达与临床指标的相关性,结果显示RA滑膜PGC-1β+细胞比例与ESR、CRP呈显著正相关(r=0.278、0.219,均P<0.05),且与mTSS、关节间隙狭窄评分、关节侵蚀评分呈显著正相关(r=0.301、0.271、0.321,均P<0.05)。滑膜衬里下层CD68+巨噬细胞数与CRP、DAS28-CRP、mTSS、关节间隙狭窄评分、关节侵蚀评分呈正相关(r=0.237~0.375,均P<0.05),CD38+浆细胞数及CD15+中性粒细胞数与CRP均呈正相关(r=0.286、0.357,均P<0.05,表1)。进一步采用多重线性回归分析RA滑膜PGC-1β表达、衬里下层CD68+巨噬细胞数与mTSS的相关性,建立回归模型(F=8.713,P=0.004,R2=0.097),结果示自变量滑膜PGC-1β+细胞比例与因变量mTSS正相关(β=0.312,P=0.004),而自变量衬里下层CD68+巨噬细胞数未进入方程(P=0.139,表2)。
RA患者膝关节滑膜PGC-1β表达、衬里下层炎症细胞数与临床指标的相关性
RA患者膝关节滑膜PGC-1β表达、衬里下层炎症细胞数与临床指标的相关性
| 临床指标 | PGC-1β+细胞比例 | CD3+T细胞 | CD20+B细胞 | CD38+浆细胞 | CD68+巨噬细胞 | CD15+中性粒细胞 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| r值 | P值 | r值 | P值 | r值 | P值 | r值 | P值 | r值 | P值 | r值 | P值 | |
| 病情活动指标 | ||||||||||||
ESR(mm/h) | 0.278 | 0.011 | 0.095 | 0.397 | -0.005 | 0.963 | 0.158 | 0.153 | 0.173 | 0.117 | 0.199 | 0.077 |
CRP(mg/dl) | 0.219 | 0.047 | 0.054 | 0.631 | 0.110 | 0.327 | 0.286 | 0.009 | 0.375 | <0.001 | 0.357 | 0.001 |
DAS28‑CRP | -0.080 | 0.474 | -0.118 | 0.292 | -0.162 | 0.149 | -0.141 | 0.203 | 0.237 | 0.031 | 0.140 | 0.216 |
| 影像学关节破坏指标 | ||||||||||||
mTSS | 0.301 | 0.006 | 0.123 | 0.272 | 0.102 | 0.366 | 0.172 | 0.120 | 0.259 | 0.018 | -0.074 | 0.515 |
关节间隙狭窄评分 | 0.271 | 0.013 | 0.085 | 0.446 | 0.026 | 0.816 | 0.153 | 0.168 | 0.249 | 0.023 | -0.042 | 0.711 |
关节侵蚀评分 | 0.321 | 0.003 | 0.174 | 0.119 | 0.180 | 0.109 | 0.202 | 0.067 | 0.246 | 0.025 | -0.081 | 0.474 |
注:RA为类风湿关节炎;PGC-1β为过氧化物酶体增殖物激活受体γ辅激活因子1β;ESR为红细胞沉降率;CRP为C反应蛋白;DAS28-CRP为28个关节疾病活动度评分;mTSS为改良Sharp评分总分
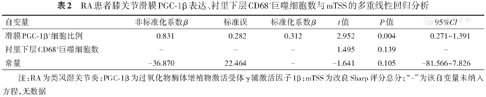
RA患者膝关节滑膜PGC-1β表达、衬里下层CD68+巨噬细胞数与mTSS的多重线性回归分析
RA患者膝关节滑膜PGC-1β表达、衬里下层CD68+巨噬细胞数与mTSS的多重线性回归分析
| 自变量 | 非标准化系数β | 标准误 | 标准化系数β | t值 | P值 | 95%CI |
|---|---|---|---|---|---|---|
| 滑膜PGC‑1β+细胞比例 | 0.831 | 0.282 | 0.312 | 2.952 | 0.004 | 0.271~1.391 |
| 衬里下层CD68+巨噬细胞数 | - | - | - | 1.495 | 0.139 | - |
| 常量 | -36.870 | 22.464 | - | -1.641 | 0.105 | -81.566~7.826 |
注:RA为类风湿关节炎;PGC-1β为过氧化物酶体增殖物激活受体γ辅激活因子1β;mTSS为改良Sharp评分总分;“-”为该自变量未纳入方程,无数据
滑膜炎是RA关节的主要病理改变,表现为滑膜衬里层滑膜细胞数量异常增多及衬里下层大量T淋巴细胞、B淋巴细胞、浆细胞、巨噬细胞等炎症细胞浸润[11]。早期病理研究已证实,RA患者腕关节、掌指关节与膝关节滑膜中细胞的种类及计数均无明显差异,提示可通过对RA患者某一关节的病理活检可反映其全身的滑膜炎情况[12]。其中,滑膜衬里下层浸润的巨噬细胞在RA炎症反应及关节软骨和骨破坏的病理过程中起核心作用[13]。RA滑膜巨噬细胞不仅分泌大量的TNF-α、IL-1β、IL-6等促炎因子,还可分泌CCL2、CCL3、CCL5等趋化因子,募集单核细胞和中性粒细胞进入关节滑膜,导致炎症反应[14]。除了促炎作用,更重要的是,单核-巨噬细胞在巨噬细胞集落刺激因子和NF-κB受体活化因子配体激活受体配体(RANKL)的调控作用下可融合为高度分化的具有骨吸收能力的破骨细胞,并在TNF-α、IL-1β、IL-6、IL-17等促炎细胞因子的作用下骨吸收能力明显增强,直接造成关节骨破坏[15, 16]。笔者前期研究发现,RA患者滑膜衬里下层CD68+巨噬细胞数与RA病情活动指标及影像学关节破坏评分呈正相关[17],并且通过佐剂性关节炎大鼠模型证实膝关节滑膜衬里下层巨噬细胞增多并与关节破坏程度正相关[18]。Bresnihan等[19]的一项队列研究证实RA滑膜衬里下层CD68+巨噬细胞数量的增加与RA病情活动加重呈正相关。然而,目前RA滑膜及关节局部巨噬细胞向破骨细胞分化的调控机制尚未明确。
PGC1是一类重要的转录调控因子,PGC1家族包括3个成员:PGC-1α、PGC-1β和PGC1相关辅助活化因子。PGC-1β与首先发现的PGC-1α具有广泛的同源性,但PGC-1β缺乏SR功能区,所以不受寒冷、饥饿、耐力运动等急性刺激的翻译后调控,在调节炎症反应及骨破坏方面发挥重要作用[3]。笔者的前期研究发现,RA滑膜成纤维样滑膜细胞中PGC-1β表达上调,并通过激活NF-Κb p65上调TNF-α、IL-6、IL-8等促炎因子的表达[4]。本研究发现RA滑膜PGC-1β表达与衬里下层T细胞、B细胞、浆细胞和巨噬细胞浸润呈正相关,且与患者炎症指标ESR、CRP水平呈显著正相关,提示RA滑膜高表达的PGC-1β可能参与滑膜炎症过程。
既往研究发现,PGC-1β及雌激素受体相关受体α(ERR-α)协同激活过氧化物酶增殖活化受体(PPAR)γ通路促进破骨细胞的分化活化,敲除髓系细胞PGC-1β基因的小鼠出现破骨细胞形成障碍而导致骨量增加[20]。体外实验发现,小鼠骨髓细胞转铁蛋白缺失导致细胞内铁的富集可刺激巨噬细胞增殖并上调其PGC-1β表达,从而促进破骨细胞的形成[21]。新近研究又发现,敲除髓系细胞PGC-1β基因的小鼠尽管破骨细胞形成不受影响,其骨吸收能力及线粒体生物合成功能也明显抑制[22]。笔者前期研究发现RA患者外周血单核细胞(巨噬细胞及破骨细胞前体细胞)中PGC-1β表达升高,通过激活活化的T细胞核因子-1上调靶基因组织蛋白酶K、抗酒石酸酸性磷酸酶、基质金属蛋白酶9的表达,促进破骨细胞分化及骨吸收功能[23]。本研究发现RA滑膜PGC-1β+细胞比例和滑膜衬里下层CD68+巨噬细胞数均与mTSS显著正相关,而进一步多重线性回归分析发现,滑膜PGC-1β+细胞比例与mTSS显著正相关,而衬里下层CD68+巨噬细胞数未能纳入回归方程,提示具有调控破骨细胞分化活化功能的PGC-1β滑膜表达水平可能较衬里下层巨噬细胞数量与RA关节破坏的关系更密切,RA滑膜PGC-1β可能在关节破坏中发挥重要的调控作用。
总之,RA滑膜PGC-1β表达与RA患者滑膜局部及全身炎症水平、影像学关节破坏程度呈正相关,提示其可能通过促进滑膜衬里下层炎症细胞浸润、促进巨噬细胞向破骨细胞分化活化从而参与RA滑膜炎及关节破坏过程。
所有作者均声明不存在利益冲突



























