
采用主客观评价系统分别评价深度学习方法在动静脉期CT上的分割效果,并探索影响动静脉期胰腺分割差异的因素及影响静脉期胰腺分割的相关因素。
回顾性收集2019年1至11月北京协和医院放射科218例胰腺CT扫描数据,每例均包含动脉期和静脉期图像,并按照训练集+验证集与测试集为7∶3的比例将数据随机划分为训练集(139例)、验证集(20例)及测试集(59例),使用训练集训练二阶段全局局部渐进融合网络,在验证集上寻找最优分割效果的模型参数,对测试集进行预测并对结果进行主观及客观评价。主观评价基于胰腺与周围器官的临界区域,采用李克特5分量表;客观评价采用Dice相似系数(DSC)。采用配对t检验或Wilcoxon配对秩检验比较动静脉期主客观评分的差异。
在十二指肠、十二指肠空肠曲、左肾上腺、门脉、肠系膜上静脉、脾动脉及脾静脉处胰腺临界区域动脉期主观评分[M(Q1, Q3)]分别为4(4, 5)、5(4, 5)、5(4, 5)、4(4, 5)、5(4, 5)、5(5, 5)及4(3, 5)分,静脉期主观评分[M(Q1, Q3)]分别为4(4, 4)、5(4, 5)、5(4, 5)、5(4, 5)、5(5, 5)、4(3, 4)、5(5, 5)分,以上临界区域的胰腺动、静脉期主观评分差异均有统计学意义(均P<0.05);静脉期DSC略高于动脉期,差异无统计学意义(DSC:0.923比0.921,P=0.952)。胰腺与十二指肠空肠曲、胃、左肾上腺存在脂肪间隙组在静脉期主观评分分别为4.64、4.68及4.63分,无脂肪间隙组的主观评分分别为4.56、4.62及4.56分,胰腺与十二指肠空肠曲、胃、左肾上腺有、无脂肪间隙两组间的主观评分差异均有统计学意义(t=2.147、2.112、2.277,均P<0.05)。除外脾,胰腺临界区域与其余周围器官的密度差在动静脉分割的差异均有统计学意义(均P<0.05)。
利用双期CT构建深度学习胰腺自动分割模型,并对分割效果进行主客观评价,主观评价可以提高今后胰腺临界区域的分割能力。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
胰腺解剖结构复杂、形态多变且相对于腹部容积体积较小,故胰腺的精准分割一直是一项极具挑战性的任务。目前已有多项国内外研究应用不同的深度学习方法进行胰腺自动分割,且已达到不错的分割效果[1, 2, 3, 4]。值得注意的是,以上研究均是基于公开数据集胰腺静脉期CT图像分割,动静脉期胰腺分割效果对比尚未见报道,理论上动脉期与静脉期联合,可以更好地显示胰腺及其周围细微结构(动静脉系统、十二指肠等),有助于更准确的胰腺分割。Dice相似系数(DSC)是最常用的评价分割效果的客观指标,但其评价的是基于整个胰腺的分割效果,对于胰腺与周围器官局部分割效果的评价作用有限,故本研究拟采用主观和客观评价系统分别评价新的深度学习方法在动静脉期的分割效果。主观评分可以详细显示局部胰腺分割效果,弥补DSC在细节上的缺失,有助于模型的进一步优化,为下一步胰腺疾病的诊断及临床治疗提供可靠的影像学依据。此外,本研究亦探索影响动静脉期胰腺分割差异的因素及影响静脉期胰腺分割的相关因素,为临床上进一步提高胰腺分割效果提供参考。
本文为应用型研究,回顾性搜索2019年1至11月北京协和医院放射科影像数据库,按照纳入、排除标准收集218例胰腺扫描原始图像,整理记录患者的临床及影像学资料,包括性别、年龄、轮廓改变(正常胰腺、胰腺内病变不改变胰腺轮廓、胰腺病变改变胰腺轮廓)及胰腺内病变密度,按照训练集+验证集与测试集为7∶3的比例将以上数据随机分为训练集(139例)、验证集(20例)及测试集(59例),记录59例测试集的胰腺与周围器官是否存在脂肪间隙。纳入标准:(1)CT图像清晰完整,包括动、静脉两期数据;(2)图像质量满足胰腺轮廓勾画要求,包括无明显伪影,图像层厚1 mm,胰腺轮廓清晰(包含或不包含病变)。排除标准:胰腺术后患者。将上述原始数据匿名后上传至深睿医疗标注平台(https://label.deepwise.com/Login/),一名医师手动勾画动静脉期胰腺轮廓,另外一名高年资医师审核。本研究已通过北京协和医院伦理委员会审核(HS-2753),所有患者知情同意豁免。
使用128排CT设备(Siemens SOMATOM Definition Flash, 德国西门子公司)进行胰腺增强扫描。扫描参数:管电压120 kVp,使用管电流自动调节技术,旋转时间0.5 s,矩阵512×512,层厚1 mm,层间距1 mm。对比剂采用典比乐(370 mgI/ml, 上海博莱科信谊药业有限责任公司),注射速度4.0 ml/s,剂量1.2 ml/kg。扫描时间:采用主动脉触发扫描,触发阈值100 HU,约15 s后进行动脉期扫描,动脉期扫描完成后约30 s进行静脉期扫描。
使用二阶段全局局部渐进融合网络,该深度网络是通过两个阶段的特征学习结合胰腺的全局信息和局部信息,进而实现高度准确的分割结果。在第一阶段,通过设计全局信息引导的胰腺分割模块来指导网络学习胰腺在腹部中的相对位置,从而有效抑制其他腹部结构的干扰,可以有效降低假阳性率;在第二阶段,通过设计局部信息细化胰腺分割模块来进一步优化胰腺局部轮廓的细节。
主观和客观评价系统均以测试集数据为基础。
1. 主观评价系统:(1)主观评分为评价模型识别的胰腺轮廓与医师手工勾画的胰腺轮廓的吻合程度,采用李克特5分量表,包括局部评分和整体评分两部分,局部评分指的是与周围器官(包括十二指肠、胃、十二指肠空肠曲、脾、左肾上腺、门脉、肠系膜上静脉、肠系膜上动脉、脾动脉、脾静脉)临界的胰腺组织的评分;整体评分是以上局部评分之和的平均值;(2)主观评分标准:1分:胰腺轮廓未识别,吻合差;2分:胰腺轮廓识别差,只有部分吻合;3分:胰腺轮廓可以识别,部分吻合好;4分:胰腺轮廓可以识别,大部分吻合好;5分:胰腺轮廓清楚,基本吻合。
2. 客观评价系统:客观评价方法采用DSC。两名医师先分别评价动脉期,2周后评价静脉期的分割效果,当两者得分不一致时,引入高年资医师评分(图1)。
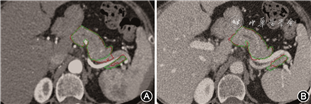

两名影像科医师在商业视图软件(Centricity Radiology RA 1000,美国GE公司)分别测量胰腺临界区域与周围器官的密度,1个月后其中一名医师重复测量以上数值,以3次测量数据的平均值作为胰腺与周围器官的最终测得值,两者的差值作为胰腺临界区域与周围器官的密度差。
采用SPSS 25.0统计软件包进行数据分析和处理。训练集+验证集及测试集的性别比例、胰腺轮廓及胰腺内病变密度均为计数资料,采用χ2检验;训练集+验证集患者年龄符合偏态分布,测试集患者年龄符合正态分布,两者间比较采用秩和检验。胰腺各临界区域动、静脉期分割的主客观评分均符合偏态分布,以M(Q1,Q3)表示,采用Wilcoxon配对秩检验。不同胰腺轮廓(正常、轮廓不变及轮廓改变)及胰腺与各临界器官之间有和无脂肪间隙的动、静脉期主、客观评分,胰腺临界区域与邻近脏器的动、静脉期密度差,符合及近似正态分布的数据以表示,偏态分布的数据以M(Q1,Q3)表示,动静脉期两组主、客观评分进行比较时,两组的差值符合正态分布的采用配对t检验,不符合的采用秩和检验。对基于静脉期的三组胰腺轮廓间的主客观评分采用Kruskal-Wallis H检验,基于静脉期的胰腺与邻近脏器有及无脂肪间隙两组间的对比采用独立样本t检验。采用Pearson相关性分析胰腺与周围脏器之间的密度差与静脉期主观评分的相关性,采用组间相关系数检验(ICC)比较两名医师密度测量的一致性,一位重复测量的医师所测得的两次数据用于评价观察者自身可信度(ICC1),两位医师的测量值用于评价观察者间可信度(ICC2)。双侧检验,检验水准α=0.05。
训练集及验证集与测试集在性别、年龄、胰腺轮廓及胰腺病变密度之间的差异均无统计学意义(均P>0.05)(表1)。
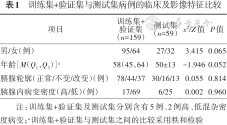
训练集+验证集与测试集病例的临床及影像特征比较
训练集+验证集与测试集病例的临床及影像特征比较
| 项目 | 训练集+ 验证集 (n=159) | 测试集 (n=59) | x2/Z值 | P值 |
|---|---|---|---|---|
| 男/女(例) | 95/64 | 27/32 | 3.415 | 0.065 |
| 年龄[M(Q1,Q3)]a | 58(45,64) | 50±13 | -1.946 | 0.052 |
| 胰腺轮廓(正常/不变/改变)(例) | 78/44/37 | 30/16/13 | 0.055 | 0.814 |
| 胰腺内病变密度(高/低)(例) | 17/69 | 6/25 | 0.002 | 0.960 |
注:训练集+验证集及测试集分别含有5例、2例高、低混杂密度病变;a训练集+验证集与测试集之间的比较采用秩和检验
在十二指肠、十二指肠空肠曲、左肾上腺、门脉、肠系膜上静脉、脾动脉及脾静脉处胰腺临界区域动静脉期分割差异有统计学意义(均P<0.05)。在胃、脾、肠系膜上动脉处胰腺临界区域及整体主观评价上,动静脉分割差异无统计学意义(Z=-1.043、-0.577、-0.632、-1.342,均P>0.05)。静脉期DSC略高于动脉期(0.923比0.921),差异无统计学意义(Z=-0.060,P=0.952)(表2)。
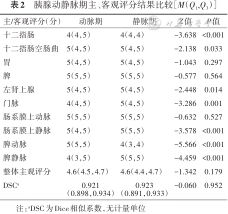
胰腺动静脉期主、客观评分结果比较[M(Q1,Q3)]
胰腺动静脉期主、客观评分结果比较[M(Q1,Q3)]
| 主/客观评分(分) | 动脉期 | 静脉期 | Z值 | P值 |
|---|---|---|---|---|
| 十二指肠 | 4(4,5) | 4(4,4) | -3.638 | <0.001 |
| 十二指肠空肠曲 | 5(4,5) | 5(4,5) | -2.138 | 0.033 |
| 胃 | 5(4,5) | 5(4,5) | -1.043 | 0.297 |
| 脾 | 5(5,5) | 5(5,5) | -0.577 | 0.564 |
| 左肾上腺 | 5(4,5) | 5(4,5) | -2.448 | 0.014 |
| 门脉 | 4(4,5) | 5(4,5) | -3.286 | 0.001 |
| 肠系膜上动脉 | 5(5,5) | 5(5,5) | -0.632 | 0.527 |
| 肠系膜上静脉 | 5(4,5) | 5(5,5) | -3.578 | <0.001 |
| 脾动脉 | 5(5,5) | 4(3,4) | -5.566 | <0.001 |
| 脾静脉 | 4(3,5) | 5(5,5) | -4.459 | <0.001 |
| 整体主观评分 | 4.6(4.5,4.7) | 4.6(4.4,4.7) | -1.342 | 0.179 |
| DSCa | 0.921 (0.898,0.934) | 0.923 (0.891,0.933) | -0.060 | 0.952 |
注:aDSC为Dice相似系数,无计量单位
不同胰腺轮廓动静脉期分割差异均无统计学意义(均P>0.05);基于静脉期,胰腺轮廓差异无统计学意义。胰腺与胃之间存在脂肪间隙时,胰腺-胃临界区域在动、静脉期的DSC评分分别为0.92±0.03、0.93±0.02,差异有统计学意义(t=-2.040,P=0.041),胰腺与其余周围器官之间的脂肪间隙所致动、静脉期分割差异均无统计学意义(均P>0.05);胰腺与十二指肠空肠曲、胃、左肾上腺的脂肪间隙有无在静脉期主观评分差异均有统计学意义(t=2.147、2.112、2.277,均P<0.05)(表3)。两名影像医师两次测量结果的ICC值均介于0.81~1.00,具有高度一致性(表4)。除外胰腺与脾的密度差,胰腺临界区域与其余周围器官的密度差所致动静脉分割差异均有统计学意义(均P<0.05);胰腺临界区域与左肾上腺的密度差与胰腺静脉期分割效果具有相关性(r=0.305, P=0.019)(表5)。
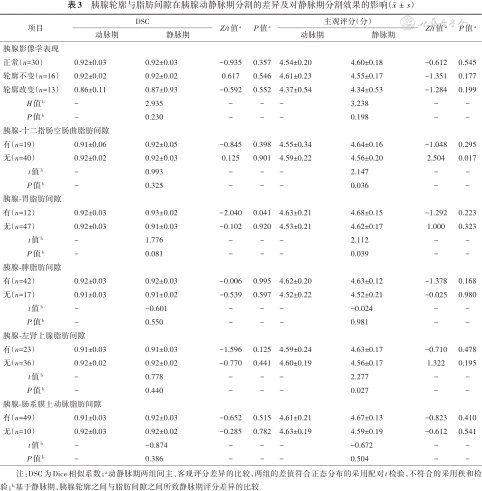
胰腺轮廓与脂肪间隙在胰腺动静脉期分割的差异及对静脉期分割效果的影响()
胰腺轮廓与脂肪间隙在胰腺动静脉期分割的差异及对静脉期分割效果的影响()
| 项目 | DSC | Z/t值a | P值a | 主观评分(分) | Z/t值a | P值a | ||
|---|---|---|---|---|---|---|---|---|
| 动脉期 | 静脉期 | 动脉期 | 静脉期 | |||||
| 胰腺影像学表现 | ||||||||
| 正常(n=30) | 0.92±0.03 | 0.92±0.03 | -0.935 | 0.357 | 4.54±0.20 | 4.60±0.18 | -0.612 | 0.545 |
| 轮廓不变(n=16) | 0.92±0.02 | 0.92±0.02 | 0.617 | 0.546 | 4.61±0.23 | 4.55±0.17 | -1.351 | 0.177 |
| 轮廓改变(n=13) | 0.86±0.11 | 0.87±0.93 | -0.592 | 0.552 | 4.37±0.54 | 4.34±0.53 | -1.284 | 0.199 |
| H值b | - | 2.935 | - | - | - | 3.238 | - | - |
| P值b | - | 0.230 | - | - | - | 0.198 | - | - |
| 胰腺-十二指肠空肠曲脂肪间隙 | ||||||||
| 有(n=19) | 0.91±0.06 | 0.92±0.05 | -0.845 | 0.398 | 4.55±0.34 | 4.64±0.16 | -1.048 | 0.295 |
| 无(n=40) | 0.92±0.02 | 0.92±0.03 | 0.125 | 0.901 | 4.59±0.22 | 4.56±0.20 | 2.504 | 0.017 |
| t值b | - | 0.993 | - | - | - | 2.147 | - | - |
| P值b | - | 0.325 | - | - | - | 0.036 | - | - |
| 胰腺-胃脂肪间隙 | ||||||||
| 有(n=12) | 0.92±0.03 | 0.93±0.02 | -2.040 | 0.041 | 4.63±0.21 | 4.68±0.15 | -1.292 | 0.223 |
| 无(n=47) | 0.92±0.03 | 0.91±0.03 | -0.102 | 0.920 | 4.53±0.21 | 4.62±0.17 | 1.000 | 0.323 |
| t值b | - | 1.776 | - | - | - | 2.112 | - | - |
| P值b | - | 0.081 | - | - | - | 0.039 | - | - |
| 胰腺-脾脂肪间隙 | ||||||||
| 有(n=42) | 0.92±0.03 | 0.92±0.03 | -0.006 | 0.995 | 4.62±0.20 | 4.63±0.12 | -1.378 | 0.168 |
| 无(n=17) | 0.91±0.03 | 0.91±0.02 | -0.539 | 0.597 | 4.52±0.22 | 4.52±0.21 | -0.025 | 0.980 |
| t值b | - | -0.601 | - | - | - | -0.024 | - | - |
| P值b | - | 0.550 | - | - | - | 0.981 | - | - |
| 胰腺-左肾上腺脂肪间隙 | ||||||||
| 有(n=23) | 0.91±0.03 | 0.91±0.03 | -1.596 | 0.125 | 4.59±0.24 | 4.63±0.17 | -0.710 | 0.478 |
| 无(n=36) | 0.92±0.02 | 0.92±0.02 | -0.770 | 0.441 | 4.60±0.19 | 4.56±0.17 | 1.322 | 0.195 |
| t值b | - | 0.778 | - | - | - | 2.277 | - | - |
| P值b | - | 0.440 | - | - | - | 0.027 | - | - |
| 胰腺-肠系膜上动脉脂肪间隙 | ||||||||
| 有(n=49) | 0.91±0.03 | 0.92±0.03 | -0.652 | 0.515 | 4.61±0.21 | 4.67±0.13 | -0.823 | 0.410 |
| 无(n=10) | 0.92±0.03 | 0.92±0.02 | -0.285 | 0.782 | 4.63±0.19 | 4.59±0.19 | -0.612 | 0.541 |
| t值b | - | -0.874 | - | - | - | -0.672 | - | - |
| P值b | - | 0.386 | - | - | - | 0.504 | - | - |
注:DSC为Dice相似系数;a动静脉期两组间主、客观评分差异的比较,两组的差值符合正态分布的采用配对t检验,不符合的采用秩和检验;b基于静脉期,胰腺轮廓之间与脂肪间隙之间所致静脉期评分差异的比较
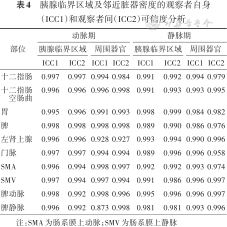
胰腺临界区域及邻近脏器密度的观察者自身(ICC1)和观察者间(ICC2)可信度分析
胰腺临界区域及邻近脏器密度的观察者自身(ICC1)和观察者间(ICC2)可信度分析
| 部位 | 动脉期 | 静脉期 | ||||||
|---|---|---|---|---|---|---|---|---|
| 胰腺临界区域 | 周围器官 | 胰腺临界区域 | 周围器官 | |||||
| ICC1 | ICC2 | ICC1 | ICC2 | ICC1 | ICC2 | ICC1 | ICC2 | |
| 十二指肠 | 0.997 | 0.997 | 0.994 | 0.984 | 0.991 | 0.992 | 0.994 | 0.979 |
| 十二指肠空肠曲 | 0.996 | 0.996 | 0.996 | 0.998 | 0.991 | 0.993 | 0.993 | 0.995 |
| 胃 | 0.995 | 0.996 | 0.991 | 0.993 | 0.998 | 0.999 | 0.984 | 0.982 |
| 脾 | 0.998 | 0.998 | 0.998 | 0.998 | 0.989 | 0.990 | 0.986 | 0.976 |
| 左肾上腺 | 0.996 | 0.996 | 0.928 | 0.927 | 0.993 | 0.994 | 0.990 | 0.996 |
| 门脉 | 0.997 | 0.997 | 0.994 | 0.994 | 0.989 | 0.996 | 0.996 | 0.958 |
| SMA | 0.996 | 0.994 | 0.998 | 0.997 | 0.992 | 0.992 | 0.993 | 0.974 |
| SMV | 0.997 | 0.994 | 0.997 | 0.994 | 0.991 | 0.986 | 0.996 | 0.997 |
| 脾动脉 | 0.998 | 0.992 | 0.998 | 0.996 | 0.995 | 0.996 | 0.996 | 0.997 |
| 脾静脉 | 0.996 | 0.992 | 0.873 | 0.998 | 0.981 | 0.981 | 0.993 | 0.996 |
注:SMA为肠系膜上动脉;SMV为肠系膜上静脉
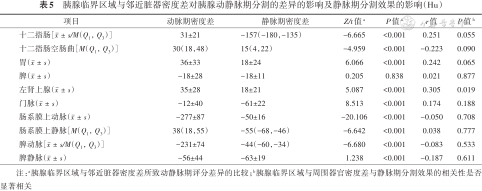
胰腺临界区域与邻近脏器密度差对胰腺动静脉期分割的差异的影响及静脉期分割效果的影响(Hu)
胰腺临界区域与邻近脏器密度差对胰腺动静脉期分割的差异的影响及静脉期分割效果的影响(Hu)
| 项目 | 动脉期密度差 | 静脉期密度差 | Z/t值a | P值a | r值 | P值b |
|---|---|---|---|---|---|---|
| 十二指肠[/M(Q1, Q3)] | 31±21 | -157(-180,-135) | -6.665 | <0.001 | 0.251 | 0.055 |
| 十二指肠空肠曲[M(Q1, Q3)] | 30(18,48) | 15(4,22) | -4.959 | <0.001 | -0.223 | 0.090 |
| 胃() | 36±33 | 18±24 | 6.066 | <0.001 | 0.242 | 0.065 |
| 脾() | -18±28 | -18±11 | 0.205 | 0.838 | 0.021 | 0.877 |
| 左肾上腺() | 35±28 | 18±21 | 5.087 | <0.001 | 0.305 | 0.019 |
| 门脉() | -12±40 | -61±22 | 8.513 | <0.001 | 0.174 | 0.188 |
| 肠系膜上动脉() | -277±87 | -50±16 | -20.106 | <0.001 | -0.050 | 0.708 |
| 肠系膜上静脉[M(Q1, Q3)] | 38(18,55) | -55(-68,-46) | -6.642 | <0.001 | 0.038 | 0.777 |
| 脾动脉[/M(Q1, Q3)] | -231±74 | -44(-60,-34) | -6.680 | <0.001 | -0.083 | 0.533 |
| 脾静脉() | -56±44 | -63±19 | 1.238 | <0.001 | -0.187 | 0.611 |
注:a胰腺临界区域与邻近脏器密度差所致动静脉期评分差异的比较;b胰腺临界区域与周围器官密度差与静脉期分割效果的相关性是否显著相关
本研究基于动静脉双期CT数据构建胰腺自动分割模型,并从主观及客观两个方面对胰腺分割效果进行评价比较,双期DSC评分差异无统计学意义,但是在除脾之外的其他周围器官,动静脉期主观评分差异有统计学意义。主观评分可以弥补客观评分在细节上的缺失,对分割模型的优化有一定的参考意义。此外,研究进一步探索引起动静脉期分割差异及影响静脉期分割效果的可能因素,其中,除胰腺轮廓改变外,胰腺与部分周围器官的脂肪间隙及密度差对动静脉期胰腺分割有显著影响。
腹部CT检查是评估腹部结构及病变最常用的影像学方法之一,多层螺旋CT由于其广泛的适用性及较高的空间分辨力,是临床诊断胰腺疾病的首选[5, 6]。胰腺CT分割的难度在于胰腺形态多样、上腹部器官多而拥挤,且胰腺本身与邻近脏器密度相近[7],故准确率低于其他腹部器官,如肝、脾等[8, 9]。
既往大量研究[1, 2,10, 11]是基于公开数据集,仅有静脉期图像,且小肠内有高密度对比剂充盈,增加了胰腺与周围小肠的对比度,而本研究是回顾性收集本院病例,入组病例肠腔均没有对比剂,分割难度更高,本研究基于动静脉双期CT图像,且均有较好的分割效果,DSC达0.9以上。主观评分的价值在于对胰腺临界区域分割效果的直观评价,本研究中,胰腺与十二指肠、十二指肠空肠曲、左肾上腺、门脉、肠系膜上静脉、脾动、静脉的临界区域,动静脉分割差异显著,考虑与动静脉期胰腺及周围器官的密度差有关;胰-脾临界区动静脉期分割差异无统计学意义,且其密度差差异也无统计学意义,考虑一方面胰脾之间大多存在脂肪间隙,另一方面与脾本身轮廓清晰且与周围器官分界清晰有关;胰-肠系膜上动脉临界区分割差异无统计学意义,考虑与胰腺和肠系膜上动脉之间多存在脂肪间隙有关。胰-左肾上腺临界区域密度差与静脉期胰腺分割显著相关,考虑肾上腺与胰腺部分影像特征相似,比如形态不规则,与周围脏器关系密切,与本研究中密度差及脂肪间隙是影响胰腺分割的因素相似,Bagheri等[12]提出腹部脂肪及胰腺邻近区域的密度是影响胰腺分割的相关因素,因为在脂肪衬托下,胰腺更容易与邻近结构区分出来。
本研究有一定的局限性,首先,本研究为回顾性单中心研究,设置内外验证的多中心研究对模型优化有更重要的意义;其次,本研究只是构建胰腺分割的初步模型,入组的均为正常胰腺或胰腺轮廓清晰的病例,具有一定的选择偏倚。
总之,本研究基于双期CT构建胰腺自动分割模型,并对分割结果进行主、客观评价,对分割影响因素进行初步探索,有助于模型进一步优化,为未来胰腺相关病变的模型构建奠定基础。
曲太平和李秀丽主要负责数据的标准化处理和胰腺分割模型的构建,不涉及经济利益,其他作者均声明不存在利益冲突



























