
探讨腹腔镜新型W-H胃底折叠术治疗质子泵抑制剂(PPI)依赖性胃食管反流病(GERD)的疗效。
回顾性分析2018年10月1日至2019年4月30日于火箭军特色医学中心接受腹腔镜W-H胃底折叠术的PPI依赖性GERD患者临床资料。问卷随访治疗前后的GERD症状评分、症状主观缓解程度、PPI停药情况、疗效满意度以及术后并发症情况。
本研究共纳入GERD患者80例,其中男49例、女31例,中位年龄58岁;其中85%(68例)合并食管炎,77.5%(62例)合并裂孔疝。手术时间为67(52,73)min,无术中并发症和中转开腹。术后随访时间为16(14,18)个月,术后各GERD相关症状评分较术前均下降,差异均有统计学意义(均P<0.05);消化道和呼吸道总体症状的主观缓解程度分别为100(90,100)%和100(80,100)%。随访期间PPI停药率为83%(69/80),疗效满意率为93%(75/80)。术后并发症包括吞咽困难、腹胀、排气增多和腹泻,发生率分别为61%(49/80)、8%(6/80)、5%(4/80)和4%(3/80),有16%(13/80)的患者遗留长期偶尔吞咽不畅。无死亡、症状学复发和再手术病例。
新型W-H胃底折叠术的中期疗效良好,有显著的GERD症状控制率和PPI停药率。术后吞咽困难较常见,但多为自限性,且不影响手术疗效的满意度。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
胃食管反流病(GERD)是消化道反流物对食管和气道等反流通道的刺激和损伤所造成的不适症状、终末器官效应和(或)并发症的一种疾病[1]。GERD已成为一种常见的、危害性较大的慢性疾病[2]。质子泵抑制剂(PPI)按需治疗能长期、有效地控制多数GERD。然而部分GERD患者为PPI依赖性,需要长期PPI维持治疗,甚至不能有效改善症状,这类GERD患者具有抗反流手术指征[3]。现行的胃底折叠术仍存在诸多不足,完全胃底折叠(Nissen胃底折叠)虽然疗效略为持久,但操作复杂,吞咽困难以及腹胀等术后并发症发生率较高;部分胃底折叠(Toupet和Dor胃底折叠)的术后并发症虽然较完全胃底折叠有所改善,但其发生率也并非令人满意,并且疗效持久性略低于完全折叠[4]。火箭军特色医学中心在完成数千例经典的完全和部分胃底折叠术的长期实践基础上[5, 6],设计和应用了新型W-H部分胃底折叠术(以设计和应用者吴继敏和胡志伟姓氏首字母命名),以期同时提高抗反流手术的安全性和疗效。本文重点对腹腔镜新型W-H胃底折叠术的手术方式进行介绍,并对本中心应用该术式治疗PPI依赖性GERD的中期结果进行分析报道。
1. 病例来源:本研究为回顾性队列研究,以2018年10月1日至2019年4月30日在火箭军特色医学中心胃食管外科住院接受新型W-H胃底折叠术的GERD患者为研究对象。纳入标准:(1)年龄>18周岁;(2)有明显的反流[反酸和(或)反食]、烧心和嗳气等典型GERD症状,合并或不合并咳嗽、哮喘和咽炎等呼吸道症状超过半年,且依赖PPI等药物维持治疗超过3个月;(3)对需要PPI等药物长期维持治疗或PPI疗效不满意;(4)半年内的胃镜检查有明确的食管炎(合并或不合并食管裂孔疝),或24 h pH-阻抗监测为病理性酸反流。排除标准:(1)食管高分辨率测压显示贲门失弛缓症、胡桃夹食管或食管流出道梗阻;(2)既往食管、胃等部位手术史;(3)凝血功能障碍、严重心肺功能障碍。本研究符合《赫尔辛基宣言》原则及相关伦理要求。
2. 术前检查:(1)胃镜评估:①食管炎洛杉矶分级:非糜烂性反流病(NERD)、LA-A、LA-B、LA-C和LA-D;②Hill分级评估贲门区的解剖学形态:胃小弯顶端正常而突出的组织皱褶,褶皱紧紧包绕内镜为Ⅰ级;存在皱褶,但围绕镜身间断开闭(通常与呼吸相关)为Ⅱ级;皱褶不明显,且与食管裂孔自由开放,可见微小裂孔疝为Ⅲ级;皱褶消失,食管开放,食管裂孔明显增大,可见明确的裂孔疝为Ⅳ级。(2)24 h pH-阻抗监测:DeMeester评分≥14.72或酸反流时间百分比≥4.2%定义为病理性酸反流。(3)高分辨率测压:下食管括约肌(LES)压力低于13 mmHg (1 mmHg=0.133 kPa)为LES压力过低;腹段LES下缘在腹腔内为正值,其下缘进入胸腔内为负值;LES压力带下缘位于膈肌压力带之上而与之分离,导致腹段LES长度变为负值定义为食管裂孔疝;无效吞咽百分比≥50%定义为无效食管动力(IEM)[7]。
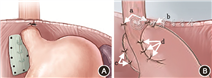
3. 腹腔镜W-H胃底折叠术:(1)患者体位及打孔:患者仰卧位,双下肢分开呈“大”字体位,头高脚低约30°至45°,四肢固定于手术台。主刀站于患者两腿之间,扶镜手位于患者右侧,一助位于患者左侧。于脐正上方作1 cm大小切口,穿入气腹针建立气腹(12~14 mmHg),然后置入1 cm的套管针及腹腔镜镜头;腹腔镜直视下于左锁骨中线肋缘下另作1 cm切口,置入1 cm的套管针,再于右锁骨中线肋缘下、左腋前线平脐及剑突下,分别作3个0.5 cm小切口置入相应套管针(图1)。(2)食管下段游离和食管裂孔修补:离断肝胃韧带(通常不保留迷走神经肝支),暴露右侧膈肌脚,探查增大的食管裂孔和疝入的胃等组织,将疝入胸腔的组织还纳至腹腔,离断食管右侧及前方的膈食管膜,并沿食管向纵膈内游离食管下段5~6 cm;从食管左侧离断食管后方疝囊,暴露并离断左膈肌脚下段膈食管膜(可保留左膈肌脚上段紧邻食管的膈食管膜),腹段食管后方制造窗孔长3~4 cm,进一步游离食管下段,使腹段食管长度≥2.5 cm。3-0不可吸收线于食管后方间断缝合两侧膈肌脚缩小食管裂孔至完整包绕食管(针距<1 cm)。取裁剪成"U"形的牛心包(冠昊)或复层猪小肠黏膜下层(COOK)软组织修补片,用可吸收钉(Tyco 5 mm)固定于食管后方膈肌脚以加强食管裂孔修补(图2A、B,图3A)。(3)W-H胃底折叠+膈食管膜重建:①切除胃食管结合部前方的脂肪垫,将胃底摆放于自然状态,将胃底右侧缝合固定于左侧膈肌脚,可同时缝合固定胃底、膈肌和食管,完成His角重建和左侧膈食管膜重建;②将胃底后壁拉到食管后方,自上而下缝合2针固定于食管后方的膈肌上,完成食管后90°折叠;③再将胃底前壁拉到食管正前方,自上而下与食管缝合2~3针,其中第1针同时缝合胃底、膈肌顶端和食管前方,完成食管前90°折叠和食管前方膈食管膜重建;④将食管右侧缝合固定于右侧膈肌脚,完成右侧膈食管膜重建(图2C、D,图3B)。
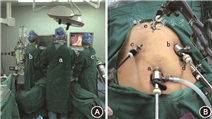

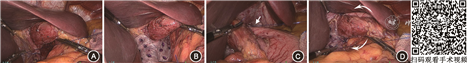

腹腔镜下食管裂孔疝修补术+新型W-H胃底折叠术的基本操作方法和步骤。包括手术入路、术野暴露、食管裂孔的解剖和食管下段分离、食管裂孔疝缝合修补和补片加强修补、膈食管膜重建和食管左侧180度折叠。
手术操作者:胡志伟

4. 观察项目及标准[5]:(1)术中并发症(包括出血、胃肠穿孔、气胸、脾损伤和肝损伤等)、中转开腹率、死亡率和手术时间(切皮至关腹)。(2)术前和术后症状评分问卷随访:①症状发作频率评分:0分为无症状;1分为发作<1次/周;2分为发作1~2次/周;3分为3~4次/周;4分为5~6次/周;5分为>6次/周。②症状严重程度评分:0分为无症状;1分为症状轻微;2分为轻度,有不适感,但不影响正常生活;3分为中度,影响正常生活及工作;4分为重度,非常不适,严重影响正常生活及工作;5分为非常严重,生活不能自理或者威胁生命,甚至需要一次或多次抢救。发病频率评分+症状严重程度评分为0~10分。纳入考察的消化道症状包括反酸、反食、烧心、嗳气、腹胀、腹痛和胸/背痛等,呼吸道症状包括咳嗽、哮喘、咽部异物感等。(3)视觉模拟评分(VAS)法评价术后较术前各单独症状和总体症状的主观缓解程度(0~100%,0为症状不变,100%为症状完全消失)。同时调查患者对手术整体疗效的满意度(分为非常满意、满意、可以接受、不满意,非常不满意,其中可以接受、不满意和非常不满意统称为欠满意)。(4)术后PPI用药情况与术前进行比较(分为停药、减量≥1/2、减量<1/2、不变)。(5)术后并发症(包括吞咽困难、腹胀、嗳气困难、排气增多、腹痛、腹泻和便秘等),对术后吞咽困难进行分类和评分:无吞咽困难为0分,自限性轻度吞咽困难为1分,自限性明显吞咽困难或长期轻度吞咽困难均为2分,自限性明显吞咽困难后出现长期轻度吞咽困难为3分,长期明显吞咽困难为4分(明显吞咽困难表现为进食时经常发生吞咽困难,轻度吞咽困难表现为进食过快、大块食物或干硬食物偶尔出现吞咽不畅)。(6)术后症状学复发率和再手术率。
5. 统计学处理:应用 SPSS 17.0 软件对数据进行分析。不符合正态分布的计量资料以M(Q1,Q3)表示,不同组间的比较采用Mann-Whitney U非参数检验,同一指标的前后比较采用Wilcoxon W符号秩检验。计数资料以例(%)表示,两组间阳性率的比较采用χ²检验。双侧检验,检验水准α=0.05。
1. 一般资料:本研究纳入PPI依赖性GERD患者80例,其中男49例、女31例,中位年龄58岁。术后随访时间为16(14,18)(12~19)个月。患者术前的性别、年龄、症状分类、PPI疗效、胃镜结果、24 h pH-阻抗监测结果和食管高分辨率测压结果见表1。胃镜检出滑动型食管裂孔疝为60%(48/80),混合疝为18%(14/80),其余23%(18/80)的患者为贲门Hill分级Ⅲ级, 23%(18/80)的患者检出多发性胃息肉。
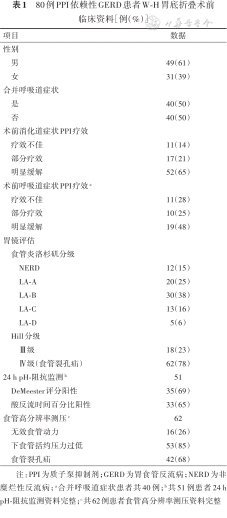
80例PPI依赖性GERD患者W-H胃底折叠术前临床资料[例(%)]
80例PPI依赖性GERD患者W-H胃底折叠术前临床资料[例(%)]
| 项目 | 数据 | |
|---|---|---|
| 性别 | ||
| 男 | 49(61) | |
| 女 | 31(39) | |
| 合并呼吸道症状 | ||
| 是 | 40(50) | |
| 否 | 40(50) | |
| 术前消化道症状PPI疗效 | ||
| 疗效不佳 | 11(14) | |
| 部分疗效 | 17(21) | |
| 明显缓解 | 52(65) | |
| 术前呼吸道症状PPI疗效a | ||
| 疗效不佳 | 11(28) | |
| 部分疗效 | 10(25) | |
| 明显缓解 | 19(48) | |
| 胃镜评估 | ||
| 食管炎洛杉矶分级 | ||
NERD | 12(15) | |
LA-A | 20(25) | |
LA-B | 30(38) | |
LA-C | 13(16) | |
LA-D | 5(6) | |
| Hill分级 | ||
Ⅲ级 | 18(23) | |
Ⅳ级(食管裂孔疝) | 62(78) | |
| 24 h pH-阻抗监测b | 51 | |
| DeMeester评分阳性 | 35(69) | |
| 酸反流时间百分比阳性 | 33(65) | |
| 食管高分辨率测压c | 62 | |
| 无效食管动力 | 16(26) | |
| 下食管括约压力过低 | 53(85) | |
| 食管裂孔疝 | 42(68) | |
注:PPI为质子泵抑制剂;GERD为胃食管反流病;NERD为非糜烂性反流病;a合并呼吸道症状患者共40例;b共51例患者24 h pH-阻抗监测资料完整;c共62例患者食管高分辨率测压资料完整
所有患者的手术技术成功率为100%,无术中并发症、无中转开腹和死亡。手术时间67(52,73)(43~102)min。术前胃镜检查为贲门松弛(Hill分级Ⅲ级)而无裂孔疝的18例患者,在术中可观察到其中14例有滑动型食管裂孔疝。手术放置牛心包补片和复层猪小肠黏膜下层补片的比例分别为41%(33/80)和59%(47/80)。
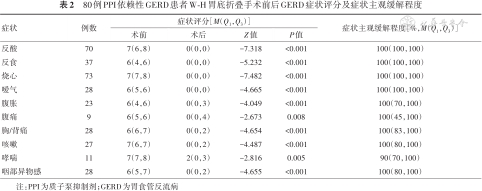
2. W-H胃底折叠术疗效:术后患者的消化道和呼吸道各症状评分较治疗前均下降,差异均有统计学意义(均P<0.05);消化道总体症状的主观缓解程度为100(90,100)%,呼吸道总体症状(40例)的主观缓解程度为100(80,100)%,各单一症状的主观缓解程度见表2。合并呼吸道症状的40例患者的消化道总体症状主观缓解程度略高于呼吸道总体症状主观缓解程度,但差异无统计学意义(Z=-1.294,P=0.196)。患者中有3例合并呕吐症状,均完全消失;2例合并频繁呃逆,均完全消失;3例合并声音嘶哑,均明显缓解;6例合并口酸/口苦等口腔症状,其中3例明显缓解、1例部分缓解、2例无效;1例喉痉挛完全缓解;1例顽固性贫血完全缓解。两种补片的疗效满意度相比差异无统计学意义(χ²=3.859,P=0.277)。
80例PPI依赖性GERD患者W-H胃底折叠手术前后GERD症状评分及症状主观缓解程度
80例PPI依赖性GERD患者W-H胃底折叠手术前后GERD症状评分及症状主观缓解程度
| 症状 | 例数 | 症状评分[M(Q1,Q3)] | 症状主观缓解程度[%,M(Q1,Q3)] | |||
|---|---|---|---|---|---|---|
| 术前 | 术后 | Z值 | P值 | |||
| 反酸 | 70 | 7(6,8) | 0(0,0) | -7.318 | <0.001 | 100(100,100) |
| 反食 | 37 | 6(4,6) | 0(0,0) | -5.232 | <0.001 | 100(100,100) |
| 烧心 | 73 | 7(7,8) | 0(0,0) | -7.482 | <0.001 | 100(100,100) |
| 嗳气 | 28 | 6(5,6) | 0(0,0) | -4.665 | <0.001 | 100(100,100) |
| 腹胀 | 23 | 6(4,6) | 0(0,3) | -4.049 | <0.001 | 100(70,100) |
| 腹痛 | 9 | 6(5,6) | 0(0,4) | -2.673 | 0.008 | 100(45,100) |
| 胸/背痛 | 28 | 6(6,7) | 0(0,2) | -4.654 | <0.001 | 100(83,100) |
| 咳嗽 | 27 | 7(6,7) | 0(0,2) | -4.487 | <0.001 | 100(80,100) |
| 哮喘 | 11 | 7(7,8) | 2(0,3) | -2.816 | 0.005 | 90(70,100) |
| 咽部异物感 | 28 | 6(5,7) | 0(0,2) | -4.655 | <0.001 | 100(80,100) |
注:PPI为质子泵抑制剂;GERD为胃食管反流病
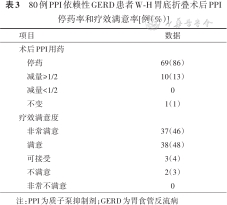
术后随访期间的停药率为86%(69/80);疗效满意率为93%(75/80),疗效欠满意但可以接受的比例为4%(3/80),疗效不满意的为3%(2/80)(表3)。认为疗效可接受的3例患者的总体症状主观缓解程度分别为20%、50%和60%。疗效不满意的2例患者中,1例总体症状主观缓解程度为20%,另外1例反酸和烧心完全缓解,而咳嗽和哮喘没有缓解。
80例PPI依赖性GERD患者W-H胃底折叠术后PPI停药率和疗效满意率[例(%)]
80例PPI依赖性GERD患者W-H胃底折叠术后PPI停药率和疗效满意率[例(%)]
| 项目 | 数据 |
|---|---|
| 术后PPI用药 | |
停药 | 69(86) |
减量≥1/2 | 10(13) |
减量<1/2 | 0 |
不变 | 1(1) |
| 疗效满意度 | |
非常满意 | 37(46) |
满意 | 38(48) |
可接受 | 3(4) |
不满意 | 2(3) |
非常不满意 | 0 |
注:PPI为质子泵抑制剂;GERD为胃食管反流病
3.术后并发症、复发和再手术:所有患者无术中出血、胃肠穿孔和肝脾损伤等严重并发症;无术中和术后死亡病例;术后无症状学复发和再手术病例。患者术后考察的并发症包括吞咽困难、腹胀、嗳气困难、排气增多、腹痛、腹泻和便秘,发生率分别为61%(49/80),8%(6/80),0(0/80),5%(4/80),0(0/80),4%(3/80)和0(0/80)。在术后吞咽困难的患者中,自限性轻度吞咽困难为27%(21/80),缓解时间为1.3(0.6,2.9)个月,自限性明显吞咽困难为24%(19/80),缓解时间为1.8(1,2.6)个月,16%(13/80)的患者遗留长期偶尔轻度吞咽困难,无长期明显吞咽困难的患者。1例患者因明显吞咽困难而在术后3个月接受探条扩张治疗后明显缓解。两种补片的吞咽困难评分相比差异无统计学意义(Z=-0.759,P=0.448)。无效食管动力患者(16例)的吞咽困难评分与食管动力相对正常患者(46例)的吞咽困难评分相比差异无统计学意义(Z =-0.059,P =0.953)。患者术后出现的轻度腹胀、排气增多、腹泻和便秘均于术后3个月至半年内逐渐缓解。
胃底折叠术已被证明可以有效控制反流,提高生活质量,减少用药,降低治疗成本,但术后并发症和复发率或多或少仍然存在[3, 8]。Nissen[9]最早于1936年描述了Nissen胃底折叠术, Dallemagne等[10]于1991年实施了第一例腹腔镜下的Nissen胃底折叠术,标志着抗反流手术进入微创时代。为了使抗反流手术能够最大限度地提高症状控制率,减少术后吞咽困难和胃肠功能紊乱等副作用,以及降低复发率,外科医生不断尝试对抗反流术式的折叠方式进行改良。1965年,Nissen和Rossetti[11]报道了不分离胃短血管的完全胃底折叠术(Nissen-Rossetti胃底折叠术)。1985年之后,DeMeeter等[12]和Donahue等[13]将Nissen胃底折叠的纵向长度从5 cm缩短至1.5~2.0 cm 的“短松”Nissen胃底折叠开始流行。Toupet[14]提出了前置180°和后置270°部分胃底折叠术,以期简化手术操作并减少术后吞咽困难等并发症。有学者应用前置90°胃底折叠术,进一步减少了折叠的度数,以期进一步减少术后并发症[15]。还有一些外科医生干脆不进行胃底折叠,Segol等[16]、Müller-Stich等[17]和Li等[18]在食管裂孔疝修补之后仅做His角重建,他们认为这种手术方式最接近前肠的自然状态,可能对胃肠功能的干扰最小。
研究显示,与裂孔疝修补后加做胃底折叠相比,裂孔疝修补后仅做His角重建的疗效多在一年内迅速消失,从而导致了大量的复发和再手术[16, 17, 18],从而证明裂孔疝修复之后进行胃底折叠是非常有必要的。总体上,完全胃底折叠(Nissen)的抗反流作用和持久性优于部分胃底折叠,而部分胃底折叠(Toupet和Dor)术后早期的吞咽困难等并发症的发生率和严重程度要低于完全折叠,二者的优点和缺点相互抵消后,患者的远期疗效满意情况是相似的[19, 20, 21]。Nijjar等[22]的研究亦显示前置90°胃底折叠术的长期抗反流疗效明显低于Nissen胃底折叠术,上述研究表明,完全胃底折叠术后并发症的发生率最高且明显,而仅有90°的胃底折叠的抗反流能力又明显不足。故本中心先重建His角,再围绕食管分别向前和向后分别做两个90°的折叠,即食管左侧180°折叠,该术式优点在于折叠度数等同于Dor胃底折叠(180°),折叠缝合张力进一步减小,更无需离断胃短血管,且形态更加符合生理特点。
除胃底折叠方式的改变外,本术式进一步增强了腹段食管的有效长度和食管裂孔的严密关闭。在抗反流手术发明的早期就已经证明不做食管裂孔修补,仅实施Nissen胃底折叠术极易导致裂孔疝和症状复发,表明食管裂孔修复也是抗反流手术的关键一环[23]。长期随访的数据表明,解剖学复发仍然是现行经典抗反流手术的主要问题,症状学复发可高达10%~62%[8],一期腹腔镜抗反流术后复发而需要长期用药或二期抗反流手术的患者高达17.7%[24]。最近的一项研究显示巨大食管裂孔疝抗反流术后5年的解剖学复发高达39.3%~56.7%[25]。而抗反流术后5年和10年的累积再手术率分别为5.2%和6.9%[26]。复发后的胃镜和钡餐造影检查以及二次手术的术中所见显示,解剖学复发的大多数原因是由于食管裂孔一期手术关闭不严或再次增大导致腹段食管回缩,进而折叠的胃再次疝入胸腔[8, 26, 27],表明抗反流术后复发不单是折叠方式的问题,而维持足够长度的腹段食管和更加完善食管裂孔的修复(包括膈食管膜重建)对于预防复发可能更为关键。与其他中心相似,本术式也需要游离食管下段使腹段食管达2.5 cm以上[3, 4]。然而与其他中心不同的是,本术式还对手术破坏的膈食管膜进行了缝合重建并固定了腹段食管,以减少腹段食管回缩和折叠瓣疝入胸腔的可能。另外,与其他中心相比,本术式强调更严密的食管裂孔关闭,使修复后的真性食管裂孔(不含薄弱的疝囊组织)能够更加严密贴合食管,并常规使用“U”型生物补片加强食管裂孔疝修补。本研究患者随访1年以上无症状学复发,表明上述技术措施可能有助于增强抗反流结构的耐久性。
本研究显示,新型W-H胃底折叠术对GERD的典型症状、不典型症状以及气道症状均有显著的缓解作用,患者的疗效满意率为93%,停药率为86%。该结果与本中心之前报告的Nissen、Toupet和Dor胃底折叠术有相似的疗效满意率[5, 6],与其他中心所报道的胃底折叠术也有相似的抗反流疗效[3, 4]。表明新型W-H胃底折叠术同样可以高效控制各种形式的胃食管反流,从而有替代经典胃底折叠术的潜能。
本研究中,仍有5例患者没有对手术疗效给出满意评价,均是因为术后症状改善不充分,而没有因术后并发症而造成对手术疗效不满意的情况。表明症状的控制情况是患者对该术式疗效满意度评价的关键。虽然本研究患者报告的术后吞咽困难发生率较高,但为自限性,可在2个月内自行缓解,仅1例需要内镜下探条扩张干预,即使有16%的患者遗留偶尔轻微的吞咽困难,但不影响其生活和对手术疗效的评价,并且随着随访时间的延长,遗留的这些轻度吞咽困难也在缓慢缓解。导致患者报告的吞咽困难发生率较高的可能原因包括:相对严密的食管裂孔关闭和膈食管膜重建,未采用术中胃镜或术中探条,术后发生的所有偶尔轻的微吞咽困难均计入了术后吞咽困难并发症等[5]。其他少数自限性并发症状包括腹胀、排气增多和腹泻多于半年内自行缓解。这也是本研究患者对手术整体疗效的满意率能达到93%的原因。
综上,腹腔镜新型W-H胃底折叠术在His角和膈食管膜重建的基础上进行前置90°和后置90°折叠形成了更加接近原生理形态的食管左侧180°折叠,同时减少了分离胃短血管的风险,又简化了手术操作。该术式疗效良好,和经典胃底折叠术有相似的症状控制率和PPI停药率,且不易复发,有替代经典胃底折叠术的潜能。虽然该术式的术后吞咽困难仍较常见,但为自限性。另外,该术式的客观检查、长期疗效,以及与其他术式的对比仍需进一步研究。
所有作者均声明不存在利益冲突



























