
调查临床实验室开展CD34+细胞计数的检测现状,分析存在的问题,为制定质量改进方案提供依据。
以参加CD34+细胞计数全国室间质量评价活动的101家实验室为调查对象,通过问卷调查和质评物检测,收集相关检测方法学信息及质评物检测结果。参考国内外指南文件确定CD34+细胞计数的质量控制要求,对调查实验室的遵循情况进行分析。分组统计质评物检测结果,并与美国病理家学会(CAP)质评数据进行比较。
共收到97家实验室回报的调查问卷信息,99家实验室回报的质评物检测结果。问卷调查数据显示实验室对设门方案、移液方式和获取细胞数等关键质量控制要求的遵循比率较高,分别为92.8%、83.9%和82.5%;而对采用全血质控品开展室内质量控制、溶血素的选择、处理样品是否洗涤、是否报告绝对计数以及仪器的质量控制等要求的遵循比率较低,分别为5.2%、28.9%、39.2%、46.4%和55.7%。质评物检测结果显示,国内实验室CD34+相对计数的变异系数与CAP质评数据相近,但绝对计数的变异系数大于CAP质评数据。
临床实验室对部分质量控制要求的遵从性较差,绝对计数结果的实验室间差异较大,建议实验室加强CD34+细胞计数质量控制相关培训,特别是绝对计数方法和技术要求的培训。

造血干细胞移植已广泛用于多种恶性血液系统疾病、实体肿瘤、自身免疫性疾病和基因缺陷病等的治疗[1, 2, 3, 4]。准确计数CD34+细胞对于确认造血干细胞的动员效果、确定采集时间、植入数量以及移植后的监测等至关重要[2,5]。流式细胞仪计数CD34+细胞因其操作简便、定量快速等特点,已被广泛用于临床实验室造血干细胞数量的检测[4,6]。1996年国际血液治疗与移植工程学会(ISHAGE)提出关于CD34+细胞计数的ISHAGE方案后[7],多个标准化机构也陆续发布了指南文件[4,8, 9, 10, 11, 12, 13],但国外多项研究数据显示CD34+细胞计数的实验室间变异仍较大[14, 15, 16, 17],实验室对指南建议的遵循情况较差[17, 18],而关于国内临床实验室CD34+细胞计数检测现状的研究未见报道。考虑到实验室质量控制与改进的需求,国家卫生健康委临床检验中心(NCCL)对参加全国CD34+细胞计数室间质量评价(EQA)的实验室进行了问卷调查和质评物检测调查,旨在了解我国临床实验室开展CD34+细胞计数的检测现状及存在问题,为制定质量改进方案提供参考依据。
选取2020年参加NCCL开展的“流式细胞分析:CD34+干细胞计数”全国EQA活动的101家实验室,覆盖全国25个省份或直辖市。
参考国内外指南文件[4,7, 8, 9, 10, 11, 12],设计CD34+细胞计数调查问卷,内容包括实验室所使用的检测仪器和试剂种类、标本染色和处理方式、检测设门方案及细胞获取数量、绝对计数方法以及实验室质量控制信息等。以二维码形式发放至实验室,填写人员扫描二维码填报“CD34+细胞计数调查回报表”。
将2个浓度水平的质评物(编号为202001、202002)以快递邮寄(加冰袋冷藏运输)方式发放。要求各实验室按各自的检测程序对CD34+细胞计数方法进行检测,通过NCCL网络回报系统提交检测结果,并以邮件形式回报检测结果分析图。
1. 问卷调查结果统计:使用Microsoft Excel软件进行统计学分析。参考英国国家室间质评机构(UK NEQAS)调查方法[19],并结合国内外指南文件[4,8, 9, 10, 11, 12, 13],确定CD34+细胞计数的质量控制要求;根据问卷调查结果,对调查实验室的遵循比率进行统计。遵循比率指调查中实际遵循某项质量控制要求的实验室数占应遵循该项质量控制要求的所有实验室数的比例。
2. 质评物检测结果统计:参考美国病理家学会(CAP)的EQA统计方法对质评物检测结果进行离群值剔除[20]:计算原始数据的均值()和标准差(s),剔除超出的数据后重新计算和s,进行两次迭代以剔除剩余离群值。按仪器品牌进行分组:BD仪器组和Beckman Coulter仪器组;各组CD34+细胞计数为偏态分布数据,采用M(Q1,Q3)表示,并计算实验室间变异系数(CV),将统计结果与2019年CAP质评数据进行比较[21]。质评物CD34+绝对计数检测结果按绝对计数平台方法(单双平台)、溶血素类型(是否含固定剂)和样品处理方式(是否进行洗涤)重要影响因素进行分组,比较各组间的离散度情况。
共回收97家(96.0%)实验室回报调查问卷表,其中包括65家综合性医院、3家血液病医院、5家脐带血造血干细胞库、19家干细胞生物技术公司以及5家第三方医学检验机构。99家(98.0%)实验室回报质评物检测结果,其中相对计数检测结果回报99家,绝对计数检测结果回报66家。
1. 仪器品牌与型号:实验室所使用的流式细胞仪品牌主要为美国BD公司(54家,占55.7%)和美国贝克曼库尔特(Beckman Coulter)有限公司(39家,占40.2%),主要仪器型号包括BD FACS Canto系列(40家)、Beckman Coulter Navios(17家)、Beckman Coulter FC500(15家)和BD FACS Calibur(12家)。
2. 试剂种类:97家实验室中有20家(20.6%)使用CD34+细胞检测试剂盒;77家实验室使用自选抗体,其中30家(39.0%)在使用新批次抗体时会进行抗体滴定;54家(55.7%)使用同型对照抗体;11家(11.3%)实验室使用活力染料如7-AAD检测标本细胞活力。结果见表1。

参加CD34+细胞计数质量评价的实验室检测试剂种类分布
参加CD34+细胞计数质量评价的实验室检测试剂种类分布
| 调查内容 | 实验室数(家) | 构成比(%) |
|---|---|---|
| 检测抗体种类 | ||
CD34+细胞计数试剂盒 | 20 | 20.6 |
实验室自选抗体 | 77 | 79.4 |
| 是否对自选抗体进行滴定 | ||
是 | 30 | 39.0 |
否 | 47 | 61.0 |
| CD34抗体标记荧光素 | ||
PE | 92 | 94.8 |
其他 | 5 | 5.2 |
| CD45抗体标记荧光素 | ||
FITC | 60 | 61.8 |
PerCP | 25 | 25.8 |
其他 | 12 | 12.4 |
| 是否使用同型对照 | ||
是 | 54 | 55.7 |
否 | 43 | 44.3 |
| 是否使用细胞活力染料 | ||
是 | 11 | 11.3 |
否 | 86 | 88.7 |
注:PE为藻红蛋白;FITC为异硫氰酸荧光素;PerCP为多甲藻叶绿素蛋白
3. 实验室对质量控制要求的遵循情况:97家实验室对国内外指南建议的质量控制要求遵循情况如表2所示[4,8, 9, 10, 11, 12, 13]。对于检测通用性要求,90家(92.8%)实验室采用国内外指南推荐的ISHAGE设门方案,85家(87.6%)实验室在样品制备后1 h内上机进行检测,80家(82.5%)实验室获取至少100个CD34+细胞或75 000个CD45+细胞,遵循比率较高;但仅有5.2%的实验室能够在检测当天使用CD34+细胞质控品对检测过程进行质量控制,28.9%的实验室使用不含固定剂的溶血素裂解红细胞,遵循比率较低。在绝对计数方法中,采用单平台和双平台方法的实验室对于计数相关器具的质量控制要求遵循比率相对较高。
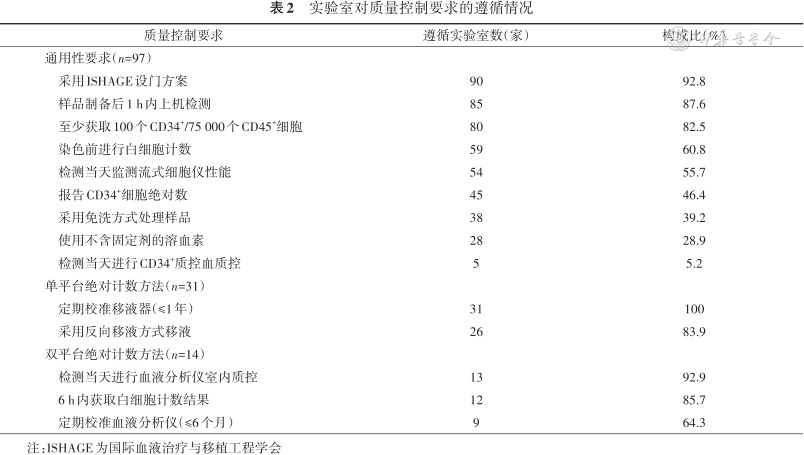
实验室对质量控制要求的遵循情况
实验室对质量控制要求的遵循情况
| 质量控制要求 | 遵循实验室数(家) | 构成比(%) |
|---|---|---|
| 通用性要求(n=97) | ||
采用ISHAGE设门方案 | 90 | 92.8 |
样品制备后1 h内上机检测 | 85 | 87.6 |
至少获取100个CD34+/75 000个CD45+细胞 | 80 | 82.5 |
染色前进行白细胞计数 | 59 | 60.8 |
检测当天监测流式细胞仪性能 | 54 | 55.7 |
报告CD34+细胞绝对数 | 45 | 46.4 |
采用免洗方式处理样品 | 38 | 39.2 |
使用不含固定剂的溶血素 | 28 | 28.9 |
| 检测当天进行CD34+质控血质控 | 5 | 5.2 |
单平台绝对计数方法(n=31) | ||
定期校准移液器(≤1年) | 31 | 100 |
采用反向移液方式移液 | 26 | 83.9 |
| 双平台绝对计数方法(n=14) | ||
检测当天进行血液分析仪室内质控 | 13 | 92.9 |
6 h内获取白细胞计数结果 | 12 | 85.7 |
定期校准血液分析仪(≤6个月) | 9 | 64.3 |
注:ISHAGE为国际血液治疗与移植工程学会
1. CD34+细胞计数结果和实验室间离散度情况:对各组数据进行离群值剔除后,使用实验室数超过10家的仪器品牌组包括BD仪器组和Beckman Coulter仪器组(BC组),结果与CAP质评数据进行比较,见表3。高浓度标本相对计数和绝对计数检测结果的CV小于低浓度标本,BD组的CV总体而言要小于BC组,国内实验室相对计数检测结果的CV与CAP数据相比较为接近,而绝对计数结果的CV要大于CAP数据。
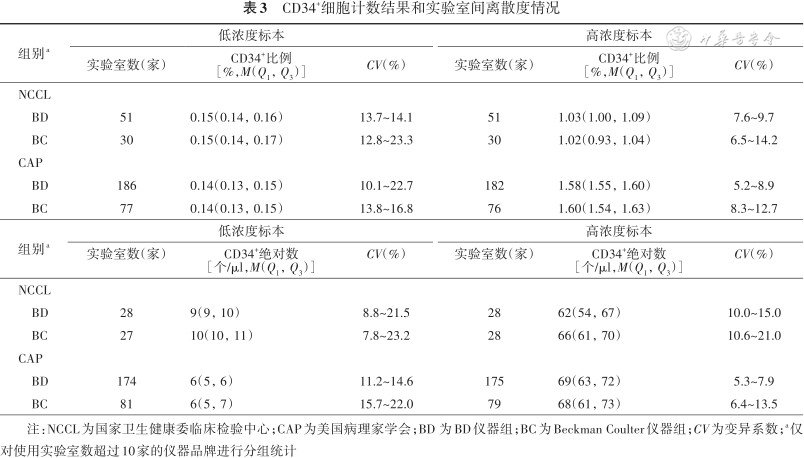
CD34+细胞计数结果和实验室间离散度情况
CD34+细胞计数结果和实验室间离散度情况
| 组别a | 低浓度标本 | 高浓度标本 | ||||
|---|---|---|---|---|---|---|
| 实验室数(家) | CD34+比例 [%,M(Q1,Q3)] | CV(%) | 实验室数(家) | CD34+比例 [%,M(Q1,Q3)] | CV(%) | |
| NCCL | ||||||
BD | 51 | 0.15(0.14,0.16) | 13.7~14.1 | 51 | 1.03(1.00,1.09) | 7.6~9.7 |
BC | 30 | 0.15(0.14,0.17) | 12.8~23.3 | 30 | 1.02(0.93,1.04) | 6.5~14.2 |
| CAP | ||||||
BD | 186 | 0.14(0.13,0.15) | 10.1~22.7 | 182 | 1.58(1.55,1.60) | 5.2~8.9 |
BC | 77 | 0.14(0.13,0.15) | 13.8~16.8 | 76 | 1.60(1.54,1.63) | 8.3~12.7 |
| 组别a | 低浓度标本 | 高浓度标本 | ||||
| 实验室数(家) | CD34+绝对数 [个/μl,M(Q1,Q3)] | CV(%) | 实验室数(家) | CD34+绝对数 [个/μl,M(Q1,Q3)] | CV(%) | |
| NCCL | ||||||
BD | 28 | 9(9,10) | 8.8~21.5 | 28 | 62(54,67) | 10.0~15.0 |
BC | 27 | 10(10,11) | 7.8~23.2 | 28 | 66(61,70) | 10.6~21.0 |
| CAP | ||||||
BD | 174 | 6(5,6) | 11.2~14.6 | 175 | 69(63,72) | 5.3~7.9 |
BC | 81 | 6(5,7) | 15.7~22.0 | 79 | 68(61,73) | 6.4~13.5 |
注:NCCL为国家卫生健康委临床检验中心;CAP为美国病理家学会;BD 为BD仪器组;BC为Beckman Coulter仪器组;CV为变异系数;a仅对使用实验室数超过10家的仪器品牌进行分组统计
2. 按照计数影响因素分组的离散度情况:质评物绝对计数检测结果按照计数影响因素分组的统计结果如表4所示,其中遵循指南要求的单平台方法组、溶血素不含固定剂组和样品免洗处理组CV相对较小。
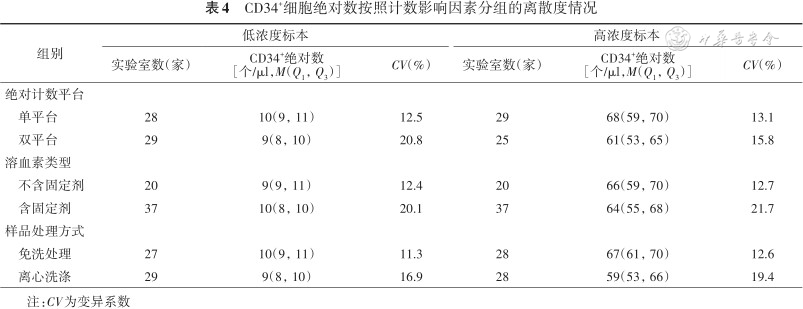
CD34+细胞绝对数按照计数影响因素分组的离散度情况
CD34+细胞绝对数按照计数影响因素分组的离散度情况
| 组别 | 低浓度标本 | 高浓度标本 | ||||
|---|---|---|---|---|---|---|
| 实验室数(家) | CD34+绝对数 [个/μl,M(Q1,Q3)] | CV(%) | 实验室数(家) | CD34+绝对数 [个/μl,M(Q1,Q3)] | CV(%) | |
| 绝对计数平台 | ||||||
单平台 | 28 | 10(9,11) | 12.5 | 29 | 68(59,70) | 13.1 |
双平台 | 29 | 9(8,10) | 20.8 | 25 | 61(53,65) | 15.8 |
| 溶血素类型 | ||||||
不含固定剂 | 20 | 9(9,11) | 12.4 | 20 | 66(59,70) | 12.7 |
含固定剂 | 37 | 10(8,10) | 20.1 | 37 | 64(55,68) | 21.7 |
| 样品处理方式 | ||||||
免洗处理 | 27 | 10(9,11) | 11.3 | 28 | 67(61,70) | 12.6 |
离心洗涤 | 29 | 9(8,10) | 16.9 | 28 | 59(53,66) | 19.4 |
注:CV为变异系数
CD34+细胞计数是评估外周血、骨髓和脐带血中造血干细胞数量的重要指标。在临床干细胞移植实践中,用于移植的CD34+细胞数量通常十分有限,需要准确判断移植物中CD34+细胞数量是否能够满足重建造血的要求,计数结果假性偏低可能会导致花费不必要的努力来获取额外的细胞,假性偏高则可能对受者的生命造成严重危害[22, 23]。对于脐带血造血干细胞库,则需对新鲜脐带血中的CD34+细胞总数进行检测,以判断每份脐带血是否具有冻存价值[24]。因此,保证临床实验室CD34+细胞计数结果的可靠性具有十分重要的临床意义。
本次调查主要参考2007年美国临床和实验室标准协会(CLSI)发布的H42-A2指南文件[10]、2017年澳大利亚流式细胞学会(ACS)发布的CD34造血祖细胞计数指南[11]、2015年中国免疫学会血液免疫分会临床流式细胞术学组发布的《CD34阳性细胞绝对计数的流式细胞术测定指南》[4]等文件的要求,就CD34+细胞计数质量控制的关键环节进行问卷与检测调查,并将调查结果与日本室间质评调查数据和CAP室间质评数据[21]进行比较,以提出质量改进建议。
各实验室对设门方案选择、获取细胞数量和移液方式的选择(常规使用方式分为正向移液和反向移液[25])等质量控制要求的遵循比率较高。(1)设门方案的选择:92.8%的实验室均采用指南推荐的ISHAGE设门方案[4,10, 11],在2017年日本室间质评调查和2012年UK NEQAS调查[17]中采用该设门方案的实验室比例分别为87.0%和80.6%。与国外调查相比,我国临床实验室对于ISHAGE设门方案的使用比例较高。(2)需获取的细胞数量:指南要求获取细胞数应至少满足两个条件之一:获取100个CD34+细胞或者75 000个CD45+细胞[4,10, 11]。本次调查中有82.5%的实验室符合要求,该比例略低于日本的调查数据(87.8%)。获取CD34+细胞数不足可能导致检测结果存在较大差异,建议实验室以至少获取100个CD34+细胞数为检测终止条件,而对于CD34+细胞浓度极低的标本,在可用检测样本量有限的情况下,应至少获取75 000个CD45+细胞以达到所需的精密度要求。(3)移液方式的选择:移液体积的准确性是影响单平台绝对计数结果准确性的主要因素之一[6,26, 27]。各指南均明确指出,在使用单平台方法时,应采用反向移液方式进行移液[4,10, 11]。本次调查中使用单平台方法的实验室符合要求的比例为83.9%,建议未采用反向移液方式的实验室按指南要求进行改进。
实验室对仪器性能监测、质控品检测、样品处理方式和结果报告等质量控制要求的遵循比率相对较低。(1)仪器性能监测:指南要求实验室检测当天使用商品化微球对仪器进行校准和监测[4,10, 11],以确保仪器的检测状态满足要求,本次调查中有44.3%的实验室未能在检测当天对流式细胞仪的性能进行监测。(2)室内质量控制:使用CD34+细胞质控品开展室内质量控制可有效保证检测结果的精密度,如CAP核查表中要求实验室在检测当天至少使用2个浓度水平(其中一个应处于或接近临床决定水平)的阳性质控品开展室内质控[28]。本次调查中仅5.2%的实验室能够在检测当天进行CD34+细胞质控品的检测。原因为进口CD34+细胞全血质控品价格昂贵且有效期很短,部分质控品适用性也存在一定问题,限制了实验室室内质控活动的规范开展[29]。(3)样品处理:CLSI和ACS指南建议采用免洗方式处理样品[10, 11],国内指南考虑到我国实验室多使用自行组合的抗体,有些抗体不适用于免洗方式,因此仅要求单平台方法的样品处理采用免洗方式[4]。本次调查中使用自行组合抗体的实验室中有31.2%采用免洗处理,使用厂商提供试剂盒的实验室中有70.0%采用免洗处理,本次质评物绝对计数分组统计结果显示,免洗处理组的离散度要小于离心洗涤组。建议对于使用自行组合抗体的实验室应确认所用抗体是否支持免洗处理,选用支持免洗处理的抗体,以避免洗涤造成有核细胞的丢失;对于使用单平台计数方法且选用商品试剂盒的实验室,对样品处理时不能进行洗涤[10]。(4)溶血素种类的选择:CLSI和ACS指南建议使用不含固定剂的溶血素(如NH4Cl溶液)裂解红细胞[10, 11],国内指南可能考虑到临床实际情况,仅在进行细胞活力检测时要求使用不含固定剂的溶血素[4]。本次调查实验室使用该不含固定剂的溶血素的比例仅为28.9%,远低于日本调查中的93.9%,质评物分组统计结果显示,不含固定剂组检测结果的离散度要小于含固定剂组。建议实验室使用不含固定剂的溶血素处理样品,并置于4 ℃条件下、1 h内上机检测,以避免固定剂影响检测结果的准确性[7]。(5)绝对计数结果的报告:有53.6%的实验室在常规检测中未报告绝对计数结果,而临床医生需要根据绝对计数结果计算移植物中CD34+细胞总数[30],因此建议实验室开展绝对计数检测以满足临床需求。对于绝对计数方法的选择,国内外指南均建议首选单平台方法[4,10, 11],与双平台方法相比,单平台可减小实验室间变异[4,8,17],更利于实现检测方法的标准化。本次质评物绝对计数检测结果中,单平台组具有更小的实验室间差异。目前基于荧光计数微球的单平台方法需要使用绝对计数管或额外购买荧光计数微球,成本较高,部分临床实验室仍在使用双平台方法(本次调查数据为31.1%,CAP数据为23.2%)。
质评物检测结果显示,BD组与BC组相比,其相对计数和绝对计数检测结果的离散度均更小,这与CAP质评数据较为一致。造成本次调查中BC组离散度较大的主要原因是组内有5家干细胞工程公司在检测时获取CD34+细胞数过少,导致检测结果明显偏低。此外,本次回报绝对计数的实验室中有32.8%在临床常规检测中并不报告绝对计数结果,检测人员可能缺乏绝对计数经验,导致质评物绝对计数检测结果出现较大差异。建议各实验室加强CD34+细胞绝对计数质量控制相关培训,制定符合指南要求的标准操作程序,以提高CD34+细胞计数的检测能力。
本次调查结果表明,在单双平台选择、溶血素类型和样品处理方式等方面遵循指南要求的实验室间检测结果的差异相对较小,未遵循指南相关要求的实验室间差异均较大。为此,本研究参考各指南文件并结合本次调查结果给出CD34+细胞计数的具体改进意见或建议,以供临床实验室参考:(1)检测当天使用商品化微球监测流式细胞仪性能;(2)检测当天使用CD34+细胞质控品进行室内质控;(3)对自行组合的抗体进行滴定实验,以确定最佳的抗体用量;(4)使用免洗抗体标记细胞,以减少有核细胞丢失;(5)使用不含固定剂的溶血素裂解红细胞,并置于4 ℃条件下、1 h内上机检测,若使用含有固定剂的溶血素建议对制备后样品的稳定性进行评估;(6)获取至少100个CD34+细胞,对于CD34+细胞浓度极低的标本,在可用检测样本量有限的情况下,至少获取75 000个CD45+细胞以达到所需的精密度要求;(7)采用规范的ISHAGE设门方案进行数据采集与分析;(8)同时报告CD34+细胞相对计数和绝对计数结果;(9)在采用单平台方法计数时,使用反向移液方式进行移液,并定期(≤1年)校准移液器;(10)在采用双平台方法计数时,检测当天对血液分析仪开展室内质控,标本采集后6 h内获取白细胞计数结果,并定期(≤6个月)校准血液分析仪;(11)根据标本所用抗凝剂和放置条件,对标本采集后的稳定性进行评估;(12)参加室间质量评价。
所有作者均声明不存在利益冲突



























