
采用基于体素形态学和基于球谐函数点分布模型技术,比较分析内侧颞叶癫痫(mTLE)海马体积和表面局部形态的改变特征。
回顾性收集2009年7月至2019年2月东部战区总医院66例mTLE患者[男31例,女35例,年龄17~48(28±8)岁],以及80名年龄性别匹配的健康对照者[男38名,女42名,年龄19~46(27±7)岁],采集全脑结构磁共振高分辨率T1加权成像(3DT1)数据。分别采用基于体素的形态学分析方法测量海马体积,基于球谐函数形状技术测量海马表面形态改变,比较分析mTLE患者相对于健康对照海马萎缩模式;使用Pearson相关分析观察mTLE海马形态学变化与病程的关系。
与健康对照组相比,mTLE组病侧海马体积明显减小(Z值:-1.55±0.57比0.38±0.58,P<0.001),并与病程呈负相关(r=-0.297,P=0.016)。表面形态学分析精细地显示,mTLE患者病侧海马萎缩主要发生在海马的头部、中部外侧和后尾部,其位移值与病程呈明显负相关(r =-0.336,P=0.006),并与海马灰质体积呈正相关(r=0.336,P=0.006)。
基于体素形态学分析展示海马体积整体减小,而基于表面形状的形态学测量可描绘海马萎缩的局部形态学变化。

内侧颞叶癫痫(mTLE)是最常见的耐药性癫痫类型,以海马硬化(HS)为最主要的病理学基础[1]。其在磁共振成像(MRI)上主要表现为海马形态的萎缩和信号的异常[2]。基于MRI的定量形态学测量是目前诊断海马硬化的主要方式;除了手动描记法外,计算机辅助的海马形态学测量技术,如基于体素的形态学分析(VBM)越来越多地用于海马体积测量及临床研究中[3]。除此之外,脑结构表面形态学测量是近年来发展的新指标。相比单纯体积测量,其可以更精细地在某脑结构层面反映表面形态、位置等结构指标变化[4]。本研究使用一种新的方法——基于球谐函数点分布模型(SPHARM-PDM)[5]表面形态学测量技术,与传统VBM技术相比较,全面观察mTLE海马形态学改变特征[6],并分析其与疾病临床指标间的关系。
本研究为病例对照研究,回顾性收集2009年7月至2019年2月在东部战区总医院诊断为伴单侧海马硬化的mTLE资料。入组标准:(1)诊断参照2014年国际抗癫痫联盟(ILAE)诊断标准[7],由2名高年资神经内科医师根据患者临床症状和神经电生理结果共同诊断;(2)常规MRI表现为单侧海马硬化,并且无其他明显结构性异常;(3)无其他明显神经精神疾病;(4)能够配合完成全程头颅MRI检查;(5)右利手。共纳入66例mTLE患者,男31例,女35例,年龄17~48(28±8)岁;左右侧各33例;病程2~520(146±115)个月。纳入同期在本院进行体检的健康对照者。入组标准:(1)年龄≥17岁;(2)无严重神经系统疾病或其他严重疾病史;(3)无精神疾病史及家族史;(4)能够配合完成全程头颅MRI检查;(5)右利手。共纳入80名健康对照者,男38名,女42名,年龄19~46(27±7)岁。本研究经东部战区总医院道德伦理委员会审核批准(2018NZKY-020-02),知情同意豁免。
脑影像数据采集通过SIEMENS Trio 3T高场超导磁共振扫描仪(德国西门子公司),配以8通道头颅线圈。受试者仰卧于MRI检查床,闭目平卧,头部固定,同时使用耳塞减小扫描噪声。高分辨脑结构T1加权像(T1WI)使用三维磁化准备快速梯度回波(MPRAGE)序列进行,扫描参数如下:重复时间(TR)2 300 ms、回波时间(TE)2.98 ms、反转时间(TI)400 ms,翻转角(FA)9°,视野(FOV)256 mm × 256 mm,矩阵256 × 256,激励次数(NEX)1次,层厚 1 mm,层间距0,扫描时间590 s,矢状位扫描,共176层,扫描范围覆盖全脑。此外,还采集二维(2D)-T1WI、2D-T2加权像(T2WI)、弥散加权成像(DWI)和T2-液体衰减反转恢复(FLAIR)序列,用于临床诊断。
在数据质控后,为了增加样本量以提高统计力度,首先将右侧海马硬化的mTLE患者图像进行左右翻转,使得所有患者的病灶均位于左侧。VBM分析采用cat12软件(http://dbm.neuro.uni-jena.de/cat/),将配准到标准蒙特利尔神经病研究所(Montreal neurological institute,MNI)空间的脑图像分割成灰质、白质和脑脊液,获得全脑灰质体积(GMV)脑图,以8 mm×8 mm×8 mm半高全宽(FWHM)的高斯核进行平滑处理。
表面形态分析使用fMRIPrep(https://fmriprep.org/en/stable/)工具包,图像预处理包括图像降噪、颅骨剥离、皮层重建及图像配准等,平滑(采用半高全宽的8 mm的三维高斯核)处理后供下一步使用。海马分割由FSL-FIRST(v5.0.9;https://fsl.fmrib.ox.ac.uk/fsl/fslwiki/FIRST/)进行,自动测定海马体积,并线性配准到MNI152空间。从二进制海马分割中提取三维表面网格,并用SPHARM-PDM进行参数化[4,8]。为了保证海马分割的球形拓扑,对不均匀的边界进行最小程度地平滑[9]。基于参数化的曲面网格,得到一个点分布模型,允许受试者之间的形状固有点对应[10, 11]。并从80名健康对照者中生成了一个约有4 046个顶点的海马模板,所有海马体表面都与之对齐。使用点对网格方法计算平均模板表面和个体海马表面网格上每个点之间的最短垂直距离来生成位移值。向内位移(负位移值)对应于萎缩,向外位移(正位移值)对应于扩张。
1.一般资料:采用SPSS 25.0软件进行临床数据统计分析。年龄为计量资料,符合正态分布,以表示,组间比较采用两样本t检验;性别为定性资料,以频数描述,组间比较采用χ²检验。
2.组间比较:基于体素的统计学分析采用spm8软件(http//www.fil.ion.ucl.ac.uk/spm)进行,应用错误发现率(FDR)的多重检验校正后以P<0.05认为差异具有统计学意义,获得统计脑图。基于球谐函数表面形态分析用Surfstat软件(http://www.math.mcgill.ca/keith/surfstat/),计算海马体积及顶点位移向量两个参数。为了使数据更加正态分布和标准化,海马参数(即海马体积、病侧海马表面形状位移)用换算出来的Z值表示[Z=(x-μ)/σ,其中x为某一具体分数,μ为平均数,σ为标准差;相除之后无单位,所以Z值化后无单位],采用SPSS 25.0软件进行组间比较。最后,对表面形状位移差异图的统计结果进行全族误差率(FWE)的多重比较校正。
3.相关分析:采用相关分析研究形态学指标与病程临床变量之间的关系。选取两组间差异有统计学意义的区域作为感兴趣区,提取感兴趣区内形态学指标平均值,采用Pearson相关,分别计算海马体积、位移值与病程的相关关系;再计算病侧海马表面形状位移值和海马灰质体积的相关性。双侧检验,检验水准α=0.05。
66例mTLE患者,男31例,女35例,年龄17~48(28±8)岁。80名健康对照者,男38名,女42名,年龄19~46(27±7)岁。两组性别比、年龄差异均无统计学意义(均P>0.05)。
mTLE组Z值化后的病侧海马体积较健康对照组明显减小[(-1.55±0.57)比(0.38±0.58),t=20.16,P<0.001]。mTLE组病侧海马表面形状位移较健康对照组也明显减小[(-0.68±0.31)比(0.17±0.25),t=18.23,P<0.001](图1)。VBM分析显示GMV减小的区域主要在病侧海马及丘脑。基于球谐函数表面形态学分析显示病侧海马萎缩,在海马头部、中部外侧和后尾部萎缩最为严重;而对侧海马未见明显萎缩或扩张(图2)。
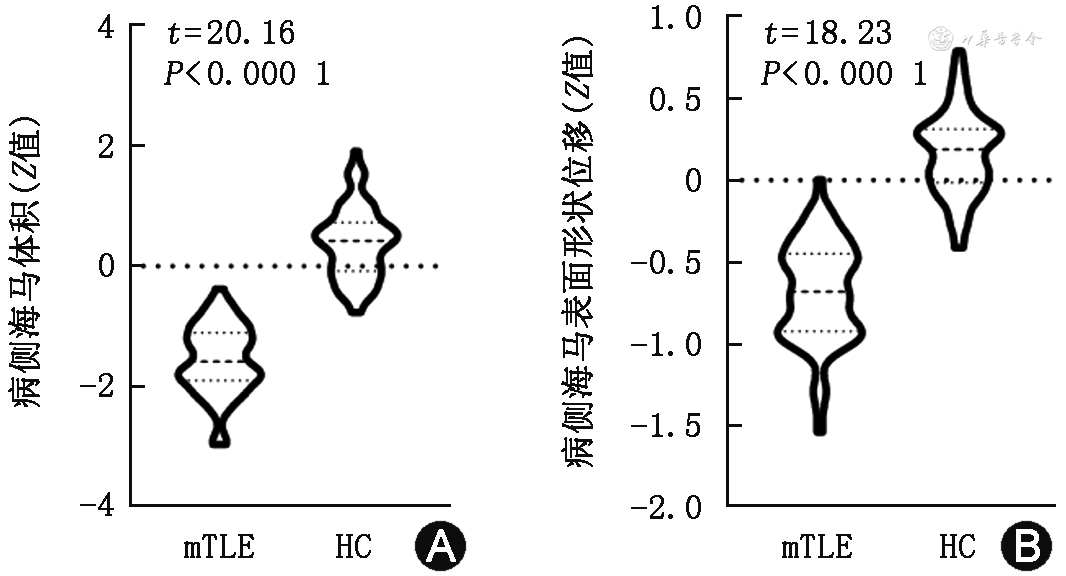

注:mTLE为内侧颞叶癫痫;HC为健康对照;纵坐标病侧海马体积和病侧海马表面形状位移均为Z值后,也就是标准化后的数值,故无单位
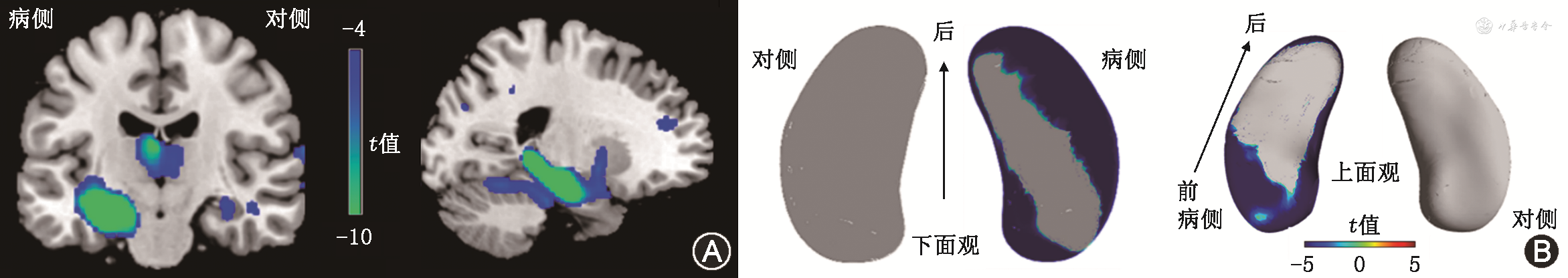

注:mTLE为内侧颞叶癫痫;HC为健康对照;VBM为基于体素的形态学分析;FDR为错误发现率;FWE为全族误差率
在mTLE患者中,病侧海马体积及表面形状位移均与病程呈负相关(r值分别为-0.297、-0.336,均P<0.05)。此外,病侧海马表面形状位移值改变与海马体积值的改变明显呈正相关(r=0.679,P<0.001),与VBM分析提取的海马GMV也呈正相关(r=0.336,P=0.006)(图3)。
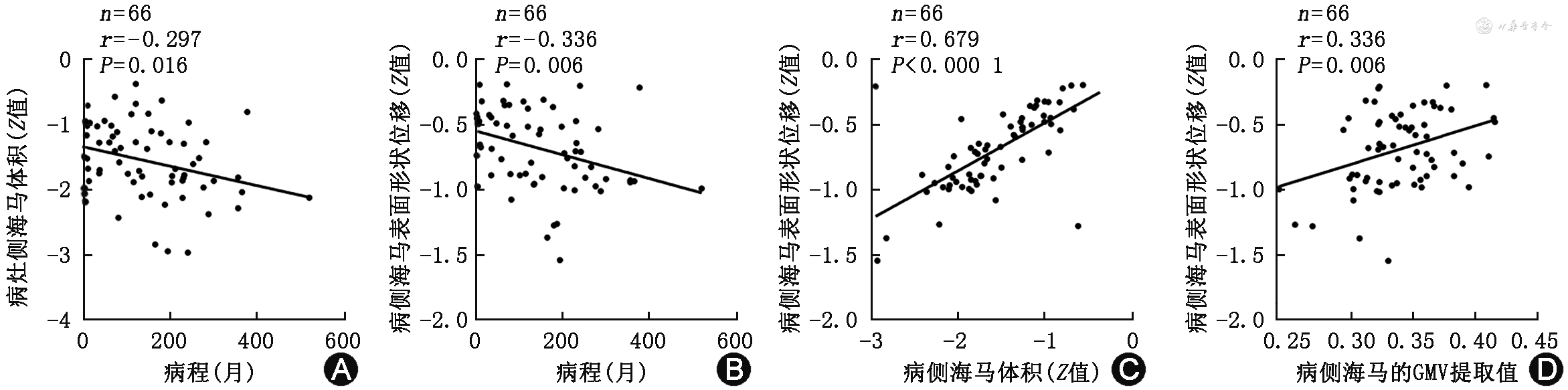

注:mTLE为内侧颞叶癫痫;GMV为灰质体积
mTLE的核心病理类型是海马硬化,而海马萎缩是海马硬化的主要特征。对于萎缩的评判大多依靠医生的主观评价以及对海马整体体积的测量。既往研究,多选择海马作为感兴趣区域,计算感兴趣区内的体素数量来估算海马总体积,mTLE患者病侧海马体积明显减小[12]。但有研究表明,对于部分颞叶癫痫患者,其视觉和定量分析均显示无海马萎缩,但其病理确诊是海马硬化[13]。虽然在常规MRI上可以直观地检测到海马硬化,但其识别的准确性在很大程度上取决于分析人员的技能以及是否获得了适当的MRI序列[14]。因此,形态分析显示海马特定的区域形态变化,有助于确定颞叶癫痫患者的结构异常[15]。
本研究发现除病侧海马体积明显减小外,基于球谐函数表面形态分析这一新指标可以观察到海马萎缩区域具体表现在头部、中部外侧和后尾部。Hogan等[16]发现在10例分别患有左颞叶癫痫和右颞叶癫痫的患者中,海马的萎缩在中外侧头部和后尾部。随后也有研究证实,mTLE表现出一致的海马萎缩,特别是在海马头部内侧、外侧以及尾部和CA1-3区[15,17],与本研究结果一致。此外,海马表面形态分析也发现海马形态及其对认知功能的影响,言语回忆延迟与左侧海马上外侧头萎缩有关,视觉回忆延迟与右侧海马下内侧表面萎缩有关,这是全局体积测量无法观察到的[18]。
此外,本研究发现随着病程延长,病侧海马萎缩更为严重。一项研究发现,在mTLE患者中,无癫痫发作的患者海马体积无明显变化,而持续癫痫发作的患者同侧海马体积下降,这与癫痫持续时间相关,所以,海马硬化患者有进行性的海马萎缩[19]。这一结果与本研究一致,即海马体积及海马萎缩程度与癫痫病程呈显著负相关,应予以积极治疗。将海马表面形状位移与不同方法提取的海马体积值相关,结果表明,均呈显著正相关。所以,表面形态分析可以反映体积及形态的改变。综上,利用自动化MRI分析,可以观察mTLE海马次级区域的萎缩模式及其与临床病程的关系。
然而,本研究存在一些不足之处:由于未考虑偏侧化,本研究的发现揭示了左侧和右侧mTLE常见的病理生理学变化,而不是左侧或右侧mTLE患者特有的机制。此外,mTLE患者抗癫痫药物等因素未列入本研究,由此造成的混淆未能排除。最后,本研究只采集了部分患者的认知及行为学数据,在之后的研究中,将完善mTLE患者临床量表及信息,来进一步分析海马表面形态学改变与认知损害的关系,从而为临床诊疗提供更加可靠的影像学依据。
本文使用一种新的方法——基于球谐函数表面形态学对mTLE患者海马进行局部形态分析,发现海马特异的局部结构损伤:主要位于海马头部、中部外侧和后尾部,补充和提高了基于VBM的形态学分析指标,具有比较健康结构和病理结构局部形态变化的优势。
所有作者均声明不存在利益冲突



























