
本研究总结分析了54例IgG4相关性自身免疫性胰腺炎(IgG4-AIP)患者的超声造影表现,男40例,女14例,年龄26~76(59.1±10.2)岁。结果发现IgG4-AIP的超声造影增强模式呈多样化,有部分AIP患者尤其是肿块型AIP患者在疾病初期的超声造影表现与胰腺癌的超声造影表现有类似,在增强早期、增强晚期和延迟期均会有不同程度的低增强表现,因此仅靠超声造影表现对其进行鉴别诊断是不可取的,应综合评估。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
自身免疫性胰腺炎(AIP)是一种比较少见的胰腺慢性增生性炎性疾病,以胰腺纤维化、淋巴细胞浆细胞浸润为特征,临床上主要表现为梗阻性黄疸、腹部不适等症状。AIP可分为2个亚型:Ⅰ型AIP(淋巴浆细胞硬化性胰腺炎)与Ⅱ型AIP(原发性导管中心性胰腺炎)。Ⅰ型AIP又称为IgG4相关性AIP(IgG4-AIP),以IgG4(+)浆细胞浸润伴导管周围纤维化为病理特点,实际上是lgG4相关性疾病在胰腺的局部表现[1];Ⅱ型AIP在病理上没有IgG4(+)淋巴细胞浸润,以中性粒细胞性上皮损伤为特点。在亚洲AIP患者中以Ⅰ型多发,约占总病例数的96%[2]。由于部分医师对IgG4-AIP缺乏了解重视,且其临床症状及影像学的表现缺乏特异性,与胰腺癌难以鉴别,因此在临床上经常被误诊和漏诊。本研究通过对54例IgG4-AIP患者接受系统性治疗前后的超声声像图特征及超声造影表现特点进行回顾性总结分析,旨在提高对此类疾病的认识,为该疾病的诊断以及治疗评估提供超声影像学方面的参考。
1. 研究对象:本研究为病例系列分析。回顾性收集2017年9月至2019年8月至解放军总医院第一医学中心就诊的54例IgG4-AIP患者的完整病历资料,其中男40例,女14例,年龄26~76(59.1±10.2)岁。入选患者均符合国际胰腺病协会于2010年制定的《AIP诊断标准国际共识》[3],且依从性良好,均在本院进行多次治疗至随访终点。期间收集患者治疗前首次就诊及治疗后最后一次就诊时的胰腺常规超声声像图及超声造影声像图特征。本研究符合《赫尔辛基宣言》对伦理的要求。
2. 影像检查方法:所用的超声仪器为Resona 7超声仪(深圳迈瑞生物医疗电子股份有限公司),使用C5-1探头;超声造影剂为SonoVue(意大利Bracco公司)。对每例患者在治疗前和治疗后均行常规超声和超声造影两种检查。进行常规超声检查时先行常规二维灰阶超声检查,对患者的胰腺回声、病灶的部位、数目、大小、形态特征、主胰管走行、管径及胆总管是否受累进行评估,再行彩色多普勒血流成像(CDFI)检查对患者胰腺及病灶的血供情况进行观察;而后切换至超声造影模式,在低机械指数下(MI:0.05~0.20)行超声造影检查,每次使用造影剂前加入5 ml生理盐水,充分震荡混匀后按照0.03 ml/kg经肘正中静脉团注Sonovue混悬液,再用5 ml生理盐水冲管。实时连续观察并存储记录造影剂注入后3 min内胰腺病灶的增强-消退过程。入组的患者图像资料均由两名有经验的超声医师进行判断(均具有5年以上超声造影经验),对有不同意见者,经讨论得出最后结论。
3. 超声造影评估方法:根据2017版EFSUMB超声造影指南[4],可将胰腺超声造影时相分为增强早期(即动脉期,10~30 s)、增强晚期(即静脉期,30~120 s)和延迟期(>120 s)。对于胰腺局灶性受累者,病灶的增强水平以胰腺组织的增强水平作为参照;对于胰腺弥漫性受累者,以邻近胰腺的正常组织的增强水平作为参照。增强的强度可依次划分为无增强<低增强<稍低增强<等增强<稍高增强<高增强;根据病灶内造影剂的分布特征,可将内部增强水平均质一致的定义为均匀增强,而内部增强水平不一致的定义为不均匀增强。
4. 统计学分析:使用SPSS 19.0统计软件进行统计学处理。患者一般资料采用、率、百分比表示。
1. 治疗前首次就诊时胰腺常规超声表现:在54例IgG4-AIP患者中,治疗前常规超声表现为胰腺弥漫性受累者共17例(31.5%),表现为局灶性受累者共37例(68.5%);其中(1)17例胰腺弥漫性改变者:形态上表现为胰腺形态饱满,胰头平均厚约(31.8±8.5)mm,胰体平均厚约(23.5±5.6)mm,胰尾平均厚约(25.2±4.8)mm;实质回声弥漫性增粗、减低、欠均匀;有2例可见主胰管轻度扩张,内径分别为3.2 mm和4.5 mm;(2)37例胰腺局灶性受累者:形态上表现为与周围胰腺组织相比呈低回声或稍低回声的局部病变,边界尚清;其中14例病灶位于胰腺头部,2例位于胰腺颈部,13例位于胰腺体部,8例位于胰腺尾部,病灶最大径范围为15.2~50.1 mm;血流显示方面有2例病灶CDFI示其内可见少许血流信号,其余35例病灶CDFI示其内未见血流信号;14例位于胰头部的病灶中,有6例可见主胰管不规则扩张,5例可见胆总管扩张(其中有3例同时合并肝内胆管扩张),扩张的胰管内径平均值为(3.9±0.7)mm,扩张的胆总管内径平均值为(13.2±2.5)mm。
2. 治疗后末次就诊时胰腺常规超声表现:(1)17例胰腺弥漫性受累者中,有12例胰腺大小形态基本恢复如常[胰头平均厚约(26.3±4.3)mm,胰体平均厚约(18.4±3.6)mm,胰尾平均厚约(17.6±4.1)mm],5例胰腺腺体变薄,体积稍小[胰头平均厚约(22.5±3.8)mm,胰体平均厚约(13.5±1.9)mm,胰尾平均厚约(12.8±2.2)mm],主胰管均未见扩张(2例治疗前主胰管轻度扩张者在治疗后宽度恢复正常);(2)37例胰腺局灶性受累者中,有24例在治疗后仍表现为低回声或稍低回声的局部病变(最大径范围为13.7~35.2 mm),其余13例病变局部回声与周围胰腺组织相比已无明显差别;6例治疗前主胰管扩张者在治疗后检查时,有5例胰管宽度已恢复正常,1例仍有轻度扩张,内径为3.1 mm;5例治疗前胆总管扩张者,治疗后胆总管和肝内胆管宽度均恢复正常。在治疗后,胰腺弥漫性和局灶性受累者的常规超声图像表现均有不同程度的变化。
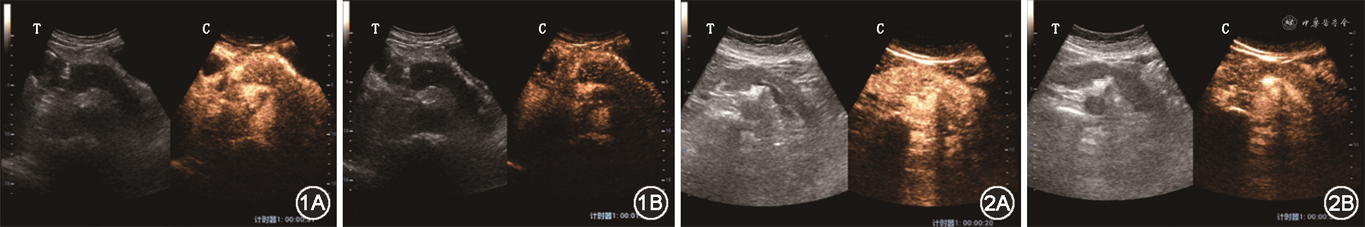
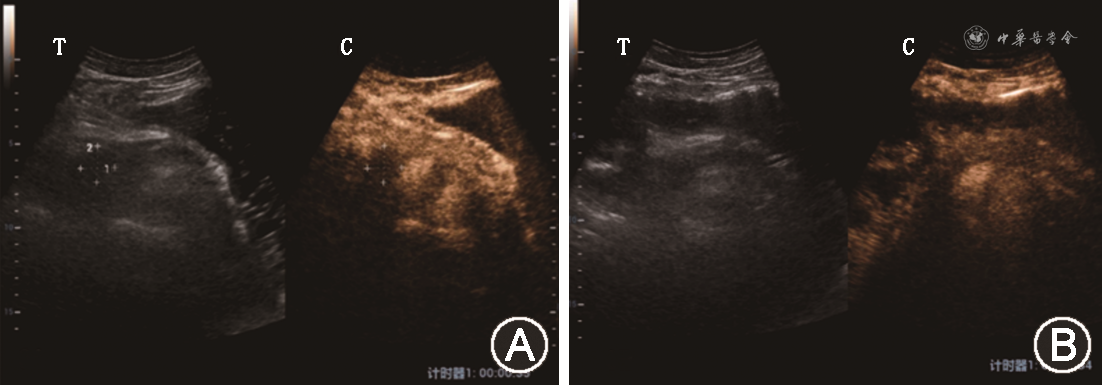
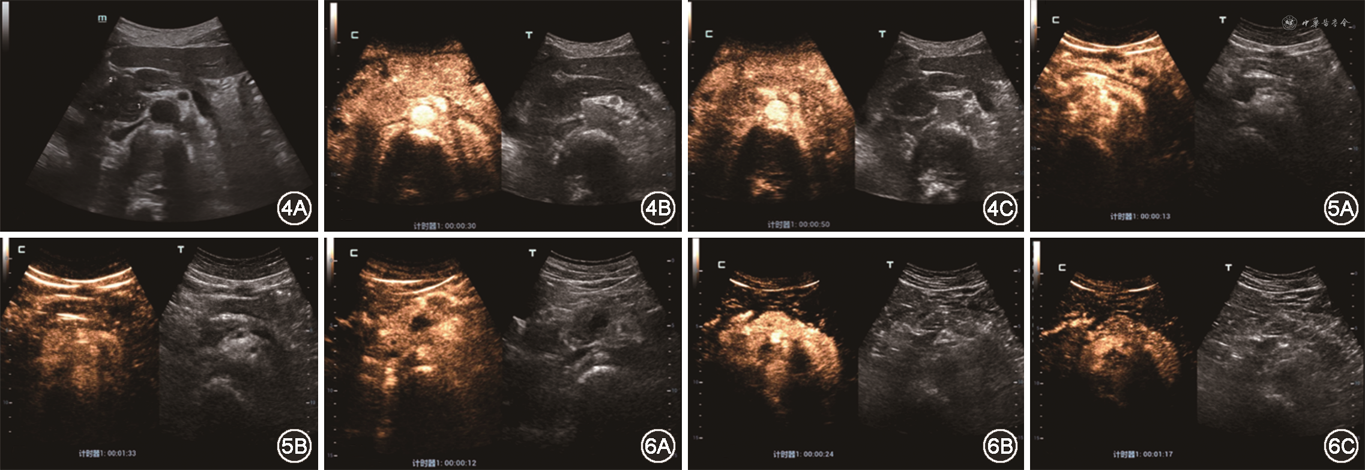
3. 治疗前首次就诊时胰腺超声造影表现:(1)17例胰腺弥漫性受累者中,有9例胰腺整体在增强早期、增强晚期、延迟期依次表现为稍低增强-低增强-低增强(图1),有5例在增强早期、增强晚期、延迟期依次表现为等增强-低增强-低增强(图2),有3例在增强早期、增强晚期、延迟期依次表现为稍高增强-低增强-低增强;(2)37例胰腺局灶性受累者中,有25例病灶在增强早期、增强晚期、延迟期均表现为低增强-低增强-低增强(图3),7例在增强早期、增强晚期、延迟期均表现为等增强-等增强-等增强(图4),2例在增强早期、增强晚期、延迟期依次表现为稍高增强-低增强-低增强,3例在增强早期、增强晚期、延迟期依次表现为稍高增强-等增强-等增强。



4. 治疗后末次就诊时胰腺超声造影表现:在治疗后,54例患者中有31例患者的胰腺超声造影表现发生了改变,其中有29例患者在增强早期-增强晚期-延迟期3期中,至少有1期出现了造影强度的增高;有2例患者出现了造影强度的减低。该结果提示在治疗结束后,病灶处的微循环灌注也有所恢复。
17例胰腺弥漫性受累者中:(1)共有8例患者治疗后在增强早期-增强晚期-延迟期3期中至少有1期出现了造影强度的增高:其中有5例患者胰腺整体的增强模式由治疗前的稍低增强-低增强-低增强变为治疗后的高增强-稍低增强-稍低增强(图5),2例由治疗前的稍低增强-低增强-低增强变为治疗后的等增强-低增强-低增强,1例由治疗前的等增强-低增强-低增强变为治疗后的等增强-等增强-等增强;(2)共有2例患者在治疗后出现了造影强度的减低:由治疗前的稍低增强-低增强-低增强变为治疗后的低增强-低增强-低增强;(3)共有7例患者在治疗前后造影强度没有发生变化,其中有4例在治疗前后均表现为等增强-低增强-低增强,3例在治疗前后均表现为稍高增强-低增强-低增强。
37例胰腺局灶性受累者中:(1)共有21例患者治疗后在增强早期-增强晚期-延迟期3期中至少有1期出现了造影强度的增高,其中有15例患者由治疗前的低增强-低增强-低增强变为治疗后的等增强-等增强-等增强(图6),4例由治疗前的低增强-低增强-低增强变为治疗后的高增强-低增强-低增强,1例由治疗前的稍高增强-低增强-低增强变为治疗后的稍高增强-稍低增强-稍低增强,1例由治疗前的稍高增强-低增强-低增强变为治疗后的稍高增强-等增强-等增强;(2)共有16例患者治疗前后在造影强度上没有发生变化,其中有6例在治疗前后均表现为低增强-低增强-低增强,7例在治疗前后均表现为等增强-等增强-等增强,3例在治疗前后均表现为稍高增强-等增强-等增强。
由于IgG4-AIP与胰腺癌的临床治疗手段截然不同,因此在术前对二者进行鉴别诊断具有重要的临床意义。目前有多种影像学方法可以对AIP进行诊断评估,包括CT、MRI、超声及超声内镜等,但两者的鉴别尤其是肿块型AIP与胰腺癌的鉴别仍比较困难。并且由于CT检查具有一定辐射性,而MRI检查操作比较复杂,因此并不适用于AIP激素治疗后的疗效随访评估,因此超声检查仍是诊断AIP的重要影像学检查方法。
随着超声造影检查的应用范围越来越广泛,该技术也开始被用于IgG4-AIP的鉴别诊断,但到目前为止,关于AIP的超声声像图特征及超声造影方面的研究仍较少,且结论不一。多数研究都认为IgG4-AIP在超声声像图上主要表现为弥漫型和肿块型两种类型,弥漫型多表现为胰腺整体受累,胰腺弥漫性肿大,部分可呈“腊肠样”改变,被膜欠光滑,回声不均匀减低,胰管扩张较少见;而肿块型多表现为胰腺局灶性受累,常累及胰头和胰尾,胰腺局部肿大,病灶局部回声多减低、欠均匀,边界欠清。本研究的54例IgG4-AIP患者首次就诊时,常规超声结果与该结论基本一致。笔者发现与胰腺癌相比,IgG4-AIP较少造成主胰管扩张,可能是由于在该病变中,胰管周围更容易形成间质纤维化及淋巴细胞浸润,从而造成胰管较长狭窄[5]。这54例患者均在本院进行多次治疗至随访终点,末次就诊时,常规超声表现与首次就诊时有所改变,且扩张的胰管和胆管已基本恢复正常。以往有研究认为在超声图像上,肿块型IgG4-AIP病灶区的血流信号较周围正常胰腺组织增多,而胰腺癌为乏血供病变,因此可对两者的鉴别提供一定帮助[6]。但本研究中,在患者治疗前和治疗后行超声检查时,CDFI示病灶内均未见血流信号明显增多,部分病灶内仅可见少许血流信号,因此在此基础上进行了超声造影检查。
目前已有的研究对IgG4-AIP的超声造影表现结论不一。以往大部分研究都认为IgG4-AIP在增强早期表现为等增强或高增强,增强晚期不会有明显消退,因此在延迟期仍表现为等增强或高增强[7, 8];而胰腺癌的超声造影表现则与此不同,由于胰腺癌属于乏血供肿瘤,在增强早期、增强晚期和延迟期均表现为低增强,因此造影表现的不同可作为对两者,尤其是胰腺癌与肿块型AIP进行鉴别诊断的诊断依据[9, 10]。但有学者对此提出了不同的观点,Wang等[11]在研究中发现,很大一部分肿块型AIP病灶在增强早期、增强晚期和延迟期都表现为等增强混合低增强,而不仅仅表现为与周围胰腺组织一致的等增强。而在杨宇等[6]的研究中,局限性AIP患者在行超声造影检查时,造影剂进入时间较周边正常组织晚,呈低增强,且病灶内未见充盈缺损。这些发现提示,IgG4-AIP的造影模式表现多样,其原因可能和疾病进程相关。本研究的54例IgG4-AIP患者首次就诊时的17例弥漫性受累者中,有9例在增强早期-增强晚期-延迟期依次呈稍低增强-低增强-低增强;而37例局灶性受累者中,有25例在增强早期-增强晚期-延迟期依次呈低增强-低增强-低增强。这可能是由于在病程初期,胰腺组织内大量炎症细胞浸润,胰腺内的静脉因炎性细胞浸润发生闭塞,呈闭塞性脉管炎改变,小动脉周围可伴有纤维化,并且由于内膜肥厚,小动脉内腔会有不同程度的狭窄,因此病变区域在超声造影图像上会呈低增强改变。而在临床治疗过程中,这一病理改变可能会有一定改善。在治疗结束后的末次超声检查时,有29例患者在增强早期-增强晚期-延迟期3期中,至少有1期出现了造影强度的增高。提示在治疗结束后,随着临床症状完全消失,原异常血清学指标降至正常水平,病灶处的血流灌注也有所恢复。这种改变也可间接证明,随着IgG4-AIP患者的病情好转,胰腺内的微循环灌注状态也得到了一定的改善和恢复。
综上所述,常规二维超声结合超声造影是一种方便快捷、安全无创且价格相对低廉的检查手段,其不仅对IgG4-AIP有一定的鉴别诊断价值,并且在该病的治疗过程中,还可对其治疗效果进行评估。但本研究发现,IgG4-AIP的超声造影增强模式呈多样化,这可能与其炎症本身和纤维化的进展相关。传统上认为的AIP在超声造影增强早期表现为高增强或等增强,在增强晚期和延迟期不会出现明显消退,仍表现为高增强和等增强的观点并不能一概而论。有一部分AIP患者尤其是肿块型AIP患者在疾病初期的超声造影表现与胰腺癌的超声造影表现有类似,在增强早期、增强晚期和延迟期均会有不同程度的低增强表现,因此仅靠超声造影表现对其进行鉴别诊断是不可取的,还应结合其临床检查结果、实验室检查结果或者是组织病理学检查结果进行综合评估。下一步拟扩大样本量进一步研究,为可疑胰腺占位和胰腺弥漫性病变患者的超声排查和鉴别诊断工作提供更多的诊疗依据。
所有作者均声明不存在利益冲突



























