
评估维得利珠单抗对炎症性肠病患者的短期疗效及安全性。
连续纳入北京协和医院2021年5月1日至10月31日开始使用维得利珠单抗的中重度活动期炎症性肠病患者,观察临床特征并进行疗效和安全性评估,计算临床应答率、生物学应答率及内镜应答率,多因素分析用于评估短期临床疗效和安全性的独立影响因素。
共纳入炎症性肠病患者78例,男44例,女34例,年龄(40.5±11.9)岁。维得利珠单抗治疗14周时临床缓解率、临床应答率、生物学缓解率、生物学应答率及内镜缓解率分别为60.3%(47/78)、85.9%(67/78)、70.5%(55/78)、43.6%(34/78)和47.0%(31/66)。体质指数(BMI)≥18.5 kg/m2(HR=5.04,95%CI:1.50~16.91,P=0.009)和治疗6周时达生物学缓解(HR=15.22,95%CI:3.16~73.38,P=0.001)是治疗14周时内镜缓解的影响因素。57例患者出现不良反应,发生率为73.1%,主要表现为肝肾损害(37.2%)和感染(26.9%)。
维得利珠单抗治疗中重度活动期炎症性肠病14周后超半数患者可达临床缓解,基线BMI水平和治疗6周时生物学缓解是14周黏膜愈合的影响因素。短期治疗不良反应发生率不低,但严重不良反应罕见。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
炎症性肠病(inflammatory bowel disease,IBD)是一种肠道慢性复发性炎症性进展性疾病[1],随着病程的延长和病变范围的扩大癌变风险增加。IBD的治疗模式已从症状控制演变为早期干预、达标治疗和严格控制的新趋势[2],早期干预的“降阶梯”方法可能显著改变疾病的进展[3]。IBD最新治疗目标已从选择IBD的治疗目标(selecting therapeutic targets in inflammatory bowel disease,STRIDE)的临床缓解+内镜缓解[4]向STRIDE Ⅱ的临床应答+临床缓解+生物学指标+内镜缓解[5]演变。早期达到IBD临床缓解和内镜缓解可以获得更好的长期结局[6]。
生物制剂的应用使实现上述目标成为可能的同时,其疗效与安全性问题受到关注。维得利珠单抗是一种完全人源化的肠道选择性生物制剂,可特异性地拮抗α4β7整合素,阻止T淋巴细胞迁徙到肠道炎症区域[7, 8]。目前维得利珠单抗被推荐用于对皮质类固醇、免疫抑制剂或肿瘤坏死因子(TNF)阻滞剂无反应的活动性IBD患者[9, 10, 11],其疗效已在GEMINI试验[12, 13, 14]及不少欧美地区的研究[15, 16, 17, 18, 19, 20]中得到证明。根据维得利珠单抗的作用机制,相较于其他全身作用生物制剂和免疫抑制剂其理论安全性更高。而GEMINI的长期安全性(long-term safty,LTS)研究结果[21]及其他安全性评估研究[22]进一步证实了维得利珠单抗的安全性。自2020年12月维得利珠单抗正式纳入中国医保目录,患者使用人数明显增多。尽管如此,我国关于其有效性的影响因素及其不良反应的临床真实数据仍然有限。本研究旨在利用单中心IBD随访数据探索维得利珠单抗治疗IBD的短期疗效及药物安全性。
连续纳入北京协和医院2021年5月1日至10月31日开始使用维得利珠单抗的IBD患者,通过医院门诊系统以及医院信息系统(hospital information system,HIS)查阅病历资料并进行随访。纳入标准:(1)通过临床表现、内镜改变和影像学检查等综合评估确诊IBD[23, 24];(2)首次使用维得利珠单抗时处于中度或重度活动[溃疡性结肠炎(Ulcerative colitis,UC)患者为完整Mayo评分≥6分,克罗恩病(Crohn′s disease,CD)患者为Harvey-Bradshow指数(Harvey-Bradshow index,HBI)≥8];(3)在研究期间进行维得利珠单抗4程以上治疗,并在4程治疗后至少进行1次随访。排除标准:首次使用维得利珠单抗前合并白细胞减低或确诊恶性肿瘤。本研究已通过北京协和医院伦理委员会批准(伦理号:S-K2041)。
1. 治疗方法:本研究使用维得利珠单抗(安吉优,日本Takeda公司,进口药品注册证号:S20200006)。用药方法:患者在0、2、6、14周进行治疗(即4程治疗),每次300 mg维得利珠单抗,输注前用无菌注射用水复溶,并在给药前使用250 ml无菌0.9%氯化钠溶液或250 ml无菌乳酸林格氏液稀释,通过静脉滴注给药并持续30 min以上。输注完成后,用30 ml无菌0.9%氯化钠溶液或30 ml无菌乳酸林格氏液冲洗管腔。
2. 临床资料收集:记录进行维得利珠单抗治疗前的基线资料,包括人口学资料[性别、年龄、吸烟史、体质指数(body mass index,BMI)]、临床特征(起病时间、蒙特利尔分型、既往史、家族史)、药物使用史(糖皮质激素、免疫抑制剂和生物制剂)和治疗前血清学检查和内镜检查结果。治疗2、6和14周的临床表现(便次、便血、腹痛、肠外表现)、实验室检查[血常规包括白细胞、中性粒细胞和血红蛋白、血清白蛋白,炎症指标包括超敏C反应蛋白(high sensitivity C-reactive protein,hsCRP)、红细胞沉降率、白细胞介素6和TNF-α,维生素D]和14周后的内镜检查结果。记录治疗期间的所有药物不良反应。
UC患者的临床分型采用蒙特利尔分型[25],临床活动度采用改良的Mayo评分,内镜活动度采用Mayo内镜下评分评估[10]。CD患者临床分型采用蒙特利尔分型,临床活动度采用HBI,内镜活动度采用简化的CD内镜下评分(simplified endoscopic score for Crohn′s disease,SES-CD)评估[26]。
3. 疗效评价:主要结局为临床缓解率、临床应答率和内镜缓解率,次要结局为生物学缓解率、生物学应答率和不良反应发生率。UC患者的临床缓解定义为完整Mayo评分≤2分且无一项分项评分>1分,临床应答定义为完整Mayo评分降幅≥30%及降幅≥3分(便血的分项评分降幅≥1分或该分项评分为≤1分),内镜缓解定义为Mayo内镜下评分≤1分[12]。CD患者的临床缓解定义为HBI<5,临床应答定义为HBI下降≥3,内镜缓解定义为内镜下黏膜无病变[4,27]。生物学缓解定义为hsCRP水平正常(<3 mg/L),生物学应答定义为基线水平异常的hsCRP降至正常或下降幅度≥50%[28]。
4. 安全性评估:治疗期间的所有药物不良反应包括输液反应、使用后药物反应记录,肝功能异常定义为转氨酶或胆红素大于正常参考值上限,肾功能异常定义为血清肌酐大于正常参考值上限,白细胞减低定义为血常规检查中白细胞绝对值<4×109/L或中性粒细胞<2×109/L,肠道/呼吸道/皮肤感染定义为通过粪便、呼吸道分泌物或皮肤渗出物检测出明确病原体,严重不良反应是指由于药物不良反应如严重过敏和感染、粒细胞缺少等导致治疗终止。恶性肿瘤为治疗期间报告并经病理证实的所有恶性肿瘤。
使用SPSS 26.0统计软件进行数据分析。符合正态分布的连续变量以表示,组间比较采用独立样本t检验;不符合正态分布的连续变量以M(Q1,Q3)表示,组间比较采用Wilcoxon秩和检验;分类变量以例数和百分比表示,组间比较采用χ2检验或Fisher精确概率检验。内镜缓解的影响因素采用多因素Cox回归模型,使用Kaplan-Meier曲线进行生存分析,单因素分析中P≤0.10的变量纳入多因素分析模型。均为双侧检验,检验水准α=0.05。
共纳入78例IBD患者,包括65例UC和13例CD,其中男44例(56.4%),女34例(43.6%),年龄(40.5±11.9)岁,病程为7.7(4.0,12.6)年,随访过程中8例(10.3%)患者终止治疗,只有1例(7.7%)因顾虑肺部感染而停药。UC患者E2型54例(83.1%),E3型11例(16.9%),CD患者A1、A2和A3分型分别为2例(15.4%)、9例(69.2%)和2例(15.4%),L2、L3和L3+L4分型分别为1例(7.7%)、11例(84.6%)和1例(7.7%),B1、B2和B2+B3分型分别为2例(15.4%)、7例(53.8%)和4例(30.8%),其中有肛周病变的3例(23.1%)。UC患者内镜下Mayo评分为(2.46±0.64)分,CD患者SES-CD为5.0(4.5,8.0)分。78例患者维得利珠单抗治疗前糖皮质激素、免疫抑制剂和TNF-α抑制剂的使用率分别为89.7%、46.3%和33.3%,用药过程中同时使用糖皮质激素、免疫抑制剂的UC患者比例均高于CD患者,但差异无统计学意义(均P>0.05)。UC和CD患者吸烟史、基线实验室检查指标水平差异均无统计学意义(均P>0.05)(表1)。
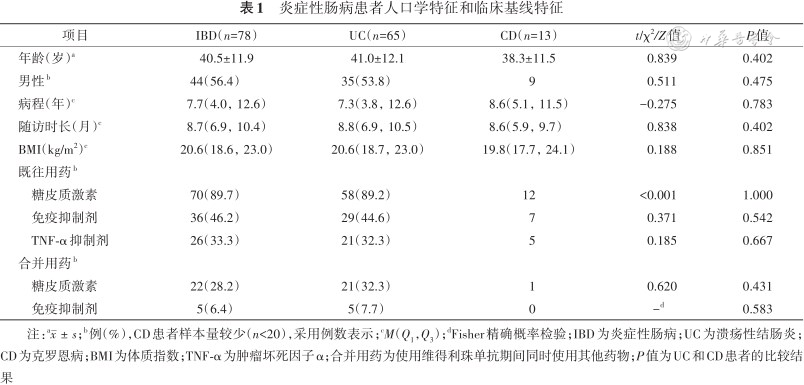
炎症性肠病患者人口学特征和临床基线特征
炎症性肠病患者人口学特征和临床基线特征
| 项目 | IBD(n=78) | UC(n=65) | CD(n=13) | t/χ2/Z值 | P值 |
|---|---|---|---|---|---|
| 年龄(岁)a | 40.5±11.9 | 41.0±12.1 | 38.3±11.5 | 0.839 | 0.402 |
| 男性b | 44(56.4) | 35(53.8) | 9 | 0.511 | 0.475 |
| 病程(年)c | 7.7(4.0,12.6) | 7.3(3.8,12.6) | 8.6(5.1,11.5) | -0.275 | 0.783 |
| 随访时长(月)c | 8.7(6.9,10.4) | 8.8(6.9,10.5) | 8.6(5.9,9.7) | 0.838 | 0.402 |
| BMI(kg/m2)c | 20.6(18.6,23.0) | 20.6(18.7,23.0) | 19.8(17.7,24.1) | 0.188 | 0.851 |
| 既往用药b | |||||
| 糖皮质激素 | 70(89.7) | 58(89.2) | 12 | <0.001 | 1.000 |
| 免疫抑制剂 | 36(46.2) | 29(44.6) | 7 | 0.371 | 0.542 |
| TNF-α抑制剂 | 26(33.3) | 21(32.3) | 5 | 0.185 | 0.667 |
| 合并用药b | |||||
| 糖皮质激素 | 22(28.2) | 21(32.3) | 1 | 0.620 | 0.431 |
| 免疫抑制剂 | 5(6.4) | 5(7.7) | 0 | -d | 0.583 |
注:a;b例(%),CD患者样本量较少(n<20),采用例数表示;cM(Q1,Q3);dFisher精确概率检验;IBD为炎症性肠病;UC为溃疡性结肠炎;CD为克罗恩病;BMI为体质指数;TNF-α为肿瘤坏死因子α;合并用药为使用维得利珠单抗期间同时使用其他药物;P值为UC和CD患者的比较结果
维得利珠单抗治疗2周和6周时的总体生物学缓解率和总体生物学应答率均分别为66.7%和35.9%。治疗2周时无论是生物学缓解率还是生物学应答率在UC和CD患者间差异均无统计学意义,而6周时UC患者生物学缓解率明显高于CD患者(48/65比4/13,P=0.007)。在维得利珠单抗治疗14周时的生物学缓解率和生物学应答率分别为70.5%和43.6%,而临床缓解率和临床应答率分别为60.3%和85.9%,有31例(47.0%)患者实现内镜下黏膜愈合,且在UC中均高于CD患者,但差异均无统计学意义(均P>0.05)(表2)。
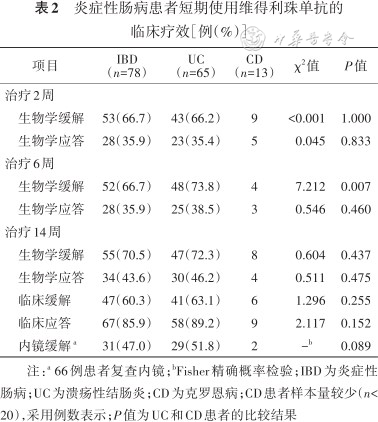
炎症性肠病患者短期使用维得利珠单抗的临床疗效[例(%)]
炎症性肠病患者短期使用维得利珠单抗的临床疗效[例(%)]
| 项目 | IBD (n=78) | UC (n=65) | CD (n=13) | χ2值 | P值 |
|---|---|---|---|---|---|
| 治疗2周 | |||||
| 生物学缓解 | 53(66.7) | 43(66.2) | 9 | <0.001 | 1.000 |
| 生物学应答 | 28(35.9) | 23(35.4) | 5 | 0.045 | 0.833 |
| 治疗6周 | |||||
| 生物学缓解 | 52(66.7) | 48(73.8) | 4 | 7.212 | 0.007 |
| 生物学应答 | 28(35.9) | 25(38.5) | 3 | 0.546 | 0.460 |
| 治疗14周 | |||||
| 生物学缓解 | 55(70.5) | 47(72.3) | 8 | 0.604 | 0.437 |
| 生物学应答 | 34(43.6) | 30(46.2) | 4 | 0.511 | 0.475 |
| 临床缓解 | 47(60.3) | 41(63.1) | 6 | 1.296 | 0.255 |
| 临床应答 | 67(85.9) | 58(89.2) | 9 | 2.117 | 0.152 |
| 内镜缓解a | 31(47.0) | 29(51.8) | 2 | -b | 0.089 |
注:a 66例患者复查内镜;bFisher精确概率检验;IBD为炎症性肠病;UC为溃疡性结肠炎;CD为克罗恩病;CD患者样本量较少(n<20),采用例数表示;P值为UC和CD患者的比较结果
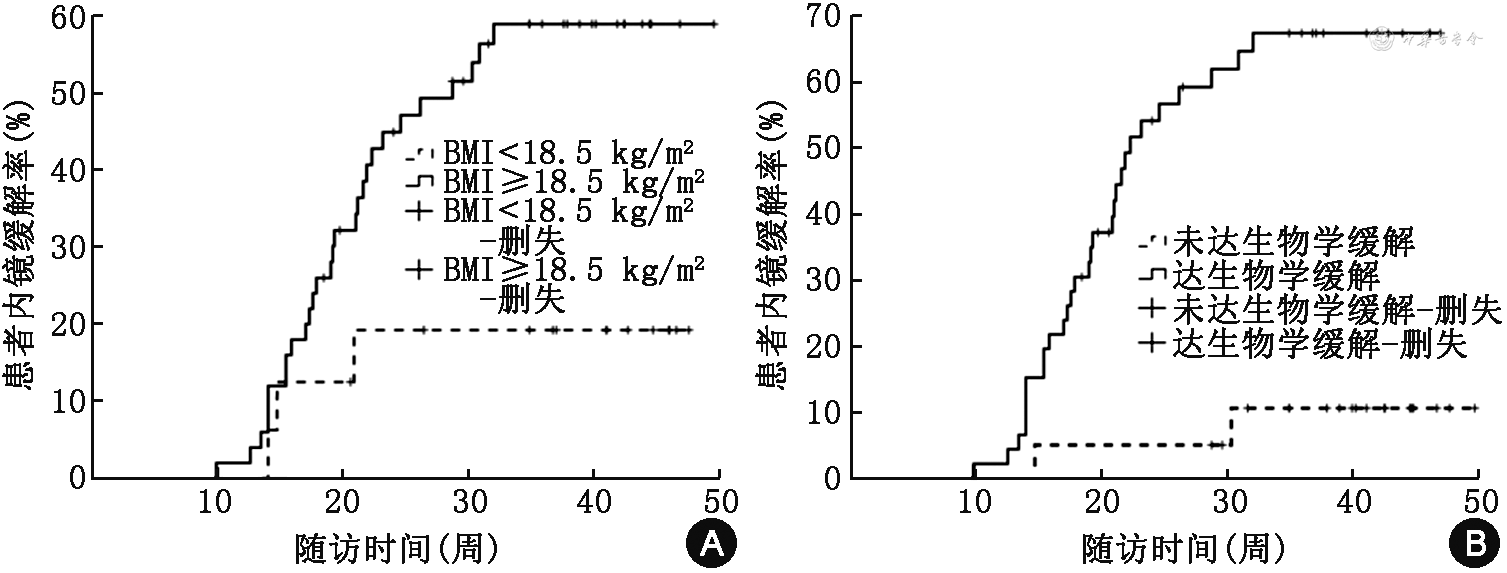
78例IBD患者中66例行内镜复查,有31例(47.0%)在14周达到内镜缓解,其中UC患者29例(51.8%,29/56),CD患者2例(2/10)。对实现黏膜愈合的患者进行单因素和多因素Cox回归分析(表3),结果显示,维得利珠单抗治疗前基线BMI≥18.5 kg/m2(HR=5.04,95%CI:1.50~16.91,P=0.009)和6周时达生物学缓解是治疗14周内镜缓解率的影响因素(HR=15.22,95%CI:3.16~73.38,P=0.001),是维得利珠单抗短期治疗实现黏膜愈合的预测因子。Kaplan-Meier生存曲线显示,相比BMI<18.5 kg/m2的患者,BMI≥18.5 kg/m2的患者更早达到内镜下缓解(HR=3.71,95%CI:1.13~12.22,P=0.021,图1A)。同时,维得利珠单抗治疗6周时达生物学缓解的患者比未达生物学缓解的患者更早实现黏膜愈合(HR=10.24,95%CI:2.43~43.16,P<0.001,图1B)。
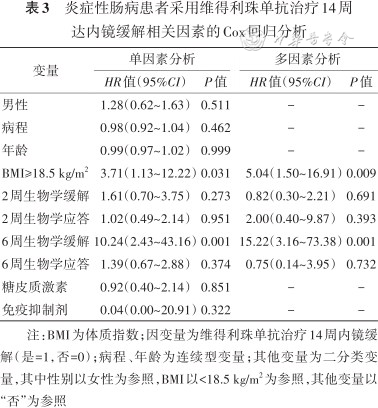
炎症性肠病患者采用维得利珠单抗治疗14周达内镜缓解相关因素的Cox回归分析
炎症性肠病患者采用维得利珠单抗治疗14周达内镜缓解相关因素的Cox回归分析
| 变量 | 单因素分析 | 多因素分析 | |||
|---|---|---|---|---|---|
| HR值(95%CI) | P值 | HR值(95%CI) | P值 | ||
| 男性 | 1.28(0.62~1.63) | 0.511 | - | - | |
| 病程 | 0.98(0.92~1.04) | 0.462 | - | - | |
| 年龄 | 0.99(0.97~1.02) | 0.999 | - | - | |
| BMI≥18.5 kg/m2 | 3.71(1.13~12.22) | 0.031 | 5.04(1.50~16.91) | 0.009 | |
| 2周生物学缓解 | 1.61(0.70~3.75) | 0.273 | 0.82(0.30~2.21) | 0.691 | |
| 2周生物学应答 | 1.02(0.49~2.14) | 0.951 | 2.00(0.40~9.87) | 0.393 | |
| 6周生物学缓解 | 10.24(2.43~43.16) | 0.001 | 15.22(3.16~73.38) | 0.001 | |
| 6周生物学应答 | 1.39(0.67~2.88) | 0.374 | 0.75(0.14~3.95) | 0.732 | |
| 糖皮质激素 | 0.92(0.40~2.14) | 0.851 | - | - | |
| 免疫抑制剂 | 0.04(0.00~20.91) | 0.322 | - | - | |
注:BMI为体质指数;因变量为维得利珠单抗治疗14周内镜缓解(是=1,否=0);病程、年龄为连续型变量;其他变量为二分类变量,其中性别以女性为参照,BMI以<18.5 kg/m2为参照,其他变量以“否”为参照

有57例患者在维得利珠单抗治疗过程中出现不良反应,共95例次,总体发生率为73.1%(57/78)。其中UC 49例,CD 8例。如表4所示,维得利珠单抗治疗的不良反应涉及全身多个系统,包括皮肤、关节、眼部、血液系统、消化系统、内分泌系统、神经系统、心血管系统及呼吸系统。其中肝肾损害发生率最高,达37.2%。其次是感染,发生率为26.9%,主要包括肠道感染(15.4%)、呼吸道感染(3.8%)及皮肤感染(7.7%)。肠外表现(20.0%)及白细胞降低(15.8%)并不少见,其中肠外表现相关不良反应包括皮肤病变(7.7%)、关节痛(9.0%)及葡萄膜炎(1.3%)。有2例(2.6%)患者在治疗期间报告并病理证实恶性肿瘤,包括宫颈癌1例和肺癌1例。仅有1例(1.3%)UC患者因肺部感染空洞增大而终止治疗,其余患者均继续使用维得利珠单抗治疗,且继续用药后不良反应可缓解或消失。
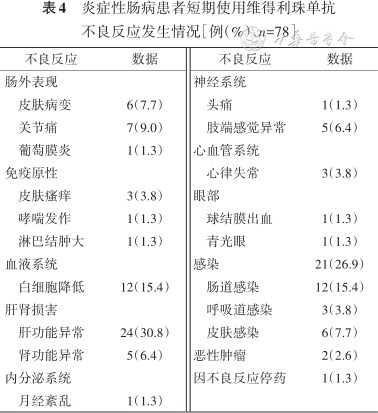
炎症性肠病患者短期使用维得利珠单抗不良反应发生情况[例(%),n=78]
炎症性肠病患者短期使用维得利珠单抗不良反应发生情况[例(%),n=78]
| 不良反应 | 数据 | 不良反应 | 数据 |
|---|---|---|---|
| 肠外表现 | 神经系统 | ||
| 皮肤病变 | 6(7.7) | 头痛 | 1(1.3) |
| 关节痛 | 7(9.0) | 肢端感觉异常 | 5(6.4) |
| 葡萄膜炎 | 1(1.3) | 心血管系统 | |
| 免疫原性 | 心律失常 | 3(3.8) | |
| 皮肤瘙痒 | 3(3.8) | 眼部 | |
| 哮喘发作 | 1(1.3) | 球结膜出血 | 1(1.3) |
| 淋巴结肿大 | 1(1.3) | 青光眼 | 1(1.3) |
| 血液系统 | 感染 | 21(26.9) | |
| 白细胞降低 | 12(15.4) | 肠道感染 | 12(15.4) |
| 肝肾损害 | 呼吸道感染 | 3(3.8) | |
| 肝功能异常 | 24(30.8) | 皮肤感染 | 6(7.7) |
| 肾功能异常 | 5(6.4) | 恶性肿瘤 | 2(2.6) |
| 内分泌系统 | 因不良反应停药 | 1(1.3) | |
| 月经紊乱 | 1(1.3) |
本研究显示出维得利珠单抗在中重度IBD患者中良好的短期治疗效果,但安全性不容忽视。通过对北京协和医院接受该药物治疗的患者的临床资料进行回顾性分析,本研究结果显示约50%的UC患者治疗14周分别达到临床缓解和内镜缓解。虽然CD患者的黏膜愈合率仅1/5(2/10),但近半数(6/13)的患者实现了临床缓解。和其他研究结果一致,本研究中IBD患者总体缓解率约40%,表明有近一半的IBD患者可以从维得利珠单抗治疗中获益[29, 30, 31, 32]。尽管维得利珠单抗展现了较好的短期疗效,但临床实践中仍需要确定影响药物反应的预测因素以优化治疗策略。本研究还发现,维得利珠单抗作为一种肠道特异的生物制剂,虽然目前仅1例患者因肺部感染未控制而终止治疗,然而短期治疗过程中出现的不同程度、不同系统的药物不良反应总发生率高达73.1%。本研究拓展补充了维得利珠单抗在我国患者中的治疗效果和不良反应的真实情况,鉴于该药在我国使用时间尚短、队列规模尚小,其安全性需要在更长期的临床实践过程中观察和评估。
以往的临床试验结果显示,维得利珠单抗的药物不良反应发生率较低[22,33, 34]。然而,一项回顾性研究发现,206例中重度IBD患者中只有31%有资格参加此类临床试验[35],并不能完全代表常规临床实践中的患者人群,其真实安全性有待评估。本研究结果显示,短期使用维得利珠单抗过程中总体不良反应发生率73.1%,其主要特点是涉及全身系统、广泛、严重程度较轻以及持续时间相对短暂。其中,发生一过性的肝肾损害比例最高,接近40%。有近1/3的患者发生包括肠道、呼吸道及皮肤的感染,除了1例患者终止治疗,其余均属药物可控的轻中度感染病例。与此同时,从未有过肠外表现的部分患者在治疗过程中新发肠外表现并不少见,尤其是关节症状。但随着药物使用时间延长,这些表现可逐步减轻或消失,可能是由于患者对药物产生适应,也侧面反映出维得利珠单抗不良反应相对轻微而短暂。在治疗期间,各有1例UC和CD患者分别经病理证实为肺腺癌和宫颈癌,其中1例有TNF-α抑制剂的用药史。这2例患者用药前存在一定的高危因素,如肺内小结节、宫颈人乳头瘤病毒(human papilloma virus,HPV)感染史,但均在用药后才出现症状并确诊为恶性肿瘤,不能除外药物诱发或促进恶性肿瘤的发生发展。这一发现提示即使维得利珠单抗是肠道特异性生物制剂,但用药前及治疗过程中仍需谨慎排查和评估系统肿瘤的发生风险。总之,本研究结果说明维得利珠单抗短期治疗的安全性有待斟酌,虽然药物不良反应大多可控、严重不良反应罕见,然而相比其他药物治疗,其涉及全身各系统的、轻微或一过性的不良反应发生率仍然不低。因此在临床实践中,对维得利珠单抗的使用需要临床医师充分评估其获益与风险之后慎重地选择,以优化治疗策略、最大化实现患者长期缓解。
本研究充分考虑了常见人口统计学指标和临床变量,结果显示基线高BMI水平与内镜缓解率呈正相关,BMI正常水平以上的患者相比过瘦的患者能更早实现黏膜愈合。与其他生物制剂受血药浓度影响不同,维得利珠单抗每剂使用均按标准剂量,对治疗的反应严格取决于肠道内α4β7阳性细胞的数量,疗效可能与这种细胞的分布及数量相关[36]。另外,用药前正常水平的BMI侧面反映了患者更好的营养状态、相对较轻的疾病活动度,也可能是影响疗效的潜在因素。但此结果仍需要未来更深入的研究去进一步证实内在的相关机制。此外,治疗6周时的生物学缓解与第14周更好的临床结果呈正相关,且这部分患者更早达到内镜缓解。这可能反映了维得利珠单抗抑制炎症途径的作用,而这些途径支持IBD的病理过程,短期内临床炎症指标对药物促进内镜下愈合的预测作用有助于对维得利珠单抗长期疗效的判断。
本研究的主要优势是单中心队列可确保临床数据的同一性、患者依从性,并减少患者群体的偏见,更真实地反映中国人群的临床用药情况。同时,短期治疗后几乎所有患者均进行了内镜复查评估,保证了临床数据的可用性。本研究局限性在于回顾性研究增加了研究结果偏倚的风险;其次,研究样本量相对较小、时间较短,因此在临床实践中对患者的疗效和安全性长期和大规模的评估十分必要。
综上所述,维得利珠单抗对中重度IBD患者具有诱导缓解作用,基线BMI≥18.5 kg/m2、治疗6周时生物学缓解是14周时黏膜愈合的预测因子;其药物不良反应虽然轻微而短暂,但总体发生率较高,未来需要大样本前瞻性多中心研究进一步证实。
所有作者均声明不存在利益冲突



























