
评估拉布立海小剂量方案对难治性慢性痛风性关节炎的临床疗效与安全性。
随访研究。回顾性分析2021年1月至2022年7月在中山大学孙逸仙纪念医院接受拉布立海治疗的难治性慢性痛风性关节炎患者的临床资料。所有患者均使用可耐受的最大剂量口服降尿酸药物3个月以上但血尿酸(sUA)仍>360 μmol/L、双能CT尿酸盐体积>10 cm3。小剂量拉布立海的使用方法为每次4.5~7.5 mg,间隔4周使用1次,最多使用3次。收集疗效(每次拉布立海用药前后sUA、第1次用药前和用药后12周痛风石及尿酸盐体积变化)和安全性数据。
共纳入22例患者,其中男21例(95.4%),年龄(44±15)岁,病程11(6,15)年,治疗前sUA为(667±112)μmol/L。每次拉布立海治疗后,患者sUA均低于治疗前(均P<0.001),3次治疗的sUA降低值[M(Q1,Q3)]分别为568(471,635)、187(66,335)和123(49,207)μmol/L。治疗12周时,9例患者(40.9%)的sUA<360 μmol/L,1例患者痛风石消失;所有患者尿酸盐体积较第1次治疗前降低明显[17(7,134)cm3比40(16,172)cm3,P<0.001],降低百分比为41.6%(22.9%,58.5%)。总体安全性良好,无严重不良反应发生。
小剂量拉布立海对难治性慢性痛风性关节炎安全有效,值得进一步随机对照研究。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
痛风是嘌呤代谢紊乱和(或)尿酸排泄减少引起的晶体性关节炎,未经规范降尿酸治疗,尿酸盐晶体持续沉积,可发展为慢性痛风性关节炎。笔者前期研究显示近1/4痛风患者合并痛风石[1]。慢性痛风性关节炎的治疗关键是降尿酸,美国风湿病学会痛风管理指南建议血尿酸(serum uric acid,sUA)的目标值为<360 μmol/L[2]。欧洲抗风湿病联盟指南及我国指南则建议,合并痛风石者的sUA目标值应<300 μmol/L[3, 4]。目前我国已上市的口服降尿酸药物包括别嘌醇、非布司他和苯溴马隆。然而,大约3%的痛风患者使用口服降尿酸药物不能使sUA达标[5],对此,国内外指南推荐使用尿酸氧化酶制剂,我国已上市的相关药物为拉布立海,其在我国获批的适应证为儿童白血病、淋巴瘤患者的尿酸水平控制,用于治疗痛风属于超说明书用药。《中华人民共和国医师法》使规范的超说明书用药有法可依,笔者于2022年在国内首次报道拉布立海成功治疗1例口服降尿酸药物治疗无效的慢性痛风性关节炎患者[6],现进一步回顾性收集分析使用拉布立海的患者的临床资料,探索小剂量拉布立海治疗难治性慢性痛风性关节炎的疗效与安全性。
随访研究。纳入2021年1月至2022年7月在中山大学孙逸仙纪念医院住院并使用拉布立海的难治性慢性痛风性关节炎患者。使用拉布立海的患者需符合以下全部条件:(1)诊断符合2015年美国风湿病学会/欧洲抗风湿病联盟痛风分类标准[7];(2)体格检查发现多发痛风石;(3)尽管接受了可耐受的最大剂量降尿酸药物(单药或联用)3个月以上仍sUA水平>360 μmol/L且双能CT尿酸盐体积>10 cm3;(4)患者有意愿快速溶解痛风石。排除标准包括:(1)葡萄糖-6-磷酸脱氢酶活性低于正常值下限;(2)血红蛋白<90 g/L;(3)估计肾小球滤过率<30 ml·min-1·1.73 m-2;(4)丙氨酸转氨酶或天冬氨酸转氨酶>2倍正常值上限;(5)既往生物制剂过敏史;(6)活动性荨麻疹。本研究获中山大学孙逸仙纪念医院伦理委员会批准(批件号SYSEC-KY-KS-2021-169)。
拉布立海超适应证治疗慢性痛风性关节炎已通过中山大学孙逸仙纪念医院药事委员会审批。所有患者均签署超说明书用药知情同意书。拉布立海的用药方案为每次4.5~7.5 mg,分3~5 d使用,具体剂量根据患者的尿酸盐负荷、用药后的耐受性调整。间隔4周使用1次,最多使用3次。配伍方法为每1.5 mg加入0.9%氯化钠溶液50 ml静脉滴注30 min。每次静脉滴注拉布立海前予甲泼尼龙20 mg静脉注射,预防过敏反应及痛风发作。
1. 患者一般资料:收集患者每次住院使用拉布立海和第1次使用拉布立海12周后门诊就诊的资料。使用拉布立海前的基线资料包括一般情况(年龄、性别)、痛风病情(包括病程、痛风家族史、发作累及的关节、近1年痛风发作次数、合并症、sUA、痛风石负荷、双能CT尿酸盐体积)及既往降尿酸药物使用情况。合并症包括慢性肾脏病(chronic kidney disease,CKD)、肾结石、肥胖、血脂异常、脂肪肝、2型糖尿病、高血压及冠心病。痛风石负荷包括体格检查发现的痛风石的数目及累及部位,最大痛风石的长径和短径(单位mm)。双能CT检查部位均为双手、双足、双膝关节中体格检查发现痛风石的部位,仪器为德国西门子公司SOMATOM Force型,根据仪器自带软件计算尿酸盐体积(单位cm3)。
2. 有效性评估的指标:包括每次拉布立海治疗前后sUA、12周时sUA、最大痛风石的长径及短径、双能CT尿酸盐体积(部位与使用拉布立海治疗前相同)。由于室温下拉布立海会酶促降解血液样品中的尿酸,每次拉布立海治疗结束后抽血,标本离体后立即冰浴送检sUA。
3. 安全性评估的指标:包括用药后有无不良反应、治疗前后血常规、肝肾功能结果。痛风发作情况包括痛风发作次数、累及的关节、持续时间及治疗情况。收集痛风的其他治疗情况,包括预防发作药物和降尿酸药物。
使用SPSS 24.0软件对研究数据进行统计分析。分类变量以例(%)表示。对于连续变量,符合正态分布的以表示,治疗前后的比较采用配对样本t检验;不符合正态分布的则以M(Q1,Q3)表示,治疗前后比较采用配对样本的Wilcoxon符号秩检验。双侧检验,取α=0.05。
共纳入22例患者,其中男21例(95.4%),年龄(43.6±14.6)岁,病程11(6,15)年,中位受累关节数10(6,20)个,近1年痛风发作次数20(10,27)次,sUA水平(667±112)μmol/L。11例(50.0%)患者合并肾结石,6例(27.3%)患者合并CKD 3期(表1)。

22例使用拉布立海治疗的难治性慢性痛风性关节炎患者的基线临床特征
22例使用拉布立海治疗的难治性慢性痛风性关节炎患者的基线临床特征
| 临床特征 | 数值 |
|---|---|
| 男性[例(%)] | 21(95.4) |
| 年龄(岁,) | 43.6±14.6 |
| 病程[年,M(Q1,Q3)] | 11(6,15) |
| 体质指数(kg/m2,) | 26.7±3.9 |
| 痛风石数目[例(%)] | |
| 1~10个 | 10(45.5) |
| 11~20个 | 7(31.8) |
| >20个 | 5(22.7) |
| 血尿酸(μmol/L,) | 667±112 |
| 双能CT尿酸盐体积[cm3,M(Q1,Q3)] | 40(16,172) |
| 血肌酐(μmol/L,) | 112±36 |
| 估计肾小球滤过率(ml·min-1·1.73m-2,) | 76±26 |
| 肾结石[例(%)] | 11(50.0) |
| 肥胖[例(%)] | 7(31.8) |
| 血脂异常[例(%)] | 13(59.1) |
| 脂肪肝[例(%)] | 16(72.7) |
| 2型糖尿病[例(%)] | 4(18.2) |
| 高血压[例(%)] | 9(40.9) |
| 冠心病[例(%)] | 2(9.1) |
拉布立海治疗前口服降尿酸药使用情况:既往曾接受别嘌醇治疗者18例,其中13例剂量为600 mg/d,5例合并CKD者剂量为300 mg/d;曾接受非布司他治疗者13例,其中9例剂量为40 mg/d,4例剂量为80 mg/d;曾接受苯溴马隆治疗者10例,其中8例剂量为50 mg/d,2例剂量为100 mg/d。第1次拉布立海治疗后12周口服降尿酸药使用情况:单用非布司他治疗11例,其中10例剂量为80 mg/d,1例剂量为60 mg/d;单用别嘌醇治疗2例,剂量均为600 mg/d;联合用药9例,6例为非布司他80 mg/d联合苯溴马隆50 mg/d,1例为非布司他60 mg/d联合苯溴马隆100 mg/d,1例为别嘌醇600 mg/d联合苯溴马隆50 mg/d,1例为别嘌醇600 mg/d联合苯溴马隆100 mg/d。21例患者接受0.5~1.0 mg/d的秋水仙碱预防痛风发作,1例CKD 3期患者因不耐受未接受秋水仙碱治疗。
22例患者中,19例的拉布立海方案为每次1.5 mg/d连续3 d,每4周重复1次,共3次。1例因尿酸盐负荷量大(尿酸盐体积为166 cm3),第1次方案为1.5 mg/d连续3 d,第4天加用3 mg,总量为7.5 mg;1例因痛风石导致关节功能严重受限(尿酸盐体积44 cm3),第1次给药方案为1.5 mg/d连续5 d,总量为7.5 mg。但这2例患者加量后出现头晕伴恶心,后续2次的方案不再加量,仍采用1.5 mg/d连续3 d。1例仅接受1次1.5 mg/d连续3 d治疗,后因经济原因终止治疗(纳入本文统计)。
每次拉布立海治疗后患者sUA均显著降低(均P<0.001),3次中位sUA降低值分别为568(471,635)、187(66,335)及123(49,207)μmol/L。尽管4周后在下一次拉布立海治疗前sUA均有所回升,但第2次治疗前sUA显著低于第1次治疗前(t=5.13,P<0.001),第3次治疗前亦低于第2次治疗前(t=2.62,P=0.026)。3次拉布立海治疗后sUA<360 μmol/L的患者比例分别为95.4%(21/22)、52.3%(11/21)和66.6%(14/21)。12周后sUA为(398±118)μmol/L,sUA<360 μmol/L的比例为40.9%(9/22)。22例患者中,仅3例(13.6%)在第2次使用拉布立海后sUA无明显下降,这3例患者年龄较大(分别为65、70及70岁),病程较长(分别为10、20及20年),基线尿酸盐负荷量亦较大(分别为154.1、185.9及243.4 cm3)(表2)。
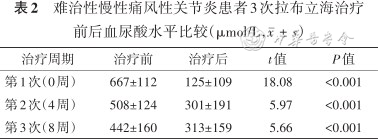
难治性慢性痛风性关节炎患者3次拉布立海治疗前后血尿酸水平比较(μmol/L,)
难治性慢性痛风性关节炎患者3次拉布立海治疗前后血尿酸水平比较(μmol/L,)
| 治疗周期 | 治疗前 | 治疗后 | t值 | P值 |
|---|---|---|---|---|
| 第1次(0周) | 667±112 | 125±109 | 18.08 | <0.001 |
| 第2次(4周) | 508±124 | 301±191 | 5.97 | <0.001 |
| 第3次(8周) | 442±160 | 313±159 | 5.66 | <0.001 |
22例患者痛风石分布最多的部位依次为足趾95.4%(21/22)、踝81.8%(18/22)及手指77.3%(17/22)。最大痛风石的长径×短径的极大值为75 mm×72 mm,极小值为10 mm×10 mm。第1次拉布立海治疗后12周时,1例(4.5%)患者痛风石消失,6例(27.3%)最大痛风石的长径或短径缩小超过10 mm。
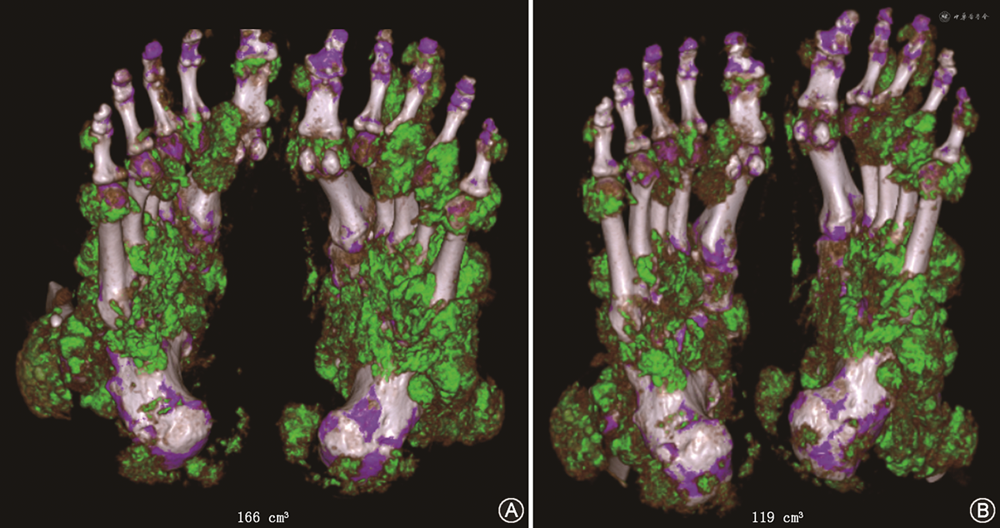
22例患者均行治疗前后双能CT检查(图1),其中行双侧足、膝、手部检查的例数分别为19、16和17例,双能CT检查部位数为3、2和1个部位者分别为10、10和2例。结果12周时95.4%(21/22)的患者尿酸盐体积减小,中位尿酸盐体积从基线40(16,172)cm3降至17(7,134)cm3(Z=-4.07,P<0.001),中位尿酸盐减少体积20(11,58)cm3,减少百分比41.6%(22.9%,58.5%)。第2次使用拉布立海后sUA水平无下降的3例患者,尽管痛风石体格检查也均无缩小,但双能CT尿酸盐减少体积及减少百分比分别为31.4 cm3(20.4%)、18 cm3(9.7%)及28.6 cm3(11.7%)。有1例患者尿酸盐体积无减少,但3次sUA降低值分别为811、128和67 μmol/L,第12周sUA为381 μmol/L,该患者口服降尿酸药物方案为非布司他80 mg/d,因合并肾结石未使用苯溴马隆。

总体安全性良好,无严重不良反应发生,不良反应见表3。所有患者均未出现过敏反应、发热、皮疹、外周水肿,2例(9.1%)患者在第1次用药的第5天静脉滴注拉布立海时出现头晕伴恶心,1例(4.5%)出现腹泻,均为拉布立海第1次给药时增加剂量者。1例(4.5%)患者第1次拉布立海治疗结束后出现静脉炎。所有患者每次拉布立海治疗前后均复查血肌酐,治疗前后血肌酐水平差异无统计学意义[(111±36)μmol/L比(116±39)μmol/L,t=-1.76,P=0.093]。1例(4.5%)患者0周和8周血肌酐升高>26.5 μmol/L,达到急性肾损伤标准,该例患者合并CKD,1个月后血肌酐恢复至基线,后续随访4个月血肌酐水平稳定。所有患者均未出现溶血、转氨酶升高等不良反应。
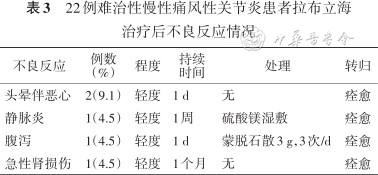
22例难治性慢性痛风性关节炎患者拉布立海治疗后不良反应情况
22例难治性慢性痛风性关节炎患者拉布立海治疗后不良反应情况
| 不良反应 | 例数 (%) | 程度 | 持续 时间 | 处理 | 转归 |
|---|---|---|---|---|---|
| 头晕伴恶心 | 2(9.1) | 轻度 | 1 d | 无 | 痊愈 |
| 静脉炎 | 1(4.5) | 轻度 | 1周 | 硫酸镁湿敷 | 痊愈 |
| 腹泻 | 1(4.5) | 轻度 | 1 d | 蒙脱石散3 g,3次/d | 痊愈 |
| 急性肾损伤 | 1(4.5) | 轻度 | 1个月 | 无 | 痊愈 |
拉布立海治疗期间均无痛风发作,治疗间隔期6例(27.3%)患者出现8次痛风发作,累及1、2和3个关节的次数分别为4、3和1次,发作时间4~7 d,在原有秋水仙碱的基础上口服依托考昔120 mg/d(3例)或甲泼尼龙24 mg/d(3例)治疗后疼痛完全缓解。
本研究纳入的患者均在使用可耐受的最大剂量口服降尿酸药物后sUA仍不能达标,属于难治性痛风患者。根据国内外指南此时可考虑使用尿酸氧化酶制剂普瑞凯希或拉布立海治疗。普瑞凯希是聚乙二醇重组的尿酸氧化酶,减少了免疫原性并延长了作用时间,已在美国获批用于治疗难治性痛风,但国内未上市。拉布立海是一种转基因的酿酒酵母菌株产生的重组尿酸氧化酶,用于痛风治疗尚无公认用法。文献报道,单次0.2 mg/kg静脉滴注[8]和每天0.02 mg/kg、连续使用3~7 d[9]均可有效降低痛风患者的sUA。在总剂量相同的情况下,拉布立海间隔4周分次使用溶解痛风石的效果优于每天连续使用[8]。多次拉布立海注射之后,输液反应和过敏反应风险增加[10],并且拉布立海使用时间超过8周后,其降尿酸效果可能下降。临床试验中也观察到,免疫原性较拉布立海低的普瑞凯希,从治疗第7周起部分患者的sUA升高[7]。综上原因,本研究拉布立海的使用方法为第1次4.5~7.5 mg,分3~5 d使用,每天剂量约0.02 mg/kg,间隔4周1次,共3次,时间累计8周。本研究中86.4%(19/22)的患者拉布立海总剂量为13.5 mg(约0.2 mg/kg),与文献每月1次0.2 mg/kg、共6个月相比,属于小剂量。
研究发现,拉布立海降尿酸效果显著。一项单臂研究纳入9例高尿酸血症合并CKD患者,平均sUA为612 μmol/L,接受单剂量0.2 mg/kg拉布立海治疗后,所有患者的sUA均迅速降低至测不出,第7天90%的患者sUA高于正常水平但低于治疗前水平[11]。39例合并CKD的痛风患者每天接受拉布立海0.02 mg/kg,连续3~7 d,平均sUA从600 μmol/L降至180 μmol/L以下,7 d后回升至360 μmol/L[9]。本研究第1次静脉滴注拉布立海后复查sUA,中位sUA降低568(471,635)μmol/L,95.4%的患者sUA<360 μmol/L,12周时sUA<360 μmol/L者占40.9%,提示对于难治性慢性痛风性关节炎患者,即使尿酸盐负荷重,小剂量拉布立海也可有效降低sUA。然而,由于拉布立海半衰期短,仅15.7~22.5 h,加上sUA降低后沉积的尿酸盐溶解使sUA回升,因此sUA不能长期维持于低水平。普瑞凯希半衰期长,临床试验中每月1次的普瑞凯希可使sUA稳定维持在300 μmol/L以下,每2周1次则可使sUA稳定维持在120 μmol/L以下[5]。
拉布立海可以溶解痛风石。国外文献报道,接受每月1次0.2 mg/kg、共6个月方案的5例患者,2例痛风石明显缩小[8]。本研究12周时1例患者痛风石消失,6例(27.3%)患者最大痛风石的长径或短径缩小超过10 mm,复查双能CT,中位尿酸盐减少体积达20(11,58)cm3,中位减少百分比为41.6%(22.9%,58.5%),提示小剂量拉布立海治疗短期内即可大量溶解尿酸盐。口服降尿酸药物溶解尿酸盐晶体速度较慢[12],使用6个月后双能CT尿酸盐体积仅从(1.3±3.8)cm3降至(0.6±2.1)cm3。普瑞凯希亦可有效溶解痛风石。在普瑞凯希平均治疗13周的情况下,双能CT检测痛风石体积从(9.15±13.26)cm3降至(1.89±2.86)cm3[13]。文献报道连续使用普瑞凯希6个月后42%的患者可观察到至少1个痛风石完全消失,即使在那些使用普瑞凯希仅在前1~2个月可维持sUA<360 μmol/L的患者仍可观察到痛风石缩小[14, 15]。因此,即使是短暂地维持sUA在较低水平仍有助于溶解痛风石。
本研究显示小剂量拉布立海治疗耐受性良好,无严重不良反应。在每次使用拉布立海前予甲泼尼龙,可避免静脉滴注期间痛风发作及过敏反应。文献报道拉布立海治疗发生过敏反应的最强预测因素为多次注射,推测与拉布立海的免疫原性有关[10]。本研究拉布立海用至第8周后停用,未发现输液反应和过敏反应。另外,本研究中每次拉布立海治疗后的sUA降低值逐渐下降,第3次sUA的降低值仅为123(49,207)μmol/L,不排除可能与免疫原性有关。部分使用普瑞凯希的痛风患者在第7周起sUA升高,且为输液反应的最强预测因素,推测与药物的免疫原性产生抗药抗体有关[5],甲氨蝶呤或吗替麦考酚酯可减少抗药抗体产生,提高治疗效果[16, 17]。
总之,本研究结果显示小剂量拉布立海作为二线治疗可有效降低难治性慢性痛风性关节炎患者的sUA水平,缩小痛风石,减少尿酸盐体积,且耐受性良好,其疗效及安全性有待进一步多中心前瞻性对照研究验证。
李谦华, 莫颖倩, 曾文橙, 等. 小剂量拉布立海治疗难治性慢性痛风性关节炎的疗效及安全性[J]. 中华医学杂志, 2023, 103(21): 1617-1622. DOI: 10.3760/cma.j.cn112137-20221124-02496.
所有作者均声明不存在利益冲突



























