
新型冠状病毒肺炎治疗药物洛匹那韦/利托那韦(LPV/r)是多种细胞色素P450(CYP450)酶的抑制剂,又是多种CYP450酶底物,此外还是P-糖蛋白的抑制剂、葡萄糖醛酸转移酶诱导剂,与很多抗肿瘤药物存在药物相互作用。药品说明书仅列举了少数抗肿瘤药物与LPV/r的相互作用,提供参考信息严重不足。本文系统总结了抗肿瘤药物及常用辅助药物和LPV/r的相互作用及处理建议。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
洛匹那韦/利托那韦(LPV/r)是一种人类免疫缺陷病毒(HIV)蛋白酶抑制剂,批准的适应证为HIV-1感染患者。目前,LPV/r被《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》推荐用于治疗新型冠状病毒肺炎患者,并已被临床证实有效[1]。肿瘤患者感染新型冠状病毒的风险为普通患者的4.3倍(1.3%比0.3%),发生重症的风险为非肿瘤患者的4.9倍(38.9%比7.9%)[2]。肿瘤患者用药复杂,很多药物可能与LPV/r存在相互作用。以下结合LPV/r和抗肿瘤药物药代动力学特点,总结LPV/r和肿瘤患者相关用药间的相互作用,以为临床用药监护提供参考。
根据Drug bank数据库资料(https://www.drugbank.ca/),洛匹那韦是CYP3A4、CYP2C8强抑制剂,CYP2D6中度抑制剂,CYP2C19、CYP2B6弱抑制剂,CYP3A4、P-糖蛋白底物,同时还是P-糖蛋白、OATP1B3、有机阴离子转运多肽1B1、OATP1B1/SLCO1B1抑制剂。利托那韦是CYP2C8、CYP3A4、CYP3A5、CYP3A7强抑制剂,CYP2B6、CYP2D6中度抑制剂,CYP3A7、CYP2B6、CYP2D6、CYP3A底物,同时还是尿苷二磷酸葡萄糖醛酸转移酶1A1(UGT1A1)诱导剂,OATP1B1/SLCO1B1的抑制剂。因此,LPV/r和其他药物特别是抗肿瘤药物合用时存在广泛的相互作用。可能会改变药物疗效和毒性,甚至引起严重和/或危及生命的不良事件。
Medscape药物相互作用数据库(https://reference.medscape.com)将相互作用分为4级:禁忌;严重,使用替换方案;密切监视;较轻微。Hiv-druginteractions数据库(https://www.hiv-druginteractions.org/checker)将相互作用分为4级:禁止合用;潜在相互作用;潜在弱相互作用;无预期相互作用。我们参考以上两个数据库的分级,将相互作用分为以下4级:1级表示合用风险很低,可安全合用;2级表示存在潜在弱相互作用,合用风险较低,但应密切监测;3级表示存在潜在较强相互作用,合用风险较高,尽量避免合用;4级表示存在严重相互作用,合用风险很高,禁止合用。
我们从Medscape和Hiv-druginteractions数据库筛选出和LPV/r存在相互作用的抗肿瘤药物,同时结合文献资料,将抗肿瘤药物和LPV/r相互作用总结如下。小分子靶向药物大多通过细胞色素P450(CYP450)代谢,因此,和LPV/r之间大多存在相互作用,主要为LPV/r抑制CYP3A4等代谢酶,提高靶向药物水平。舒尼替尼375mg和LPV/r合用时,曲线下面积(AUC)可以超过舒尼替尼500mg单用时的水平(338.1 ng·h-1·ml-1比315.2 ng·h-1·ml-1)[3]。靶向药物也可抑制或诱导LPV/r代谢相关酶改变LPV/r体内药动学,如达克替尼抑制CYP2D6,提高LPV/r体内水平,而达拉菲尼通过诱导CYP3A4,降低LPV/r体内暴露量。部分靶向药物虽和LPV/r无显著的药代动力学相互作用,但有增加不良反应的风险,如索拉非尼[4]。
大多数单克隆抗体通过蛋白水解分解代谢,临床上与LPV/r一般无显著的药代动力学相互作用,如程序性死亡受体1(PD-1)抑制剂、西妥昔单抗等,但应注意不良反应的叠加,如LPV/r和奥英妥珠单抗、吉妥珠单抗合用会增加QTc间期延长风险。另外,个别单克隆抗体部分通过CYP450代谢,如本妥昔单抗小部分通过CYP3A4/5氧化代谢,合用应密切监测。部分通过CYP450或葡萄糖醛酸化代谢的化疗药物其体内药动学可能被LPV/r改变,内分泌治疗药物也和抗病毒药物存在相互作用,详见表1,表2,表3,表4[5,6,7,8,9,10]。

洛匹那韦/利托那韦(LPV/r)与小分子靶向药物相互作用
洛匹那韦/利托那韦(LPV/r)与小分子靶向药物相互作用
| 级别 | 药名 | 相互作用结果 | 相互作用机制a | 临床用药建议 |
|---|---|---|---|---|
| 4 | cobimetinib | cobimetinib↑ | (1)抑制CYP3A4,cobimetinib的AUC提高6.7倍 | 禁忌合用 |
| 4 | 瑞格非尼 | 瑞格非尼↑ | (1)抑制CYP3A4 | 禁忌合用 |
| 4 | 依维莫司 | 依维莫司↑ | (1)抑制CYP3A4、P-糖蛋白外排转运体 | 禁忌合用 |
| 4 | 维奈妥拉 | 维奈妥拉↑ | (1)抑制CYP3A4,肿瘤溶解综合征风险增加 | 在最初的递增剂量阶段,禁忌合用。如在剂量递增后必须合用,将维奈妥拉的剂量减少至少75% |
| 3 | 阿卡替尼 | 阿卡替尼↑ | (1)抑制CYP3A4 | 避免合用,如7 d内短期联合,则暂时中断阿卡替尼 |
| 3 | avapritinib | avapritinib↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 阿法替尼 | 阿法替尼↑ | (1)抑制P-糖蛋白外排转运体 | 避免合用。合用如不能耐受,可将阿法替尼的日剂量减少10 mg |
| 3 | 阿西替尼 | 阿西替尼↑ | (1)抑制CYP3A4 | 避免合用,合用时将阿西替尼的剂量减少50% |
| 3 | 奥拉帕利 | 奥拉帕利↑ | (1)抑制CYP3A4 | 避免合用,合用时奥拉帕利的剂量降至150 mg(胶囊)或100 mg(片剂)。不要用胶囊代替片剂 |
| 3 | 奥西替尼 | 奥西替尼↑QTc间期延长↑ | (1)抑制CYP3A4;(3)QTc间期延长 | 避免合用 |
| 3 | 博舒替尼 | 博舒替尼↑利托那韦↑ | (1)抑制CYP3A4、P-糖蛋白外排转运体,博舒替尼血浆浓度提高5倍;(2)P-糖蛋白外排转运体 | 避免合用 |
| 3 | 布吉替尼 | 布吉替尼↑ | (1)抑制CYP3A4 | 避免合用,如果不能避免,则将布吉替尼的剂量减少约50%(180 mg降至90 mg,或由90 mg减至60 mg) |
| 3 | copanlisib | copanlisib↑ | (1)抑制CYP3A4 | 避免合用,如果不能避免,则将copanlisib剂量减至45 mg |
| 3 | 达克替尼 | LPV/r↑ | (2)抑制CYP2D6 | 避免合用 |
| 3 | 达拉非尼 | 达拉非尼↑LPV/r↓ | (1)抑制CYP3A4、CYP2C8;(2)诱导CYP3A4 | 避免合用 |
| 3 | 达沙替尼 | 达沙替尼↑QTc间期延长↑ | (1)抑制CYP3A4;(3)QT间期延长 | 避免合用,如不能避免,可能需减少达沙替尼剂量至20~40 mg/d |
| 3 | 康奈非尼 | 康奈非尼↑ | (1)抑制CYP3A4 | 避免合用,如果不能避免,将康奈非尼的剂量减少到1/3。在LPV/r停药3~5个半衰期,恢复原剂量 |
| 3 | 恩曲替尼 | 恩曲替尼↑ | (1)抑制CYP3A4 | 避免合用,如果不可避免,对12岁或以上体表面积>1.50 m2的患者,恩曲替尼剂量降至100 mg/d,在LPV/r停药3~5个半衰期后,恢复原剂量 |
| 3 | 厄洛替尼[5,6] | 厄洛替尼↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 凡德他尼 | QTc间期延长↑ | (3)两药均能延长QTc间期 | 避免合用 |
| 3 | gilteritinib | gilteritinib↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | glasdegib | glasdegib↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 艾代拉里斯 | 艾代拉里斯↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | ivosidenib | ivosidenib↑ | (1)抑制CYP3A4 | 避免合用,如不能避免,将ivosidenib剂量减少到250 mg/d。停用LPV/r后至少5个半衰期,增加到推荐剂量500 mg,1次/d。监测QTc间期延长的风险 |
| 3 | 卡博替尼 | 卡博替尼↑ | (1)抑制CYP3A4、MRP2 | 避免合用,如不能避免,可将卡博替尼的剂量减少40 mg/d(cometriq)或减少20 mg/d(cabmetyx)。LPV/r停用后2~3d恢复原剂量 |
| 3 | 拉罗替尼 | 拉罗替尼↑ | (1)抑制CYP3A4 | 避免合用,如不可避免,拉罗替尼减少50%。LPV/r停用3~5个半衰期后恢复原剂量 |
| 3 | 劳拉替尼 | 劳拉替尼↑( | 1)抑制CYP3A4 | 避免合用,如不可避免,劳拉替尼每日剂量减少25mg。LPV/r停用3个半衰期后恢复原剂量 |
| 3 | 芦可替尼 | 芦可替尼↑( | 1)抑制CYP3A4 | 避免合用,如不能避免,血小板计数≥100×109/L将芦可替尼起始剂量降至10 mg。血小板计数<100×109/L避免使用 |
| 3 | 罗米地辛 | 罗米地辛↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | midostaurin | midostaurin↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | 来那替尼 | 来那替尼↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | 尼洛替尼 | 尼洛替尼↑(LPV/r↑ | 1)抑制CYP3A4;(2)抑制CYP3A4、P-糖蛋白外排转运体 | 避免合用 |
| 3 | 帕比司他 | QTc间期延长↑( | 3)QT间期延长 | 避免合用 |
| 3 | pexidartinib | pexidartinib↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | 帕博西尼 | 帕博西尼↑( | 1)抑制CYP3A4 | 避免合用,如无法避免,可将帕博西尼剂量降至75 mg/d |
| 3 | 帕唑帕尼 | 帕唑帕尼↑( | 1)抑制CYP3A4 | 避免合用,如果必须联合用药,则将帕唑帕尼的剂量降至400 mg/d |
| 3 | 普纳替尼 | 普纳替尼↑( | 1)抑制CYP3A4 | 避免合用,如不能避免,则将普纳替尼的起始剂量降低至30 mg/d |
| 3 | 瑞博西尼 | 瑞博西尼↑(QTc间期延长↑ | 1)抑制CYP3A4;(3)QTc间期延长 | 避免合用,如不能避免,将瑞博西尼的起始剂量降低至400 mg/d |
| 3 | sonidegib | sonidegib↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | 色瑞替尼 | 色瑞替尼↑( | 1)抑制CYP3A4、P-糖蛋白外排转运体 | 避免合用,如不能避免,将色瑞替尼的剂量减少33% |
| 3 | tazemetostat | tazemetostat↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | 威罗菲尼 | 威罗菲尼↑(LPV/r↑QTc间期延长↑ | 1)抑制CYP3A4、P-糖蛋白外排转运体;(2)抑制P-糖蛋白外排转运体;(3)QTc间期延长 | 避免合用 |
| 3 | 依鲁替尼 | 依鲁替尼↑( | 1)抑制CYP3A4 | 避免合用 |
| 3 | duvelisib | duvelisib↑(LPV/r↑ | 1)抑制CYP3A4;(2)抑制CYP3A4 | 避免合用,当联合不可避免时,将duvelisib剂量减少至15 mg,2次/d |
| 2 | fedratinib | LPV/r↑( | 1)抑制CYP3A4、CYP2D6 | 密切监测 |
| 2 | 吉非替尼 | 吉非替尼↑( | 1)抑制CYP3A4 | 密切监测 |
| 2 | 克唑替尼 | 克唑替尼↑(LPV/r↑ | 1)抑制CYP3A4;(2)抑制P-糖蛋白外排转运体 | 密切监测 |
| 2 | 拉帕替尼 | LPV/r↑( | 2)抑制CYP3A4、P-糖蛋白外排转运体 | 密切监测 |
| 2 | 乐伐替尼 | QTc间期延长↑( | 3)QTc间期延长 | 密切监测 |
| 2 | 帕纳替尼 | LPV/r↑( | 2)抑制P-糖蛋白外排转运体 | 密切监测 |
| 2 | 硼替佐米 | 硼替佐米↑( | 1)抑制CYP3A4 | 密切监测 |
| 2 | 舒尼替尼[3] | 舒尼替尼↑( | 1)抑制CYP3A4 | 密切监测 |
| 2 | 索拉非尼[4] | QTc间期延长↑( | 3)QTc间期延长 | 密切监测 |
| 2 | 他拉唑帕尼 | 他拉唑帕尼↑( | 1)抑制P-糖蛋白外排转运体 | 密切监测 |
| 2 | vismodegib | vismodegib↑( | 1)抑制P-糖蛋白外排转运体 | 密切监测 |
| 2 | 伊马替尼[7,8] | 伊马替尼↑( | 1)抑制P-糖蛋白外排转运体 | 密切监测 |
| 1 | ixazomib | -( | 1)抑制CYP3A4;(2)CYP3A4 | 临床研究发现合用没有产生有临床意义的改变 |
注:AUC为曲线下面积;MRP2为多药耐药相关蛋白2;a(1)表示LPV/r对靶向药物的影响机制;(2)表示靶向药物对LPV/r的影响机制;(3)表示不良反应的叠加

洛匹那韦/利托那韦(LPV/r)与单克隆抗体药物相互作用
洛匹那韦/利托那韦(LPV/r)与单克隆抗体药物相互作用
| 级别 | 药名 | 相互作用结果 | 相互作用机制a | 临床用药建议 |
|---|---|---|---|---|
| 3 | 曲妥珠单抗-美坦新偶联物 | 曲妥珠单抗-美坦新偶联物↑细胞毒性成分DM1↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 奥英妥珠单抗 | QTc间期延长↑ | (3)QTc间期延长 | 避免合用,如果不能避免,治疗前后监测心电图和电解质,并定期监测治疗期间的临床指标 |
| 2 | enfortumab vedotin | enfortumab vedotin↑ | (1)抑制CYP3A4 | 密切监测 |
| 2 | 吉妥珠单抗 | QTc间期延长↑ | (3)QTc间期延长 | 密切监测 |
| 2 | polatuzumab vedo-tin | polatuzumab vedotin↑ | (1)抑制CYP3A4 | 密切监测 |
| 2 | 本妥昔单抗 | 本妥昔单抗↑ | (1)抑制CYP3A4 | 密切监测 |
注:a(1)表示LPV/r对单克隆抗体的影响机制;(2)表示单克隆抗体对LPV/r的影响机制;(3)表示不良反应的叠加

洛匹那韦/利托那韦(LPV/r)与内分泌治疗药物相互作用
洛匹那韦/利托那韦(LPV/r)与内分泌治疗药物相互作用
| 级别 | 药名 | 相互作用结果 | 相互作用机制a | 临床用药建议 |
|---|---|---|---|---|
| 4 | 戈舍瑞林 | QTc间期延长↑ | (3)QTc间期延长 | 禁忌合用 |
| 4 | 亮丙瑞林 | QTc间期延长↑ | (3)QTc间期延长 | 禁忌合用 |
| 4 | 阿帕鲁胺 | LPV/r↓ | (2)诱导CYP3A4 | 禁忌合用 |
| 3 | 曲普瑞林 | QTc间期延长↑ | (3)QTc间期延长 | 避免合用 |
| 3 | 他莫昔芬 | 他莫昔芬↑ | (1)抑制CYP3A4 | 避免合用 |
| 2 | darolutamide | darolutamide↑ | (1)抑制CYP3A4 | 密切监测 |
注:a(1)表示LPV/r对内分泌治疗药物的影响机制;(2)表示内分泌治疗药物对LPV/r的影响机制;(3)表示不良反应的叠加
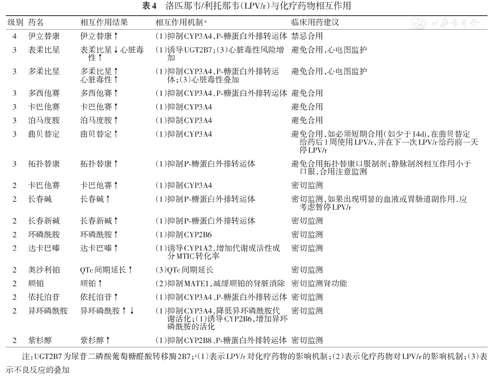
洛匹那韦/利托那韦(LPV/r)与化疗药物相互作用
洛匹那韦/利托那韦(LPV/r)与化疗药物相互作用
| 级别 | 药名 | 相互作用结果 | 相互作用机制a | 临床用药建议 |
|---|---|---|---|---|
| 4 | 伊立替康 | 伊立替康↑ | (1)抑制CYP3A4,P-糖蛋白外排转运体 | 禁忌合用 |
| 3 | 表柔比星 | 表柔比星↓心脏毒性↑ | (1)诱导UGT2B7;(3)心脏毒性风险增加 | 避免合用,心电图监护 |
| 3 | 多柔比星 | 多柔比星↑心脏毒性↑ | (1)抑制CYP3A4,P-糖蛋白外排转运体;(3)心脏毒性叠加 | 避免合用,心电图监护 |
| 3 | 多西他赛 | 多西他赛↑ | (1)抑制CYP3A4,P-糖蛋白外排转运体 | 避免合用 |
| 3 | 卡巴他赛 | 卡巴他赛↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 泊马度胺 | 泊马度胺↑ | (1)抑制CYP3A4 | 避免合用 |
| 3 | 曲贝替定 | 曲贝替定↑ | (1)抑制CYP3A4 | 避免合用,如必须短期合用(如少于14d),在曲贝替定给药后1周使用LPV/r,并在下一次LPV/r给药前一天停LPV/r |
| 3 | 拓扑替康 | 拓扑替康↑ | (1)抑制P-糖蛋白外排转运体 | 避免合用拓扑替康口服制剂;静脉制剂相互作用小于口服,合用注意监测 |
| 2 | 卡巴他赛 | 卡巴他赛↑ | (1)抑制CYP3A4 | 密切监测 |
| 2 | 长春碱 | 长春碱↑ | (1)抑制P-糖蛋白外排转运体 | 密切监测,如果出现明显的血液或胃肠道副作用,应考虑暂停LPV/r |
| 2 | 长春新碱 | 长春新碱↑ | (1)抑制P-糖蛋白外排转运体 | 密切监测 |
| 2 | 环磷酰胺 | 环磷酰胺↑ | (1)抑制CYP2B6 | 密切监测 |
| 2 | 达卡巴嗪 | 达卡巴嗪↑ | (1)诱导CYP1A2,增加代谢成活性成分MTIC转化率 | 密切监测 |
| 2 | 奥沙利铂 | QTc间期延长↑ | (3)QTc间期延长 | 密切监测 |
| 2 | 顺铂 | 顺铂↑ | (2)抑制MATE1,减缓顺铂的肾脏消除 | 密切监测肾功能 |
| 2 | 依托泊苷 | 依托泊苷↑ | (1)抑制CYP3A4、P-糖蛋白外排转运体 | 密切监测 |
| 2 | 异环磷酰胺 | 异环磷酰胺↑↓ | (1)抑制CYP3A4,降低异环磷酰胺代谢活化;(1)诱导CYP2B6,增加异环磷酰胺的活化 | 密切监测 |
| 2 | 紫杉醇 | 紫杉醇↑ | (1)抑制CYP2B8、P-糖蛋白外排转运体 | 密切监测 |
注:UGT2B7为尿苷二磷酸葡萄糖醛酸转移酶2B7;a(1)表示LPV/r对化疗药物的影响机制;(2)表示化疗药物对LPV/r的影响机制;(3)表示不良反应的叠加
肿瘤患者常常需要合并使用辅助药物,如防治不良反应类药物、抗骨转移药物、镇痛药等。我们参考Hiv-druginteractions、Drugbank数据库及文献资料,对辅助用药和LPV/r之间的相互作用总结如下。
主要以原型经肾脏排泄,体外不抑制CYP450酶,无药代动力学相互作用;但联合应用可增加肾毒性、低钙血症、肌病、横纹肌溶解症和肌红蛋白尿、心脏不良反应的风险或严重程度。临床处理建议:注意监测双膦酸盐不良反应。
(1)5-羟色胺3(5-HT3)受体拮抗剂:5-HT3受体拮抗剂经肝药酶代谢,且增加QTc间期延长风险。临床处理建议:谨慎合用,必须合用时可优先考虑主要由CYP2D6代谢的帕洛诺司琼、托烷司琼,避免主要由CYP1A2和CYP3A4代谢的昂丹司琼。(2)神经激肽1(NK-1)受体拮抗剂:阿瑞匹坦主要由CYP3A4代谢,其次由CYP1A2、CYP2C19代谢。合用可能减少阿瑞匹坦代谢,增加药效和不良反应。临床处理建议:注意监测阿瑞匹坦不良反应。(3)地塞米松:LPV/r可降低地塞米松的代谢。地塞米松是CYP3A诱导剂,慢性或大剂量使用可显著降低LPV/r的血药浓度。临床处理建议:注意监测。(4)甲氧氯普胺:甲氧氯普胺主要由CYP2D6部分代谢,合用可能会减少甲氧氯普胺的代谢。临床处理建议:注意监测甲氧氯普胺不良反应。
(1)吗啡:吗啡主要被葡萄糖醛酸化成吗啡-3-葡萄糖醛酸及药理活性吗啡-6-葡萄糖醛酸。LPV/r诱导葡萄糖醛酸作用,降低吗啡浓度,但促进活性代谢物吗啡-6-葡萄糖醛酸的形成。吗啡和吗啡-6-葡萄糖醛酸是P-gp的底物,联合给药可增强阿片类中枢作用。临床处理建议:注意监测吗啡过量中毒症状。(2)羟考酮[11]:羟考酮主要通过CYP3A代谢。联合应用使羟考酮的AUC增加2.6倍。临床处理建议:使用其他替换药物。(3)芬太尼[12]:芬太尼经CYP3A4代谢,利托那韦使芬太尼清除率下降67%,AUC增加83%。临床处理建议:使用其他替换药物。(4)美沙酮:LPV/r通过抑制CYP3A4增加美沙酮水平,但通过P-糖蛋白途径将药物泵出中枢。临床处理建议:密切监测。
LPV/r与大多数肿瘤靶向治疗药物、部分化疗药物、部分单克隆抗体、部分内分泌治疗药物和辅助治疗药物均存在药物相互作用,与少数抗肿瘤药物合用甚至可导致严重不良反应或致死性危险,因此,肿瘤患者应用LPV/r应进行密切的药物相互作用监护,以提高患者用药的有效性和安全性。
所有作者均声明不存在利益冲突



























