
铁缺乏(ID)/缺铁性贫血(IDA)在临床较为常见,但因临床表现隐匿,是多种慢性病的合并症,往往导致重视不足、诊治延误和不良后果。我国ID/IDA诊断率不足、治疗率偏低的情况较为明显,临床亟需重视并加以规范化诊治。本文全面分析了我国ID/IDA诊治现状、面临的问题及原因,对ID/IDA的诊断指标和治疗方案进行了探讨,并对高危人群的诊治提出建议,旨在注重临床实用性和可操作性,为ID/IDA的规范化诊治提供参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,每年从第1期至第10期共刊发10篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获得5分。
铁缺乏(iron deficiency,ID)和缺铁性贫血(iron deficiency anemia,IDA)是普遍影响儿童、绝经前女性(尤其是孕妇)和老年人的全球性健康问题,同时也是多种疾病的常见合并症[1]。由于其表现隐匿,往往导致诊治延误和不良后果,是危害我国患者健康的重要问题之一。对ID/IDA的及早识别和合理治疗是临床工作的重要任务,但是,目前患者和临床医师对该病重视不足,在某种程度上尚存在诊治欠规范的问题,亟需进一步加强ID/IDA的规范化诊治。本文根据近年来ID/IDA的研究进展进行探讨,提出相应的诊治意见和建议,期望为临床实践中ID/IDA的规范化诊治提供参考。
ID/IDA可对多系统器官功能造成损害,导致生长发育迟缓、行为障碍、认知功能损害、体能受损、围产期及围术期并发症等一系列健康问题[1, 2, 3],并严重影响消化系统疾病、慢性肾脏疾病、心力衰竭和肿瘤等慢性疾病的预后[1,4, 5]。对这类患者需及早筛查,对无输血指征的患者尽早采取铁剂治疗以尽快纠正ID[6]。
根据调查,我国轻度贫血得到诊治者不到20%,极重度贫血者也仅有50%得到诊治,ID/IDA存在明显诊断不及时及治疗率偏低的情况[7]。一项基于全国术前贫血数据库的回顾性横断面研究中,27.57%的患者术前存在贫血,仅12.25%的贫血患者术前接受了贫血相关治疗[8]。另一项对全国97家医院成年恶性肿瘤患者进行的横断面研究中,我国恶性肿瘤患者贫血发生率为49.24%,但其中高达92.84%的患者未给予任何纠正贫血的措施和治疗,在接受贫血治疗的患者中铁剂治疗比例仅6.59%[9]。造成上述现象的原因,除主观上重视不够外,主要跟以下4个方面有关。
1.我国贫血的诊断标准较低:世界卫生组织(WHO)对贫血诊断标准,成年男性血红蛋白(Hb)<130 g/L,成年女性(非妊娠)Hb<120 g/L称为贫血[10],中国标准[6]低于WHO诊断标准(表1),导致部分患者得不到治疗或充分治疗。

贫血诊断标准
贫血诊断标准
| 标准类型 | Hb(g/L) | ||
|---|---|---|---|
| 成年男性 | 成年女性 | 孕妇 | |
| WHO贫血诊断标准 | <130 | <120 | <110 |
| 中国贫血诊断标准 | <120 | <110 | <100 |
注:WHO为世界卫生组织;Hb为血红蛋白
2.口服铁剂依从性差且随访指导欠缺:轻度贫血常选择口服铁剂治疗,但部分患者口服铁剂后出现严重胃肠道不良反应,导致依从性差。Meta分析显示,与静脉铁剂相比,口服铁剂显著增加胃肠道不良反应风险(OR=3.05,95%CI 2.07~4.48,P<0.000 1)[11]。另一项单中心横断面研究中,37.5%的口服铁剂者发生胃肠道不良反应,其中66%的患者因胃肠道不良反应而放弃治疗[12]。在未坚持治疗的患者中,3.1%的患者表示不知道应持续治疗多长时间,4.1%的患者症状缓解后自行停药。
3.对静脉铁剂认识不足,启动治疗时间较晚且剂量不足:中国真实世界研究中患者使用静脉铁剂的基线Hb为81.1 g/L[13],而国外真实世界研究中使用静脉铁剂的基线Hb平均为96 g/L[14],提示中国启动静脉铁剂治疗时间较晚。
根据贫血程度计算,中度以上IDA患者铁需求量常需≥1 000 mg[15, 16],而中国真实世界研究中IDA患者蔗糖铁使用总剂量均值为511 mg,仅12.2%的患者使用剂量达到或超过1 000 mg[13],铁剂使用剂量不足则直接导致治疗效果不达标。我国IDA患者铁剂平均治疗剂量无法满足患者对铁的实际需求,究其原因,首先是临床对IDA重视不足,其次因依从性、住院时间、输液便利度等条件限制,常无法完成足剂量铁剂应用。此外,对静脉铁剂安全性的顾虑也导致使用较为保守,很多临床医生因担心发生危及生命的全身性过敏反应而尽量避免使用静脉铁剂。
4.IDA的诊治缺乏规范性:真实世界研究发现,仅有不到3%的患者在用药前进行铁指标检测,很多贫血应用静脉铁剂治疗者其电子病例诊断中并未体现IDA,且缺乏足够的Hb随访数据,铁剂使用量与患者基线Hb水平也未呈现相关性[13],提示临床实践中可能并未严格按照患者基线Hb水平准确计算铁需求,或即使计算了铁需求但并未实现足量补铁。
以上诊治现状和问题,提示在临床实践中IDA的规范化诊治及随访等亟需改进。
常见症状有乏力、嗜睡、注意力不集中、头痛、头晕、耳鸣。其他可见易怒/抑郁、脱发、头发或皮肤干燥、匙状甲、口角炎、运动耐量下降和不宁腿综合征。有些患者可能表现为异食癖,多见于女性和儿童,原因尚不清楚。体征可见面色苍白、舌乳头减少、唇裂、口角开裂[3,17]。但这些症状和体征是非特异性的。Blank等[18]研究显示,35%有缺铁症状的患者在首次就诊时被误诊为抑郁症、焦虑症、倦怠或慢性疲劳等。因此,怀疑IDA时需进行实验室检查以进一步明确诊断。
1.血常规:Hb水平是诊断贫血的标准,但是对铁状态的诊断缺乏特异性和敏感性,须与其他铁代谢指标结合进行诊断。不过,一旦确诊IDA,跟踪治疗反应中的Hb浓度则是一个很好的衡量指标。IDA显示小细胞低色素性贫血,平均红细胞体积(MCV)<80 fl,平均血红蛋白量(MCH)<27 pg,平均血红蛋白浓度(MCHC)<32%[6],但与血清铁等铁代谢指标相比,这些变化相对较晚,MCV在非缺铁状态下(如地中海贫血或炎症性贫血)也可能降低[17]。
2.骨髓铁染色:是评估铁含量的金标准。骨髓穿刺因其侵袭性不常规用于ID/IDA诊断,但对复杂病例的诊断仍有价值。
3.转铁蛋白饱和度(TSAT):是反映体内储存铁能否有效利用的指标,TSAT<20%提示ID。TSAT是根据铁和总铁结合能力(TIBC)计算的,其水平受这些值变化的影响,也受患者炎症和营养状态的影响,导致诊断ID/IDA的可靠性降低,且日内变化较大[5]。
4.血清铁:日内变化较大,受外部因素影响也大,其水平随感染、炎症和恶性肿瘤而降低,随肝脏疾病而升高[19]。因此,单独血清铁不能评价机体内铁水平,必须结合其他指标进行分析。
5.血清铁蛋白(SF):是IDA诊断的主要指标,反映体内铁储存状态。SF<30 μg/L诊断ID的敏感度和特异度分别为92%和98%[15]。SF是一种急性期反应蛋白,在慢性炎症、感染、恶性肿瘤或肝病情况下可能升高,需同时测定C反应蛋白(CRP)以排除炎症,结合SF浓度和CRP的测定是目前用于评估铁储备的一种简单、可靠的筛查方式。SF在肥胖人群中也会升高[3]。
6.TIBC:用以检测外周血中转铁蛋白(TRF)含量,不饱和铁和血清铁的总和代表TIBC,ID/IDA时TRF上升[6]。
7.网织红细胞:是反映骨髓造血功能及判断贫血疗效的重要指标,网织红细胞增多常见于IDA。
8.可溶性(血清)转铁蛋白受体水平(sTfR):是反映有核红细胞铁元素需求的指标,虽不受炎症的影响,但缺乏特异性,检测方法尚未正式标准化[6]。
9.网织红细胞血红蛋白含量(CHr):直接反映Hb合成的最新状态,是ID的早期诊断指标。在欧美已被公认为诊断ID的标志物,CHr<29 pg可准确评估ID,受炎症的影响小于SF和TSAT[19]。对于CHr敏感度和特异度的最佳参考值,目前尚未形成共识。CHr也有一定局限性,网织红细胞寿命仅1 d左右,检测到的CHr仅能反映很短时间内可利用铁的状态[5]。
10.铁调素:是调控铁浓度的重要激素,铁摄入增加、炎症、感染均可刺激其产生。受检测方法的限制不能广泛开展,阈值也需要标准化[6]。慢性肾脏病(CKD)患者铁调素水平通常高于一般人群,可作为评估CKD患者铁状态和铁反应性的生物标志物[20]。
1.妊娠期:越来越多的国家不建议以一刀切的标准来定义妊娠期贫血,而是更推荐以时间依赖性的Hb水平进行定义。WHO[21]和美国妇产科学会(ACOG)[22]对贫血的诊断标准为妊娠早期和晚期Hb<110 g/L,妊娠中期Hb<105 g/L。《英国妊娠期缺铁管理指南》建议,妊娠期血清铁蛋白<30 μg/L提示ID,但高于该水平也不能除外ID的可能性,其他铁代谢标志物不推荐用于孕期筛查[23]。
2.CKD:CKD患者ID的诊断标准尚未确立。《中国肾性贫血诊治临床实践指南》建议,非透析患者或腹膜透析患者SF≤100 μg/L且TSAT≤20%为绝对ID,SF>100~500 μg/L且TSAT≤20%为功能性ID;血液透析患者SF≤200 μg/L且TSAT≤20%为绝对ID[5]。
3.肿瘤:中国临床肿瘤学会(CSCO)指南建议,肿瘤患者Hb≤110 g/L或低于基线值≥20 g/L时需启动贫血评估[24]。很多情况下,患者Hb基线值比较高,易于掩盖贫血,故对近期检查Hb下降值≥20 g/L者需要关注。一般而言,SF水平越低则存在IDA的可能性越高,但在癌症情况下应注意慢性炎症状态可使SF水平出现假性升高。在非空腹情况下接受铁指标检测,也可能出现假性升高。
4.炎症性肠病(IBD):欧洲克罗恩病和结肠炎组织(ECCO)共识建议定期筛查IBD患者的血细胞计数、SF和TSAT[25]。ID/IDA诊断取决于炎症程度,对于无临床、内镜或生化证据的活动性IBD患者,其诊断标准为血清SF<30 μg/L,但存在炎症的情况下,SF达到100 g/L仍可能缺铁。
5.心力衰竭:心力衰竭时SF水平会升高,因此ID的定义与一般人群不同。中国专家共识的定义为:SF<100 μg/L时称为绝对ID,SF介于100~300 μg/L且TSAT<20%时称为功能性ID[26]。
6.围手术期:我国普通外科专家共识[27]和妇科围手术期专家共识[16]建议,Hb低于正常值时应进行铁相关指标检查。在非炎症状态下,血清SF<30 μg/L提示绝对ID;SF为30~100 μg/L、TSAT<20%伴或不伴CRP>5 mg/L时,可诊断为慢性炎症性贫血伴ID。
所有IDA患者和绝大部分ID但无贫血的患者,无论有无相应症状,均应立即接受治疗。有症状的ID患者,即使未出现贫血,也建议开始补铁治疗,特别是患有基础疾病或可能导致不良结局的关键时期(如心力衰竭、肿瘤、妊娠、术前等)更应积极干预,同时尽可能消除病因。对于无症状的ID患者,也应给予干预措施以预防铁储备进一步下降。
ID/IDA的治疗目标是补充铁储备,使Hb和SF恢复正常水平。各指南/共识对特殊人群治疗目标提出了建议:中国专家共识建议孕妇铁剂补充量的计算应以怀孕前体重为准,目标Hb达110 g/L即可[28]。中国指南建议肾性贫血治疗的Hb靶目标为Hb≥110 g/L,但不超过130 g/L[5]。CSCO指南[24]和ECCO共识[25]均建议,IBD患者补铁治疗后4周内Hb至少增加20 g/L是可接受的反应速度,可继续给药直至ID/IDA恢复。中国专家共识提出,心力衰竭合并ID患者的铁需求量中位水平为1 000 mg,可作为补铁的大致目标[26]。
ID/IDA的治疗包括口服铁剂、静脉铁剂和输血。ID/IDA严重程度、Hb下降速度、基础疾病对铁的耐受及需求量、年龄、性别、经济因素、患者偏好等都是临床做出决策前需综合考虑的问题。
1.口服铁剂:原则上ID/IDA患者都可以尝试应用,但不适用于活动性IBD、不耐受者及正在服用促红细胞生成素者[29]。目前市面可及口服铁剂品种较多,但临床效果均不稳定,个体差异较大,约10%~40%的口服铁剂者出现胃肠道不良反应,包括腹泻或便秘,不能完全坚持规定疗程,纠正贫血及补充铁储备需时较长(3~6个月)[30]。为克服胃肠反应及增加生物利用度,目前已有新型铁剂如麦芽酚铁剂、纳米铁剂进入临床试验,期待早日上市。研究表明,患者对小剂量口服铁剂的耐受性更好(每天开始逐渐增加剂量)。小剂量口服铁剂可使铁吸收量最大化,疗效却并未下降,胃肠道反应减少,从而提高耐受性和依从性[31, 32]。合用维生素C也有助于口服铁剂吸收。指南建议每月检查血常规和铁含量,一旦Hb正常,继续口服铁3个月以补足铁储备[29]。
2.静脉铁剂:相较于口服铁剂,静脉铁剂能快速补充铁,治疗时间短,不良反应少,无胃肠道负担,患者依从性更好。
(1)静脉铁剂发展史:①1932年上市第一代注射铁剂,因释放大量游离铁引起重度毒性反应,现已停用。②1991年第二代铁剂低分子右旋糖酐铁上市,免疫原性较之前产品降低,通过复杂碳水化合物包裹铁,更紧密结合铁,发生不良事件风险明显低于第一代铁剂[33]。蔗糖铁是目前常用的二代静脉铁剂,由碳水化合物外壳包裹氢氧化铁核心形成的球形微粒,分子稳定性较差,铁结合不够紧密导致不稳定铁释放较多[34]。受此限制,蔗糖铁单次仅可输注100~200 mg,再次输注至少隔日进行,导致部分患者无法坚持多次输注和完成足量补铁。③2007年开启第三代注射铁剂时代。第三代静脉铁剂包括异麦芽糖酐铁和羧基麦芽糖铁等,改进了碳水化合物及其复合物与铁结合的结构,稳定性更高,在巨噬细胞摄取前不会将大量不稳定的非转铁蛋白结合铁(NTBI)/游离铁释放到血液中,减轻由于NTBI/游离铁导致的不良反应,进而可在短时间内给予更高剂量[33]。研究表明,相比蔗糖铁多次给药,第三代静脉铁剂一次性给药1 000 mg在2周内可快速提升Hb(P<0.000 1),改善SF和TSAT也显著优于蔗糖铁1 000 mg分多次给药[35]。安全性较蔗糖铁得到很大提升[36]。目前两药均已在我国获批。
(2)静脉铁剂适应证:①口服铁剂不耐受,如老年人、妊娠中晚期伴胃肠道症状、IBD等胃肠道疾病者。②口服铁剂疗效差,口服治疗4周后Hb提升<10 g/L者,如持续性失血超过了口服铁剂补充能力、解剖或生理情况影响口服铁剂吸收、合并炎症或慢性疾病导致功能性缺铁、接受红细胞生成刺激剂治疗者。③临床需快速补铁,如中重度贫血、妊娠中晚期需快速纠正ID/IDA、手术预期失血量>500 ml或<6周内需行手术的ID患者。④患者意愿及生活质量需求,不愿忍受胃肠道反应,不接受耗时数月的治疗或不愿频繁就诊,更愿意通过1~2次就诊就补足贮存铁者[6,28]。
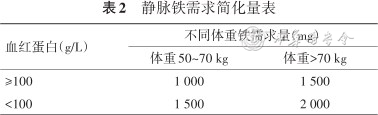
(3)静脉铁剂剂量:传统使用Ganzoni公式计算铁需求量,但该公式易出现误差,且可能低估铁需求量[23]。国内外指南/共识多支持使用简化的估算量表[25,28, 29](表2),即根据患者体重和Hb估计总铁需求量。研究证实,治疗后SF>400 μg/L能预防未来1~5年内缺铁的复发,因此建议这类患者补铁目标为SF超过400 μg/L。
静脉铁需求简化量表
静脉铁需求简化量表
| 血红蛋白(g/L) | 不同体重铁需求量(mg) | |
|---|---|---|
| 体重50~70 kg | 体重>70 kg | |
| ≥100 | 1 000 | 1 500 |
| <100 | 1 500 | 2 000 |
(4)静脉铁剂的安全性及其管理:静脉铁剂的安全性一直备受临床关注[37, 38]。静脉铁剂可能引起过敏反应,包括可能危及生命的全身性过敏反应,但实际上这些严重过敏反应极其罕见,其发生率被大大高估了。Meta分析显示,相比口服铁剂,静脉铁剂未导致严重不良事件风险增加,在超过10 000例接受静脉铁剂治疗的患者中,既无死亡也无全身性过敏反应发生[39]。除严重过敏反应外,大多数静脉铁剂引起的直接反应是Fishbane反应或孤立的症状/体征。Fishbane反应为一种轻度急性不良反应,静脉铁剂治疗者中发生率约1/100,其发病机制尚不明确,可能由于未结合的不稳定铁与内皮细胞相互作用释放一氧化氮所致。临床特征为短暂面部潮红、肌痛(急性胸部和/或背部疼痛)伴关节痛,胸闷有时伴呼吸困难。该反应为自限性,在停止静脉铁剂输注后数分钟内消退,如缓慢重新输注,通常不会再次出现[30,40]。孤立的症状/体征为非过敏性输注反应,可见荨麻疹、瘙痒、皮疹、轻度低血压/高血压、心动过速、恶心、头痛等[41]。上述症状如在暂停输注或减慢输注后缓解,即可判定为轻微输液反应,一般不需中止静脉铁剂的继续使用[28]。
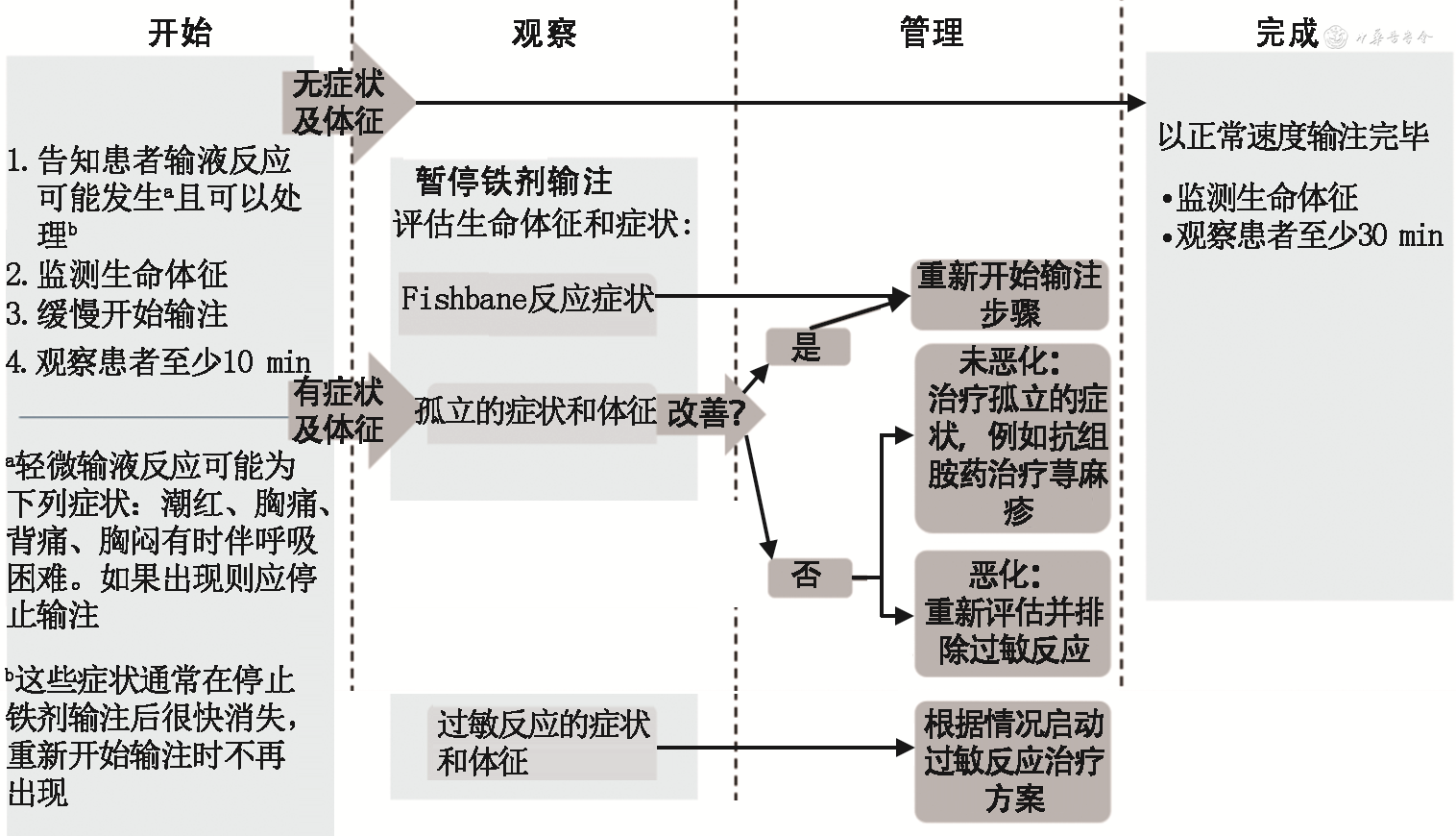
对静脉铁剂输液反应的管理,关键在于减轻患者和医护人员的顾虑、减缓输注速度、识别是Fishbane反应症状、孤立的症状/体征还是过敏反应症状,并给予适当治疗,以消除紧张甚至误判为严重过敏反应而导致过度治疗。图1是在参照国际公认的输液反应管理流程[41]基础上提出的简化流程图,以方便协助医护人员对急性输液反应进行规范化管理,供临床参考。

3.输血治疗:红细胞输注适用于急性或贫血症状严重影响到生理机能的IDA患者,国内输血指征是Hb<60 g/L(国外为Hb<80 g/L),老年和心脏功能差者可适当放宽至≤80 g/L[6]。输血是临床常用、但也是过度使用的医疗行为之一,宜限制不必要的输血,减少不良反应、有效降低医疗成本。治疗症状性IDA时,有时可能需要有限输入浓缩红细胞,这种情况下输血后仍需补铁治疗[37]。
我国ID/IDA患病率较高,但针对患者的相关科普知识及针对医生的多学科合作均不到位,诊治问题比较严峻,加强对ID/IDA的认知及规范诊治显得格外重要。须提高临床对高危人群的筛查意识,重视对复杂疾病状态下ID/IDA的识别,积极明确潜在病因,并根据临床实际情况权衡不同治疗方法的风险/获益制定规范化的治疗和随访方案,才能实现对ID/IDA的及时诊断和合理治疗。随着新型口服铁剂及第三代静脉铁剂不断研发和应用探索,减少不良反应发生率、缩短治疗时间、提高患者依从性、快速安全有效地纠正患者ID已成为发展趋势。
廖敏婧, 张连生. 铁缺乏及缺铁性贫血规范化诊治[J]. 中华内科杂志, 2023, 62(6): 722-727. DOI: 10.3760/cma.j.cn112138-20230210-00074.
所有作者声明无利益冲突
1.中度贫血是指()
A.血红蛋白110~120 g/L
B.血红蛋白100~120 g/L
C.血红蛋白60~90 g/L
D.血红蛋白60~80 g/L
2.缺铁性贫血的临床表现可除外()
A.颅骨改变
B.明显贫血时可有心脏扩大
C.可有髓外造血表现,如肝脾大
D.可有异食癖,如食泥土、煤渣
3.缺铁性贫血属于()
A.正常细胞性贫血
B.单纯小细胞性贫血
C.大红细胞性贫血
D.小细胞低色素性贫血
4.下列缺铁性贫血的实验室检查中正确的是()
A.血清铁正常,网织红细胞明显增多
B.血清总铁结合力增高
C.骨髓增生程度减低,巨核细胞缺如
D.血清叶酸、维生素B12水平降低
5.常见铁剂主要有()
A.输血
B.口服铁剂和静脉铁剂
C.营养保健品
D.食疗



























