
肠系膜下动静脉瘘(IMAVF)是指肠系膜下动脉与肠系膜下静脉之间的异常交通,临床上较为罕见。本文报道1例患者短期内出现无明显诱因的门脉高压、顽固性腹水、胃底食管静脉曲张及上消化道出血的症状,CT检查提示肠系膜下动脉远端与肠系膜下静脉之间存在动静脉瘘,经介入栓塞局部动静脉瘘后,患者病情好转出院。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者,男性,76岁,于2021年8月5日因腹胀进行性加重伴腹围进行性增大、尿量减少就诊于长春市中医院,2021年8月6日胃镜报告单提示食管-胃底静脉曲张。2021年8月11日CT提示肝硬化、脾大、腹水、门脉高压伴广泛腹膜炎。给予螺内酯160 mg、每天1次口服,呋塞米40 mg、每天1次口服,腹胀未见明显减轻。2021年10月9日转入吉林大学第一医院。入院查体一般状态可,有肝掌,移动性浊音阳性。余无其他阳性体征。血常规:淋巴细胞百分比17%,单核细胞百分比11%,淋巴细胞绝对值0.85×109/L,红细胞3.78×1012/L,血红蛋白(Hb)108 g/L,红细胞压积(HCT)32.8%,血小板计数(PLT)112×109/L。尿常规:尿蛋白(PRO)1+。血生化:尿素(干化学)11.76 mmol/L,肌酐133.7 μmol/L,钠136.0 mmol/L,二氧化碳结合力21. 80 mmol/L。D-二聚体5.66 mg/L 纤维蛋白原当量(FEU),纤维蛋白(原)降解产物(FDP)13.83 μg/ml。凝血常规:凝血酶原时间(PT)(CA)13.6 s,凝血酶原活动度(PTA)(CA)73%,纤维蛋白原(FBG)(CA)5.67 g/L。肝功能:丙氨酸转氨酶58.6 U/L,天冬氨酸转氨酶49.4 U/L,碱性磷酸酶152.7 U/L,白蛋白35.5 g/L。血清乙型、丙型肝炎抗体阴性。诊断性腹腔穿刺抽出淡黄色腹水,腹水常规提示白细胞总数277×106/L、雷氏试验阴性、蛋白 10.87 g/L,考虑腹水漏出液可能大。给予患者螺内酯100 mg、呋塞米40 mg、每日3次口服。2021年10月21日患者24小时尿量2 400 ml,体重下降1 kg,继续使用该利尿剂方案,但患者大量腹水原因仍未明确。
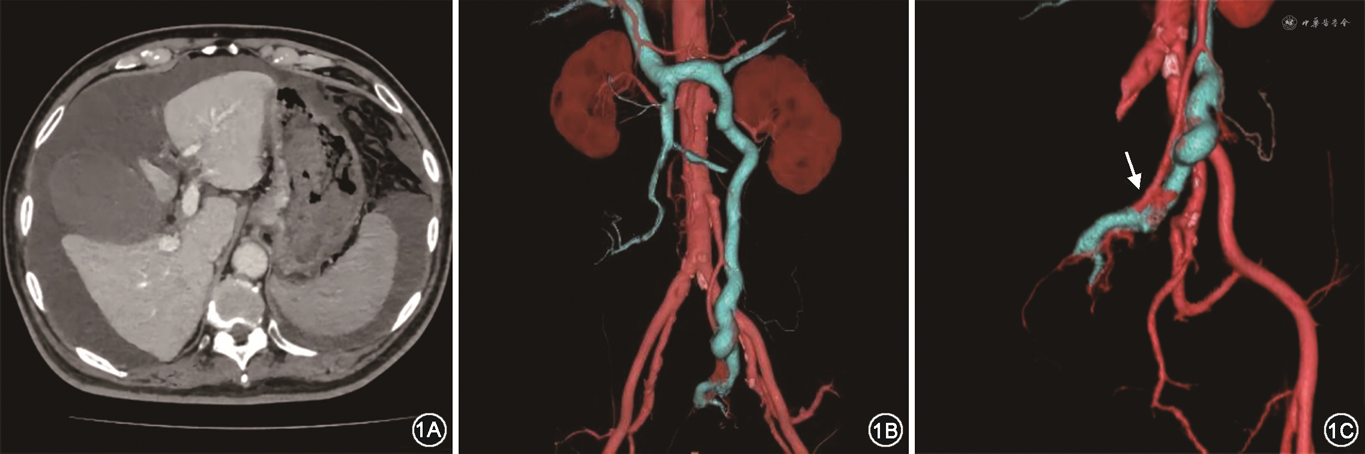
2021年11月3日,患者全腹增强CT及腹部血管三维重建结果示大量腹水,门静脉主干及脾静脉增宽、食管胃底静脉迂曲增粗,动脉期门静脉、脾静脉及肠系膜下静脉提前显影,肠系膜下静脉明显增宽,肠系膜下动脉远端的直肠上动脉与肠系膜下静脉在骶前相互沟通,形成紊乱血管网,提示直肠上动脉与肠系膜下静脉之间存在动静脉瘘(图1),余未见明显异常。患者于2021年11月4日20:20相继排5次暗红色便,血压降至72/47 mmHg(1 mmHg=0.133 kPa),行急诊胃镜检查见距门齿约30 cm以下食管至贲门4条曲张静脉,形态呈结节状,最粗直径约0.6 cm,曲张静脉间可见血管网,红色征阳性;胃内少许咖啡色液,胃底可见团块样曲张静脉,表面可见血栓,给予组织胶4.5 ml分4点注射;十二指肠球部及降段可见少许暗红色血液,冲洗后可见十二指肠乳头对侧黏膜略凹陷、有活动性渗血,给予止血夹2枚。观察再未有活动性出血。术后患者生命体征平稳,未再出现消化道出血。

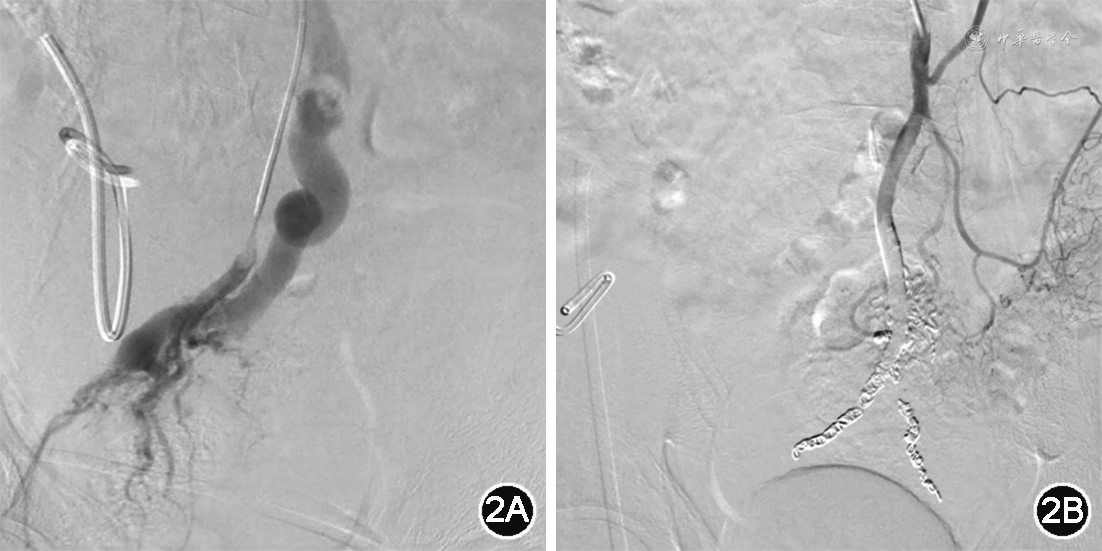
2021年11月20日患者转入介入治疗科行肠系膜下动脉造影及栓塞术。造影见肠系膜下动脉略增粗,肠系膜下静脉提前显示且明显增粗、局部见紊乱血管网,证实存在肠系膜下动静脉瘘(图2A)。为缓解门静脉高压、避免再次消化道出血风险,分2次分别超选左侧直肠上动脉、右侧直肠上动脉使用弹簧圈进行栓塞,应用组织胶与碘油(1︰5)适量予以巩固栓塞,复查造影,局部紊乱血管及肠系膜下静脉显影消失(图2B)。患者未出现消化道出血,腹水量减少、病情好转后出院。

肠系膜下动静脉瘘极为罕见,截至目前国外仅40余例病例报道,国内鲜见相关文献。肠系膜下动静脉瘘的病因可分为先天性、继发性(医源性)、特发性。先天性动静脉畸形发生于未分化的胚胎血管、无法分化为动脉和静脉,导致动脉和静脉之间形成异常血管交通。继发性(医源性)肠系膜下动静脉瘘可能发生于钝性或穿透性腹部损伤、动脉插管、胆道造影、脾门静脉造影或各种外科手术后,如左半结肠切除术或乙状结肠切除术[1]。本例患者为老年男性、无腹部手术或创伤病史,分析可能为特发性病因。
肠系膜下动静脉瘘所导致的病理生理变化通常与瘘管外组织的动脉血流量减少和瘘管远端静脉压增加有关。一方面动脉血的分流导致结肠缺血、黏膜充血和水肿;另一方面,从肠系膜下动脉分流进入门静脉系统的动脉血,使门脉系统的血流量增加、肝血管阻力代偿性增加[2],存在严重的分流时心输出量从体循环分流到肠系膜,导致肾脏灌注不足和全身性低血压。肾素-血管紧张素-醛固酮系统/血管紧张素系统的激活导致水钠潴留,进而引起全身容量超负荷[3]。因此肠系膜下动静脉瘘可出现各种症状,如腹痛、腹部肿块、缺血性结肠炎、消化道出血及门脉高压,甚至心力衰竭[4]。在既往的国外文献报道中,大多数患者以缺血性结肠炎、下消化道出血为主要症状。本例患者主要表现为上消化道出血合并门脉高压及腹水,属于肠系膜下动静脉瘘不典型的临床表现之一,文献仅有两例报道[3,5]。临床上导致门静脉高压和消化道出血的病因多样[6],对于此类少见病因,极易被临床漏诊和忽视。
由于发病率低,肠系膜下动静脉瘘目前尚无统一的诊断标准。结肠镜、腹部增强CT、数字减影血管造影技术在疾病确诊中分别具有一定作用。结肠镜可显示缺血性结肠炎患者的黏膜异常和血管形态的扭曲、脆性增加等改变[7]。数字减影血管造影可以相对准确地显示动静脉瘘的位置、数量、分流大小、评估周围内脏血管分支,并可在诊断同时进一步进行栓塞治疗。腹部增强CT除可以显示上述信息外,还可以显示继发的门脉高压、腹水、腹部肿块,在显示肠壁的增厚、水肿、肠壁周围脂肪间隙的改变及评估瘘口宽度方面也有显著优势。
目前,有关肠系膜下动静脉瘘的治疗多是采用血管栓塞治疗或手术。血管栓塞术具有创伤小、易重复的优点,适用于已确定瘘口部位或因并发症而难以手术的病例,其缺点是可能会导致广泛的动脉血栓形成,甚至器官缺血,或因栓塞不彻底而复发[8]。手术可切除局部动静脉瘘,同时根据肠管受累程度考虑是否切除邻近肠管。手术虽然治愈的可能性大,但应警惕大出血的风险[9]。另外对于肠系膜下动脉瘤引起的肠系膜下动静脉瘘,也有文献报道称可进行保守治疗,随访5年后发现动脉瘤缩小、扩张的静脉收缩被血栓取代[2]。
本病例患者既往体健,临床症状表现为无明显诱因的进行性腹胀,门静脉高压和消化道出血。虽然经胃镜下证实为上消化道出血并进行胃镜下止血治疗,但临床一直未能找到导致门静脉高压及顽固性腹水的原因。全腹增强CT发现肠系膜下动脉远端的直肠上动脉及肠系膜下静脉之间存在异常交通。为改善患者门脉高压、减轻消化道出血风险,采取介入栓塞术封堵直肠上动脉及其分支。术后患者腹水量减少,随访至今未再出现消化道出血症状,但应警惕动静脉瘘复发风险。
综上所述,对于出现不明原因的门脉高压、腹水及消化道出血症状时,应考虑到肠系膜下动静脉瘘此类罕见原因导致的可能,以实现尽早干预治疗,降低患者病死率和改善预后。
肖涵, 宋庆, 王彦添, 等. 特发性肠系膜下动静脉瘘致大量腹水合并消化道出血1例[J]. 中华内科杂志, 2023, 62(7): 852-854. DOI: 10.3760/cma.j.cn112138-20220718-00528.
所有作者声明无利益冲突



























