
罕见病影响全球3亿多人口,提高疾病筛查与诊断能力对改善患者预后、减少医疗资源消耗至关重要。随着信息技术飞速进步,临床决策支持系统(clinical decision support system,CDSS)为疾病筛查与诊断提供了技术支撑,特别是在病历电子化时代,CDSS在数据集成、行为干预等方面有了更大进展,但同时亦面临诸多挑战。本文通过对罕见病 CDSS的进展进行综述,剖析存在的挑战与发展方向,为国内罕见病筛诊领域CDSS的建设提供参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,每年共刊发10篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获5分。
罕见病是指发病率极低的一类疾病,又称孤儿病。世界卫生组织将罕见病界定为患病人数占总人口65/10万~100/10万的疾病,目前已发现近8 000种。据统计,罕见病的患病率虽低,但全球总患者人数超过3亿,在我国至少影响2 000万人群,且约80%的罕见病由遗传缺陷导致,多具有遗传异质性,儿童期发病占75%以上[1]。罕见病具有诊断困难、治疗难度偏大、有效治疗药物偏少等特点。人工智能的发展推动临床决策支持系统(clinical decision support system,CDSS)不断被研发,可在医疗中提供疾病预警、诊疗建议、医嘱监测等智能服务,并已成功应用于静脉血栓栓塞症(venous thromboembolism,VTE)、脓毒症、心血管疾病等领域,为破解不同科室、不同资历医生的疾病识别等难题提供了新方法。CDSS的发展为罕见病的筛查和诊断带来了希望,有望通过人工智能技术改善罕见病的漏诊、误诊,提高诊疗质量,为患者争取了治疗时间,并减少医疗资源消耗。现结合常见疾病筛查诊断的CDSS应用,对罕见病诊断领域的CDSS进展进行回顾,剖析存在的挑战与发展方向,为国内罕见病筛查诊断的CDSS建设提供参考。
由于罕见病种类繁多,单个病种病例少,临床表型与常见病重叠较大,大部分医务人员缺乏相关诊疗经验,早期识别意识较薄弱,导致罕见病容易误诊或漏诊,患者往往面临漫长、曲折的求医历程。以溶酶体贮积症(lysosomal storage diseases,LSDs)的戈谢病(Gaucher disease,GD)为例,临床误诊率为61.9%,患者平均确诊时间为4.48年[2]。由于罕见病病情进展迅速,累及多器官、多系统,延迟诊断将耽误患者的最佳治疗时机,给家庭和社会带来沉重的负担。为破解罕见病诊疗难题,近年来,我国通过发布首批罕见病目录,组建全国罕见病诊疗协作网等措施,对提升临床的认知度和诊疗能力提供了政策保障。
罕见病的临床表现多样且复杂,血液内科、肾内科、呼吸内科、神经内科、消化内科、遗传代谢科、内分泌科、心血管内科等内科科室均是常见的就诊科室,其诊疗过程亦需多学科团队联合会诊。罕见病筛查和诊疗中使用CDSS,可弥补临床医生因对罕见病认知不足而导致的漏诊、误诊,扩大罕见病筛查覆盖率,提升多学科会诊效率,从而为患者争取最佳的治疗时机。随着罕见病诊疗知识在全球范围内的普及与深入认识,以及医院临床数据的积累,为建立罕见病筛查的人工智能模型奠定了基础。而CDSS在VTE、脓毒症、心血管疾病、ICU、肿瘤等领域积累的数据分析、机器学习、语言处理、人机交互等应用经验,有望将积累的罕见病诊疗经验落地于临床诊疗中,为医生提供罕见病筛查预测和诊疗建议。
1. CDSS定义:Van Bemmel和Musen[3]将CDSS定义为将临床数据作为输入信息,将结论作为输出信息,有助于临床医生决策,并被认为具有“智能性”的软件。与传统将疾病知识、药品说明书等知识录入系统供医生查询浏览的知识库不同,CDSS提供的是决策支持,而非信息支持。
大多数CDSS包括三个核心要素:推理引擎、知识库和人机交互接口,在应用中,以Web式应用程序、或与医院电子病历系统和医嘱系统集成,基于知识库、自然语言处理、逻辑推理等人工智能方法,挖掘患者病历数据中的关键特征,发现知识关联,并输出对疾病风险评估、治疗方案、异常指标预警等不同知识内容,通过人工智能驱动的接口引擎,推送给医生参考。
2. CDSS发展史:CDSS研究始于20世纪50年代末,限于当时的系统集成能力,其应用多局限于学术研究或作为独立专家系统存在。20世纪70年代末,我国医学专家开始系统的研发,涉及中西医不同领域。自90年代始,CDSS的研发、应用及论文发表数量均快速增长,基于Web形式的CDSS相继出现。2009年后,欧美国家逐步在其国内推进电子病历系统的使用,为嵌入类CDSS的发展提供了良好环境,使其可无缝接入医院信息系统,契合医疗业务流程提供决策支持,更贴近临床工作需求。
罕见病领域的临床决策工具,研究起步较晚,绝大多数系统的开发集中在2000年以后,且主流应用是基于Web的交互式系统,如人类染色体不平衡和表型数据库(database of chromosomal imbalance and phenotype in humans using ensemble resources,DECIPHER)[4]、表型中心门户网站(PhenomeCentral)[5]等,允许医生在线上注册免费使用,通过患者基因型与表型数据的整合分析匹配相似病例。自2019年始,罕见病的CDSS发展迅速,单个疾病的预测模型成为研究热点,但多停留在系统模型设计或内部验证。
我国罕见病CDSS的发展受益于国家政策对智慧医院建设的强力推动,使医院电子病历的使用率大幅提升,为临床决策支持工具的应用奠定基础。智慧医疗评价体系中设置的CDSS评分项目,推动更多医院在电子病历中建设相应模块,并逐步探索多元化业务场景,罕见病辅助诊疗研究由此加速推进,自2021年起逐渐向系统嵌入类方向发展。
3. CDSS与医疗场景紧密结合的实现方式:要实现CDSS在患者治疗期间适当时间点有效传达疾病预测或诊断建议,原理主要包括以下步骤:(1)构建系统的知识图谱(包括疾病知识等)或规则引擎(如疾病推理流程),使用真实病例数据训练与验证疾病预测模型;(2)将已优化的预测模型嵌入医院信息系统,通过智能接口实时采集医疗环境中的诊疗数据;(3)医护人员进行电子病历书写等操作时,系统利用自然语言处理方法抽取患者病历文本中的实体与实体间的关系,及对应的知识图谱或规则引擎进行映射,形成一套完整的建议方案,在人机交互接口处进行提醒,使医护人员在诊疗过程中可实时获得有用信息,提高医疗质量与效率。
Gao等[6]的研究显示,在VTE的预防中,CDSS可从院内电子病历、实验室信息系统等信息平台自动收集和分析患者信息,通过提取-转换-加载、自然语言处理等技术,结合系统嵌入的VTE评估量表、临床指南,向临床医生提供及时准确的提醒和决策支持,CDSS的风险预警与预防建议采取了卡控方式,即在电子病历系统上自动弹出大窗提醒,临床医生若不接受建议,须在弹窗中输入合理的解释才可保存病历,由此加强行为干预力度。
预测单个疾病通常使用基于机器学习的CDSS,无须构建大型医学知识库,主要通过定义疾病预警规则,在人工智能算法的驱动下,采用医院多个数据源进行识别预测变量和计算结果。Al-Jaghbeer等[7]的研究显示,在多家医院的电子病历系统中部署CDSS,通过监测患者的血肌酐变化,在电子病历中相应指标旁提醒疑似急性肾损伤(acute kidney injury,AKI),并依据改善全球肾脏病预后组织(kidney disease improving global outcomes,KDIGO)指南进行AKI分级。这种通过识别预测变量自动筛查高危患者的方法,可帮助医生在繁忙的临床工作中准确把握疾病评估节点,全面挖掘高风险群体,同时省去翻阅病历、人工评估等操作,提高临床工作效率。
CDSS在医学领域已广泛应用,疾病预测(通常为单个疾病的预测)是其中较为成熟的领域,与医院电子病历集成的算法模型自2014年后持续增加,2020年后在国内进入新的应用阶段,目前已覆盖VTE、脓毒症、AKI、恶性肿瘤、心血管疾病、眼病等疾病领域,主要采用电子警报、医嘱套餐、患者数据报告等表达形式供医生查阅,且已有大量研究文献从模型性能、临床行为改善程度、患者预后等不同维度验证CDSS的干预效果。
2019年,Mayo诊所的研究人员基于454 789份患者心电图数据,利用人工智能技术制作的卷积神经网络模型[8],可通过健康人群与心房颤动患者的心电图的差异性分析,作出心房颤动的诊断,模型的曲线下面积(AUC)达0.87。2021年,Goh等[9]的研究显示,使用人工智能算法与真实临床数据构建的脓毒症预测模型,在脓毒症患者确诊前12 h获得理想预测准确率为94%,敏感度为87%,并具有将脓毒症早期检出率提高32%的能力。
在眼科领域,视网膜病变是糖尿病常见的并发症,但有较多患者不能及时筛查。澳大利亚一项使用人工智能进行糖尿病视网膜病变筛查的真实世界研究显示[10],使用CDSS自动分析患者视网膜图像,可同时筛查青光眼、视网膜病变和年龄相关性黄斑变性,系统的AUC为0.92,敏感度为96%,助力实现视网膜病变的准确快速评估。
Zhou等[11]的研究显示,通过将CDSS嵌入临床工作流程中,提醒医生VTE相关风险和及时用药,可使院内使用药物抗凝率提高14.57%,VTE发生率降低19.35%。Al-Jaghbeer等[7]对入院前无终末期肾病的528 108例者进行多中心、连续性分析发现,通过CDSS的实时风险预警与病情分级,使AKI患者粗病死率从10.2%降至9.4%,平均住院时间减少0.3 d,提示实施CDSS有助于改善患者预后,减少医疗资源消耗。
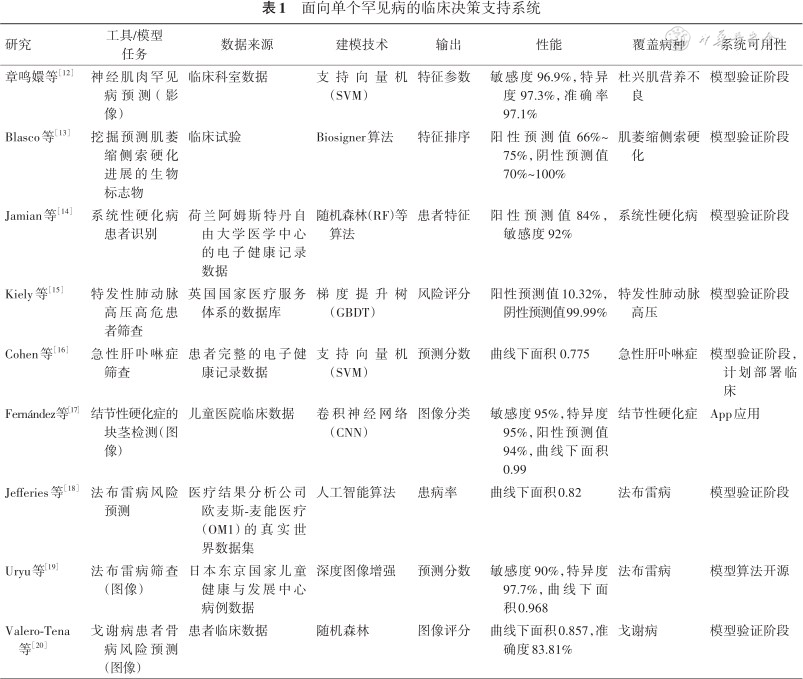
面向单个罕见病的临床决策支持系统
面向单个罕见病的临床决策支持系统
| 研究 | 工具/模型 任务 | 数据来源 | 建模技术 | 输出 | 性能 | 覆盖病种 | 系统可用性 |
|---|---|---|---|---|---|---|---|
| 章鸣嬛等[12] | 神经肌肉罕见病预测(影像) | 临床科室数据 | 支持向量机(SVM) | 特征参数 | 敏感度96.9%,特异度97.3%,准确率97.1% | 杜兴肌营养不良 | 模型验证阶段 |
| Blasco等[13] | 挖掘预测肌萎缩侧索硬化进展的生物标志物 | 临床试验 | Biosigner算法 | 特征排序 | 阳性预测值66%~75%,阴性预测值70%~100% | 肌萎缩侧索硬化 | 模型验证阶段 |
| Jamian等[14] | 系统性硬化病患者识别 | 荷兰阿姆斯特丹自由大学医学中心的电子健康记录数据 | 随机森林(RF)等算法 | 患者特征 | 阳性预测值84%,敏感度92% | 系统性硬化病 | 模型验证阶段 |
| Kiely等[15] | 特发性肺动脉高压高危患者筛查 | 英国国家医疗服务体系的数据库 | 梯度提升树(GBDT) | 风险评分 | 阳性预测值10.32%,阴性预测值99.99% | 特发性肺动脉高压 | 模型验证阶段 |
| Cohen等[16] | 急性肝卟啉症筛查 | 患者完整的电子健康记录数据 | 支持向量机(SVM) | 预测分数 | 曲线下面积 0.775 | 急性肝卟啉症 | 模型验证阶段,计划部署临床 |
| Fernández等[17] | 结节性硬化症的块茎检测(图像) | 儿童医院临床数据 | 卷积神经网络(CNN) | 图像分类 | 敏感度95%,特异度95%,阳性预测值94%,曲线下面积 0.99 | 结节性硬化症 | App应用 |
| Jefferies等[18] | 法布雷病风险预测 | 医疗结果分析公司欧麦斯-麦能医疗(OM1)的真实世界数据集 | 人工智能算法 | 患病率 | 曲线下面积0.82 | 法布雷病 | 模型验证阶段 |
| Uryu等[19] | 法布雷病筛查(图像) | 日本东京国家儿童健康与发展中心病例数据 | 深度图像增强 | 预测分数 | 敏感度90%,特异度97.7%,曲线下面积0.968 | 法布雷病 | 模型算法开源 |
| Valero-Tena等[20] | 戈谢病患者骨病风险预测(图像) | 患者临床数据 | 随机森林 | 图像评分 | 曲线下面积0.857,准确度83.81% | 戈谢病 | 模型验证阶段 |
罕见病诊断领域的CDSS应用,一般基于机器学习模型或知识库[如人类表型本体(HPO)等],通过影像分类、疾病表型和基因型分析、真实世界数据分析等方法进行疾病预测,多以分数的形式输出结果。依据现有罕见病CDSS的决策任务,其大致可分为面向单个罕见病的CDSS和面向多种罕见病的CDSS两大类。
1.面向单个罕见病的CDSS:面向单个罕见病的CDSS主要使用机器学习模型,从电子病历等真实世界数据中挖掘出隐藏的患者表型,为疾病诊断提供更丰富的知识源。Jefferies等[18]建立了一个大样本法布雷病的队列(4 978例患者),从患者病历中提取出数百个疾病表型并进行机器学习模型校准,该模型通过计算测试集中的患者表型与法布雷病表型的对应性,筛选出高危患者。结果显示,人工智能工具在使用结构化病历数据识别法布雷病方面表现出色(AUC为0.82)。Uryu等[19]在后续研究中,为解决罕见病病例不足的难题,开发了一种新的图像增强方法,对有限的图像数据进行人工扩张,提高算法模型的泛化能力,该模型可从尿沉渣图片中识别未确诊的法布雷病患者,敏感度为90%,AUC为0.968,目前研究人员已将这项算法开源在Github平台(https://github.com/huryu/DL_Fabry)。
2019年,Kiely等[15]纳入141个临床变量构建特发性肺动脉高压(IPAH)的预测模型,根据变量的重要性对测试患者进行风险评分,输出为IPAH阳性或阴性的结果,模型的阴性预测值和特异度均接近100%,提示人工智能算法可在真实世界中进行低成本的罕见病筛查,促进早期诊断。2022年,一种算法工具在戈谢病骨骼病变预测中同样获得不俗的表现[20],研究人员构建的随机森林算法模型通过分析戈谢病患者的磁共振成像(MRI),准确预测了患者发生严重骨病的可能性,同时提出“首次治疗年龄”“结构磁共振成像(S-MRI)”两项变量可能是关键预测因素,有助于医生评判患者病情进展。
此类CDSS在预测神经肌肉罕见病、急性肝卟啉症(acute hepatic porphyrias,AHP)等疾病的未知患者[12, 13, 14, 15, 16, 17, 18, 19, 20],以及在罕见病治疗效果、疾病进展、病死率等未来事件预测中,均取得令人振奋的效果,在成为嵌入类系统上呈现出巨大潜力,但这些已发表的研究绝大多数处于验证阶段,需在真实临床中应用观察。
2022年,我院在戈谢病领域先行先试,构建了嵌入电子病历系统的戈谢病临床筛诊决策支持系统,在门诊和住院的诊疗中助力医生尽早识别疑似患者,推动戈谢病患者的早期筛查早期诊断。戈谢病是溶酶体贮积症的一种,与遗传关系密切,常在幼年发病,通过筛查可尽早发现、治疗与管理,由于戈谢病临床症状缺乏特异性,极易误诊、漏诊,截至目前我国尚无大样本流行病学统计数据,对戈谢病进行早期诊断具有重要的社会意义。戈谢病早期诊断专家共识[21]提供了一个基于临床特征变量和专家权重意见构建的积分制(point scoring system,PSS)评分体系,可用于筛选识别高危戈谢病风险患者,但仅在欧美人群中进行了验证,对我国人群的适用性仍有待验证,故迫切需要建立一个符合我国人群的戈谢病筛查模型。
我院在PSS评分体系模型基础上,结合我国儿童戈谢病诊治专家共识[22],筛选了脾肿大(包括脾脏切除史)、神经系统体征(或脑电图改变)、血小板减少、肝肿大等11个戈谢病相关的临床症状/体征作为人工智能模型的预测变量,设定3个模型预警的触发条件:(1)戈谢病家族史阳性;(2)有神经系统体征或脑电图异常,同时满足另一项与戈谢病相关的症状/体征;(3)有脾肿大体征或既往脾切除史,且有发育迟缓表现或骨损害或高铁蛋白血症相关表现,并同时满足一项与戈谢病相关的症状/体征。人工智能模型可自动获取门诊/住院患者的既往就诊记录、主诉/症状、检查项目、检验指标等病历数据,将具有高危因素的患者实时推荐给医生,并建议医生下达葡萄糖脑苷脂酶检测医嘱(戈谢病诊断的金标准),同时提供戈谢病相关文献、一键会诊等功能,帮助医生快速判别,或向院内罕见病中心多学科联合诊疗团队发出会诊通知,使高危患者在早期受到关注,降低误诊和漏诊、延迟诊断的发生。该系统对11个变量的识别准确率和召回率的均值达92.15%,反映其有能力帮助医生早期识别戈谢病高危患儿,及时诊断。
目前该模型已在医院临床科室正式应用,并基于国内多家儿童专科医院的戈谢病患者数据进行优化迭代,未来将通过院间合作进行多中心应用观察,建立符合我国戈谢病人群的筛查模型,制定我国戈谢病的临床筛诊决策支持系统,为我国戈谢病患儿的筛诊提供高效、可靠的工具。由于戈谢病高危筛查模型实现了与电子病历系统的高度集成,能自动从临床业务系统中获取患者的数据,无须医生介入其演算过程,使临床能够接受与诊疗业务一体化的智能提示,促进模型的实际应用。
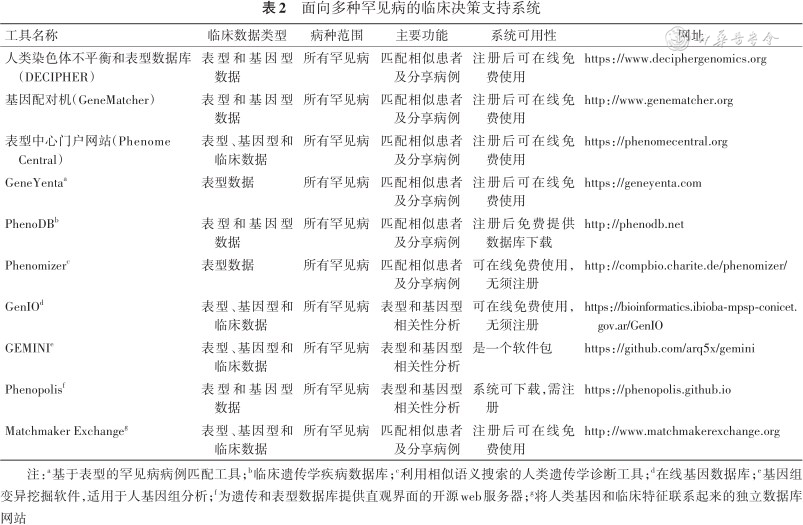
2. 面向多种罕见病的CDSS:面向多种罕见病的CDSS,主要是基于人类表型本体(human phenotype ontology,HPO)、在线人类孟德尔遗传病(online Mendelian inheritance in man,OMIM)等数据库开发的Web应用程序,如2000年以来相继出现人类染色体不平衡和表型数据库(DECIPHER)、基因配对机(GeneMatcher)、利用相似语义搜索人类遗传学诊断工具(Phenomizer)等(表2),现已构建完善,可免费供医生和研究人员使用,针对所有罕见病范围进行预测,辅助医生进行罕见病基因型与表型信息的整合分析。
面向多种罕见病的临床决策支持系统
面向多种罕见病的临床决策支持系统
| 工具名称 | 临床数据类型 | 病种范围 | 主要功能 | 系统可用性 | 网址 |
|---|---|---|---|---|---|
| 人类染色体不平衡和表型数据库(DECIPHER) | 表型和基因型数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后可在线免费使用 | https://www.deciphergenomics.org |
| 基因配对机(GeneMatcher) | 表型和基因型数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后可在线免费使用 | http://www.genematcher.org |
| 表型中心门户网站(PhenomeCentral) | 表型、基因型和临床数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后可在线免费使用 | https://phenomecentral.org |
| GeneYentaa | 表型数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后可在线免费使用 | https://geneyenta.com |
| PhenoDBb | 表型和基因型数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后免费提供数据库下载 | http://phenodb.net |
| Phenomizerc | 表型数据 | 所有罕见病 | 匹配相似患者及分享病例 | 可在线免费使用,无须注册 | http://compbio.charite.de/phenomizer/ |
| GenIOd | 表型、基因型和临床数据 | 所有罕见病 | 表型和基因型相关性分析 | 可在线免费使用,无须注册 | https://bioinformatics.ibioba-mpsp-conicet.gov.ar/GenIO |
| GEMINIe | 表型、基因型和临床数据 | 所有罕见病 | 表型和基因型相关性分析 | 是一个软件包 | https://github.com/arq5x/gemini |
| Phenopolisf | 表型和基因型数据 | 所有罕见病 | 表型和基因型相关性分析 | 系统可下载,需注册 | https://phenopolis.github.io |
| Matchmaker Exchangeg | 表型、基因型和临床数据 | 所有罕见病 | 匹配相似患者及分享病例 | 注册后可在线免费使用 | http://www.matchmakerexchange.org |
注:a基于表型的罕见病病例匹配工具;b临床遗传学疾病数据库;c利用相似语义搜索的人类遗传学诊断工具;d在线基因数据库;e基因组变异挖掘软件,适用于人基因组分析;f为遗传和表型数据库提供直观界面的开源web服务器;g将人类基因和临床特征联系起来的独立数据库网站
DECIPHER[4]开发较早,除匹配相似患者外,亦可从全基因组关联分析中解释合理的致病性遗传变异。DECIPHER使用HPO术语储存患者表型,目前存有172 000多个表型术语,51 000多个变体,已成为临床解释致病变异的常规工具。而表型中心门户网站(PhenomeCentral)[5]同样使用HPO注释患者表型,根据表型间的语义相似性筛选数据库中的相似患者,并给出潜在的共享遗传机制。这些工具通过持续增加罕见病表型术语、变体,以及医生上传、共享病例的方式,使数据库体量持续增大,辅助临床医生的罕见病认知与诊断。
此外,随着计算机视觉等技术的快速发展,医学领域开发了多种面部表型系统,自动识别患者的面部特征,为遗传诊断提供证据。一项遗传综合征面部识别研究[23]通过构建算法框架DeepGestalt,可对200余种遗传综合征的面部畸形进行量化分析,其后在502张图像的测试中准确率达91%,基于DeepGestalt框架研发的智能应用程序Face2Gen,目前已免费开放使用,成为临床诊断遗传病的重要选择。
尽管罕见病CDSS系统前景光明,但作为一种将人工智能技术与医疗数据结合的工具,在开发和实施方面仍存在CDSS普及率不足、医院数据信息孤岛、数据质量较低、缺乏框架标准等诸多挑战。
1. 医院CDSS普及率较低。CDSS作为提高患者安全和医疗质量的重要手段,许多国家将其视为电子病历系统有效使用的关键模块。然而,我国医院CDSS的普及率较低。2020年4-5月,舒婷等[29]对全国31个省市的1 013所医疗机构进行问卷调研显示,199所(19.64%)医疗机构有CDSS,其中123所(12.14%)医疗机构的CDSS在全院使用,76所医疗机构的CDSS在科室使用,426所医疗机构未使用,但已有使用计划。根据2021年全国二级公立医院和三级公立医院绩效考核数据,3 349家参加电子病历应用功能水平分级评价的医院中,0.3%的医院达到5级,三级公立医院中电子病历5级及5级以上占9.75%。而电子病历应用水平达到5级才能实现中级医疗决策支持,即“基于集成的病人信息、利用知识库实现决策支持服务”。因此推断,多数医院仍未实现中级医疗决策支持,CDSS的普及率有待提升。与此同时,受单病种质量控制、公立医院绩效考核等影响,国内医院更重视利用CDSS进行常见疾病的规范化管理,一定程度上影响罕见病CDSS的发展与实施。
2. 医院内数据孤岛。医院经过多年的信息化建设,部署的信息系统达到上百甚至几百个,基于传统的医疗模式,医院信息系统之间普遍缺少统一规划、编码,未考虑系统交互、数据共享等,数据储存在各自系统中形成信息孤岛,难以产生数据价值。2019年,广东工业大学的团队提出了一种名为Dic-Att-BiLSTM-CRF(DABLC)的神经网络命名实体识别(named entity recognition,NER)方法。DABLC应用高效的精准字符串匹配方法,将疾病实体与基于其构建的疾病字典进行匹配,结合了外部字典资源和深度注意力神经网络的优点,有助于识别罕见疾病和复杂疾病的名称,并减少标签不一致的影响[28],相似的方法已在常见病领域中广泛应用。在缺乏相关监管和标准的前提下,可探索由人工智能实现罕见病数据的标准化和结构化,进而实现数据在不同平台的互联互通。
3. 数据质量。医院在信息化建设过程中积累了海量的医疗数据,但缺乏大数据质量校验和建设规范,难以为算法模型训练及应用提供高质量的数据,尤其是罕见病的临床罕见特点,限制了大样本病例获取,需要研究人员挖掘新方法弥补这种缺陷。此外,电子病历数据的多源异构性、离散性、高维度的特性突出[24],可能会增加选择数据集成算法的难度。最后,国内人工智能技术利用偏向大而全,缺乏框架标准和监管标准;罕见病CDSS多未与医疗场景紧密结合,诊疗干预程度与临床使用率有限等,均是需要解决的问题。
CDSS的应用亦需关注提升知识库的标准程度和量级。知识库的标准程度影响计算机生成建议的特异性,关系到医生采纳该建议的概率。近年来,在全球多个国际组织机构与医疗专家的长期合作下,罕见病知识体系正在发展扩大,逐步形成了疾病知识库、表型知识库与基因知识库三大类知识资源,其中较为权威和丰富的包括基于HPO、OMIM、罕见疾病数据库(Orphanet)、人类基因组变异数据库(clinically validated variants database,ClinVar)等,为罕见病诊疗提供了重要帮助。在国内,中文临床术语体系的缺失,影响中文电子病历系统中对HPO概念的识别,限制了基因数据的分析效率。为推动HPO本土化,2016年我国成立了中文人类表型标准用语联盟(CHPO)[25],通过人类表型本体中词汇的汉化翻译,指导中文使用者的临床和科研工作。但要将新的临床证据、研究成果等新知识纳入到现有的知识库,仍是一项繁琐、专业的工作。
CDSS从早期学术研究至深入医疗领域只历经了短短几十年,本意是帮助医生将医学证据和患者信息整合到量身定制的日常实践策略中,增强其对指南的依从性。随着CDSS应用价值获得广泛认可,医院实际需求与国家政策支持推动CDSS应用广度拓展至临床科研、医务管理、医保控费等领域。如,CDSS可为临床科研提供受试者筛选、研究数据采集与稽查等服务,提高科研效率与质量。借助CDSS提取的指标数据,医院亦可实时监控医疗活动过程中的诊疗行为,改变事后抽查病历的滞后性管理模式。
辅助临床进行精准的疾病风险预测及质量管控仍是CDSS最有意义的探索方向,尤其在误诊、漏诊现象突出的罕见病领域。罕见病的尽早诊断与治疗,不仅关乎患者的人生,亦关乎整个家庭的命运,多数欧美国家已将其纳入国家发展战略。1983年,美国颁布《孤儿药法案》促进制药企业研发罕见病药物。2013年,英国发布《英国罕见病和国家战略》,指导开展罕见病患者服务及为科学研究。我国相应的政策亦在持续出台,以提高罕见病诊断与治疗的可及性。而CDSS的进步可为罕见病诊断提供技术支撑,其在各种决策任务中的表现,亦被证明可有效增强医生的疾病识别与诊断能力,提高疾病风险筛查效率与覆盖面,使疾病的早期识别具备现实性。现有罕见病的CDSS,在临床使用中需吸纳其他疾病领域的成功实践,加快推进嵌入类系统的优化及实施,将罕见病CDSS的智能提示与临床业务紧密贴合,改善临床罕见病的诊断能力。
虽然罕见病领域的CDSS发展滞后于其他疾病领域,但随着我国罕见病诊疗协作网的成立与智慧医院建设的不断推进,相关智能应用亦在不断拓展,见于诊前、诊后的环节。如陈一龙等[26]构建了一个服务患者的罕见病就医决策平台,通过人机交互智能问答,智能筛查罕见病并推荐就医渠道,为实现“针对性配医”夯实基础,改善罕见病患者的诊前服务。李景宇等[27]在院内建立了智慧化连续性健康管理体系,已为5种罕见病的200余例患者提供健康管理。
此外,随着电子病历智能化时代的到来,以及戈谢病临床筛查诊断决策支持系统的应用进展,未来可将这种医学知识工程和人工智能方法用于更多的罕见病,由点到面逐步构建全面的罕见病筛查诊断网络,并推行至县域级医院应用,助力解决优质医疗资源分布不均、总量不足的问题,提高基层的疾病早期识别能力,为罕见病的同质化筛查、诊断、治疗、管理打好基础。
陈婷, 吕海涛. 罕见病临床决策支持系统的进展和挑战[J]. 中华内科杂志, 2023, 62(7): 869-875. DOI: DOI:10.3760/cma.j.cn112138-20230321-00164.
所有作者声明无利益冲突
1.罕见病早期诊断的挑战是()
A.种类繁多,单个病种发病率低,医务人员积累相关诊疗经验较少
B.临床表型缺乏特异性
C.对疾病认知不足,临床误诊、漏诊多见
D.以上均是
2.罕见病患者临床表现多样,常见就诊科室是()
A.血液科、肾内科
B.神经内科、呼吸科
C.遗传代谢科、内分泌科
D.以上均是
3.目前CDSS已在哪种罕见病风险预测中使用()
A.法布雷病
B.戈谢病
C.肺动脉高压
D.以上均有
4.CDSS作为电子病历系统的关键模块,若实现中级医疗决策支持,电子病历应用水平至少达几级()
A.3级
B.4级
C.5级
D.6级
5.我国CDSS可用于以下哪方面()
A.临床科研
B.医务管理
C.疾病风险预测和管理
D.以上均可



























