
患者男,50岁,因乏力伴血糖升高15年、腹泻近2年就诊。病初诊断为2型糖尿病,经反复胰腺炎、胰十二指肠切除术后,出现高低血糖交替、脂肪泻等严重胰腺内、外分泌功能不全表现,辅助检查提示1型糖尿病相关抗体阴性、C肽明显下降、脂溶性维生素降低,无明显胰岛素抵抗,考虑合并胰源性糖尿病。予患者小剂量胰岛素、补充胰酶及微量营养素、少食多餐等治疗后,患者腹泻缓解、血糖控制满意。本文旨在提高广大临床医师对反复胰腺炎或胰腺术后出现胰源性糖尿病的重视,及时干预并监测,减少并发症的出现。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
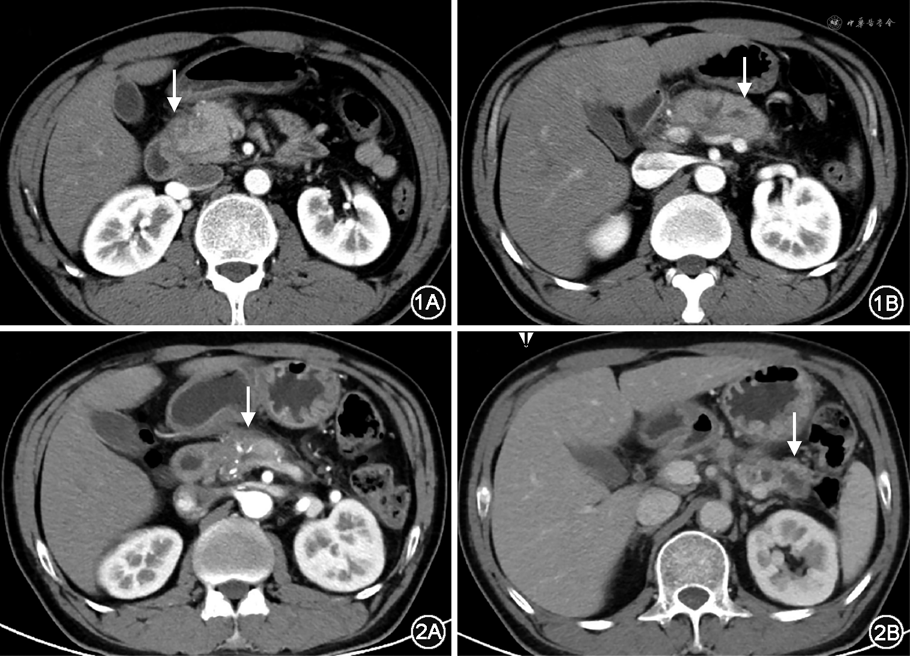
患者男性,50岁。因乏力伴血糖升高15年、腹泻近2年于2022年6月就诊北京协和医院内分泌科。2007年患者无诱因出现乏力,就诊外院发现血糖升高(具体不详),否认多饮、多尿、口干及体重下降,病初体重约75 kg(体重指数25.35 kg/m2),饮食控制不佳,喜饮酒;当地医院诊断为“2型糖尿病”,予二甲双胍及预混胰岛素(具体剂型及剂量不详)治疗,监测空腹血糖(FBG)8~10 mmol/L,餐后血糖(PBG)12~19 mmol/L,乏力较前好转,否认低血糖及糖尿病酮症酸中毒(DKA)症状。后自行停用二甲双胍。2009年患者因血糖控制不佳,调整治疗方案为:三餐前门冬30胰岛素+睡前甘精胰岛素皮下注射(剂量不详,偶有漏打),监测FBG 4~6 mmol/L,餐后2 h血糖(2hPBG)7~10 mmol/L,外院查空腹C肽0.23 nmol/L,餐后C肽0.93 nmol/L。2012年起患者每年数次于进食油腻食物后出现急性上腹痛,外院胰腺CT考虑急性胰腺炎(图1),均予保守治疗后好转,监测血糖大致同前,体重无明显变化。2020年7月再次于进食油腻饮食后出现上腹部剧痛,伴恶心、呕吐,胰腺增强CT诊断胰管结石、急性胰腺炎(图2),行胰十二指肠切除术(pancreaticoduodenectomy,PD)(胰头部切除)+胰管取石术。病理:慢性胰腺炎,伴部分腺体萎缩,间质显著纤维化和玻璃样变,可见胰管明显扩张,伴多发结石形成,周围淋巴结呈反应性增生。术后出现重度腹泻,频率可>10次/d,进餐后加重,便中可见未消化的食物残渣及油滴,无黏液、脓血,否认明显臭味,术后未再出现腹痛、呕吐。术后1个月内体重下降11 kg(75 kg➝64 kg),此后2年内进行性下降约11 kg(64 kg➝53 kg)。长期站立后易出现双下肢可凹性水肿,偶伴眼睑水肿,平卧休息可缓解。术后调整降糖方案为三餐前门冬胰岛素6、6、6 U+睡前甘精胰岛素12 U,监测血糖波动较大:腹泻稍轻时(6~8次/日)FBG 5~8 mmol/L,2 h PBG 8~12 mmol/L;腹泻较重时(10余次/日)自行停用胰岛素,血糖波动大(1.9~29 mmol/L),频繁于饥饿或腹泻后出现低血糖发作,进食后缓解。2022年1月,患者出现双小腿及足部麻木、脚踩棉花感,偶有过电样疼痛,血糖水平基本同前。2022年6月就诊本科门诊,考虑术后合并胰源性糖尿病,予胰酶肠溶胶囊150 mg、每日3次,腹泻减少为每日6~8次,便中油滴明显减少,为进一步诊治收入院。病程中,患者否认视物模糊、明显泡沫尿、肢端溃疡、偏身出汗等。否认糖皮质激素及干扰素长期应用史;无脸变圆红、皮肤紫纹,无面容改变、手足增大,无皮肤游走性红斑。精神、睡眠差,情绪略焦虑,食欲尚可,近半年每日主食约200~300 g,肉类及水果较少;近半年体重稳定,大便如上述,小便正常,夜尿0~1次。既往史:否认高血压、冠心病史,因胰管结石行手术治疗,术中输血2 600 ml。个人、婚育史:20余岁起,每日饮白酒约250~500 g、每日吸烟20~40支;配偶及2个女儿体健。家族史:否认胰腺炎、糖尿病家族史。

体格检查:血压109/68 mmHg(1 mmHg=0.133 kPa),心率63次/min,无体位性低血压,体形偏瘦(体重指数17.92 kg/m2),未见皮下脂肪萎缩,黑棘皮征(-),腹部可见多处手术瘢痕,无库欣及肢大体貌,粗测双眼视力大致正常,腹软、无压痛、反跳痛,Murphy征(-),肠鸣音稍活跃,双小腿及足背可凹性水肿,双足背动脉搏动减弱,双足浅感觉稍减退。
患者中年男性,慢性病程。起病隐匿,病初即应用胰岛素治疗,血糖控制可;随着胰腺炎反复发生,血糖逐渐控制不佳;行胰腺手术后血糖波动大,视物模糊、双足麻木疼痛逐渐加重,否认出现酮症酸中毒。入院后完善常规检查:血常规:白细胞计数5.63×109/L,血红蛋白110 g/L,平均红细胞体积96.5 fl,平均红细胞血红蛋白浓度333 g/L,余正常;铁4项:总铁结合力30.9 μmol/L(44.6~80.4 μmol/L)(括号内为正常参考值,下同),铁蛋白395 μg/L(14~307 μg/L),血清铁14.8 μmol/L(8.9~30.4 μmol/L),转铁蛋白饱和度47.8%(25%~50%),维生素B12、叶酸正常。血生化:白蛋白30 g/L(35~52 g/L),前白蛋白192 mg/L(200~400 mg/L),钾、钠、氯正常,尿酸452 μmol/L(210~416 μmol/L),γ-谷氨酰转移酶(GGT)841 U/L(10~60 U/L)。血脂:总胆固醇(TC)3.57 mmol/L,甘油三酯(TG)1.31 mmol/L,低密度脂蛋白胆固醇(LDL-C)1.77 mmol/L,游离脂肪酸405 μmol/L。尿常规:尿糖、酮体(-)。糖尿病分型:1型糖尿病抗体谱(抗胰岛素抗体、抗胰岛细胞抗体、抗谷氨酸脱羧酶抗体、抗IA2抗体)均阴性;甲状腺功能及相关抗体:三碘甲状腺原氨酸0.86 nmol/L(1.02~2.96 nmol/L),四碘甲状腺原氨酸45.01 nmol/L(55.34~160.87 nmol/L),余均正常;胰高血糖素、生长激素、胰岛素样生长因子、促肾上腺皮质激素、血皮质醇均正常。糖尿病评估:糖化血红蛋白(HbA1c)7.4%,糖化白蛋白(GA)33.8%;FBG 8.2 mmol/L、空腹C肽0.08 nmol/L;2hPBG 12.2 mmol/L、餐后2hC肽0.13 nmol/L;尿白蛋白与肌酐比值1 mg/g,泌尿系超声未见异常;眼科查眼底未见糖尿病视网膜病变。心肌酶、心电图、超声心动图正常;外周动脉彩超:双侧颈动脉、锁骨下动脉、双下肢动脉粥样硬化伴多发斑块形成,右侧颈动脉分叉处、左侧颈内动脉、双侧锁骨下动脉起始段、左侧股总动脉管腔轻度狭窄;右侧股总动脉中度狭窄。彩超提示残余尿量0 ml;肌电图:上下肢周围神经损害。
结合患者糖尿病分型及并发症评估结果,考虑本例患者的病程包括两个阶段:第一阶段为病初至胰腺炎反复发作,患者虽起病较早,但病初体型超重,不规律应用胰岛素治疗血糖控制尚可,胰岛功能尚可,无自发酮症倾向,本次入院查1型糖尿病抗体阴性,且胰腺切除约一半情况下依然保留部分胰岛β细胞功能,故无1型糖尿病或成人隐匿性自身免疫糖尿病明确证据,与2型糖尿病临床特点基本符合。患者起病时虽已大量饮酒多年,不除外可能存在亚临床期的慢性胰腺炎,对血糖升高产生一定影响,但2012年胰腺CT未见明确慢性胰腺炎征象,故胰源性糖尿病无法诊断。结合患者上述临床特点,推测疾病早期分型以2型糖尿病为主,长期大量饮酒及可疑存在的慢性胰腺炎对血糖升高可能也有一定影响。第二阶段为明确出现反复发作的急性胰腺炎、胰腺切除术后。因患者明确存在长期大量饮酒史,否认儿童期存在反复腹痛的病史及胰腺炎家族史,考虑可基本除外胰腺纤维钙化性糖尿病。
进一步完善术后并发症评估:血淀粉酶22 U/L,血脂肪酶17 U/L;便苏丹Ⅲ染色(+);粪常规+潜血(应用胰酶肠溶胶囊150 mg、每日3次):潜血(-),中量淀粉颗粒和脂肪滴;粪难辨梭菌培养、真菌培养(-)。腹部彩超:胰腺结构显示欠清,胰腺区可见导管样回声,探及长度约2.8 cm。腹部CT平扫+胰腺薄扫:术后改变,胰管内引流管置入后改变,胰腺体尾部形态不规整,多发低密度影及钙化灶,结合病史符合慢性胰腺炎表现。微量营养素及微量元素测定:维生素E 4.6 mg/L(5.5~17.0 mg/L),维生素A 0.20 mg/L(0.33~0.78 mg/L),铜360 μg/L(750~1 450 μg/L),钼2.14 μg/L(0.30~2.00 μg/L),硒26 μg/L(70~150 μg/L),锌425 μg/L(660~1 100 μg/L),钴、铬、锰、镍、锶均正常。钙磷代谢:血钙2.27 mmol/L,血磷1.41 mmol/L,25羟维生素D 56.8 nmol/L(75.0~125.0 nmol/L),甲状旁腺激素3.32 pmol/L,β-胶原降解产物测定0.46 μg/L(0.26~0.51 μg/L),总1型胶原氨基端延长肽50.1 μg/L(15.1~58.6 μg/L),24 h尿钙3.58 mmol。胸腰椎侧位X线片:部分腰椎高度稍减低,退行性变。骨密度:股骨颈T值-2.0;全髋T值-1.9;腰椎(L)1~4 T值-2.3。
患者否认胆囊结石、高钙血症,结合其长期大量饮酒史及油腻食物进食较多,考虑为酒精性胰腺炎可能性大、脂源性胰腺炎不除外。患者反复胰腺炎及胰腺手术治疗后血糖波动较大,需高度怀疑合并胰源性糖尿病。Ewald和Bretzel[1]既往总结的胰源性糖尿病诊断标准如下:(1)主要标准(需全部符合):①存在胰腺外分泌功能不全;②胰腺病变影像学证据;③通过自身免疫指标排除1型糖尿病。(2)次要标准:①胰岛β细胞功能受损;②无明显胰岛素抵抗;③肠促胰素分泌障碍;④血清脂溶性维生素水平降低。本例患者第二阶段病程明确存在脂肪泻、消瘦,影像学及病理提示胰腺存在长期炎症,1型糖尿病相关抗体谱阴性,满足全部主要诊断标准。同时患者空腹及餐后C肽明显下降,提示胰岛β细胞功能受损;体形消瘦、无黑棘皮征、胰岛素应用量较少,提示无明显胰岛素抵抗;维生素A、E、D均降低;满足3条次要诊断标准。故本例患者目前可明确诊断胰源性糖尿病。
胰源性糖尿病是继发于胰腺外分泌疾病的一种特殊类型的糖尿病,也称为3c型糖尿病(type 3c diabetes mellitus),约占所有糖尿病住院患者的9%[2]。慢性胰腺炎和急性胰腺炎为胰源性糖尿病最常见的原因,其他原因包括胰腺癌、胰腺手术切除、囊性纤维化、自身免疫性胰腺炎、血色病等。PD术后新发胰源性糖尿病约占16%[3];术前已患糖尿病的患者中,约一半患者术后糖尿病病情加重[4]。
本例患者既往反复出现胰腺炎,手术虽保留约一半胰腺,但残留的胰腺内、外分泌功能仍较差,胰腺CT提示剩余胰腺组织亦存在慢性胰腺炎影像学表现。因此,多因素共同导致本例患者出现胰源性糖尿病。慢性胰腺炎导致胰源性糖尿病的致病机制主要包括:(1)胰岛素分泌减少:慢性胰腺炎所致炎症环境、胰腺内炎症因子及细胞因子浓度的增加,可抑制胰岛β细胞功能[5, 6, 7, 8];同时,胰腺外分泌组织纤维化,可破坏胰岛组织,进而影响胰岛素的分泌[9, 10]。(2)肝脏胰岛素抵抗:胰腺分泌的胰多肽可调节肝胰岛素受体的表达和敏感性,慢性胰腺炎、胰腺癌等多种常见的胰源性糖尿病原因均可导致胰多肽水平下降[10, 11];此外,胰腺炎可导致促炎信号通路激活,加重胰岛素抵抗[12, 13]。(3)肠促胰素作用改变:胰源性糖尿病患者对胰高糖素样肽-1(GLP-1)的敏感性似乎无明显下降,而易对葡萄糖依赖性促胰岛素多肽(GIP)产生抵抗;同时胰腺炎患者存在营养吸收障碍,而营养吸收受损可能导致肠促胰素的分泌减少,进而导致餐后胰岛素分泌减少,但目前研究结论尚不统一。
本例患者血糖波动较大、易出现高低血糖交替,但病程中未出现DKA。胰源性糖尿病患者低血糖发作的发生率高达79%[14]。导致血糖波动的因素主要包括:胰高血糖素不足[15]、胃肠道吸收功能差[16]、胰腺外分泌功能受损,同时因此类患者胰高血糖素分泌亦下降,脂肪储备少,故不易出现DKA。
除胰源性糖尿病外,PD术后还可出现胰腺外分泌功能不全表现,包括肠道消化功能受损(脂肪泻、胀气和消化不良)和/或营养不良(体重减轻、脂溶性维生素及矿物质缺乏等)。术后超过一半的患者需要补充外源性胰酶[17]。此外,PD术式中胃窦切除导致内因子丢失,影响维生素B12的吸收[18];胰酶减少会引起脂溶性维生素缺乏,如维生素A、D、E、K[18];部分消化道切除会导致经该部位吸收的矿物质缺乏[19],如铁(多于空肠上段吸收)、铜(多于胃部及小肠上部吸收)、锌(多于十二指肠、小肠吸收)。针对上述问题,目前临床可实现的评估方法包括:(1)营养不良评估:第一步,使用NRS 2002工具进行营养风险筛查,营养风险筛查阳性患者NRS 2002≥3分;第二步,通过营养不良评定标准诊断有无营养不良;第三步,诊断是否属于重度营养不良[20]。(2)其他实验室指标:总白蛋白、白蛋白及前白蛋白,血红蛋白、绝对淋巴细胞计数[21],血清淀粉酶及脂肪酶,粪便弹性蛋白酶1 的酶免疫测定(评估胰腺外分泌功能的最佳检测方法[14])、粪便常规及苏丹Ⅲ染色,视黄醇结合蛋白、转铁蛋白、叶酸、微量元素及脂溶性维生素水平,骨密度、身体成分分析等。经评估,本例患者存在营养风险(NRS-2002 3分),因其体重下降约30%,进一步评估其为重度营养不良,同时合并低白蛋白血症、维生素A、D、E不足以及多种微量元素缺乏。
PD术后管理及治疗主要包括:(1)胰腺外分泌功能障碍[14]:补充胰酶、少食多餐并避免难以消化的食物。胰酶替代从低剂量开始,根据饮食脂肪含量、大便性状及症状按需逐渐加量;不超过150 mg‧kg-1‧d-1,分3~4次口服,建议少食多餐并避免难以消化的食物[21]。(2)胰源性糖尿病:予小剂量胰岛素控制血糖,避免出现低血糖。北京协和医院一项全胰切除术后随访10年的研究结果显示,予患者胰岛素30.5 U/日(0.48 U/kg体重),88%患者可达正常HbA1c,平均每月4次低血糖[22]。另一项研究显示,基础胰岛素用量约0.4 U/kg,占总胰岛素应用量的30%[23]。其他药物治疗方面,目前尚无针对胰源性糖尿病的降糖药物有效性安全性研究,均需慎用。(3)营养素缺乏:保持充足能量摄入,约35 kcal‧kg-1‧d-1;平衡蛋白饮食,按需补充乳清蛋白粉;脂溶性维生素缺乏方面,需监测目前水平后按需随餐补充。
本例患者治疗方面:(1)糖尿病方面:因患者胰岛功能差,予基础+餐时胰岛素治疗,因其易出现夜间及晨起低血糖,故予甘精胰岛素调整为晨起6 U联合门冬胰岛素三餐前6、6、4 U皮下注射。监测血糖:FBG 3.9~7.4 mmol/L,2hPBG 6.3~14.3 mmo/L。糖尿病神经病变方面,予甲钴胺片0.5 mg、每日3次,复合维生素B 1片、每日2次治疗。(2)腹泻方面:逐渐加量胰酶肠溶胶囊至600 mg、每日3次,腹泻次数下降至3~4次/日,大便基本成形,复查苏丹Ⅲ染色(-)、便常规未见油滴及淀粉颗粒。(3)营养不良方面:予以补充碳酸钙200 mg、每日3次,维生素D3 800 U、每日1次,复合维生素B 1片、每日1次及乳清蛋白粉30 g、每日1次。监测血红蛋白116 g/L,白蛋白34 g/L,体重2周内增加约2 kg。
本例报道的不足之处在于,由于起病时间较为久远,既往诊疗经过(包括病初胰岛素抵抗情况、胰腺影像学、具体治疗方案及疗效等)均难以追溯,故病初糖尿病与胰腺疾病相关性目前难以完全明确。
综上所述,本文报道了1例病初诊断2型糖尿病可能性大的患者,经反复胰腺炎、PD术后出现严重胰腺内、外分泌功能不全,结合组织病理,最终明确合并胰源性糖尿病的病例。该患者胰岛β细胞功能下降原因较为复杂,除PD术外,既往长期慢性胰腺炎及反复出现的急性胰腺炎亦存在较大影响。提示临床医师在胰腺炎及胰腺手术后需积极对患者胰腺内、外分泌功能进行评估,及时干预并监测,以减少并发症的出现。
宋桉, 张睿, 池玥, 等. 第501例——血糖升高、反复胰腺炎、胰十二指肠切除术后、营养不良[J]. 中华内科杂志, 2023, 62(7): 891-895. DOI: 10.3760/cma.j.cn112138-20221120-00870.
所有作者声明无利益冲突



























