
镶嵌体(mosaicism)是指个体存在两个或以上遗传学差异的细胞类型的现象。镶嵌体主要发生于受精卵形成后(postzygotic)发育分化过程中细胞基因突变。并由于基因突变发生于细胞发育不同时间或阶段,因而其遗传学变异细胞似“马赛克”式(mosaic)镶嵌分布于机体组织或器官,其相关疾病呈现为节段性、区域性、灶性分布,即镶嵌式疾病(mosaic disease)。镶嵌体现象从本质上揭示了遗传性疾病、发育性疾病、肿瘤,以及细胞和机体衰老之间的共性、联系与差异性。尤其体细胞镶嵌性基因突变从分子水平揭示了发育畸形及相关综合征、错构瘤、肿瘤发生基础,以及之间的关联性,为重新认识这些疾病提供了新的基础。镶嵌体现象涉及发育、肿瘤及分子病理学多个病理领域。本文将简述镶嵌体基本概念,以体细胞镶嵌性疾病为主,概述其特点,讨论其与散发肿瘤的关系,以及病理学及分子病理学检测等问题。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,2022年从第1期至第10期共刊发10篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获5分。
镶嵌体(mosaicism)是指个体存在两个或以上遗传学差异的细胞类型的现象,普遍存在于多细胞生物体。其遗传学改变(基因突变或染色体倍体异常)通常发生于受精卵的发育分化过程中,因而其遗传学变异细胞似“马赛克”式(mosaic)镶嵌分布于机体组织或器官,其相关疾病呈现为节段性、区域性、灶性分布,即镶嵌式疾病(mosaic disease)[1, 2]。镶嵌体主要来自受精卵形成后(postzygotic)细胞的有丝分裂过程中,基因突变发生的时间或阶段性而影响不同细胞谱系,发育早期突变影响谱系多,而后期则受累谱系少。镶嵌体(mosaicism)与嵌合体(chimerism)有着根本的区别,后者是指个体有异体细胞的嵌入,如妊娠时不同受精卵之间、胎儿与母体之间细胞的相互输入,以及器官、骨髓移植、输血等形成医源性嵌合体[3]。
人们在早期对低等生物的研究中发现了镶嵌体现象,并且在人体疾病中也观察到一组有着与发育相关的分布呈节段性、区域性的皮肤及血管疾病,从而提出镶嵌式基因突变的可能。在最近几年,随着高通量测序等检测技术的运用,对镶嵌体及其疾病有了更全面和飞跃的认识[4]。镶嵌体现象揭示了遗传性疾病、发育性疾病、肿瘤,以及细胞和机体衰老之间的共性、联系与差异。尤其体细胞镶嵌性基因突变从分子水平揭示了发育畸形及相关综合征、错构瘤、肿瘤发生基础,以及之间的关联性。不仅如此,也提示体细胞基因组在生命过程中的动态改变,并可能为器官(如中枢神经系统、肝脏)器官实现功能成熟和多样性机制[4, 5, 6]。因此,镶嵌体现象涉及围产期、皮肤、神经、儿科及各系统肿瘤病理及分子病理学多个病理领域。
本文将就镶嵌体基本概念,以体细胞镶嵌性疾病为主,概述其特点,讨论其与散发肿瘤的关系,分析其相关病理学及分子病理学检测等问题。
1.镶嵌体类型:由于基因突变可以发生于受精卵发育中的各种阶段,因此,镶嵌体式突变可以为局限于体细胞、生殖细胞、或者前两者的混合,呈现各自特殊临床表现和遗传子代的可能性(表1,图1)。(1)体细胞镶嵌体(somatic mosaicism):为经典的镶嵌体类型,即受精卵在有丝分裂及分化过程中个别体细胞的基因突变,可以发生于胚胎发育的不同阶段、不同分化潜能的体细胞,因此,其特征是基因突变仅局限于部分体细胞,其突变不具遗传性,随着个体的死亡而消失[6, 7]。(2)性腺镶嵌体(gonadal mosaicism):即局限于性腺(睾丸或卵巢)生殖细胞的镶嵌体。受精卵在有丝分裂向原始生殖细胞分化过程中的生殖细胞基因突变,局限于个体的性腺细胞,通常具有遗传性。但与体系镶嵌体形成相似,生殖细胞的发育阶段基因突变发生的时间性也影响其遗传性频率[8]。(3)性腺体系镶嵌体(Gonosomal或Somatogonadal mosaicism):即基因突变的镶嵌体存在与性腺与体细胞,一般为受精卵的早期分裂形成,其变异分布于原始生殖细胞及体细胞,具有遗传性[6, 7]。(4)局限胎盘镶嵌体(confined placental mosaicism,CPM):一种较为特殊的镶嵌体,主要为胎儿与胎盘之间染色体数目不一致(多为常染色体三体),非整倍体局限于胚胎外成分(绒毛、滋养叶细胞),而胎儿正常[9]。
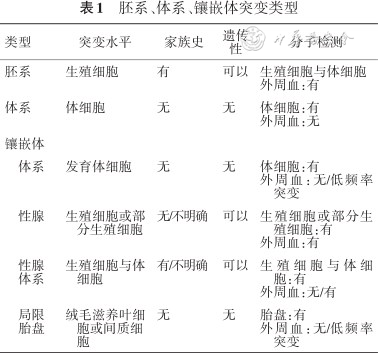
胚系、体系、镶嵌体突变类型
胚系、体系、镶嵌体突变类型
| 类型 | 突变水平 | 家族史 | 遗传性 | 分子检测 |
|---|---|---|---|---|
| 胚系 | 生殖细胞 | 有 | 可以 | 生殖细胞与体细胞 外周血:有 |
| 体系 | 体细胞 | 无 | 无 | 体细胞:有 外周血:无 |
| 镶嵌体 | ||||
体系 | 发育体细胞 | 无 | 无 | 体细胞:有 外周血:无/低频率突变 |
性腺 | 生殖细胞或部分生殖细胞 | 无/不明确 | 可以 | 生殖细胞或部分生殖细胞:有 外周血:有 |
性腺体系 | 生殖细胞与体细胞 | 有/不明确 | 可以 | 生殖细胞与体细胞:有 外周血:无/有 |
局限胎盘 | 绒毛滋养叶细胞或间质细胞 | 无 | 无 | 胎盘:有 外周血:无/低频率突变 |
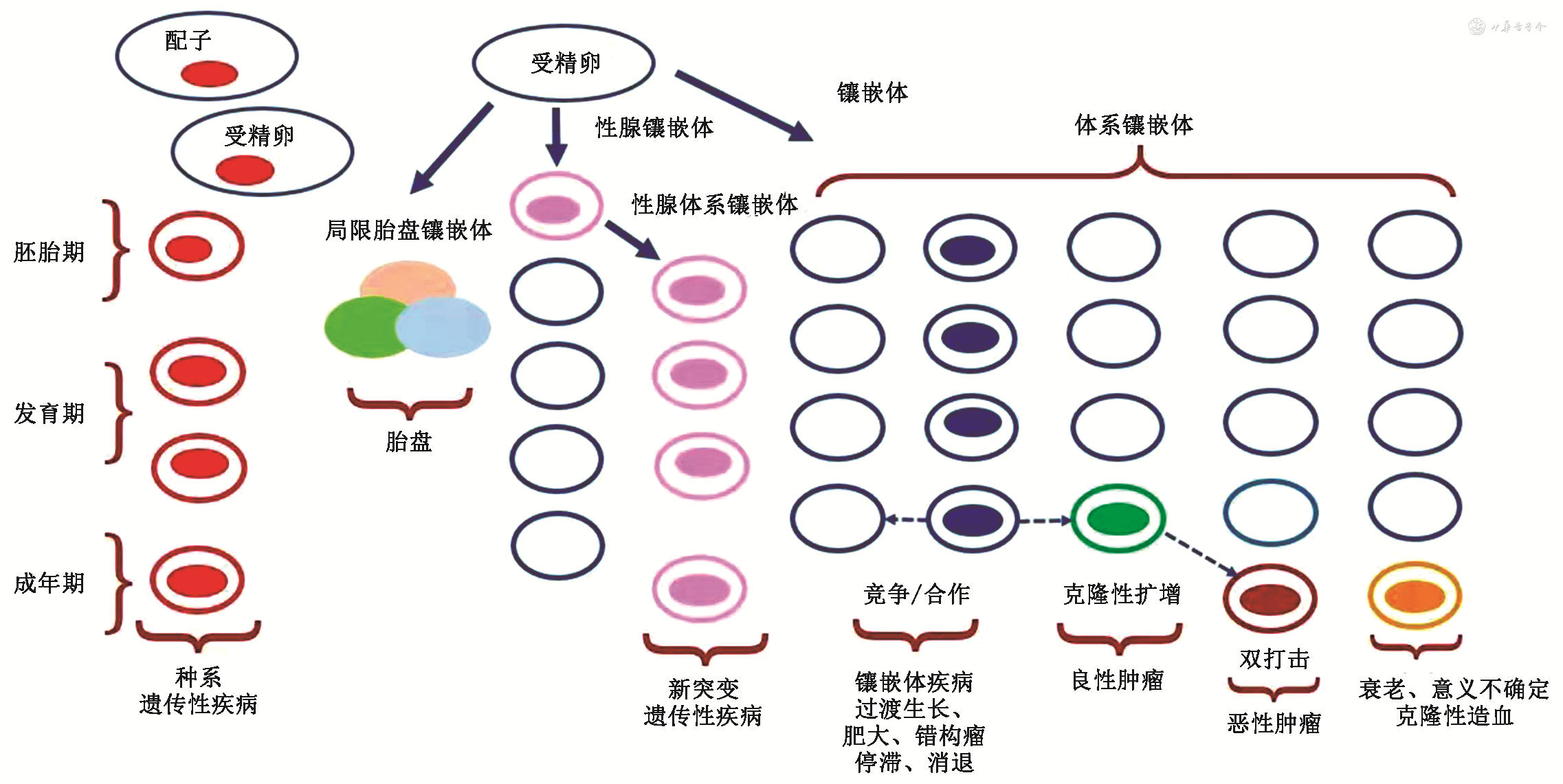

2.镶嵌体基因突变发生水平与特点:镶嵌体涉及的分子改变以各种方式基因突变或染色体倍体、结构异常,少数情况还有表观遗传学、线粒体DNA突变等[2,4]。体细胞镶嵌性疾病主要为DNA突变,以点突变为主,少数为结构变异(基因易位,缺失)。镶嵌体基因突变通常为非致死性(至少对胚胎发育),多数突变为功能获得性突变,少数为功能失活性,有时致病作用需要第2个等位子突变才致病(two-hits)。体细胞镶嵌体基因突变在突变方式、突变热点方面与胚系突变、散发肿瘤突变通常一致[1,3]。
体细胞镶嵌性疾病主要有下列几类:第一,遗传性疾病的体细胞镶嵌体形式:当常染色体显性遗传性疾病的致病基因其突变发生在体细胞时,即表现为镶嵌式疾病,临床病变呈明显的区域性与节段性,病变累及一个或几个组织或细胞群体,不具遗传性,如神经纤维瘤病(Neurofibromatosis Type 1,NF1);第二,具有遗传性与镶嵌式两种方式,而以体细胞镶嵌体疾病多见:如下述“RASopathies”;第三,仅为体细胞镶嵌体疾病形式:这类基因突变可能对生殖细胞具有致死作用而仅能表现为体细胞镶嵌体疾病,主要有PI3K、AKT、IDH1/2、GPCR基因突变相关疾病。这些信号通路基因的作用主要为调节细胞生长和增殖并具有功能上的联系,病变有重叠性。其临床表现为皮肤色素斑或痣、组织过生长性肥大、错构瘤,甚至恶性肿瘤。
1.神经纤维瘤病(NF1):为最常见常染色体显性遗传性疾病之一,胚系NF1基因突变临床表现为多发特征性神经纤维瘤,以及多样性皮肤病变,如咖啡牛奶斑、腋下与腹股沟雀斑、Lisch结节。其他还可出现嗜铬细胞瘤,视神经胶质瘤,特异蝶翼、椎体、胫骨等骨病变[10]。镶嵌体(或节段性,Segmental)神经纤维瘤病来自NF1基因突变发生胚胎时期时部分体细胞突变(也可累及性腺,形成性腺体系镶嵌体)。病变呈节段性分布,局限于1~2个躯体节段。在同一患者病变类型也相对单一,如仅皮肤牛奶咖啡斑或雀斑,仅皮肤结节性神经纤维瘤,或仅丛状神经纤维瘤[11]。
2.RASopathies:为一组新近确认涉及RAS/RAF/MEK/ERK通路的综合征,具有胚系和镶嵌体突变两种形式。胚系“RASopathies”累及多器官且具有遗传性,主要有:努南(Noonan)综合征(PTPN11、SOS1、KRAS、NRAS、RAF1基因),弥漫性黑痣综合征(LEOPARD;PTPN11、RAF1基因),先天性水痘综合征(HRAS基因),自身免疫性淋巴增生性综合征(NRAS基因),CFC(Cardio-facio-cutaneous)综合征(BRAF、KRAS、MAP2K1、MAP2K2基因)等[10]。镶嵌体RASopathies主要为RAS基因突变,多为涉及表皮细胞异常增生性痣综合征,包括:角质形成表皮痣(HRAS、NRAS、KRAS基因),皮脂腺痣(HRAS、KRAS基因),皮脂腺痣综合征(HRAS、KRAS基因)等,病变呈局限及节段性分布[11]。
3.PI3K/PTEN/AKT/TSC/mTORC1信号通路基因突变:在本组信号通路疾病中,PI3K AKT与IDH突变对于生殖细胞发育为致死性,因此仅表现为体细胞镶嵌体疾病,其突变位点、方式与其在人散发肿瘤中相一致[12, 13]。(1)PIK3CA突变:导致PROS综合征(PI3K-related overgrowth syndrome),主要表现为节段性、局部过度生长、异常血管增生、指端异常、脑皮质畸形以及结缔组织异常增生。可以有CLOVE综合征(先天性脂肪瘤样过度生长、血管畸形、表皮痣),巨脑-毛细血管畸形综合征,纤维脂肪增生,半侧巨脑等[13]。(2)AKT1/2/3突变:均可导致相关表现为皮肤、骨骼,脂肪及中枢神经组织畸形、过度生长等症候群。如AKT1体细胞镶嵌体突变与普洛提斯症候群(Proteus syndrome)综合征,表现为非对称、进行性、错构性过度生长综合征:过度骨化、脑迴形结缔组织痣、血管畸形、囊性肺疾病[13]。(3)软骨瘤及软骨瘤病:异柠檬酸脱氢酶IDH1与IDH2激活突变导致Ollier病或Maffucci综合征以多发性内生性软骨瘤、血管畸形、组织过度生长为特征,均为散发病例,没有家族性和胚系突变(偶有报道)[14]。在本组信号通路疾病中PTEN和TSC1/2基因突变既可为胚系,也可为体细胞镶嵌式突变。如PTEN胚系突变错构瘤综合征与镶嵌体Solamen综合征,胚系TSC突变的多发性神经皮肤错构瘤与镶嵌体TSC突变局限或节段性错构瘤[13]。
4.G蛋白偶联受体信号通路(G-protein coupled receptor,GPCR)基因突变:细胞膜GPCR突变多为体系镶嵌突变,既往病理学对这类疾病多认为是发育异常或瘤样病变。(1)脑三叉神经血管瘤综合征(Sturge-Weber syndrome,SWS):是一种累及颜面部皮肤、中枢神经系统及眼部的神经皮肤综合征,为GNAQ基因突变(部分为GNA11)所致。表现为颜面部葡萄酒色斑、脉络膜以及软脑膜血管畸形,甚至葡萄膜黑色素瘤。其分布近似三叉神经范围[15]。(2)先天性血管瘤(congenital hemangioma,CH):为GNAQ或GNA11基因体系镶嵌突变所致。此类血管瘤(孤立皮肤斑块或突起,血管扩张),出现于宫内妊娠12周。出生后临床上可有两种过程:RICH(rapid involuting CH)型,于出生后1年可大部分消退,而NICH(non-involuting CH)型则可持续存在。GNAQ或GNA11基因突变见于成人血管瘤[16]。(3)骨纤维结构不良(fibrous dysplasia,FD):由GNAS突变导致。受精卵早期的GNAS基因突变导致McCune-Albright Syndrome:即多骨纤维结构不良,并有功能亢进性内分泌疾病以及皮肤牛奶咖啡斑。而后期基因突变则多为局限于单骨的纤维结构不良[17]。
体细胞镶嵌体疾病本质是部分体细胞基因突变所致,因此,从广义上肿瘤也是一种镶嵌体疾病[18, 19]。尤其是两者涉及相同的癌基因与肿瘤抑制基因突变,具有相同的基因突变谱,并且镶嵌体疾病相当部分可有良性肿瘤甚至恶性肿瘤。但体细胞镶嵌体疾病与散发性肿瘤还是有一些区别:(1)基因突变时间:镶嵌体基因突变为受精卵发育中,影响一个或几个细胞群体,而散发性肿瘤为一个发育成熟体细胞基因突变克隆性增生形成。(2)镶嵌体一般为单个基因突变(可以2次突变),而恶性肿瘤通常具有多个基因的累积突变。(3)镶嵌体基因突变必须对发育细胞无致死作用,其突变谱更具有选择性,而肿瘤基因突变多于成熟细胞,具有更广泛基因突变谱。(4)临床表现方面,镶嵌体一般为区域性、节段性分布,其病变与原组织关系密切,组织病理为与发育畸形相关的错构瘤、过度生长、或结构异常,多个器官或组织综合征(症候群),且多为良性病变。而即使良性肿瘤也与原发组织无结构联系,细胞类型单一,而恶性肿瘤可失去与原组织的结构与分化特征。(5)部分镶嵌体疾病可以随机体生长发育而停滞或消退,而肿瘤一般不可逆转。但镶嵌体疾病与散发肿瘤有重叠性,如两者涉及相同的基因与突变谱,在病理上畸形、过度生长、良性肿瘤、恶性肿瘤之间有重叠。如在血管病变中镶嵌体疾病与散发肿瘤的关系也体现非常明显:镶嵌体血管疾病主要以儿童先天性血管瘤、伴有血管畸形过程生长综合征,其血管病变主要为血管、淋巴管扩张、增多,其结构与正常血管相似,并且部分血管疾病可以停滞或消退,而成人基因突变所致血管肿瘤则主要为内皮细胞分化的各种形态,可无正常血管结构,一般呈进展性[15, 16]。然而,不难理解,儿童恶性肿瘤与镶嵌体早期基因突变具有较为密切关系,其基因突变可能较早发生于组织发育中,因而胚胎性肿瘤多,但这方面的证据尚待积累。同时,部分成人肿瘤可能始于胚胎发育时的基因突变。同时,镶嵌体与肿瘤的联系还体现在以下方面。
1.克隆性镶嵌体(clonal mosaicism)形成与肿瘤发生:突变细胞如果没有形成一定数量构成的群体时一般技术很难检测,而当扩展到一定细胞数量才能被临床所发现,形成所谓克隆性镶嵌体(clonal mosaicism)。目前已经证实克隆性镶嵌体可能为疾病的前驱改变。如约50%人慢性淋巴细胞性白血病(CLL),部分淋巴细胞第13号染色体缺失可以在CLL发生前出现,最长可达14年。其他如滤泡性淋巴瘤、套细胞淋巴瘤可以于诊断前长期携带染色体易位[20]。近年来发现,随年龄增长出现的造血干细胞基因突变,并且形成克隆性细胞群体的现象,所谓意义不确定克隆性造血(clonal hematopoiesis of indeterminate potential,CHIP)。CHIP的存在与骨髓异常造血及白血病的早期发病相关,并且这类骨髓在移植后会较快形成白血病而影响骨髓移植的效果[20, 21]。
2.癌化场效应(cancerization field effects):癌化场效应是指恶性肿瘤所在周围组织或者器官具有肿瘤发生的倾向,临床上通常可出现多发肿瘤、相邻部位复发肿瘤。镶嵌体为此现象提供了一种解释,这些肿瘤周围组织中已经具有基因突变细胞的镶嵌式分布,及构成所谓癌化土壤(oncogenic soil),酝酿癌细胞形成(cancer seed)[19]。
随着分子检测技术灵敏度的不断提高,愈来愈多的克隆性镶嵌体可以被发现,将为肿瘤发生、癌前病变的确定、早期筛查与诊断提供帮助。
1.大体病理学:镶嵌体疾病呈现解剖学部位的区域性或节段性表现,尤其在体表,并累及多个细胞谱系,如表皮、黑色素细胞、周围神经细胞,以及内皮细胞、脂肪、纤维组织等。常表现为:(1)皮肤病变:表皮痣、皮肤色素斑,血管畸形所致葡萄酒色斑;(2)肢体部分非对称性、非均衡性肥大;(3)错构瘤或良性肿瘤局部肿物。
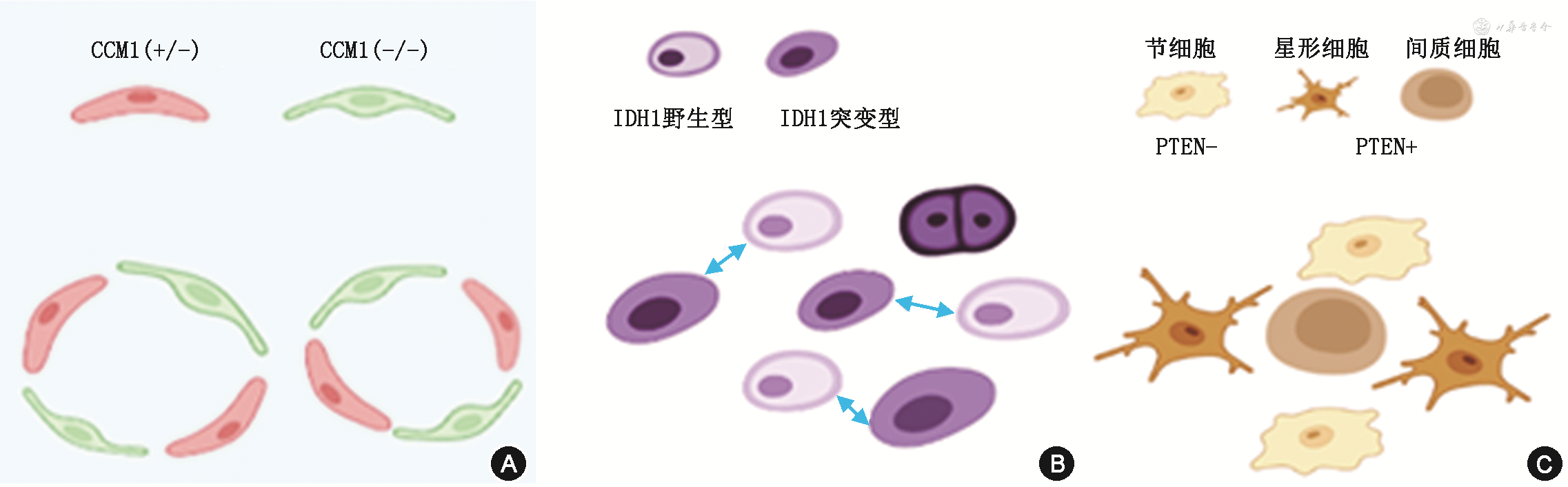
2.组织病理学:镶嵌体疾病组织学导致良性肿瘤或者恶性肿瘤其组织病理学与散发肿瘤基本一致。其他主要为过度生长改变,如表皮或附属器痣、色素痣,血管畸形、脂肪及纤维结缔组织错构瘤等。近年来,利用免疫组织化学对镶嵌体疾病突变基因的组织检测发现一些特点。Rath等[22]对一项脑海绵状血管畸形(cerebral cavernous malformations,CCMs)病例研究表明:在一胚系CCM1患者血管内皮细胞发现CCM1的第二次突变,并且血管病变中的内皮细胞具有胚系CCM1杂合突变(+/-),以及CCM1双突变内皮细胞(CCM1-/-)所内衬,表明其CCM1的二次突变所致,也表明病变组织有突变与非突变细胞构成(图2A)。另外,利用抗IDH1 R132H突变抗体检测Ollier病患者内生性软骨瘤显示其肿瘤细胞部分为IDH1 R132H突变阳性,与野生型肿瘤细胞呈镶嵌式分布(图2B)[23]。而镶嵌式PTEN失活突变导致的胶质神经元性错构瘤(glioneuronal harmatoma)组织中,仅节细胞失去PTEN表达,而星形细胞及内皮细胞则具有PTEN的表达(图2C)[24]。因此,这些有限的研究提示镶嵌体病变可能为突变与非突变细胞混合构成,形成“马赛克式”改变,表现为所谓“发育畸形”。类似这样肿瘤与非肿瘤成份共同的现象也存在于部分良性肿瘤,如乳腺纤维腺瘤、骨巨细胞瘤,但一般此类肿瘤中肿瘤细胞与非肿瘤细胞在类型有所不同[25, 26]。随着镶嵌体基因突变的免疫组织化学检测抗体的开发,如PIK3CA、AKT1等,相信有关镶嵌体疾病的组织病理学特点会有更多的发现。
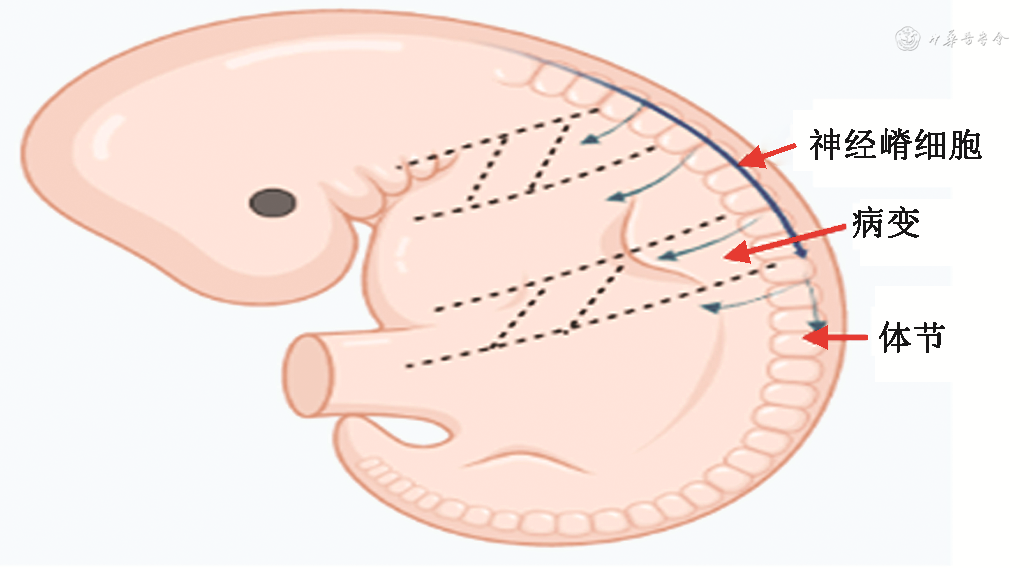
3.体细胞镶嵌性疾病发生机制:镶嵌体疾病的区域性或节段性表现可能与胚胎发育时期体节(somites)的形成,以及多潜能分化能力的神经嵴细胞(neural crest cells)在各体节的迁入有关(图3)。基因突变的细胞在特定体节发育不同阶段形成各区段的骨、软骨、肌肉的病损,而神经嵴细胞迁移进入不同的体节分化形成黑色素细胞、神经纤维,以及内皮细胞、脂肪、纤维组织等也导致区域性病变[27, 28]。如将突变GNAS导入鸡胚的体节可以诱导类似的体节性表型,类似于进行性骨性异常增生患者GNAS突变导致的皮肌节分布样的异位骨化[29]。而PIK3CA-突变相关过度生长症候群的不同临床解剖学方式与其基因-突变发生时间有关[30]。镶嵌体疾病基因突变所致细胞过度生长分子机制与肿瘤相似。但也有一些差异,部分镶嵌体疾病与年龄和发育相关,如前述先天性血管瘤(CH)始于宫内发育期,但出生后其病变呈现两种不同过程,RICH于出生一年内病变消退,而NICH却持续存在,提示其他基因改变会影响突变细胞的功能表型[18]。部分骨纤维结构不良也呈现随年龄增加而出现病变停止的现象,可能为GNAS激活突变干扰骨骼干细胞的自我更新(self-renewal)通路所致,当病变持续时基因突变细胞失去自我更新,通过凋亡消失,而无突变的正常细胞得以生长,逆转FD表型[31, 32]。因此,在镶嵌体疾病中基因突变细胞尚处于相对优势(relative dominance),其激活信号通路也刺激周围同类细胞及正常细胞产生发育畸形或错构瘤表现,而随着克隆竞争取得绝对优势(absolute dominance)后则发展为克隆性的良性肿瘤性病变。因此,在基因突变的时间与空间、突变基因的是否具有主导性、突变细胞与非突变细胞的关系方面与肿瘤具有一些差异,肥大、畸形、错构瘤与肿瘤为形成一个疾病的谱系改变,在一定条件下可以转化(图1),其具体详细过程尚待阐明。

体细胞镶嵌体疾病本质为基因突变所致,所有分子检测方法均适用,如PCR、二代测序、荧光原位杂交检测染色体异常等。但由于镶嵌体为部分细胞的基因突变,因此其检测通常需要高度灵敏的分子检测技术[33],并根据不同镶嵌体类型,采取相应的病变组织、外周血、唾液、生殖细胞(睾丸穿刺)进行检测(表1)。同时,家族遗传信息在鉴别中极为重要:体细胞系无家族史,性腺体系混合型可有家族史,一般只有经大量流行病分析无家族式发病情况下才能确定为体系镶嵌体。另外,在组织病理标本基因突变相应免疫组化检测也值得开展。
体细胞镶嵌体基因突变的存在,尤其是克隆性镶嵌体形成将影响甚至干扰临床分子检测。年龄相关体细胞基因突变,在计算TMB(tumor mutation burden)时应加以考虑[34],而液体活检、肿瘤早期筛查也应考虑镶嵌体的影响。滋养叶细胞的镶嵌体可使NIPT检测时可出现假阳性结果,目前已经提出了相应对策[35]。
镶嵌性现象揭示了发育体细胞基因突变相关疾病的分子基础,但仍有许多问题尚待探讨,如:(1)镶嵌体疾病临床表型与细胞基因突变时间性与空间性的更为详尽的关系;(2)发育畸形、错构瘤、瘤病与散发性良性肿瘤的差异的普遍性;(3)镶嵌体疾病基因突变细胞与周围非突变细胞相互作用与疾病进展的关系;(4)婴幼儿多发的恶性肿瘤,以及与儿童类型相似部分成人肿瘤的发生与胚胎早期细胞镶嵌体突变是否有关系。随着单细胞基因组测序技术的发展以及人类细胞图谱(human cell atlas)计划的推进,镶嵌体现象将会在分子与细胞层面得到细致的探讨,为我们揭示机体发育中个别细胞基因突变如何通过胚胎发育影响不同的细胞群体,如何通过与周围细胞的相互作用而选择性进展导致克隆性镶嵌体、发育畸形或肿瘤。同时,镶嵌体也对疾病的分子检测、肿瘤的液体活检与早期筛查提出了新的要求。
作者声明无利益冲突
1. 镶嵌体是指()
A. 个体有两种或以上类型细胞
B. 个体有母体细胞
C. 个体有两种或以上遗传特性差异细胞
D. 个体接受了异体细胞移植
2. 有关镶嵌体描述错误的是()
A. 镶嵌体基因突变发生于受精卵形成后细胞分裂
B. 镶嵌体基因突变可有多种类型
C. 镶嵌体基因突变较多发生于肿瘤相关基因
D. 镶嵌体基因突变一般为显性作用
3. 镶嵌体疾病临床表现的特点主要是()
A. 病变为血管畸形
B. 病变为区域性、节段性分布
C. 病变可随年龄改变
D. 病变为组织过度增生
4. 有关镶嵌体疾病基因检测描述错误的是()
A. 外周血检测一般为低频突变或阴性
B. 外周血检测可发现异倍体细胞
C. 部分患者其家庭成员外周血检测可基因突变
D. 外周血检测基因突变丰度可近50%
5. 主要表现为镶嵌体疾病的基因突变为()
A. NF
B. P53
C. AKT1
D. TSC1/2



























