
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者男,58岁,2019年6月出现咳嗽咳痰,痰中带血,无发热,胸部CT示,左侧肺门占位,长径约为47.6 mm,中央型肺癌可能,纵隔多发肿大淋巴结,左侧胸膜增厚,左侧胸膜腔少量积液。2019年7月16日行支气管镜检查病理示,鳞状细胞癌(中分化),基因检测示,表皮生长因子受体、间变性淋巴瘤激酶、ROSI均为阴性,肿瘤突变负荷为9.55;TNM分期为cT3N2M1,Ⅳa期。
患者于2019年7—8月行一线GP方案(吉西他滨1.6 g第1天和第8天,顺铂40 mg,第1~3天)化疗2个周期,出现3级化疗相关消化道不良反应,化疗后未复查CT评估疗效。2020年6月患者出现腹胀、嗜睡、恶心呕吐。复查胸部CT示,左肺门软组织影(长径为90.8 mm)及右肺下叶结节(长径为23.8 mm),提示肺内病灶增大,新发右肺转移,考虑病情进展,经患者及家属商议,决定行免疫治疗。2020年6月12日给予信迪利单抗200 mg静脉滴注,同时口服安罗替尼12 mg(第1~14天)行抗血管生成靶向治疗。2020年6月28日患者因持续恶心呕吐再次入院,肝功能示,谷氨酸氨基转移酶(alanine aminotransferase, ALT)为542 U/L、天门冬氨酸氨基转移酶(aspartate transaminase, AST)为475 U/L、总胆红素(total bilirubin, TBIL)为33.61 mmol/L、直接胆红素(direct bilirubin, DBIL)为18.79 mmol/L。给予复方甘草酸苷、异甘草酸镁保肝治疗。6月29日复查肝功示,ALT为712 U/L,AST为695 U/L,TBIL为31.9 mmol/L,DBIL为19.06 mmol/L,自身抗体谱均为阴性,甲型、乙型、丙型肝炎病毒均为阴性。复查胸腹部CT示,左肺下叶占位,纵隔内多发肿大淋巴结,少量心包积液,双侧少量胸腔积液,脂肪肝,少量腹水。考虑诊断为免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)相关肝损伤G3级。2020年6月29日给予甲强龙80 mg/d静脉滴注,同时予保肝退黄治疗。6月30日复查肝功示,ALT为634 U/L、AST为393 U/L、TBIL为26.25 mmol/L、DBIL为16.78 mmol/L。考虑治疗有效,继续予甲强龙80 mg/d静脉滴注。7月4日复查肝功示,ALT为249 U/L、AST为58 U/L、TBIL为28.52 mmol/L、DBIL为20.6 mmol/L,肝功下降至G2级,于7月5日甲强龙减量至60 mg/d。7月7日复查肝功示,ALT为148 U/L,AST为40 U/L,TBIL为45.57 mmol/L,DBIL为32.62 mmol/L,继续予激素治疗,患者喘憋气短加重,咳吐腥臭痰。7月10日复查肝功示,ALT为435 U/L,AST为245 U/L,TBIL为95.89 mmol/L,DBIL为67.62 mmol/L,提示肝损伤复发,建议患者完善肝穿刺活检明确病理情况,患者及家属拒绝,决定接受临终关怀护理而未进行治疗。患者于2020年7月12日死亡。患者胸部CT情况见图1。
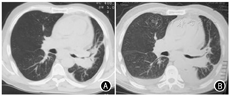

ICIs是一种重要的肿瘤免疫治疗新手段,目前,免疫治疗已成为黑色素瘤、肺癌和转移性肾癌等肿瘤的标准治疗方法。针对非小细胞肺癌患者的临床研究表明,在不考虑程序性死亡受体配体1(programmed cell death-ligand 1, PD-L1)表达水平的情况下,信迪利单抗联合吉西他滨和铂类对比安慰剂联合吉西他滨和铂类,延长了患者的无进展生存时间[1]。但免疫系统的过度激活也可能导致免疫功能紊乱,对自身正常组织和器官造成损伤,这些不良反应称为免疫治疗相关不良反应,肝脏是肿瘤免疫治疗中少见的损伤器官之一,重度肝损伤复发较罕见[2]。
本例患者既往无病毒性肝炎、自身免疫性肝炎、严重脂肪肝和酒精肝病史,在使用信迪利单抗治疗前肝功能无异常,首次输注信迪利单抗治疗16 d后出现恶心、纳差、乏力等消化道症状,无明显阳性体征,实验室检查示ALT、AST、TBIL、DBIL均升高,腹部CT未见肝转移,无其他肝损伤药物服用史。结合病史及用药史,我们确定患者重度肝损伤与ICIs治疗有关。
信迪利单抗是我国上市的一种靶向程序性死亡受体1(programmed cell death-1, PD-1)的全人源化IgG4单克隆抗体,它可以阻断免疫抑制途径中PD-L1和PD-L2,诱导T细胞激活,当T细胞靶向特定的肿瘤细胞抗原时,可导致肿瘤死亡[3]。
ICIs治疗肺癌患者出现肝损伤的发生率约为1%~7%,但重度肝损伤发生率较低(1%~3%)[4]。信迪利单抗安全性评价与国内已批准上市的PD-1抑制剂(帕博利珠单抗、纳武利尤单抗)相似,且无意料之外脱靶引起的安全性问题[5]。当ICIs与其他抗肿瘤药物联合治疗时,其不良反应可能叠加,不良反应的风险和严重程度均可增加[6]。在非小细胞肺癌患者中,ICIs相关肝损伤的中位发生时间为用药后1.9~25.4周[7],当2种ICIs联合使用时,不良反应发生的时间明显提前[8]。这也提示我们免疫治疗尤其是联合用药初期应格外警惕肝损伤的发生。
ICIs相关性肝损伤通常表现为免疫介导性肝炎,患者无特异性临床症状,实验室检查为血清ALT和AST升高,伴或不伴有血清胆红素升高,血清自身免疫性肝炎相关标志物呈阴性。2018年NCCN指南指出,目前对于ICIs相关肝损伤的发生尚无准确预测指标,但关注患者的临床症状及肝脏实验室检查指标有助于早期识别和诊疗[9]。肝脏活检是诊断肝损伤和评估损伤严重程度的重要方法,且有助于指导糖皮质激素用药[10]。治疗方面,首先应根据患者症状及实验室检查进行肝脏损伤分级,对于ALT和AST≥5倍参考值上限,总胆红素≥3倍参考值上限的重度肝损伤患者,应当立即停用ICIs,予甲强龙1~2 mg/(kg·d)静脉滴注冲击治疗,待肝脏损伤降至2级后糖皮质激素逐渐减量,而对于在2~3 d内对激素治疗无反应的患者,可加用吗替麦考酚酯1 000 mg,2次/d,不推荐加用英夫利昔单抗[11,12]。
免疫相关性肝损伤一般经治疗8~12周可恢复[12],重度致死性肝损伤发生率约为0.042%~0.62%[8,9,10,11,12,13]。考虑提示发生重度肝损伤风险的可能有:联合用药包括2种ICIs联合应用,以及联合应用酪氨酸激酶抑制剂及克唑替尼[14];出现胆红素升高的黄疸;激素减量后出现肝损伤复发;影像学表现为肝转移病灶伴有出血[15]。
综上所述,鉴于国内ICIs的使用时间较短,关于重度免疫相关性肝损伤的报道尚缺乏。结合本案报道及相关文献,重度肝损伤发病迅速,存在复发风险,且缺乏准确的预测及预防手段。因此对于临床医师而言,早期识别免疫相关性肝损伤,尽早进行干预,对于肝脏指标即使恢复正常仍应坚持长期随访,警惕肝损伤复发至关重要。
所有作者均声明不存在利益冲突


























