
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者,男,56岁。2014年8月25日因会阴部疼痛伴脓肿形成4年入院。既往有阴茎头硬化性苔藓样变(lichen sclerosus,LS)病史26年,尿道狭窄及尿道扩张病史20年。4年前被诊断为尿道旁脓肿及尿道外口闭塞性狭窄,于当地医院行脓肿切开引流、尿道会阴造口及耻骨上膀胱造瘘术。术后脓肿未见明显好转,脓肿扩大至会阴部并形成不愈合的尿道皮肤会阴瘘。既往无创伤、药物滥用、结石及输血等相关病史。查体可见尿道外口完全闭塞,阴茎头可见瓷白色硬化性斑块,会阴部可见一瘘口,伴脓性分泌物夹杂坏死组织流出,尿道探子示尿道皮肤会阴瘘形成(图1)。坏死组织送病理检查提示尿道高分化鳞癌。行尿道镜检查,尿道镜自膀胱造瘘口可顺利进入膀胱,可见膀胱、尿道内口及前列腺部尿道均正常,癌组织位于球部尿道,呈糜烂豆腐渣样。直肠指检前列腺正常大小,质软。双侧腹股沟淋巴结触诊未及肿大。胸腹部CT及骨盆MRI检查均未发现远处转移的证据。术前诊断为尿道高分化鳞癌(cT2N0M0)。全麻下行会阴肿瘤切除+瘘管切除术。截石位,取会阴部正中切口及沿会阴部瘘管方向的斜切口。术中可见大量豆腐渣样的脓液夹杂坏死组织自切口内涌出。切除少量阴茎段尿道残端和坏死组织一同送病理检查。切除的阴茎段尿道残端行HE染色提示典型的LS改变:表皮层过度角化,基底细胞空泡样变性,真皮硬化性透明样改变,真皮下可见淋巴细胞的带状沉积(图2)。坏死组织行HE染色检查示尿道高分化鳞癌,癌巢内可见明显的角化珠和细胞间桥。尿道癌组织行免疫组化染色检查:P53、CK5/6、P63、P40(+),Ki-67(20% +),P16、SOX-2(-)。术后行放疗联合顺铂化疗,每3个月复查1次。患者术后会阴部仍然疼痛,3个月后好转。术后5个月行PET-CT检查显示腰椎转移,术后10个月死于胸部及脑部转移。
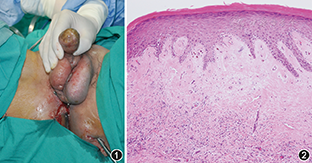

LS是一种可累及包皮、阴茎头、尿道外口及尿道的慢性进展性皮肤黏膜炎性疾病,主要表现为包皮及阴茎头的瓷白色萎缩性硬化性丘疹和斑块样改变,累及尿道可致尿道狭窄而引起排尿障碍甚至尿潴留[1]。LS亦是一种具有恶性潜能的疾病,已被欧洲泌尿外科学会指南作为阴茎鳞癌的高危因素[2]。尿道鳞癌(urethral squamous cell carcinoma,USCC)发病率低,LS合并USCC更是少见。本例的免疫组化染色检查结果与文献报道的LS合并阴茎或女性外阴鳞癌组织的结果一致[3]。另外,LS是一种可导致尿道狭窄的炎性疾病,而慢性尿道炎症和尿道狭窄已被作为USCC的发病诱因[4],以上结果均提示LS与USCC或许具有一定的相关性。LS合并USCC确诊依靠病理及免疫组化染色检查。
结合文献[5]和本例,我们认为LS合并球部USCC的恶性程度高,预后不良,但小样本资料尚不足以证实本病的生物学行为。


























