
患者,男,56岁。因膀胱癌反复复发于2021年11月29日入院。患者因膀胱癌既往有开放膀胱部分切除术史、同步放化疗治疗史、4次经尿道膀胱肿瘤切除术史。本次入院CT检查示膀胱左侧壁膀胱癌,肿瘤分期T3期;继发左肾积水。全麻下行机器人辅助腹腔镜根治性膀胱切除术+完全腹腔内原位回肠新膀胱。手术顺利,患者恢复良好,术后7 d出院。术后病理诊断为膀胱高级别尿路上皮癌,病理分期T2b期,伴左侧盆腔淋巴结转移。术后3个月复查,患者无复发表现,新膀胱功能良好,日间可完全控尿,肠道和肾功能恢复好。目前正在接受吉西他滨联合顺铂辅助化疗。对于有手术史和放疗史的膀胱癌患者,根治性膀胱切除术+原位回肠膀胱的手术难度高,术者丰富的腹腔镜手术经验和机器人辅助手术的精细化特点是完成此类手术的重要前提。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
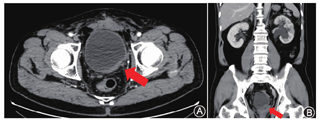
患者,男,56岁。因膀胱镜检查发现膀胱肿瘤复发1个月于2021年11月29日收入北京大学第三医院。患者2012年诊断为左侧输尿管口旁膀胱癌,其后有开放膀胱部分切除术史、同步放化疗治疗史、4次经尿道膀胱肿瘤切除术史。既往有高血压病、甲状腺功能亢进病史,药物控制良好;无严重心脑血管合并症。患者本次入院前无血尿,无尿路刺激症状,无腰痛。体质指数24.7 kg/m2,美国东部肿瘤协作组评分0分。术前前列腺特异性抗原(prostate specific antigen,PSA)为2.35 ng/ml。直肠指检:前列腺质韧,大小正常,未及结节,肛门括约肌收缩力弱。泌尿系增强CTU检查:膀胱左后壁肿物,不除外T3期膀胱癌,左肾积水较前进展,淋巴结未见明显肿大(图1)。

经全科讨论,考虑患者为中年男性,局限性膀胱癌,体能状况良好,具备术后新膀胱功能锻炼条件,且患者对原位膀胱手术意愿强烈;但患者9年前行膀胱部分切除术,3年前行膀胱同步放化疗治疗,手术区域可能存在粘连,采用机器人手术可能便于术中处理粘连问题。综合考虑患者手术获益和并发症风险,遂决定行机器人辅助腹腔镜根治性膀胱切除术+完全腹腔内回肠原位新膀胱。术中见膀胱前壁与腹壁粘连紧密,前列腺与小骨盆周围结构粘连紧密,双侧盆腔淋巴结区域纤维化明显。在机器人手术系统辅助下,首先行双侧髂血管旁淋巴结清扫,因放疗造成纤维化明显,术中注意避免损伤髂血管和闭孔神经,并从纤维化的组织中剥离出双侧输尿管。然后分离膀胱前列腺后间隙和Denoviller’s间隙,因粘连不严重,可以较好地游离至近前列腺尖部。处理膀胱前间隙时,因存在膀胱部分切术后瘢痕,分离时注意避免切破膀胱。因前列腺前方和外侧均与盆壁粘连严重,游离非常困难,结合患者术前总PSA水平为2.35 ng/ml,以及患者的肛门括约肌功能减弱,因此选择保留前列腺尖部的根治性膀胱切除术,以利于术后尿控功能恢复。最后,遵循"先吻合尿道,后构建膀胱"的原则,通过交叉折叠方式在全机器人辅助下行改良Studer原位回肠膀胱。
手术过程顺利,未中转普通腹腔镜或开放手术。手术时间381 min,膀胱全切和双侧盆腔淋巴结清扫时间150 min,原位膀胱构建时间180 min。术中出血量600 ml,未输血。术后第1天患者排气,第2天拔除胃管,第3天开始半流食,第5天拔除引流管,第7天出院。
术后病理检查提示膀胱高级别尿路上皮癌,癌组织侵犯膀胱固有肌层(深1/2),未见脉管内癌栓和神经侵犯,切缘阴性;左侧盆腔淋巴结1/3阳性,右侧盆腔淋巴结0/3阳性;前列腺为良性增生组织。术后18 d拔除双侧输尿管支架管,27 d拔除尿管。术后1个月患者因进食硬质食物,发生不全性肠梗阻,经保守治疗好转,未复发。
患者拔除尿管后开始膀胱功能训练。控尿训练采用提肛训练,收缩肛门保持5 s后放松,每组20次,3组/天,以提高控尿能力;排尿训练采用坐姿,前倾上身,鼓腹增大腹压,挤压下腹部,放松盆底肌肉,完成排尿动作。同时,嘱患者定时排尿,夜间需设置闹铃提醒排尿,从每2小时排尿1次开始,每周延长0.5小时,最后延长至每4小时排尿1次,每次排尿均记录排尿量(包含尿垫内尿量),评估膀胱容量。
术后随访3个月,患者日间可完全控尿,夜间需0~1块尿垫。排尿间隔为3.5 h,每次排尿量平均350 ml。尿动力学检查示膀胱顺应性正常,容量365 ml,无残余尿。B超检查示患者双肾轻度积水,排尿后可缓解。复查血肌酐71μmol/L。CTU检查(图2)未见肿瘤复发表现。患者术后满意度高,基本恢复正常生活。因患者术后病理提示转移淋巴结阳性,予吉西他滨联合顺铂辅助化疗。
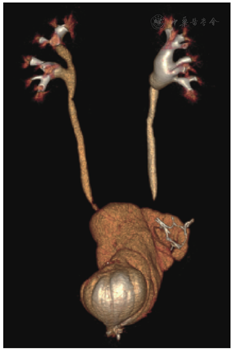

双肾盂输尿管无明显扩张积水,双肾盏杯口好,膀胱充盈好,形态符合新膀胱表现
肌层浸润性膀胱癌的保留膀胱治疗已纳入膀胱癌诊疗指南,主流方案为最大限度经尿道膀胱肿瘤切除术联合同步放化疗的三联疗法,但对患者的选择比较严格(T2期以下、单发、不合并原位癌、无肾积水等)[1]。既往研究结果显示,保留膀胱治疗后的肿瘤完全缓解率为70%~89%,5年总生存率为50%~67%,与根治性膀胱切除术患者的生存情况相似,而肿瘤复发行挽救性膀胱全切率为9%~32%[2]。范欣荣等[3]的研究结果显示,保留膀胱患者与膀胱全切患者的2年无进展生存率无明显差异,局部复发率为30.6%。
随着保留膀胱治疗的广泛开展,挽救性膀胱切除会逐渐增加,能够实施挽救性膀胱全切是开展保留膀胱治疗的必备条件。放疗会造成组织的纤维化和瘢痕化,给挽救性膀胱全切增加难度和风险,而且也被认为是原位膀胱的相对禁忌证。但Croock等[4]研究发现,既往放疗史除增加膀胱全切术中失血量外,其他并发症发生率与无放疗史患者相似。本例术中失血量为600 ml,与术中组织粘连、纤维化明显造成分离困难有关,围手术期无并发症发生。Vassantachart等[5]研究发现,既往盆腔放疗并不影响构建原位回肠膀胱,其并发症发生率与无放疗史患者相似。从原位膀胱转换成非原位膀胱的主要因素是肿瘤学因素(尿道切缘阳性、淋巴结转移等),而不是技术因素(严重粘连、尿道狭窄等)[6]。
本例既往有膀胱手术和放疗史,能顺利完成机器人辅助腹腔镜根治性膀胱切除术+完全腹腔内原位膀胱,我们总结经验:①术者应熟练掌握腹腔镜和机器人手术技巧,熟悉盆腔解剖,在游离组织过程中尽量做到解剖性游离,减少并发症发生;②术前充分评估患者括约肌功能并对前列腺进行评估,预设保留前列腺尖部的手术方案,在前列腺粘连严重的情况下,能顺利完成手术并获得良好的尿控效果;③术者应熟练掌握机器人辅助完全腹腔内回肠膀胱的重建技巧,遵循"先吻合尿道,后构建膀胱"的原则[7];④本例双侧输尿管均被纤维化腹膜覆盖,可游离长度受限,完全腹腔内构建原位新膀胱需要的输尿管长度短,有利于手术顺利完成;⑤术后需严密随访,定期监测患者肠道功能、新膀胱功能、肾功能等,并训练新膀胱的控尿、排尿功能,使患者顺利恢复。
所有作者声明无利益冲突



























