
评价新型冠状病毒灭活疫苗大规模紧急使用的安全性。
通过“疫苗接种信息采集系统”,收集在紧急使用中新型冠状病毒灭活疫苗(北京生物制品研究所、武汉生物制品研究所)接种人群的不良反应发生情况,采用流行病学与统计学方法分析相关信息。
截至2020年12月1日,共采集519 543人次接种信息,总不良反应发生率为1.06%,全身不良反应发生率为0.69%,局部不良反应发生率为0.37%。全身不良反应以疲劳(0.21%)、头痛(0.14%)、发热(0.06%)、咳嗽(0.05%)、食欲不振(0.05%)为主要表现;局部不良反应以接种部位疼痛(0.24%)、接种部位肿胀(0.05%)为主要表现。
大规模新型冠状病毒灭活疫苗(Vero细胞)(北京生物制品研究所、武汉生物制品研究所)进行紧急使用后,一般反应的发生率较低,未见严重不良反应,疫苗具有良好的安全性。

新型冠状病毒肺炎(新冠肺炎)疫情暴发初期,我国紧急布局了包括新型冠状病毒灭活疫苗(Vero细胞)(新冠灭活疫苗)在内的多条技术路线研发新冠疫苗,并在科技部、卫健委等中央各部委的大力支持下快速推进。中国生物技术股份有限公司(中国生物)下属武汉生物制品研究所(中国生物武汉所)和北京生物制品研究所(中国生物北京所)成功研发新冠灭活疫苗,分别于2020年4月12日和4月27日获得国家药监局颁发的药物临床试验批件,启动Ⅰ、Ⅱ期临床试验。中国生物武汉所、中国生物北京所的Ⅰ/Ⅱ期临床阶段性研究结果均显示,新冠灭活疫苗接种后安全性良好,未见严重不良反应[1, 2]。2剂疫苗接种后28 d,抗新冠病毒中和抗体4倍增长率接近100%。根据《中华人民共和国疫苗管理法》第二十条:应对重大突发公共卫生事件急需的疫苗或国务院卫生健康主管部门认定急需的其他疫苗,经评估获益大于风险的,国务院药品监督管理部门可以附条件批准疫苗注册申请,出现特别重大突发公共卫生事件或者其他严重威胁公众健康的紧急事件,国务院卫生健康主管部门根据传染病预防、控制需要提出紧急使用疫苗的建议,经国务院药品监督管理部门组织论证同意后可以在一定范围和期限内紧急使用。根据党中央、国务院的决策部署,经国务院联防联控机制批准,中国生物武汉所、中国生物北京所研发的新冠灭活疫苗分别于6月30日、7月23日纳入国家新型冠状病毒疫苗紧急使用。
本研究利用中国生物自主开发的“疫苗接种信息采集系统”记录接种信息及不良反应数据,通过对该系统记录的紧急使用数据进行分析,初步评价新冠灭活疫苗在重点人群中紧急使用的安全性,为新冠灭活疫苗上市后的安全性评价提供重要依据。
1. 研究对象:紧急使用期间接种新冠灭活疫苗的高风险重点人群:外交外派和中资企业出境的“一带一路”建设人员以及留学生;医疗机构的医护人员和疾控中心的一线工作人员;海关边检人员、口岸交通人员;涉及防控、治安,接触新冠病毒风险较高的各级政府部门、各企事业单位工作人员;城市一线生活服务保障人员等。
经健康筛查排除人群包括:严重过敏体质,既往注射其他疫苗时发生过严重过敏反应,或初次接种本疫苗出现过敏者;新冠肺炎既往感染者或核酸、抗体检测阳性者;严重慢性病或慢性病急性发作期患者,如药物不可控制的高血压患者;患有惊厥癫痫及进行性神经系统疾病史者;患有血小板减少症者或出血性疾病患者;正在接受免疫抑制剂治疗或免疫功能缺陷的患者;处于哺乳期或妊娠期的妇女、未来3个月内有生育计划者;14 d内接种其他灭活疫苗,28 d内接种其他减毒活疫苗者;接种前有任何不适者。
2. 研究用疫苗:新冠灭活疫苗由中国生物武汉所和中国生物北京所生产,规格:每人次用剂量200 WU/剂(武汉),每剂0.5 ml;每人次用剂量6.5 U/剂(北京),每剂0.5 ml。
3. 免疫程序:接种2剂,推荐按0~14 d,0~28 d免疫程序接种。若因紧急出境,无法按推荐程序接种者,允许同时接种2剂。
4. 信息采集:采用“疫苗接种信息采集系统”记录接种信息及安全性数据。受种者需在线填报相关个人及接种信息,包括[个人信息、健康状况(血压、体温)、免疫程序、接种部位、接种时间等]。系统分别在接种后30 min、第1~7天(每天)、第2~4周(每周最后一天)、第2~5个月(每月最后一天)发送通知,在第2剂接种后系统自动按第2剂接种后的时间发送通知,收集受种者安全性监测信息。监测信息包括:接种后30 min体温;接种部位是否出现疼痛、硬结、肿胀、皮疹、红晕及瘙痒;是否出现发热、头疼、疲劳、乏力、咳嗽、食欲不振、呕吐、腹泻、肌肉痛、过敏反应等症状。按照从严原则,默认上报的不良事件均与接种有关,均按不良反应纳入分析。通过对监测数据分析,初步评估新冠灭活疫苗用于紧急使用的安全性。
5. 统计学分析:从“疫苗接种信息采集系统”导出并整理安全性数据,对上报个案的临床诊断和不良反应再审核,并对新冠灭活疫苗的不良反应构成及报告发生率等指标进行回顾性分析。使用SPSS 23.0软件进行统计分析,采用χ2检验,P<0.05为差异有统计学意义。
1. 总体概况:“疫苗接种信息采集系统”共收集到519 543人次接种信息,监测不良反应信息5 164条,总不良反应发生率为1.06%,局部不良反应发生率为0.37%,全身不良反应发生率为0.69%。局部不良反应以接种部位疼痛、接种部位肿胀为主要表现,发生率分别为0.24%、0.05%,全身不良反应以疲劳、头痛、发热、咳嗽、食欲不振为主要表现,发生率分别为0.21%、0.14%、0.06%、0.05%、0.05%。见表1,2。
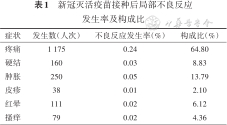
新冠灭活疫苗接种后局部不良反应发生率及构成比
新冠灭活疫苗接种后局部不良反应发生率及构成比
| 症状 | 发生数(人次) | 不良反应发生率(%) | 构成比(%) |
|---|---|---|---|
| 疼痛 | 1 175 | 0.24 | 64.80 |
| 硬结 | 160 | 0.03 | 8.83 |
| 肿胀 | 250 | 0.05 | 13.79 |
| 皮疹 | 38 | 0.01 | 2.10 |
| 红晕 | 111 | 0.02 | 6.12 |
| 搔痒 | 79 | 0.02 | 4.36 |

新冠灭活疫苗接种后全身不良反应发生率及构成比
新冠灭活疫苗接种后全身不良反应发生率及构成比
| 症状 | 发生数(人次) | 不良反应发生率(%) | 构成比(%) |
|---|---|---|---|
| 发热 | 310 | 0.06 | 9.25 |
| 头痛 | 664 | 0.14 | 19.80 |
| 疲劳 | 1 016 | 0.21 | 30.32 |
| 咳嗽 | 239 | 0.05 | 7.13 |
| 食欲不振 | 237 | 0.05 | 7.07 |
| 呕吐 | 116 | 0.02 | 3.46 |
| 腹泻 | 211 | 0.04 | 6.30 |
| 肌肉痛 | 431 | 0.09 | 12.86 |
| 过敏反应 | 127 | 0.03 | 3.79 |
2. 疫苗不良反应发生情况:中国生物北京所生产的新冠灭活疫苗共接种497 743人次,总不良反应发生率为1.02%,局部不良反应发生率为0.36%,全身不良反应发生率为0.66%。中国生物武汉所生产的新冠灭活疫苗共接种21 800人次,总不良反应发生率为0.77%,局部不良反应发生率为0.46%,全身不良反应发生率为0.31%。局部不良反应与全身不良反应的发生率在两家企业生产的新冠灭活疫苗中差异无统计学意义。见表3。

不同企业生产的两种新冠灭活疫苗不良反应发生情况
不同企业生产的两种新冠灭活疫苗不良反应发生情况
| 症状 | 中国生物北京所 | 中国生物武汉所 | ||
|---|---|---|---|---|
发生数 (人次) | 发生率(%) | 发生数(人次) | 发生率(%) | |
| 局部不良反应 | ||||
疼痛 | 1 120 | 0.23 | 55 | 0.25 |
硬结 | 148 | 0.03 | 12 | 0.06 |
肿胀 | 229 | 0.05 | 21 | 0.10 |
皮疹 | 36 | 0.01 | 2 | 0.01 |
红晕 | 104 | 0.02 | 7 | 0.03 |
搔痒 | 76 | 0.02 | 3 | 0.01 |
| 全身不良反应 | ||||
发热 | 305 | 0.06 | 5 | 0.02 |
头痛 | 652 | 0.13 | 12 | 0.06 |
疲劳 | 994 | 0.20 | 22 | 0.10 |
咳嗽 | 234 | 0.05 | 5 | 0.02 |
食欲不振 | 233 | 0.05 | 4 | 0.02 |
呕吐 | 114 | 0.02 | 2 | 0.01 |
腹泻 | 207 | 0.04 | 4 | 0.02 |
肌肉痛 | 419 | 0.08 | 12 | 0.06 |
过敏反应 | 125 | 0.03 | 2 | 0.01 |
3. 不良反应发生情况:
(1)按性别划分:“疫苗接种信息采集系统”累计记录男性接种者297 996人次,男性接种后不良反应数据2 149条;女性接种者190 418人次,女性接种后不良反应数据3 015条,女性的不良反应发生率(1.58%)高于男性(0.72%),差异有统计学意义(P<0.000 1)。见表4。

新冠灭活疫苗接种后不同特征人群不良反应发生情况
新冠灭活疫苗接种后不同特征人群不良反应发生情况
| 特征 | 接种数 (人次) | 发生数(人次) | 不良反应 发生率(%) | χ2值 | P值 |
|---|---|---|---|---|---|
| 性别 | 824.78 | <0.000 1 | |||
男 | 297 996 | 2 149 | 0.72 | ||
女 | 190 418 | 3 015 | 1.58 | ||
| 年龄组(岁) | 882.52 | <0.000 1 | |||
12~ | 716 | 81 | 11.31 | ||
19~ | 93 763 | 1 082 | 1.15 | ||
30~ | 165 480 | 1 957 | 1.18 | ||
40~ | 129 820 | 1 337 | 1.03 | ||
50~ | 87 578 | 672 | 0.77 | ||
≥60 | 11 067 | 35 | 0.32 |
(2)按年龄划分:12~18周岁人群不良反应发生率最高,达到11.31%,以疲劳及接种部位疼痛为主。其次为30~39岁人群,不良反应发生率为1.18%,不良反应发生率最低为≥60岁人群,不良反应发生率为0.32%,差异有统计学意义。见表4。
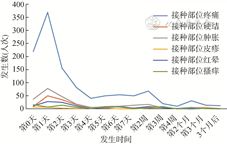
4. 不良反应发生时间分布:根据“疫苗接种信息采集系统”收集信息统计,局部反应中接种部位疼痛主要发生在接种当天及接种后24 h内;接种部位硬结主要发生在接种后的1~4 d内;接种部位肿胀、红晕、瘙痒及皮疹主要发生在接种后1周内。全身反应中接种后疲劳主要发生在接种当日及接种后的2 d内;接种后头痛主要发生在0~3 d内;肌肉痛主要发生在接种后0~3 d内,以第1天发生最多;发热、咳嗽、食欲不振、腹泻及过敏主要发生在接种后的1周内。见图1,2。



5. 接种剂次与不良反应发生情况:对于局部不良反应,间隔接种第一剂次、间隔接种第二剂次与同时接种2剂次相比,差异有统计学意义(χ2=70.493,P=4.93×10-16)。采用LSD检验分析各组间差异,间隔接种第一剂次的局部不良反应发生率为0.44%,高于间隔接种第二剂次的局部不良反应发生率(0.29%)与同时接种2剂次的局部不良反应发生率(0.34%);后两者之间差异无统计学意义。见表5。
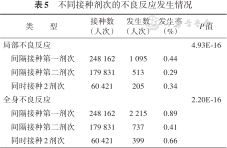
不同接种剂次的不良反应发生情况
不同接种剂次的不良反应发生情况
| 类 型 | 接种数 (人次) | 发生数 (人次) | 发生率(%) | P值 |
|---|---|---|---|---|
| 局部不良反应 | 4.93E-16 | |||
间隔接种第一剂次 | 248 162 | 1 095 | 0.44 | |
间隔接种第二剂次 | 179 831 | 513 | 0.29 | |
同时接种2剂次 | 60 421 | 205 | 0.34 | |
| 全身不良反应 | 2.20E-16 | |||
间隔接种第一剂次 | 248 162 | 2 215 | 0.89 | |
间隔接种第二剂次 | 179 831 | 737 | 0.41 | |
同时接种2剂次 | 60 421 | 399 | 0.66 |
对于全身不良反应,间隔接种第一剂次、间隔接种第二剂次与同时接种2剂次相比,差异有统计学意义(χ2=357.27,P=2.20×10-16)。采用LSD检验分析各组间差异,间隔接种第一剂次的全身不良反应发生率最高(0.89%),同时接种2剂次居中(0.66%);间隔接种第二剂次最低(0.41%)。见表5。
灭活疫苗作为所有研发技术路线中最传统、最经典的疫苗制备方式,具有生产工艺成熟、研发速度快、质控标准明确等优势,是应对新发突发传染病的有效手段[3, 4, 5]。甲型肝炎灭活疫苗、狂犬病疫苗和Sabin株脊髓灰质炎灭活疫苗等灭活疫苗在大规模人群中的应用,已经证明灭活疫苗具有良好的安全性和有效性[6, 7, 8, 9, 10, 11],在疫情防控和传染病控制中发挥了重要作用。在此次新冠肺炎疫情中,中国生物北京所与武汉所快速研发的两款灭活疫苗,经Ⅰ期、Ⅱ期临床研究和大规模紧急使用,阶段性验证了2种新冠灭活疫苗的安全性[1, 2]。
截至2020年12月1日,“疫苗接种信息采集系统”录入接种信息数据519 543人次。根据记录数据分析,中国生物下属两家企业生产的新冠灭活疫苗总不良反应发生率为1.06%,其中局部不良反应发生率为0.37%,全身不良反应发生率为0.69%,未见严重不良反应。对比Ⅱ期临床试验,中国生物北京所生产的新冠灭活疫苗总体不良反应发生率为13%,中国生物武汉所生产的新冠灭活疫苗总体不良反应发生率为19%,本研究结果远低于Ⅱ期临床阶段性结果。参考肠道病毒71型(EV71)灭活疫苗上市后大人群接种安全性分析结果[12, 13, 14],EV71灭活疫苗总不良反应发生率为1.079%~3.310%。其中,全身、局部不良反应发生率分别为1.168%~2.250%、0.091%~0.990%。甲型肝炎灭活疫苗在成人[7]和儿童中[8]的不良反应发生率分别为2.90%~35.56%、3.30%~53.61%。
与其他类型已附条件上市或批准紧急使用的新冠疫苗相比,新冠灭活疫苗的安全性较高。最近新冠疫苗研究结果显示:Ⅱ期临床试验中,北京科兴生物制品有限公司生产的新冠灭活疫苗总体不良反应发生率为19.2%[15],康希诺生物股份公司生产的腺病毒载体重组新冠疫苗的总体不良反应发生率为76%[16],安徽智飞龙科马生物制药有限公司生产的重组蛋白新冠疫苗的总体不良反应发生率为48%[17]。
在新冠灭活疫苗不良反应特征上,经统计分析结果显示,中国生物北京所与中国生物武汉所生产的新冠灭活疫苗不良反应发生率差异无统计学意义;不良反应发生时间上,主要发生在接种后0~3 d内;接种剂次差异上,第一剂次不良反应发生率高于第二剂次,同时2剂次的不良反应低于第一针,考虑同时接种2剂次的人群主要为紧急出国人员,一般为央企、国企海外务工人员,相对文化程度不高,依从性较低,因此存在报告不良反应发生率低于第一针的原因;人群特征上,男性低于女性,存在随着年龄增长逐步降低的趋势。
对比新冠灭活疫苗Ⅰ/Ⅱ期临床阶段性研究结果及海外Ⅲ期临床试验中期分析结果,接种后局部不良反应以接种部位疼痛、肿胀、红晕为主,全身不良反应以头痛、肌肉痛、腹泻(紧急使用未观察腹泻相关情况)、咳嗽、发热、乏力为主。本研究与境外Ⅲ期临床研究观察到的不良反应发生情况相吻合,但与境外Ⅲ期临床试验中期分析结果相比较,本研究不良反应发生率明显低于境外Ⅲ期临床试验中期分析结果,考虑有以下原因:(1)本研究采用被动观察收集不良事件的方法,需受种者自行登录微信小程序填写安全性不良反应信息,安全性信息填报为非强制要求,受种者的依从性和报告意识一定程度上影响了受种者应答率和监测的敏感性。而Ⅰ/Ⅱ期临床试验采用的是主动监测,导致本研究中不良发生率较低,远低于Ⅰ/Ⅱ期临床试验的结果。其次本次紧急使用对象以赴海外劳务派遣人员为主,赴境外后网络操作障碍、反馈意识较低,部分人员未能上报相关不良反应安全性信息,一定程度上影响不良反应反馈数及监测数降低。本研究结果具有一定的局限性。(2)本次紧急使用,建立了严格的健康筛查标准和工作流程,接种者多为30~50岁青壮年为主,身体素质良好,不良反应发生率较低。(3)本次调查中发现男性不良反应报告发生率低于女性,可能原因除上述海外劳务派遣人员以男性为主而反馈较低,也可能与女性较好的反馈依从性有关以及女性对不良反应引起的不适感耐受较低有关。
良好的安全性在基于疫苗本身质量标准较高的同时,也得益于在紧急使用工作所制订的严格的健康筛查条件和工作操作流程标准。严格把握接种条件、注意事项、风险提示等各项要求,确保了接种工作安全。因此,建议所有疫苗的预防接种过程中,接种人员应熟练、准确地掌握疫苗接种禁忌证,接种前充分告知受种对象有关疫苗及其预防疾病的相关知识,做好适种对象的预检工作,在有条件的情况下开展受种者的体温和血压检测,确保接种安全。
目前,新冠肺炎疫情在全球持续蔓延,对全球经济和社会正常生活造成巨大负面影响。研制安全有效的新冠疫苗,提高疫苗的接种率,逐步建立人群免疫屏障,是阻断新冠肺炎疫情持续蔓延的最有效方法。中国生物两家企业研发的新冠灭活疫苗,经大规模紧急使用接种和跟踪随访数据来看,表现出了良好的安全性,为疫苗附条件上市及上市后全国大规模人群广泛接种提供了有力支撑。
所有作者均声明不存在利益冲突



























