
1例55岁男性患者经皮穿刺心尖路径微创封堵双机械瓣置换术后二尖瓣瓣周漏,手术过程顺利,术后患者恢复良好。本文就患者一般病情、既往史、检查资料、创新手术过程、治疗及随访效果、技术讨论等总结报道。对于双机械瓣置换术后的二尖瓣瓣周漏,经皮心尖穿刺微创封堵可能是创伤小、节省时间、并发症少的优选技术。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
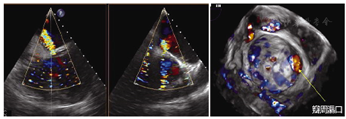
男,55岁。因"主动脉瓣、二尖瓣机械瓣置换术后11年,间歇性胸闷、气短2个月"收治入院。既往病史:2008年6月,因"风湿性心脏病、主动脉瓣关闭不全、二尖瓣狭窄伴关闭不全"于当地医院行主动脉瓣、二尖瓣机械瓣置换术。术后并发Ⅲ度房室传导阻滞,于2009年3月行心脏永久起搏器置入术。2个月前因上呼吸道感染后突发胸闷、气短,复查超声心动图提示:二尖瓣机械瓣瓣周漏,二尖瓣瓣周大量反流,中度肺动脉高压。入院后予以药物治疗改善心脏功能,稳定病情。经食管超声心动图提示:主动脉瓣、二尖瓣机械瓣置换术后,二尖瓣机械瓣2~3点位见3 mm间隙,瓣周反流7 ml(图1)。经心脏团队评估,患者系二次外科开胸手术高危患者(EuroScore Ⅱ评分10.2分,STS评分8.5分),经与患者及家属积极沟通后,决定行经皮心尖穿刺微创二尖瓣瓣周漏封堵术。该技术已通过我院临床伦理委员会审批(编号:KY20150205-1),术前常规签署手术相关知情同意书。

2019年9月10日,手术在介入手术室进行,患者取仰卧位,全身麻醉后行气管插管机械辅助通气,同时经食管超声心动图辅助术中影像学评估及全程监测心包及胸腔。术前经胸超声心动图提示:心包粘连,心动周期内左心室前壁、心尖处与胸廓位置相对固定。穿刺右侧股动脉置入6F短鞘,泥鳅导丝引导4.0左冠状动脉导管逆行至左冠状动脉开口,分别在前后位、左前斜45°、右前斜38°、足位26°进行左冠状动脉选择性造影,明确心尖无冠状动脉血管区域,同时借助X线下直头镊辅助定位,最终确定经皮穿刺进针点为左侧腋前线第5肋间(图2)。行经皮心尖穿刺,置入5F短鞘,鞘管头部放置于左心室中间。调整C臂至右前斜38°、足位26°使二尖瓣机械瓣为一个平面且左心房、左心室展开,经短鞘送入5F猪尾导管行左心室造影,提示:二尖瓣机械瓣瓣周漏,心脏收缩期反流血液迅速充盈左心房。随后,撤出5F猪尾导管,使用2.6米直头泥鳅导丝引导5F单弯导管进入左心室内,探过瓣周漏口进入左心房使单弯导管盘成圈,撤出泥鳅导丝置换为预弯头部的Amplatzer Ultrastiff加硬导丝进入左心房内打圈。撤出单弯导管及短鞘,沿加硬导丝送入COOK 5F 90 cm外周长鞘跨过瓣周漏口进入左心房,撤出加硬导丝。结合术前影像学测量,选择6 mm ADO-Ⅱ封堵器送入,X线下精准定位于瓣周漏口并展开。推拉试验证明封堵器定位牢固,X线下显示无卡瓣现象。遂释放封堵器,置换猪尾导管行术后左心室造影,结果提示:封堵器位置良好,瓣周反流消失。经食管超声心动图同样证实封堵器位置良好,二尖瓣机械瓣叶活动良好,瓣周反流消失。经外周长鞘送入第2枚6 mm ADO-Ⅱ封堵器,回撤长鞘时将封堵器紧贴左心室壁释放封堵穿刺针道,X线及超声心动图双重明确封堵器一端紧贴于心室游离壁,一端于心肌外,遂释放封堵器。术后经食管超声心动图证实无心包积液,胸腔积液。术后即刻,患者苏醒并撤除呼吸机,转至心脏重症监护室观察。3天后,复查超声心动图提示瓣周反流消失、心包、胸腔无积液,患者平稳出院。
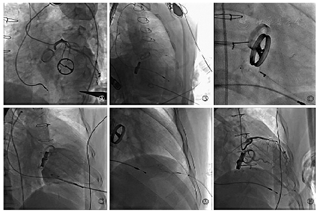

Ⓐ选择性左冠状动脉造影明确心尖无冠状动脉区域 Ⓑ经心尖左心室造影 Ⓒ顺行释放封堵器封堵瓣周漏口 Ⓓ封堵后左心室造影 Ⓔ封堵心尖穿刺针道 Ⓕ术后选择性左冠状动脉造影
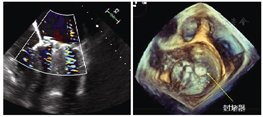
术后3个月随访,超声心动图提示二尖瓣机械瓣瓣周无反流,封堵器位置良好,二尖瓣、主动脉瓣机械瓣瓣叶活动良好;心尖穿刺处封堵器位置良好,各心室壁搏幅正常。提示经心尖穿刺封堵瓣周漏效果良好,穿刺针道预后佳,室壁运动未受影响。

人工心脏瓣膜置换术后瓣周漏(paravalvular leakage,PVL)是瓣膜置换术后特有的并发症,其发生率在国内尚无确切的统计学报道。国外文献报道,外科换瓣术后瓣周漏的发生率在主动脉瓣约为2%~10%,二尖瓣约7%~17%,二尖瓣瓣周漏发生率明显高于主动脉瓣[1]。机械瓣或生物瓣置换术后均可并发瓣周漏,并且机械瓣并发瓣周漏远较生物瓣常见[2]。
二尖瓣瓣周漏时,左心房容量负荷过度增加,随之增加左心室舒张末容量,左心室心搏量增加,心肌代偿性离心性扩大和肥厚以维持正常的前向心搏量(代偿期),持续严重的过度负荷终致左心室心肌功能衰竭,左心室舒张期末压力和左心房压力明显上升,肺瘀血出现,进而导致肺动脉高压和右心室衰竭发生[1]。传统观念认为较大的瓣周漏可引起心力衰竭、心律失常、溶血、心内膜炎等并发症,但临床发现小的瓣周漏也常引起溶血、心内膜炎等并发症。上述情况往往需要重新置换瓣膜,但再次开胸增加了手术风险及术后患者病死率[3]。
既往认为瓣周漏的治疗以再次外科手术为主,手术方式有修补术和再次人工瓣膜置换术两种。外科再次手术风险极高,病死率较高。由于瓣周漏患者多有心内膜炎、营养状况差、贫血、多器官功能不全等合并问题,故而很多临床心脏外科医师对于瓣周漏二次外科手术心存忌惮[2]。近年来,随着心内科介入技术和器械不断发展,经导管堵闭心内缺损或血管异常交通已日趋成熟。1992年Hourihan等率先报道经导管应用Rashkind PDA封堵器成功堵闭主动脉瓣PVL,随后十余年,随着弹簧圈和新型Amplatzer封堵器的问世和改进,以及实时三维超声心动图等影像学技术等发展,国外文献关于PVL介入治疗的报道日益增多,其技术成功率65%~90%,随访中大部分患者术后原有症状明显改善[4]。国内于2010年起在少数临床中心开展此项技术,并逐渐推广。由于介入技术具有微创、安全、有效、简便易行等优势,因此,越来越多的临床经验表明,瓣周漏患者在接受对症保守治疗的同时,应当首先评估是否合适介入封堵术。
二尖瓣瓣周漏一般可通过3种主要通路进行封堵:经股动脉-主动脉瓣-左心室路径,经股静脉-房间隔穿刺-左心房路径,及经心尖路径。根据不同的瓣膜置换术后情况及瓣周漏位置,所选择的封堵路径也不尽相同[3,5]。其中,双机械瓣置换术后二尖瓣瓣周漏的微创封堵尤为复杂。首先,由于主动脉瓣机械瓣影响,术中导丝导管逆行跨过主动脉瓣易导致主动脉瓣反流增加,从而影响血流动力学稳定;其次,外科手术缝合后房间隔增厚,穿刺房间隔技术非常有挑战,且因为术后心脏相对位置改变,易发生穿刺入异常位置导致的并发症;然后,经心尖切口途径创伤相对较大,易并发心尖切口部位出血、心包压塞[6,7,8]。因此,本例手术中我们创新使用经皮心尖穿刺微创封堵二尖瓣瓣周漏,并在术后使用封堵器封堵针道,从而既能快捷顺利的完成封堵,又能避免出血并发症。
目前临床上缺乏针对瓣周漏介入治疗的专用封堵器材,往往采用先天性心脏病的封堵器进行超适应证("off-label")应用。本例手术使用的ADO Ⅱ封堵器由AGA公司生产,结合了PDA封堵器和AVP血管塞的优点,结构设计方面类似于PDA封堵器,而镍钛合金丝的编排等类似于AVP血管塞,亦无阻流体填充,由144股镍钛合金丝组成自膨胀哑铃状装置,腰部直径4~8 mm,两侧盘片成斗笠状,增加了封堵效果,最初用于小型动脉导管未闭的封堵治疗,封堵器较为柔软,配用的5F鞘管,能够很好的通过内径较细或迂曲的PVL。同样,因为其柔软的特性,在封堵心尖时也起到了良好的作用,不至于扩大针道而导致出血。
我中心目前开展微创瓣周漏封堵138台,其中二尖瓣瓣周漏约占67%。随着外科换瓣手术的增多,瓣周漏的患者也在增加,我们此前的研究证实经导管微创封堵人工瓣置换术后PVL是可行和有效的,由于其具有创伤小,恢复快等特点,在具备适应证和手术高危的患者中可作为替代手术的治疗选择[9]。本例患者的成功封堵提示我们,对于双机械瓣置换术后的二尖瓣瓣周漏,经皮心尖穿刺微创封堵可能是创伤小、节省时间、并发症少的优选技术。
所有作者均声明不存在利益冲突



























