
了解新型冠状病毒肺炎(Coronavirus Disease 2019, COVID-19)确诊病例血清抗新型冠状病毒(2019 novel Coronavirus, 2019-nCoV)中和抗体动态变化规律及可能的影响因素。
采用微量中和试验检测COVID-19确诊病例血清中和抗体,采用Excel 2007和SPSS 22.0对COVID-19病例血清中和抗体检测数据进行分析。
采集、检测来自155个COVID-19病例的420份血清样本,包括急性期、恢复期和痊愈半年病例血清样本。采样时间为发病第0~221天。发病第1周血清中和抗体几何平均滴度(geometric mean titer, GMT)为1∶13,第2周为1∶31;个别病例发病第15天血清中和抗体滴度仍表现为<1∶4;发病第6~32周血清中和抗体GMT均超过1∶52(13×4)。以1∶64作为血清中和抗体保护水平分界点,急性期病例(0~14 d,0~2 w)、痊愈病例(36~63 d,6~9 w)和痊愈半年病例血清(183~210 d,27~30 w)中和抗体阳性率分别为30.56%、82.31%和86.52%。统计分析显示,除第1、2周以外,各周血清中和抗体水平无显著性差异(χ2=9.270,P=0.931)。病例血清中和抗体水平在性别、年龄、职业方面不存在统计学差异,普通型和轻型病例血清中和抗体水平不存在统计学差异(P>0.05)。
COVID-19病例血清中和抗体水平仅与疾病进程具有统计学关联;中和抗体在感染后第3周整体上可达到保护性水平,并维持至发病后第30周。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
新型冠状病毒肺炎(Coronavirus Disease 2019, COVID-19)是由新型冠状病毒(2019 novel Coronavirus, 2019-nCoV)引起的呼吸道传染性疾病。河南省COVID-19流行趋势与全国流行趋势基本相同[1,2,3]。为掌握人群感染2019-nCoV后血清中和抗体水平动态变化趋势和影响因素,河南省疾病预防控制中心以河南省信阳市为研究现场,收集COVID-19病例急性期、恢复期和痊愈半年血清样本进行抗2019-nCoV中和抗体(以下简称中和抗体)检测和结果分析。
以2020年春季信阳市COVID-19确诊病例作为研究对象。COVID-19病例诊断均采用实时荧光定量RT-PCR方法检测咽拭子样本,病毒核酸阳性即为确诊病例。临床症状轻微,影像学未见肺炎表现者为轻型病例;具有发热、呼吸道等症状,影像学可见肺炎表现者为普通型病例。
将2019-nCoV病毒悬液水浴解冻,于4 ℃、12 000×g条件下离心15 min,取上清液分装至2.0 ml细胞冻存管,每管1.0 ml。放置-80 ℃冰箱备用。
取8支1.5 ml无菌EP管作为病毒稀释管并做好标记,每管加入900 μl细胞维持液。采用无菌带滤芯加长枪头在第1支管中加入100 μl病毒原液,混匀后取100 μl加至第2支管,依次将病毒稀释为10-1至10-8倍的悬液。取96孔细胞培养板作为病毒滴定板,将病毒悬液加入板内,每稀释度8孔,每孔100 μl。最后在每孔加入1.0×105个/ml的Vero细胞悬液100 μl,同时设立细胞对照(100 μl维持液+100 μl细胞悬液),36.5 ℃连续培养7 d,观察细胞病变(cytopathic effect, CPE)。按Behrens-Kärber公式计算出2019-nCoV的CCID50。
取96孔细胞培养板作为样本稀释板,每个样本6孔,每孔加入150 μl细胞维持液并做好标记。采用无菌带滤芯枪头分别取50 μl待检血样加入第1孔和第6孔,轻轻吹吸充分混匀,然后自第1孔取50 μl稀释液加至第2孔,按照此方法将待检血样稀释为41至45。取96孔细胞培养板作为检测板,每个样本12孔,每个稀释度双孔,每孔50 μl;第11、12孔各加50 μl 4倍稀释血清作为对照。除对照孔以外,每孔加入50 μl稀释至100CCID50/50 μl的病毒悬液,对照孔加入50 μl细胞维持液,混匀后于36.5 ℃中和反应1 h,然后在每孔加入1.0×105个/ml的Vero细胞悬液100 μl,36.5 ℃连续培养7 d,观察CPE,判定结果。
参照病毒滴定,稀释病毒得到100CCID50/50 μl、10CCID50/50 μl、1CCID50/50 μl和0.1CCID50/50 μl的2019-nCoV病毒悬液。取96孔细胞培养板作为病毒回滴板,将稀释后的病毒悬液加入细胞板内,每稀释度8孔,每孔100 μl。最后在每孔加入1.0×105个/ml的Vero细胞悬液100 μl,同时设立细胞对照(100 μl维持液+100 μl细胞悬液),36.5 ℃连续培养7 d,观察CPE。
病毒回滴在32~320 CCID50/50 μl视为结果有效。当待检样本最高稀释度血清的2孔中有1孔出现CPE,另1孔没有出现CPE,该稀释度的倒数即为该样本的中和抗体效价;当高稀释度2孔完全病变,相邻低稀释度2孔完全不病变,则两者平均稀释度的倒数为该样本的中和抗体效价;当两个相邻稀释度血清均出现1孔CPE,另1孔不出现CPE,则两者平均稀释度的倒数即为该样本的中和抗体效价。
COVID-19病例样本的采集和实验活动严格遵守相关的生物安全规定。采样人员在采样过程中采取个人生物安全三级防护;所有涉及2019-nCoV活病毒的操作均在BSL-3级实验室进行;实验室废弃物严格按照相关生物安全规定进行处理。
采用Excel 2007表格录入数据,采用SPSS22.0进行数据统计分析。应用多独立样本非参秩和检验分析中和抗体时间和职业差异,应用两独立样本非参秩和检验分析中和抗体的年龄、性别和病例类型(普通型和轻型)差异,卡方检验分析中和抗体保护率差异,检验水准α=0.05。
本研究检测血清样本420份,采样时间为发病后第0~221天。样本来自155个病例,其中男性87例,女性68例,男女比例为1.28∶1。病例年龄最低6岁,最高82岁,年龄中位数52岁。所有病例采用实时荧光定量RT-PCR方法检测咽拭子样本,2019-nCoV核酸阳性即为确诊病例。
采用2019-nCoV HN02株(GenBank序列号:MT412134)作为攻击病毒,病毒CCID50/100 μl值为104。以200倍稀释的HN02株作为攻击浓度,分6个批次完成420份血清样本的检测,6个批次的病毒回滴值均为100CCID50/50 μl。病例发病1周中和抗体几何平均滴度(geometric mean titer, GMT)为1∶13,发病第2周为1∶31,两周以后中和抗体GMT均超过1∶52(13×4),详见表1。120个急性期病例中,滴度小于1∶4的病例15例,其中13例病例的采样时间间隔在5 d以内,1例病例的采样时间间隔为11 d,1例病例的采样时间间隔为15 d。
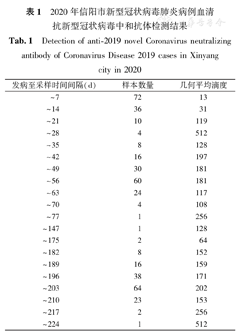
2020年信阳市新型冠状病毒肺炎病例血清抗新型冠状病毒中和抗体检测结果
Detection of anti-2019 novel Coronavirus neutralizing antibody of Coronavirus Disease 2019 cases in Xinyang city in 2020
2020年信阳市新型冠状病毒肺炎病例血清抗新型冠状病毒中和抗体检测结果
Detection of anti-2019 novel Coronavirus neutralizing antibody of Coronavirus Disease 2019 cases in Xinyang city in 2020
| 发病至采样时间间隔(d) | 样本数量 | 几何平均滴度 |
|---|---|---|
| ~7 | 72 | 13 |
| ~14 | 36 | 31 |
| ~21 | 10 | 119 |
| ~28 | 4 | 512 |
| ~35 | 8 | 128 |
| ~42 | 16 | 197 |
| ~49 | 30 | 181 |
| ~56 | 60 | 181 |
| ~63 | 24 | 117 |
| ~70 | 4 | 108 |
| ~77 | 1 | 256 |
| ~147 | 1 | 128 |
| ~175 | 2 | 64 |
| ~182 | 8 | 152 |
| ~189 | 16 | 159 |
| ~196 | 38 | 171 |
| ~203 | 64 | 202 |
| ~210 | 23 | 153 |
| ~217 | 2 | 256 |
| ~224 | 1 | 512 |
采用非参秩和检验分析中和抗体水平时间(周)变化规律,差异具有统计学意义(χ2=122.739,P=0.000);去除第1、2周数据后再行分析,差异不具有统计学意义(χ2=9.270,P=0.931)。
420份血清样本含发病后第1次采集血清样本120份,对应120个病例。其中,男性64例,女性56例,男女比例1.14∶1;年龄最低者9岁,最高83岁,年龄中位数52岁;民工66人,商业服务17人,家务待业15人,教师学生7人,干部8人,离退职工5人,医生2人;普通型病例92例,轻型病例28例。采用非参秩和检验分析中和抗体水平性别、年龄(以10为层级)、职业和病例类型变化规律,差异均无统计学意义(P>0.05)。详见表2。
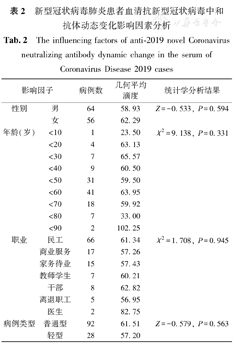
新型冠状病毒肺炎患者血清抗新型冠状病毒中和抗体动态变化影响因素分析
The influencing factors of anti-2019 novel Coronavirus neutralizing antibody dynamic change in the serum of Coronavirus Disease 2019 cases
新型冠状病毒肺炎患者血清抗新型冠状病毒中和抗体动态变化影响因素分析
The influencing factors of anti-2019 novel Coronavirus neutralizing antibody dynamic change in the serum of Coronavirus Disease 2019 cases
| 影响因子 | 病例数 | 几何平均滴度 | 统计学分析结果 | |
|---|---|---|---|---|
| 性别 | 男 | 64 | 58.93 | Z=-0.533,P=0.594 |
| 女 | 56 | 62.29 | ||
| 年龄(岁) | <10 | 1 | 23.50 | χ2=9.138,P=0.331 |
| <20 | 4 | 63.13 | ||
| <30 | 7 | 65.57 | ||
| <40 | 9 | 60.50 | ||
| <50 | 31 | 59.50 | ||
| <60 | 41 | 63.95 | ||
| <70 | 18 | 59.92 | ||
| <80 | 7 | 33.00 | ||
| <90 | 2 | 102.25 | ||
| 职业 | 民工 | 66 | 61.34 | χ2=1.708,P=0.945 |
| 商业服务 | 17 | 57.26 | ||
| 家务待业 | 15 | 57.43 | ||
| 教师学生 | 7 | 60.21 | ||
| 干部 | 8 | 62.82 | ||
| 离退职工 | 5 | 56.95 | ||
| 医生 | 2 | 82.75 | ||
| 病例类型 | 普通型 | 92 | 61.51 | Z=-0.579,P=0.563 |
| 轻型 | 28 | 57.20 | ||
病例发病第1周中和抗体GMT为1∶13,以1∶52(13×4)作为中和抗体保护性滴度的分界点。
如表1所示,急性期病例(0~14 d, 0~2 w)中和抗体保护率为30.56%(33/108),恢复期病例(36~63 d, 6~9 w)为82.31%(107/130),痊愈半年病例(183~210 d, 27~30 w)为86.52%(122/141)。比较急性期、恢复期和痊愈半年病例中和抗体保护率,差异具有统计学意义(χ2=105.873,P=0.000);比较恢复期和痊愈半年病例中和抗体保护率,差异无统计学意义(χ2=0.625,P=0.429)。
本研究整体代表性较好[4,5,6]。研究显示机体感染2019-nCoV后可产生保护性中和抗体,且抗体水平随时间推移逐渐上升,两周后整体达到保护性水平,保护性可持续至发病后第30周。
我国COVID-19疫情在短期内得到了有效控制[7,8,9]。本研究显示COVID-19病例中和抗体水平在年龄、性别、职业方面均不存在统计学差异,发病第3周以来各周血清中和抗体水平不存在统计学差异,初步证实病例自2020年1~2月感染2019-nCoV以来没有再接受过2019-nCoV的有效刺激,进一步证实国内疫情防控措施成效显著。
本研究显示自然感染情况下COVID-19病例血清中和抗体整体保护率可以达到84.50%,与人工免疫效果接近[10,11]。需要注意的是,自然感染2019-nCoV具有诸多不可控因素,且感染途径和感染剂量具有随机性。尽管COVID-19病例以轻型和普通型为主,重型和危重型病例占比较小,但是中国是一个人口大国,人口密度远高于世界平均水平。一旦疫情在中国蔓延,防控压力非常艰巨。同时,本研究个别COVID-19病例在采样第15天血清中和抗体滴度仍然小于1∶4,这种现象应该引起重视,有必要针对2019-nCoV无症状感染者进行中和抗体水平的连续观察。
所有作者均声明不存在利益冲突



























