
多发性硬化(MS)是以中枢神经系统炎性脱髓鞘病变为主要特点的免疫介导性疾病,是青壮年人群神经功能残疾的最常见原因之一。明确MS的诊断和临床分型,对于MS患者的尽早治疗和治疗策略选择至关重要。临床医师可充分收集患者客观的临床证据,排除其他鉴别诊断后,参考目前的诊断标准对MS的时间多发性和空间多发性进行全面评估,并依据其临床分型标准指导治疗策略选择。目前针对MS诊断的检查技术和评估方式多处于研究探索阶段,相信未来MS诊断的敏感度和特异度将得到进一步提升。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
经全国继续医学教育委员会批准,本刊开设继教专栏,2022年从第3期开始共刊发10篇继教文章,文后附5道单选题,读者阅读后可扫描标签二维码答题,每篇可免费获得Ⅱ类继教学分0.5分,全年最多可获5分。本年度继教答题得学分活动于10月31日结束。
多发性硬化(multiple sclerosis,MS)是以中枢神经系统(central nervous system,CNS)炎性脱髓鞘病变为主要特点的免疫介导性疾病[1],在临床上以神经系统症状和体征、影像学等方面的时间多发性(disseminated in time,DIT)和空间多发性(disseminated in space,DIS)为特点。作为一种免疫相关疾病,MS主要累及青壮年。同时,由于病灶累及CNS多个部位且病情呈反复发作或进展,如不及时治疗将导致显著的神经功能残疾。因此,MS是青壮年人群神经功能残疾的最常见原因之一,MS的早诊断、早治疗对改善患者预后有重要的临床意义。
然而,由于MS临床表现复杂多样且缺乏特异性辅助检查指标,其早期诊断困难,影响早期治疗。目前国际上普遍推荐的诊断标准是2017年McDonald MS诊断标准[2]和2015年MAGNIMS MS MRI诊断标准[3]。根据国际上MS的诊断标准,同时结合我国MS患者的临床特点,我国学者制订了一系列更适合应用于我国MS患者的临床共识和指南[4, 5, 6, 7],其中最新版为中国免疫学会神经免疫分会和中华医学会神经病学分会神经免疫学组制订的《多发性硬化诊断和治疗中国专家共识(2018版)》[1]。此外,随着近年来人们对MS临床特点和发病机制的深入探讨,一些新的进展将有可能应用于MS的诊断与鉴别诊断当中。
首先,MS的诊断需要客观的临床证据,因此应以客观病史和临床体征为基本依据,充分结合各种辅助检查特别是MRI与脑脊液(cerebrospinal fluid)检查结果。其次,根据这些MS诊断的客观临床证据是否符合病变的DIS与DIT特点,判断MS的诊断是否成立。再次,在确立MS的诊断后需要进行临床分型,以指导MS的治疗策略选择。最后,还需要通过鉴别诊断排除其他相似疾病的可能性[1]。
MRI是MS诊断最重要的辅助检查手段。目前MS的诊断标准均纳入了MRI的相关证据。2021年多发性硬化磁共振成像研究组-多发性硬化中心联盟-北美多发性硬化成像协作MRI指南工作组(Magnetic Resonance Imaging in Multiple Sclerosis Study Group-Consortium of Multiple Sclerosis Centres-North American Imaging in Multiple Sclerosis Cooperative MRI Guidelines Working Group;MAGNIMS-CMSC-NAIMS)推出的最新版MS患者MRI应用共识中推荐,应根据临床需要对患者进行头颅、脊髓和视神经MRI检查[8]。我国2018年MS诊疗共识建议所有考虑MS诊断的患者进行头颅MRI检查,推荐的基本序列包括平扫(2D矢状面FLAIR、2D横断面T1、T2、DWI)及增强(横断面T1)[1, 2]。脊髓MRI检查对于以脊髓症状首发、原发-进展型MS(primary-progressive multiple sclerosis,PPMS)和一些非典型临床表现的患者可以增加诊断的可靠性,其推荐序列包括矢状面T1、T2,连续横断面T1、T2以及增强后矢状面、横断面T1[1, 2]。MRI上的视神经病灶也被纳入2015年MAGNIMS MS MRI的诊断标准中,因此,视神经MRI也有助于MS的诊断,尤其对于出现视神经受累的患者[3]。
一些新的MRI技术也逐渐开始被应用到MS的诊断中。如T2*或磁敏感加权成像序列上MS病变的“中央静脉征”可能是MS诊断的影像学标志物[9];扩散张量成像(diffusion tensor imaging)和磁化转移成像(magnetization transfer imaging)序列更容易检测和定量细微的组织异常,可能有助于预测进行性残疾和认知障碍;磁共振波谱(magnetic resonance spectroscopy)可以定量检测脑组织的不同代谢产物,显示MS的神经轴突损伤和胶质细胞活性;双重翻转复原成像(double inversion recovery)序列能够更清晰地显示灰质,便于观察灰质病变的程度和分布。但目前认为尚未有足够的证据支持在MS的诊断标准中加入上述MRI检查[10]。
脑脊液OCB是另一项被纳入MS诊断标准的辅助检查。2017年,McDonald MS诊断标准提高了脑脊液 OCB在MS诊断中的地位。推荐脑脊液 OCB可以作为DIT的替代指标。因此,对于具有典型临床孤立综合征且符合临床或MRI的DIS标准且对临床表现没有更好解释的患者,在没有其他非典型MS脑脊液表现的情况下,患者存在脑脊液 OCB时,即可诊断为MS[2]。同时,建议在拟诊为MS的非典型患者中进行脑脊液检查,有助于MS的诊断与鉴别诊断。同样的,在我国2018年的MS诊疗共识中,无论诊断原则或诊断标准都强调了脑脊液检查对于MS诊断的重要性[2]。
MS的名称源于其DIS和DIT。从概念上说,DIS是指CNS内不同解剖部位病变的发展,即CNS多灶性病变;DIT是指随着时间的推移,新的CNS损害的发展或出现[2]。2017年的McDonald MS诊断标准[2]和2015年的MAGNIMS MS MRI诊断标准[3]都有各自DIS和DIT的MRI推荐标准(表1)。

多发性硬化的空间多发性和时间多发性MRI标准
Magnetic resonance imaging criteria for dissemination in space and dissemination in time in multiple sclerosis
多发性硬化的空间多发性和时间多发性MRI标准
Magnetic resonance imaging criteria for dissemination in space and dissemination in time in multiple sclerosis
| 项目 | 2017年McDonald MS诊断标准[2] | 2015年MAGNIMS MS MRI诊断标准[3] |
|---|---|---|
| 空间多发性 | 在下述4个CNS部位中的2个或更多部位,存在1个或更多MS特征性的T2高信号病灶: | 可通过以下5个CNS区域中至少2个区域的参与b来证明: |
| 脑室旁a | ≥3个脑室旁病灶 | |
| 皮质或皮质下 | ≥1个皮质/近皮质病灶c | |
| 幕下脑区 | ≥1个幕下病变 | |
| 脊髓 | ≥1个脊髓病灶 | |
| ≥1个视神经病灶 | ||
| 时间多发性 | 任何时候同时存在钆增强和非增强病灶或与基线MRI的时间无关,与基线扫描相比,随访MRI上发现新的T2高信号病灶或钆增强病灶 | |
注:a对于年龄>50岁或有血管性危险因素的患者,临床医师需要谨慎寻找更多数量的脑室旁病灶;b如果受试者患有脑干或脊髓综合征或视神经炎,症状性病变不排除在标准之外,并有助于病变计数;c这一组合术语表示皮质旁的白质受累和(或)皮质受累,从而扩展了“皮质旁”病变这一术语;MS:多发性硬化;MAGNIMS:多发性硬化磁共振成像研究组;MRI:磁共振成像;CNS:中枢神经系统
各个版本的McDonald MS诊断标准[2,11, 12, 13]和MAGNIMS MS MRI诊断标准[3,14]是MS诊断中相辅相成的诊断标准系列。2010年McDonald MS诊断标准[13]在MRI的DIS和DIT方面采纳了2007年MAGNIMS MS MRI诊断标准的部分内容[14]。
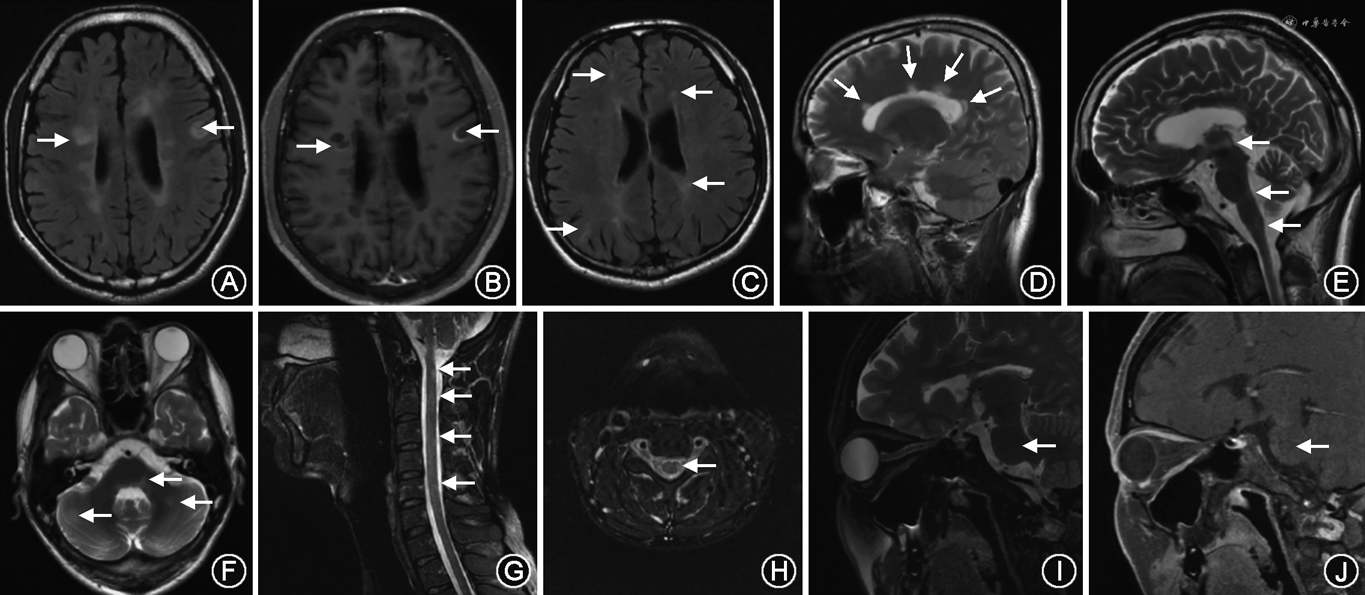
2017年新版的McDonald MS诊断标准和2015年MAGNIMS MS MRI诊断标准有很多共同点,如与既往指南相比,都纳入了皮质病灶、幕下/脊髓症状性病灶等。两版指南也均有相似的推荐,如2017年McDonald MS诊断标准建议年龄较大和有脑血管病基础的患者需要增加脑室旁病灶的数量[2],而2015年MAGNIMS MS MRI诊断标准建议增加脑室旁病灶数量至≥3个[3]。二者的不同点主要在于2015年MAGNIMS MS MRI诊断标准纳入了视神经MRI病灶,使MS的CNS典型受累区域增加至5个[3](图1),而2017年McDonald MS诊断标准认为视神经MRI病灶对MS具有诊断意义的证据尚不充分[2]。此外,2017年McDonald MS诊断标准[2]对于PPMS有其独立的诊断标准,而2015年MAGNIMS MS MRI诊断标准建议对PPMS和复发型MS采用相同的DIS标准,并建议对于临床不确定的PPMS患者应考虑将脑脊液结果作为诊断参考[3]。

具有MS相关专业知识的临床医师结合患者病史、体检结果、影像学和实验室证据作出的临床判断,仍然是诊断MS的基础[2]。同时,结合MS的诊断标准可极大地提高MS诊断的敏感度与特异度。但MS作为一种复杂疾病,对于非典型患者需要进一步的临床和放射学随访。对于成人MS,目前我国《多发性硬化诊断和治疗中国专家共识(2018版)》[2]推荐使用2017年McDonald MS的诊断标准(表2,3)。

2017年McDonald 多发性硬化诊断标准(以发作起病的患者a)[2]
The 2017 McDonald criteria for diagnosis of multiple sclerosis patients with an attack at onset
2017年McDonald 多发性硬化诊断标准(以发作起病的患者a)[2]
The 2017 McDonald criteria for diagnosis of multiple sclerosis patients with an attack at onset
| 发作类型 | 有客观临床证据的病变数量 | 诊断多发性硬化需要的附加数据 |
|---|---|---|
| ≥2次临床发作 | ≥2 | 无b |
| ≥2次临床发作 | 1(并且有明确的历史证据证明以往的发作累及不同解剖部位的1个病灶c) | 无b |
| ≥2次临床发作 | 1 | 通过不同CNS部位的额外临床发作或MRI检查证明了空间多发性c |
| 1次临床发作 | ≥2 | 通过额外的临床发作或MRI检查证明了时间多发性或具有脑脊液寡克隆带的证据d |
| 1次临床发作 | 1 | 通过不同CNS部位的额外临床发作或MRI检查证明了空间多发性c,并且通过额外的临床发作或MRI检查证明了时间多发性,或具有脑脊液寡克隆带的证据d |
注:CNS:中枢神经系统;MRI:磁共振成像;如果患者满足2017年McDonald诊断标准,并且临床表现没有更符合其他疾病诊断的解释,则可诊断为多发性硬化(MS);如因临床孤立综合征怀疑为MS,但并不完全满足2017年McDonald标准,则诊断为可能的MS;如果在疾病评估中出现其他可以更好地解释患者临床表现的诊断,则排除MS。a是指复发性MS,包括复发-缓解型多发性硬化、继发-进展型多发性硬化;b不需要额外检测来证明空间和时间多发性。然而除非患者无法应用磁共振成像(MRI),否则所有考虑诊断为MS的患者均应该接受头颅MRI检查;如果完成影像学或其他检查(如脑脊液)且结果为阴性,则在作出MS诊断之前需谨慎,并且应该考虑其他可替代的诊断;c基于2次发作的客观临床证据所作出的临床诊断是最可靠的,1次既往发作的合理历史证据可以包括伴符合既往炎性脱髓鞘发作症状和演变特点的历史事件,但至少有1次发作必须得到客观证据的支持,在没有神经系统残余客观证据的情况下,诊断需要谨慎;d尽管脑脊液特异性寡克隆区带阳性本身并未体现出时间多发性,但可以作为时间多发性的替代指标

2017年McDonald MS诊断标准(原发-进展型MS)[2]
2017 McDonald criteria for diagnosis of multiple sclerosis patients(primary progressive multiple sclerosis)
2017年McDonald MS诊断标准(原发-进展型MS)[2]
2017 McDonald criteria for diagnosis of multiple sclerosis patients(primary progressive multiple sclerosis)
| 诊断标准 |
|---|
1.独立于临床复发的残疾进展1年(回顾性或前瞻性确定) 2.加上以下标准的其中2项: A:1个或多个MS特征性T2高信号病变在以下1个或多个脑区:脑室旁、皮质或皮质下或幕下 B:脊髓中的2个或多个T2高信号病变 C:脑脊液存在特异性寡克隆区带 |
注:MS:多发性硬化
《多发性硬化诊断和治疗中国专家共识(2018版)》推荐采用2013年国际MS分型[15],即把MS分为复发-缓解型(relapsing-remitting multiple sclerosis,RRMS)、继发-进展型(secondary-progressive multiple sclerosis,SPMS)和PPMS。新的MS国际临床分型通过临床综合评估引入了“疾病进展性”(变性)和“疾病活动性”(炎性)的概念,有利于辅助MS的治疗决策和预后判断[16]。
按照“疾病进展性”的不同特点,可将MS分为:(1)复发型:主要指RRMS,其特点是复发伴发作之间神经功能障碍稳定。(2)进展型:其特点是与复发无关的、稳步增加的、客观记录到的神经功能障碍,可能出现病情波动、稳定期和叠加复发。该分型可进一步划分为:SPMS(在最初的复发-缓解过程后的进行性加重)和PPMS(从疾病开始的进行性加重)。在进展型MS中,根据“疾病活动性”取消了进展-复发型MS(progressive relapsing multiple sclerosis,PRMS)的概念,即把既往符合PRMS标准的伴有急性发作(有疾病活动)的进展型MS纳入“活动性PPMS”;把无急性发作(无疾病活动)的进展型MS纳入“非活动性PPMS”。
在诊断MS时,应根据上一年的病史判断当时的MS病程分型,以及该病程是否进展、是否活跃。并应根据随访收集的信息定期重新评估临床表型[2]。
此外,根据MS患者的发病情况及预后,我国2018年MS诊疗共识仍然保留了良性型MS和恶性型MS这两种与国际通用临床分型存在一定交叉的少见临床类型[1]。
DIS和DIT是MS病情和病程的基本特点,但并不仅见于MS。MS的诊断标准是基于充分排除其他疾病的前提下,拟对高度怀疑MS的疾病表现进行确诊而设计的。因此,MS在确诊前还需要与其他症状、体征或影像学上同样具有DIS和DIT的疾病进行鉴别诊断。其中包括其他CNS特发性炎性脱髓鞘疾病(idiopathic inflammatory-demyelinating diseases,IIDDs)、脑血管病、感染性疾病、结缔组织病、肉芽肿性疾病、肿瘤、遗传代谢性病等。
其中,需要与MS重点鉴别的疾病是其他IIDDs,尤其是视神经脊髓炎谱系疾病(neuromyelitis optica spectrum disorders)[17, 18]和抗髓鞘少突胶质细胞糖蛋白免疫球蛋白G抗体相关疾病(anti-myelin oligodendrocyte glycoprotein-IgG associated disorders)[19],具体鉴别要点详见表4。同时,MS还需要与急性播散性脑脊髓炎(acute disseminated encephalomyelitis)、视神经炎、脊髓炎、脑干脑炎、脱髓鞘假瘤等疾病相鉴别。

MS与NMOSD和MOGAD的鉴别诊断要点
Key points of differential diagnosis between MS,NMOSD and MOGAD
MS与NMOSD和MOGAD的鉴别诊断要点
Key points of differential diagnosis between MS,NMOSD and MOGAD
| 项目 | MS | AQP4-IgG阳性NMOSD | MOGAD |
|---|---|---|---|
| 生物学标志物 | 脑脊液寡克隆区带阳性 | 血清AQP4-IgG阳性 | 血清MOG-IgG阳性 |
| 性别比例(女∶男) | 1.5∶1~2∶1 | 5∶1~11∶1 | 2∶1~1∶1 |
| 好发年龄 | 20~30岁 | 20~40岁 | 儿童期较成人常见 |
| 病程 | 复发缓解型或慢性进展型 | 单相型;复发型(多见) | 单相型;复发型(常表现为视神经炎) |
| 临床表现 | 视神经炎、脊髓炎、脑干或小脑症状,认知功能障碍和累及其他MS典型脑区的症状 | 视神经炎、脊髓炎、极后区综合征、脑干综合征、嗜睡或急性间脑综合征,伴NMOSD典型脑部病灶的脑部症状 | 急性播散性脑脊髓炎样表型(儿童多见),或视神经-脊髓表型(成人多见)或脑干脑炎 |
| 头颅MRI | 脑室旁(毗邻侧脑室的大脑白质病变,直角征)、皮质/近皮质(大脑皮质内的病灶/大脑白质病变,毗邻皮质)、幕下(脑干病灶通常靠近表面、小脑脚或小脑),圆形、类圆形病变 | 延髓最后区、第三和第四脑室周围、下丘脑、丘脑病变,皮质下或深部较大融合的白质病变,胼胝体病变较长较弥散(>1/2 胼胝体)、沿锥体束走行对称较长病变 | 多发或单发白质病灶,斑片状,可伴有丘脑、海马、皮质/近皮质病灶,大病灶肿瘤样,可见软脑膜受累 |
| 脊髓MRI | 短节段病灶;偏侧 | 长节段病灶(纵向延伸超过3个椎体节段);中央 | 长或短节段病灶,横断面可见于中央或周边,累及腰髓/圆锥为相对特异性表现 |
| 视神经MRI | 短节段病灶 | 长病灶(长于视神经的1/2),视神经后段或视交叉病灶 | 长病灶(长于视神经的1/2),视神经前段病灶 |
| 脑脊液白细胞增多 | 中度(<50%的患者) | 常见(>70%的患者) | 常见(>70%的患者) |
| 治疗 | 免疫调节剂 | 免疫抑制剂 | 免疫抑制剂 |
| 预后 | 致残率高,与疾病进展相关 | 致残率高,与高复发率和发作时恢复不良相关 | 致残率低,发作后恢复较好;部分患者初次发作恢复差 |
注:MS:多发性硬化;NMOSD:视神经脊髓炎谱系疾病;MOGAD:抗髓鞘少突胶质细胞糖蛋白免疫球蛋白G抗体相关疾病;MRI:磁共振成像;AQP4:水通道蛋白4
明确MS的诊断和临床分型,对于MS患者的尽早治疗和治疗策略选择至关重要。临床医师可充分收集患者的客观临床证据,排除其他疾病后,参考目前的诊断标准对MS患者的DIT和DIS进行全面评估,并依据其临床分型标准指导治疗策略的选择。目前,关于MS诊断的更多检查技术和评估方式正在研究探讨阶段,相信在未来MS诊断的敏感度和特异度将得到进一步提高。
所有作者声明不存在利益冲突
None declared
1.多发性硬化(MS)的诊断相关辅助检查包括?
A.MRI和脑脊液寡克隆区带
B.诱发电位
C.光学相干断层扫描
D.风湿免疫相关抗体
2.在2017年McDonald MS诊断标准中,支持MS空间多发性的典型病灶部位,不包括下列哪一项?
A.脑室旁
B.皮质或皮质下
C.幕下脑区和脊髓
D.视神经
3.目前我国《多发性硬化诊断和治疗中国专家共识(2018版)》推荐的MS诊断标准是?
A.2010年McDonald MS诊断标准
B.2017年McDonald MS诊断标准
C.2007年MAGNIMS MS MRI诊断标准
D.2016年MAGNIMS MS MRI诊断标准
4.对于原发-进展型MS的诊断要点的描述,错误的是?
A.必须要2年以上的独立于临床复发的残疾进展(回顾性或前瞻性确定)
B.1个或多个MS特征性T2高信号病变在以下1个或多个脑区:脑室旁、皮质或皮质下、幕下
C.脊髓中的2个或多个T2高信号病变
D.脑脊液特异性寡克隆区带的存在
5.目前的MS病程临床分型,不包括下列哪一项?
A.复发-缓解型
B.继发-进展型
C.进展-复发型
D.原发-进展型



























