
系统性红斑狼疮(SLE)合并烟曲霉菌脑脓肿较为罕见,需要和细菌性脑脓肿及神经精神狼疮进行鉴别。文中报道2例手术确诊SLE合并烟曲霉菌脑脓肿的病例。例1为34岁女性,诊断SLE 6个月后出现抽搐及意识障碍,首次住院时因为影像学阴性被诊断为神经精神狼疮,出院后复查头颅磁共振成像发现脓肿样信号。例2为20岁男性,诊断SLE 3年后出现高热、抽搐及意识障碍,头颅影像学表现为脓肿样信号。2例患者脑脊液病原学均阴性,通过脓肿切除或引流病理确诊为烟曲霉菌脑脓肿,经予伏立康唑治疗后症状缓解、病灶消退。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
系统性红斑狼疮(systemic lupus erythematosus,SLE)患者合并中枢神经系统(central nervous system,CNS)烟曲霉菌感染在临床上较为罕见,目前国内仅有4例报道[1, 2, 3, 4],诊疗经验相对缺乏。在定性诊断方面,由于临床表现相似,需与神经精神狼疮(neuropsychiatric lupus,NPSLE)进行鉴别,影像学显示脑脓肿样改变为重要的鉴别依据。病原诊断则更为困难,部分患者的脑脊液检查均为阴性,这类患者往往需要在经验性抗感染治疗无效后行手术以明确病原。现报道2例血清及脑脊液检查均为阴性,依靠术后病理确诊SLE合并烟曲霉菌脑脓肿的病例。
临床资料 例1 患者女性,34岁,因皮肤黏膜出血、水肿、腹水于2021年3月诊断“系统性红斑狼疮”,予泼尼松55 mg 1次/d、吗替麦考酚酯1 g 2次/d、环孢素100 mg 2次/d、羟氯喹0.2 g 2次/d,辅以利尿治疗,症状逐渐好转。2021年9月初患者出现数次发作性愣神,自诉意识清楚但无法回答他人言语,每次持续约3~5 min。予停用环孢素、静脉甲泼尼龙冲击+静脉注射免疫球蛋白(intravenous immunoglobulin,IVIG)治疗。9月25日晚患者突发大叫一声,双上肢抽动后意识丧失,持续数分钟后意识转清楚。考虑NPSLE可能,收入北京协和医院风湿免疫科病房。
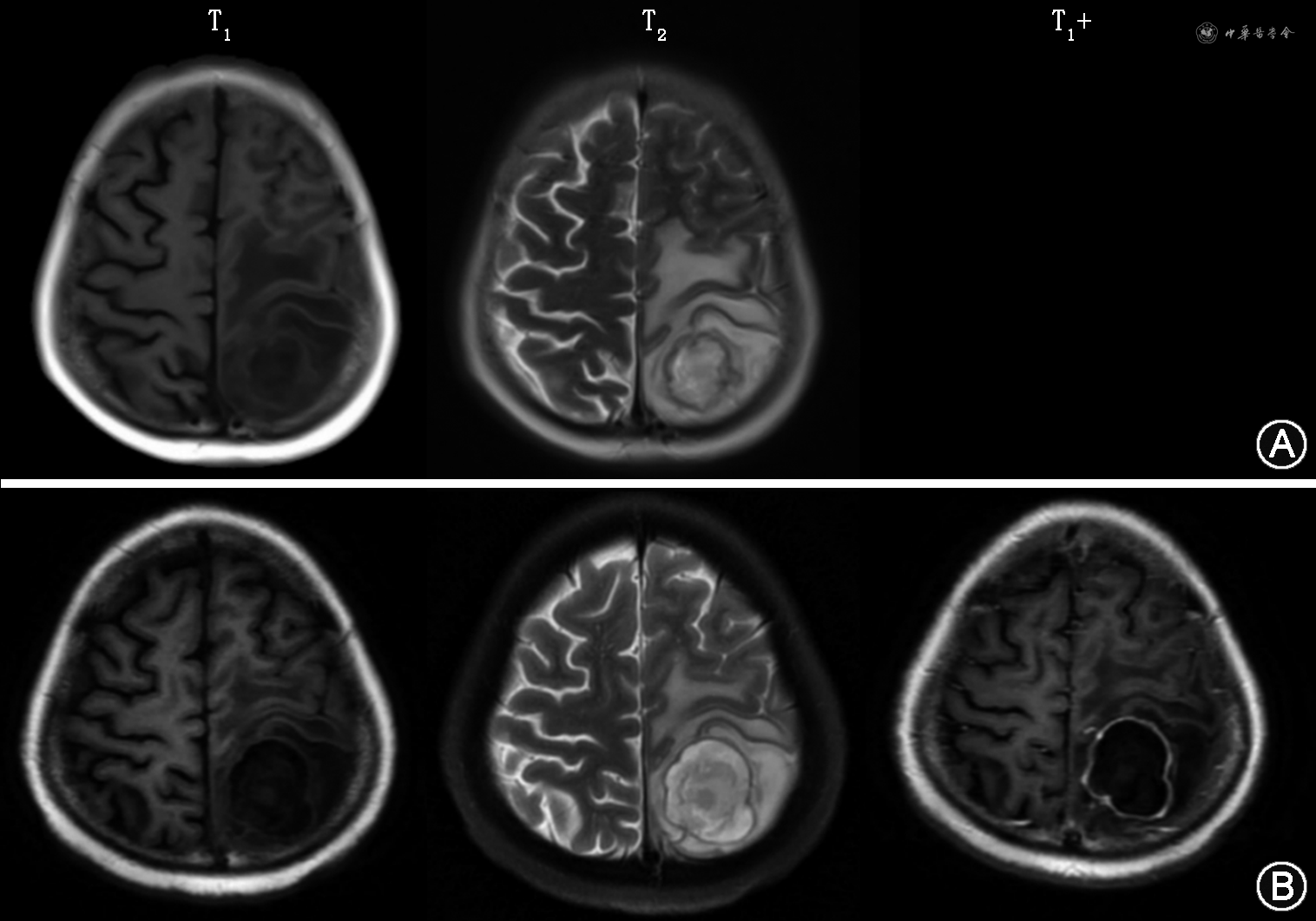
首次住院完善相关检查,血小板计数 7×109/L;尿红细胞183.6×106/L,异形红细胞占30%;血清白蛋白19 g/L,血肌酐33 μmol/L;24 h尿蛋白17.13 g;抗核抗体阳性,滴度1∶100,抗SSA抗体(++),IgG 6.64 g/L,C3 1.367 g/L,C4 0.408 g/L;头颅增强磁共振成像(MRI)及磁敏感加权成像:未见脑内病灶(图1A)。腰椎穿刺:脑脊液压力162 mmH2O(1 mmH2O=0.009 8 kPa),白细胞计数2×106/L,脑脊液蛋白、葡萄糖、氯化物无明显异常,自身免疫性脑炎+副肿瘤抗体、病原学均(-)。临床诊断:SLE,血液系统、肾脏受累,NPSLE不除外。继续口服泼尼松、羟氯喹、左乙拉西坦、厄贝沙坦,辅以IVIG等治疗后患者逐渐好转并出院。


T1+:对比度增强T1加权成像
出院后患者未有抽搐发作,2021年12月复查头颅MRI示:左侧额叶靶形T1低信号、T2高信号,增强后环形强化,周围多发大片状T1低信号、T2高信号(图1B)。考虑颅内病灶为脓肿可能,再次收入病房,完善原发病评估:血常规、血肌酐无明显异常,血清白蛋白23 g/L,24 h尿蛋白4.49 g;抗SSA、抗Ro52抗体阳性,IgG 5.87 g/L,C3、C4正常。血清(1,3)-β-D葡聚糖试验(G试验)、半乳甘露聚糖试验(GM试验)均阴性。腰椎穿刺脑脊液压力为175 mmH2O,脑脊液常规、生化、细胞学、细菌、真菌涂片培养及脑脊液第二代测序(next-generation sequencing,NGS)均为阴性。PET/CT:左额叶白质区囊性结节,仅囊壁有轻度代谢活性,最大标准摄取值7.7,伴周围大片水肿。治疗上继续予泼尼松、羟氯喹、左乙拉西坦,加以罗氏芬2 g 1次/12 h静脉点滴17 d,复查头颅增强MRI未见变化(图1C)。多学科会诊建议开颅行手术切除活组织检查(活检),术前抗感染改为美罗培南2 g 1次/8 h+万古霉素1 g 1次/12 h。2022年1月25日全身麻醉后行神经导航下左额叶脓肿切除术,组织培养提示烟曲霉菌(图2,3),NGS回报烟曲霉菌、细环病毒、人类疱疹病毒5型,病理检查(图4)示:坏死物、真菌(曲菌)菌丝及肉芽组织,周边极少许水肿的神经组织。特染结果:过碘酸雪夫染色(periodic acid-Schiff staining)阳性,六胺银染色阳性。抗感染方案遂改为伏立康唑0.2 g 1次/12 h联合美罗培南2 g 1次/8 h。患者未再出现发热及神经系统症状,原发病好转后于2022年2月24日出院。出院后继续口服伏立康唑片0.2 g 1次/12 h,于2022年3月21日及2022年4月4日规律复诊,诉无癫痫再发,复查MRI示术后改变,术区类圆形信号影呈缩小趋势,边缘少许强化,未见环形强化(图1D、E)。患者已于2022年8月20停用伏立康唑。




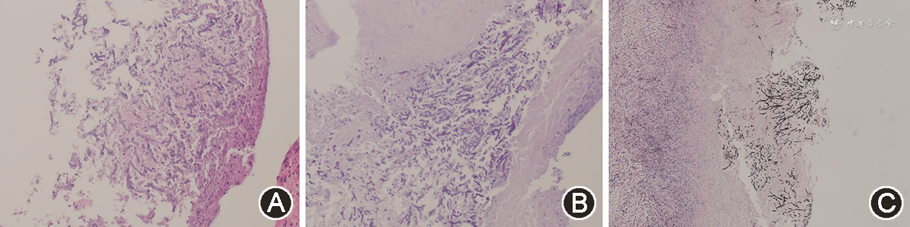

例2 患者男性,20岁,主因皮疹、双下肢水肿9年余,间断发热、抽搐3个月余入院。2011年患者出现面部红斑,伴发热、乏力,抗核抗体、抗组蛋白抗体、抗核小体抗体、抗双链DNA抗体、抗SSA抗体、抗SSB抗体均阳性,大量蛋白尿、低补体血症,肾活检示狼疮性肾炎Ⅴ型,考虑“系统性红斑狼疮,狼疮性肾炎”,予甲泼尼龙冲击,序贯泼尼松35 mg 1次/d、霉酚酸酯1 g 1次/d,激素规律减量,治疗约2年。此后病情数次波动,予足量激素联合免疫抑制剂治疗有效。2021年3月21日患者出现高热,最高体温39.4 ℃,右侧上下肢抖动,发展至全身抽搐、牙关紧闭、意识丧失,持续约30 min后自行缓解,急诊予甲泼尼龙40 mg×5 d及对症处理后好转。2021年6月9日患者再次出现发热、头痛、抽搐,体格检查发现库欣面容,颈软,无抵抗,双下肢膝腱反射活跃,病理征阳性。头颅MRI提示左侧顶枕叶占位,环形强化,伴周围大片水肿带(图5A)。考虑SLE诊断明确,合并颅内感染可能,收入北京协和医院肾内科病房。完善原发病相关评估:血常规无明显异常,血清白蛋白25 g/L,血肌酐212 μmol/L,24 h尿蛋白5.01 g,红细胞沉降率103 mm/h,超敏C反应蛋白11.38 mg/L,抗核抗体滴度1∶80,斑点型,IgG 4.82 g/L。查血清G、GM试验均阴性。腰椎穿刺脑脊液压力235 mmH2O,脑脊液蛋白0.46 g/L,脑脊液白细胞计数10×106/L,脑脊液单核细胞计数2×106/L,培养、涂片均阴性,脑脊液NGS报日本马拉色菌及溶血葡萄球菌,考虑污染可能。在治疗方面,对原发病予暂停免疫抑制剂,泼尼松减量,颅内病灶予美罗培南2 g 1次/12 h×14 d经验性抗感染、降颅压、抗癫痫治疗,复查颅内增强MRI示占位较前增大,环形强化明显(图5B)。为明确颅内感染病原,患者于2021年7月12日行神经导航下脑脓肿外引流术,缓慢抽取脓液约7 ml送检,脓液NGS回报烟曲霉菌,真菌涂片可见较多真菌丝,真菌培养发现烟曲霉菌。术后予以伏立康唑200 mg 1次/12 h治疗,监测患者体温逐渐恢复正常,原发病控制稳定后出院。出院后继续口服伏立康唑200 mg 1次/12 h,2021年10月22日线上复诊,外院复查核磁示病灶明显缩小,目前继续伏立康唑治疗中。

T1+:对比度增强T1加权成像
侵袭性曲霉病是由曲霉菌引起的深部感染性疾病,其预后十分不佳,重症病死率高达80%。CNS曲霉菌病是其中最严重的形式之一,多继发于肺曲霉菌病后的血性播散,少数也可由鼻旁窦感染后直接蔓延而来,烟曲霉菌是最常见的病原体。与其他霉菌相比,它的分生孢子直径仅2~3 μm,在环境中广泛存在,吸入后容易逃脱纤毛的清除而进入下呼吸道,且具有良好的耐热性,在人类体温范围内仍保持活性,其细胞壁中的黑色素能抵御活性氧和吞噬细胞,表面丰富的带负电荷的唾液酸则利于结合基底层蛋白,这些因素均有助于形成侵袭性感染[5, 6]。
SLE患者往往长期使用糖皮质激素及免疫抑制剂,加上自身免疫功能的紊乱,容易合并各种感染。严重的感染并发症,包括CNS感染和机会性感染,可累及高达50%的SLE患者[7, 8, 9]。但SLE合并烟曲霉菌脑脓肿较为罕见,目前国内仅有4例个案报道(表1)[1, 2, 3, 4]。2项国内SLE患者合并CNS感染的队列研究分别纳入30、38例患者,常见病原体依次为结核分枝杆菌、隐球菌和李斯特菌,烟曲霉菌感染仅各有1例报道,分别表现为肉芽肿及脑脓肿,但未进行详细描述[10, 11]。3项国内SLE合并真菌感染的队列研究分别纳入20、18、20例患者,分别包括6、3、1例烟曲霉菌感染,但烟曲霉菌感染均无CNS 受累[12, 13, 14]。

既往国内报道4例系统性红斑狼疮(SLE)患者合并烟曲霉菌脑脓肿的临床信息
Clinical manifestations of 4 reported cases of systematic lupus erythematosus(SLE)combined with Aspergillus fumigatus brain abscess in China
既往国内报道4例系统性红斑狼疮(SLE)患者合并烟曲霉菌脑脓肿的临床信息
Clinical manifestations of 4 reported cases of systematic lupus erythematosus(SLE)combined with Aspergillus fumigatus brain abscess in China
| 参考文献 | 性别/年龄(岁) | SLE受累系统 | 用药情况 | 从SLE确诊到出现神经症状的时间 | 神经系统症状 | 脑脓肿部位 | 其余系统曲霉菌感染情况 | 脑脊液 | 病原确诊依据 | 主要治疗及疗程 | 预后 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 孟强等[1] | 女/39 | 皮肤、肺脏 | 泼尼松40 mg/d | 不详 | 头痛 | 左顶枕交界 | 肺脏 | 无 | 肺活组织检查 | 伏立康唑400 mg2次/d➝200 mg2次/d,2个月 | 复查磁共振成像病灶消失,好转出院 |
| 钟琴等[2] | 女/27 | 关节,皮肤 | 泼尼松20 mg/d,吗替麦考酚酯1.5 g/d | 6个月 | 头痛,精神恍惚,恶心呕吐 | 不详 | 无 | 压力>210 mmH2O,细菌培养及墨汁染色均阴性,白细胞 4×106/L,葡萄糖3.5 mmol/L,氯化物120.8 mmol/L,蛋白0.96 g/L | 脓肿切除术 | 拒绝抗真菌治疗,脱水及对症治疗1周 | 好转出院 |
| 黄哲浩等[3] | 女/12 | 肾脏 | 泼尼松25 mg/d | 10个月 | 头痛 | 左侧基底节 | 无 | 无 | 脓液抽吸引流术 | 伏立康唑200 mg,2次/d | 术后1年复查病灶消失 |
| 范晓琳等[4] | 女/11 | 肾脏,肺脏 | 激素+环磷酰胺 | 5个月 | 呕吐,右侧肢体运动障碍 | 左侧基底节、放射冠 | 无 | 无 | 脓液抽吸引流术 | 伏立康唑 | 术后2年复查病灶消失 |
注:1 mmH2O=0.009 8 kPa
我们报道的2例患者均为青年起病,从诊断SLE到出现神经系统症状时间,例1不到1年,例2为9年余,均有足量激素及免疫抑制剂使用史,神经系统表现为意识障碍、癫痫发作、头痛、发热,脑脓肿的诊断并不复杂,但病原的确定经历曲折:经验性抗感染2周效果均不佳,直到手术明确病原,才开始应用抗烟曲霉菌治疗,伏立康唑使用数个月后复查均明显好转。加上既往报道的病例(表1),6例患者呈现出相似的特征:青年起病,有激素使用史,神经系统表现为高颅压及局部压迫症状,伏立康唑治疗效果良好。然而5例患者未发现CNS以外的病灶,提示我们对于SLE合并脑脓肿的患者,即使未发现肺部病灶,仍然要考虑烟曲霉菌感染的可能。
值得注意的是,6例患者均通过活检明确病原而非无创检查。但在临床实践中,SLE合并脑脓肿在无法除外细菌感染时,往往需要先经历一段时间的经验性抗感染,这种“实验室检查-经验性抗感染-多科会诊-手术-针对性抗感染”的诊疗路径是值得借鉴的。考虑到SLE患者常存在多系统受累,围术期风险高,应在多学科合作下进行全面的围术期管理。
我们报道的2例患者及钟琴等[2]报道1例患者的脑脊液仅表现出压力和蛋白的升高,涂片及培养均为阴性。本文2例患者行脑脊液NGS,结果亦为阴性。目前关于脑曲霉菌病的系统综述中(不限于SLE患者),85.1%的患者依靠组织病理学确诊,脑脊液培养阳性率仅19.1%,接受外科手术明确病原的患者预后相对较好[15, 16],与我们的结果一致,进一步支持烟曲霉菌脑脓肿的脑脊液培养阳性率低的结论。但Meena等[17]报道脑曲霉菌病的血清半乳甘露聚糖、脑脊液半乳甘露聚糖、脑脊液β-d-葡聚糖、脑脊液聚合酶链反应的阳性率分别为64.3%、72.9%、64.0%、70.0%。而本文的2例患者脑脊液NGS、G试验、GM试验结果均为阴性,可能与患者相对年轻、免疫状态相对较好、脓肿包裹良好有关。
NPSLE是指SLE的病程(如炎症或血栓形成)对某些神经解剖部位的原发、直接的病理学影响而导致的临床综合征[18]。根据现有的分类标准,大约20%~40%的患者有神经系统受累[19, 20, 21]。NPSLE临床表现包括头痛、脑血管疾病、认知功能障碍、癫痫发作、运动障碍、意识障碍、精神疾病、脱髓鞘疾病、脑神经病变、周围神经疾病,很难与感染进行区分[22]。而SLE合并脑脓肿在内的CNS感染的症状可因为糖皮质激素的抗炎、脱水等作用被掩盖而表现得不典型,特别是大剂量激素冲击后,极易与NPSLE相混淆[17]。
因此,对于已知存在SLE和神经系统症状的患者,需要全面进行SLE疾病活动及CNS感染相关的检查。当有其他部位狼疮活动证据时,如皮肤病变、血细胞下降、肝脏受累、肾脏受累、补体下降等,支持NPSLE的诊断,而前驱感染史、其他部位的感染证据则支持CNS感染。在脑脊液方面,炎性NPSLE可出现压力升高,细胞、蛋白增多,葡萄糖水平下降等与感染相似的表现,明显的低葡萄糖水平(<300 mg/L)支持感染,而IgG指数升高、寡克隆带阳性则支持NPSLE,但尚不清楚单独或联合应用这些指标的敏感度、特异度及预测值[23]。在影像学方面,活动性NPSLE常表现为皮质下和脑室周围白质中的小点状超信号T2加权局灶性病变。CNS感染则为脓肿、脑膜炎表现等。此外,无法除外CNS感染时往往经验性使用抗生素治疗,抗菌治疗的效果亦具有鉴别诊断价值。
本文的例1在神经系统症状出现的同时合并血小板减少、肝酶升高、肾脏受累、补体下降等SLE活动证据,且初次影像学阴性,因此第一次住院考虑为NPSLE,予规范治疗后患者症状缓解,但出院后复查影像学出现异常,考虑新发烟曲霉菌感染,但无法除外首次症状时已出现隐匿感染。这提示我们在首次脑脊液和影像学阴性时仍需要警惕后续治疗过程中出现CNS感染,或者CNS感染处于影像学不典型的早期。
所有作者声明不存在利益冲突
None declared



























