心磁图(MCG)是心肌活动产生电磁场变化的检测分析技术,在心脏疾病的诊断、风险分级、疗效评估等方面有潜在优势,特别是冠心病及心律失常方面。然而由于操作耗时、技术操作复杂、成本高等原因,现阶段MCG仍难以像心电图一样普及使用。本文就国内外MCG的发展现状及其在成人心律失常和冠心病领域的研究作综述。

除非特别声明,本刊刊出的所有文章不代表本刊编辑委员会的观点。
心磁图(magnetocardiography,MCG)是心肌活动产生电磁场变化的检测分析技术,在心脏疾病的诊断、风险分级、疗效评估等方面有潜在优势[1]。本文就国内外MCG的发展现状及其在成人心律失常和冠心病领域的研究作一综述。
1963年Baule和McFee首次在常温下非屏蔽的室内利用线圈式磁量计检测到心脏产生的磁场信号。1970年Cohen等发明了超导量子干涉仪(superconducting quantum interference device,SQUID),为MCG的发展带来了革命性突破。SQUID传感器是利用低温超导技术,在低温零下269℃使金属铌的电阻变为零而成为超导体。将超导体做成超导环并把超导环对应部位做成两个极薄的绝缘层(Josephson结点),当偏置电流通过时,超导状态破坏并产生Josephson效应及信号,经振荡器取出及放大等处理后获得明显的磁场信息。
MCG近年来已获很大发展,从单通道发展到多通道,从单点测量到多点测量[1],也出现高温超导MCG仪。目前MCG还具有检测三维信号并实现心脏三维重构的功能[2]。高温超导及小型MCG的出现可使其进一步小型化并降低成本,有望能像心电图一样方便使用[3]。
Cohen等将犬的冠状动脉闭塞,通过MCG测量ST段的变化等心肌损伤电流,首次展现出MCG对心肌缺血的诊断价值。MCG中的QT离散度、QRS波间期、ST段斜率、T波等多种参数在心肌缺血时有变化,在心肌缺血的诊断、定位、预测不良事件等方面有较大的应用潜力(图1)[4]。
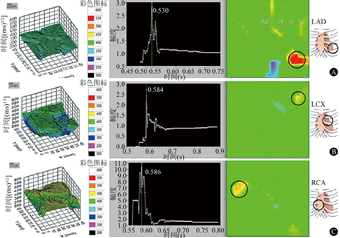
Hänninen等研究显示,冠心病患者的ST段和T波顶点的MCG磁场梯度方向有明显不同。Hailer等[5]用MCG获得ST-T段的电流密度矢量图,发现尽管所有患者心电图正常,但MCG的ST-T段的电流密度矢量图在正常组、冠状动脉狭窄的冠心病组和有冠心病症状但冠状动脉无狭窄组之间有明显差异。非冠心病患者MCG为0~2级,而冠心病患者多为3~4级。
Park等[6]用MCG、心电图、肌钙蛋白I和超声心动图等方法对185例非ST段抬高的冠心病患者行前瞻性、头对头的对比研究,采用T波开始到最高峰的间期作为缺血指标。研究发现,相比心电图、肌钙蛋白I和超声心动图,MCG对冠心病有很高的预测率。虽然在特异性方面MCG与心电图及肌钙蛋白I相近,但较超声心动图明显升高。随后用单变量分析评价静息时MCG异常对3年死亡率相对风险系数为4.58,心电图为1.69,超声心动图为1.58,肌钙蛋白I为2.48,多重分析显示MCG有很强的死亡风险预测价值[7]。Park等[8]发现,利用MCG中的ST段变异积分可以发现冠状动脉血流储备分数低于80%的冠心病。Quan等[9]利用MCG对支架内再狭窄进行研究,事先假设正常人平均电流密度和不正常的图形比率为标准值零,发现这两个参数在术后7个月支架内再狭窄组比非再狭窄组均明显升高。
Kwon等回顾性分析发现,MCG对于区分冠状动脉狭窄大于50%的患者的敏感度和特异度达84.0%和85.0%。Park等[10]对冠心病患者行多巴酚丁胺试验,显示MCG对冠状动脉狭窄大于70%的诊断准确性明显高于心电图。一组荟萃分析显示,MCG诊断冠心病的敏感度为86%,特异度为77%,MCG诊断冠心病的阳性可能性为3.92(95%CI:2.30~6.66),阴性可能性仅为0.20(95%CI:0.12~0.35),与其他现有非侵入性手段诊断率相似[11]。然而,由于MCG获得信号的特殊性,对于切线式和旋涡式的电流检测敏感度更高[12],因此MCG对冠心病诊断可能有其独特价值,甚至在冠心病的早期诊断、慢性缺血评估等方面有实用价值。
MCG晚期电活动是检测QRS终末端的电位,与心电图晚期平均信号(signal-averaged ECG,SAECG)相当。Mäkijärvi等[13]研究包括10例持续性室性心动过速在内的20例心肌梗死患者,采用3个MCG晚期参数:QRS持续时间(QRSd)、QRS波后60 ms的均方根值(root mean square,RMS60)幅度和信号幅度低于700 fT(LAS700)的持续时间,发现这3个MCG参数在有无室性心动过速的心肌梗死之间有明显差异。SAECG也能发现这些差异并较MCG略有优势。这个结果也被随后更大样本的临床研究证实,并在亚组分析中发现,对于射血分数小于40%的患者MCG预测室性心动过速较SAECG更敏感,MCG的这3个参数在组间比较均有差异,而SAECG中只有QRSd有差异[14]。另一项研究发现,在心肌梗死后7~15 d,MCG-QRSd>121 ms和SAECG-QRSd>114 ms可以预测心律失常事件和心原性猝死。
MCG也可获得QRS碎裂参数,即QRS碎裂极性变化的个数(QRS-M)和QRS碎裂积分(QRS-S)。Endt等[15]研究发现,MCG检测碎裂参数几乎可发现所有的心肌梗死后室性心动过速,并且较心电图更敏感。Korhonen等[16]研究发现,所有MCG晚期电活动及QRS碎裂参数在有无室性心动过速之间均有差异,且在射血分数小于40%组差异更明显。随后进一步发现MCG-S对室性心动过速的预测较心电图QRSd更敏感。利用7导屏蔽式MCG对158例急性心肌梗死且射血分数小于50%的患者进行研究,随访(50±15)个月发现,QRS碎裂参数积分在心律失常事件组较无心律失常事件组明显升高,死亡组较生存组也明显增加,提示QRS碎裂参数对预后有很强的预测价值。
Oikarinen等[17]对10例有室性心动过速的患者和8例无室性心动过速的患者选取MCG的2个QTd参数,即QT最高点的离散度和QT终点离散度。研究发现,室性心动过速组的QTd比无室性心动过速组明显增加(QT最高点的离散度:127±26比83±21,P=0.004;QT终点离散度:130±37比82±37,P=0.013)。Chen等[18]用64导MCG测量重型地中海贫血需长期输血患者的QT平滑指数、QT离散度及QT标准差,并用心动周期进行校正,结果发现,长期输血引起的心肌铁负荷过重使患者的心肌复极变异性大,并与心血管不良事件有关。
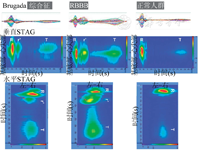
Kandori等[19]发现Brugada综合征患者在右心室流出道附近存在异常MCG。Joung等[20]用MCG中的电活动时空图(spatiotemporal activation graph,STAG)研究发现,Brugada综合征患者水平方向STAG的r'波明显,磁场图和电流密度矢量图也有明显差异,特别在T波末端的30~60 ms之间(图2)。
MCG具有定位心律失常病灶源的潜力。Weismüller等[21]用MCG得到的信息确定预激综合征又称Wolf-Parkinson-White(WPW)综合征旁路位置,与心导管测得的位置很相近。Brisinda等对1例室上性心动过速患者,利用MCG记录异常信息,结合磁共振断层成像而确定消融点并成功消融异常通道。最近一个研究显示,利用MCG区分起源于右心室流出道和主动脉窦的室性心动过速准确率达94%[22]。Fenici等[23]对28例WPW患者进行两次检查以检验测量的可重复性,对8例患者用不同的MCG仪器检查,在最大的室性预激波和(或)由一非磁性的电极经食管心房调搏诱发房室折返性心动过速期间进行评估,发现MCG对预激波的分类定位比心电图更精确,也为间隔旁路的判断提供了更多信息。
Koskinen等[24]用MCG对9例阵发性心房颤动研究发现,心房颤动患者心房信号面积和RMS40幅度明显比正常人群增加[心房信号面积(fT ms):11 800±3 680比8 040±2 070,P=0.003;RMS40:94±23比63±15,P=0.001],而心电图却无明显差异。Lehto等对26例进行电转复的持续性心房颤动患者研究发现,相比健康人群,持续性心房颤动节律恢复即刻的P波时间和P-RMS40明显升高,在复律后1个月P波时间仍明显延长。2008年Naka等报道了MCG三维重构可以帮助心房颤动射频消融。Kim等[25]发表了首个利用MCG三维重构对慢性心房颤动消融的使用价值:利用MCG发现慢性心房颤动心房不正常的电活动精确路径,从而减少手术程序。对一些特殊的电生理障碍如心房电阻滞的Bayeś综合征等MCG可能有特殊的诊断及研究价值[26]。
虽然我国有多家单位实施了MCG临床研究,然而多集中于冠心病方面,在心律失常方面的研究尚稀少。赵丹等对MCG的T峰7项参数(前磁向量、前磁移动距离、前磁向量变异率、后磁向量、后磁移动距离、后磁向量变异率、前后磁向量变化)研究发现,冠心病组与非冠心病组7项参数的差异均有统计学意义。MCG的7项参数中任意3项以上为阳性则诊断冠心病的敏感度为56.40%,特异度为90.91%。李英梅等[27]研究发现,冠心病的Rmax/Tmax比值(电流密度分布图中R波与T波的最大电流密度矢量值的比值)显著高于健康人群。布伦等检测96例不稳定型心绞痛患者(冠状动脉造影显示至少有一支血管狭窄≥70%)和106例健康人群,结果显示两组的磁偶标准记分、源磁偶标准记分、磁偶角度变化、磁偶距离变化和磁偶极值变化比值等指标有显著性差异,并显示MCG对不稳定型心绞痛诊断的阳性率显著高于心电图及超声心动图。
MCG还存在一个国产化的问题,我国现使用的MCG仪均是国外生产,一些配套的相关软件及参数都是根据国外的临床资料来设计与设置的,这些参数在我国未必全部适用。1986年,中国科技大学研制出我国第一台MCG仪,成为我国MCG研究的起点。利用心电图驱动的小线圈系统可使MCG信号不会丢失或失真,我国学者在未密闭的环境内也可获得很好的MCG信号[28]。近期由中国科学院上海微系统与信息技术研究所自行研制的国产化MCG设备取得很大进展,已在我院进入临床测试及研究阶段。有关《多通道心磁图仪临床研究探索》项目已在我院开展,希望能获得我国健康人群以及部分疾病人群的MCG数据,有利于我国自行研发的MCG向临床转化(图3)。
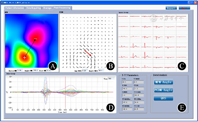

A:等磁图;B:伪电流密度图;C:空间波组图;D:时间波组图;E:等磁图分析弹窗
MCG是一种有前景的非侵入性心血管疾病诊断工具,但目前仍难以在临床广泛使用,主要原因包括:(1)使用成本高、价格贵、操作要求高及耗时等;(2)相比心电图,MCG是一个"庞然大物",使用笨拙。操作、解释和分析MCG数据需依赖经训练的人员和复杂的计算机系统,得出结论更耗时;(3)由于各厂家的MCG仪的记录通道和分析软件不同,所用的参数也不尽相同;各种MCG仪的信号采集、分析方法、通道数量、观察指标仍不统一;(4)MCG信息量大,相关数据多,仍缺乏公认的正常值和各种疾病的诊断标准;(5)MCG临床应用时间较短,病例资料积累少,需大规模的临床试验和经验总结来支持它的发展,更需要与心电图等其他无创性检查互相对比及印证。
从总体上看,MCG可高度保真的信号来源及高度复杂的矢量磁测量系统,在心脏病诊疗中展现新的广阔前景。MCG有如下特殊性:(1)MCG探头不直接接触皮肤,其基线可确定为绝对基线,而心电图基线为相对基线;(2)MCG与心电图的波形相似,但振幅和波型方面有某些差别,可能有心电图不能反映的内容;(3)对于环线电流因作用抵消而不显示电位差,可能有明显的MCG变化。MCG还可以记录三维空间的磁场向量,并可行三维重建[2];(4)MCG对心脏切线电流最敏感,能准确记录切线方向的电流。在某些病理影响时,这种切线电流效应可明显增加[29];(5)MCG具有很好的时空分析功能。应用MCG的诊断特殊性,特别在冠心病及室性心律失常领域,使其电活动异常得到早期预警,也为认知心血管的病理生理提供更多帮助。
总之,随着MCG设备技术逐渐成熟、相关分析软件的开发及临床应用研究进一步深入,MCG有希望给心血管疾病患者及医生带来更多的帮助。
无