
J波主要是因心室外膜复极1相Ito电流相对增大,使心室肌内外膜之间产生电位差引起J点上移而形成的圆顶形心电波。高危J波与恶性心律失常密切相关,是心脏性猝死的高危预警信号。

除非特别声明,本刊刊出的所有文章不代表本刊编辑委员会的观点。
1887年,英国生理学家Waller用毛细管静电计成功记录到人类第1份心电图,为现代心电图的问世奠定了基础。此后,荷兰生理学家Einthoven不断研究改进心电图描记方法,用弦线式电流计记录到第1份真正意义上的心电图,并将心电图上的五个不同波形分别命名为P、Q、R、S和T波,且一直沿用至今。随着近年对各种心电现象认识的不断深入,一些学者对某些特殊的心电波形进行了命名,J波就是其中之一。最近研究发现,J波与恶性室性心律失常关系密切,高危J波是心脏性猝死(sudden cardiac death,SCD)的重要预警心电标志[1]。
J点是指体表心电图QRS波终点与ST段起点的结合点。J点一般多位于等电位线上,可随ST段变化,上下偏移一般不超过0.1 mV。当J点从基线明显向上偏移(≥0.2 mV)并持续一定时间(≥20 ms)时,形成向上的圆顶样或驼峰样偏离基线的波,称为J波(又名Osborn波)(图1)。
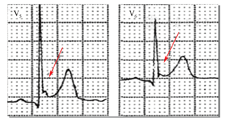

箭头所示为J点上移形成J波
根据产生原因不同J波可分为两大类:一类是遗传性J波,包括早期复极综合征J波,Brugada综合征J波及可导致特发性心室颤动的下壁导联J波;另一类是获得性J波,包括低温性J波、神经源性J波、急性缺血性J波和药物(钠通道阻滞剂)、发热等导致的J波。
越来越多的学者认为J波提示心室提前发生复极。在心室动作电位的除极和复极过程中有一重叠区,正常时该区持续时间为10 ms,形成J点,而在某些因素作用下重叠区可增宽,形成J波[2],这种心室复极提前形成J波的理论已被广泛接受。
在健康人心室三层心肌细胞中,中层M细胞和内、外膜细胞的动作电位时程持续时间长短存在显著差异,这种差异称为固有的异质性,也称为跨室壁复极离散度(transmural dispersion of repolarization,TDR)。Yan等[3]经冠状动脉灌注犬的离体心肌组织块,同步记录了跨心室壁内、中、外三层心肌细胞跨膜动作电位和对应心电图,通过比较跨膜动作电位和跨壁心电图,得到以下结果:
(1)J波与心外膜心肌细胞动作电位的l相切迹直接对应。在犬心室肌楔形组织块模型上行心内膜刺激时,心外膜心肌细胞的除极晚于心内膜,在心外膜复极1相切迹时,对应的跨室壁心电图能记录到J波;当电刺激心外膜时,则心外膜先除极,心内膜后除极,心外膜动作电位上的切迹所对应的J波融合在了QRS波群之中[3]。因此,心电图上看不到J波,提示J波与心外膜心肌细胞动作电位的l相切迹相对应(图2)[4]。
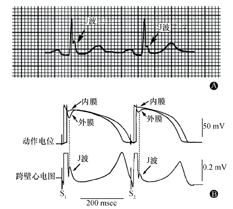

A:1名亚洲年轻健康男性的体表心电图Ⅱ导联J波(箭头所示);B:犬心室动作电位和心电图
(2)心外膜心肌细胞的1相切迹与Ito电流相关[5]。Ito电流又称瞬时外向钾电流(transient outward current),包括Itol和Ito2两种成分。其中Ito1的激活、失活和复活均呈电压依赖性,而Ito2属于Ca2+依赖性成分。当心外膜细胞0相去极化电压为-40~0 mV时,Ito1迅速激活并较快失活而导致这些心肌细胞1相的快速复极,使动作电位在1相下降较快,形成1相及2相起始部位的向下切迹。Ito是钾离子外向电流,并随除极时去极化电位的增大而增大,参与动作电位复极1相的形成。正常时心外膜动作电位Ito电流较心内膜大,并形成较深的1相切迹圆顶-穹窿与心电图的J波相对应,并发现右室心外膜心肌细胞较心脏其他部位心外膜的Ito电流密度更大。
(3)J波变化的特征具有Ito电流依赖性。使用Ito的阻滞剂4-氨基吡啶(4-AP)干预,可观察到心外膜"切迹"明显变浅,对应心电图J波降低,应用选择性钾通道开放剂时,心肌细胞1相切迹增大;将组织块灌流液的温度由正常36℃降至29℃时,心外膜心肌动作电位"切迹"更加明显,同时心电图J波也更明显地增高、增宽,当温度回升至34℃后,J波和外膜"切迹"同时恢复到接近正常水平,提示J波具有低温依赖性;当缩短刺激周长时,外膜"切迹"和J波则同时变小;反之则相反,提示J波具有慢频率依赖性,此特点是Ito电流的特征。另外,心脏Ito电流数量在年龄性别上存在差异,男性大于女性(8∶1),尤其是男性青壮年,据推测这一特点可能与性激素睾酮有关,故临床上J波综合征的患者男性青壮年居多。所有影响Ito电流及其通道活性的因素均可影响J波的形成。
总之,通过系列基础研究表明,J波是由心室复极1相和2相早期心内外膜心肌细胞Ito电流分布不均匀而产生的电位差所致[6]:心室外膜动作电位复极1相和2相早期因净外向电流是增大的,使超射电压很快降低,因此复极早期形成明显切迹圆顶-穹窿;而此时心内膜Ito电流相对小,通常没有明显切迹,这使心内膜处于高电压,心外膜相对低电压,从而产生从心内膜向心外膜的电流,因检查时电极靠近心外膜,故心电图J点上移而产生J波。其离子流机制为Ito电流增大,同时如果伴有IK1、IK-ATP等其他外向钾电流的增加和(或)INa、ICa-l的内向电流减少,使净外向电流加大,加速复极,亦可导致动作电位复极早期切迹增大,心电图J点上移产生J波。
另一种学说认为,J波是心室延迟除极波。近年研究提出,经心外膜途径消融右室流出道,可使Brugada综合征患者的右胸导联J波消失[7]。
J波可引发2相折返,在某些病理情况下1相Ito电流使心外膜动作电位切迹足够深,以致达到L型钙通道开放阈值,可能使心外膜动作电位圆顶完全消失。但在心外膜动作电位圆顶消失之前,首先表现出圆顶出现延迟,从而导致动作电位时程延长,呈现下斜型ST段抬高,这其实是一个巨大的J波,并伴有T波倒置。随后,心外膜动作电位圆顶完全消失,动作电位时程缩短(图3)。但心外膜动作电位圆顶的消失并不一致,一些区域的圆顶消失,另一些区域则处于延迟阶段,使跨室壁复极离散度更大。由于心外膜不同区域动作电位时程不同,圆顶消失区域复极速度快,类似于早期后除极的发生机制。因此,在电压差作用下低电位区域可产生一个新的动作电位,形成一短偶联间期异位搏动,从而引发心室颤动。心外膜动作电位圆顶形成于2相时期,故称为2相折返机制[8]。
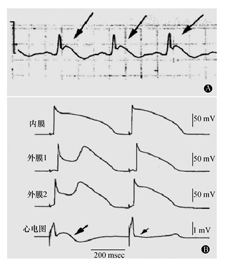

A:箭头所示圆顶延迟出现导致动作电位时程延长;B:心外膜不同区域圆顶延迟程度不同(外膜1迟于外膜2),左侧箭头示圆顶延迟出现,右侧箭头示圆顶完全消失
近年医学界一直在研究SCD的高危因素和可预测其发生的特殊心电波形,发现心电图存在J波的部分患者,常反复发生多型性室性心动过速、心室颤动甚至猝死,可以预警SCD的风险。
J波介导的2相折返可致心室颤动,心外膜动作电位1相和2相早期存在电位差诱发2相折返,同时伴有TDR增大导致的心室颤动[9,10]。动物实验与临床观察[11]均证实:(1)Ito电流的显著增加,不仅能使心外膜心肌细胞动作电位的1相切迹增大,还能使2相的穹顶和平台期消失,使动作电位时程缩短40%~70%;(2)穹顶和平台期的消失,在心电图上表现为ST段抬高,后者是心室颤动发生与维持的基质;(3)心外膜不同部位的心肌细胞存在2相穹顶正常与消失共存的情况,可形成心外膜不同部位之间的电位差,导致电激动能从电位高的心外膜部位向电位相对低的心外膜另一部位传导,从而产生了电流,局部电流达到除极阈电位时会引起一次新的除极,因各部位传导速度不均一,易产生折返,因折返发生在动作电位的2相,故称为2相折返;(4)2相折返可表现为联律间期很短的R-on-T型室性期前收缩,进而形成心室颤动[12](图4)。
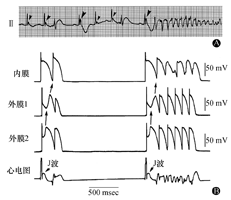

A:人心电图Ⅱ导联示J波引起多型性室性心动过速、心室颤动(箭头所示长间歇后J波增大导致R-on-T型室性期前收缩);B:J波介导2相折返引起犬室性心动过速、心室颤动:部分动作电位穹顶完全丢失(外膜1),另一部位的细胞则保留着穹顶(外膜2)
动物实验表明,急性ST段抬高型心肌缺血发生2~10 min时,心室颤动最早触发部位常在心外膜心肌缺血区的边缘,触发心室颤动的室早联律间期短,伴R-on-T现象,正是这种室性期前收缩诱发了心室颤动。Haïssaguerre等[13]对206例年龄<60岁的特发性心室颤动患者的心电图和临床特点进行研究表明,特发性心室颤动组J波发生率为31%,健康对照组人群中J波发生率仅5%,存在显著差异(P<0.01)。肖洁莹等[14]对比分析了SCD与非SCD患者的心电图表现,结果显示SCD患者心电图J波的出现率明显高于非SCD患者(95.0%比27.5%),存在显著差异(P<0.05)。
J波介导的2相折返虽然可致室性心动过速或心室颤动发生,但并非所有J波患者均存在猝死风险,高危J波主要与以下几个因素有关[15]:(1)分布导联:J波出现在下壁导联常可发生恶性室性心律失常;而在前侧壁导联者极少发生室性心动过速/心室颤动;J波发生在所有导联可发生心室电风暴;(2)振幅:与年龄、性别等变量相匹配的健康对照组相比,特发性心室颤动患者的J波振幅明显增加,J波振幅与风险显著相关[16]。Tikanen等[17]认为,当J波≥0.2 mV时风险最大;(3)动态变化:Nam等[18]和Aizawa等[19]均报道了特发性心室颤动患者可见J波幅度动态改变,尤其是室性心动过速/心室颤动发作前J波振幅可显著抬高。Derval等[20]发现,心室颤动发作前下壁导联J波的振幅从(0.26±0.10)mV增大至(0.41±0.20)mV;(4)长间歇依赖性J波振幅增高;(5)频发短偶联间期的室性期前收缩或短–长短周期现象;(6)既往多型性室性心动过速、心室颤动、不明原因晕厥史、SCD家族史等。
无



























