
托伐普坦是选择性精氨酸加压素(AVP)V2受体拮抗剂,可拮抗心力衰竭时异常增多的AVP对肾脏的抗利尿作用,迅速改善心力衰竭患者的水潴留及低钠情况。应用托伐普坦发生高钠血症的可能性小,但预后差。本文重点介绍托伐普坦在治疗心力衰竭时高钠血症的发生率、危险因素、预后、预防和治疗等的国内外研究进展。

除非特别声明,本刊刊出的所有文章不代表本刊编辑委员会的观点。
托伐普坦作为世界上首个口服的普坦类药物,为选择性精氨酸加压素(arginine vasopressin,AVP)V2受体拮抗剂,通过拮抗心力衰竭(以下简称"心衰")时异常增多的AVP对肾脏的作用,提高游离水的清除率,降低尿渗透压,提高血钠水平,可帮助心衰患者迅速改善水潴留和低钠情况[1]。2009年,托伐普坦首先被美国食品和药物管理局批准用于治疗高容量/正常容量的低钠血症,包括心衰、肝硬化及抗利尿激素分泌不当综合征,后又被批准用于传统药物治疗效果不佳的心衰患者以利尿脱水和减轻体重[2,3,4,5],以及常染色体显性遗传性多囊肾病以降低肾体积的生长速度和肾功能的下降速度[6,7,8,9]。至今已有多项临床研究证实,治疗充血性心衰时,早期应用托伐普坦联合常规利尿剂相比于仅用常规利尿剂,可迅速、持续地利尿排水,减轻体重,提高血钠水平,在短期内改善心衰患者的症状和体征,减少卧床、住院时间和在院死亡率[10,11,12,13,14]。
托伐普坦相关的常见不良反应包括多尿、口渴、乏力、恶心、呕吐、头晕、头痛、外周水肿等,对预后均无明显影响,如可耐受则不影响应用。而高钠血症为其临床上的严重并发症,虽发生率低,但预后不良。自托伐普坦上市以来,国内外对其安全性和有效性进行了多项临床研究。本文以"tolvaptan"OR"hypernatremia"为检索策略,查阅了PubMed、中国知网等数据库2000—2019年的相关综述和试验研究的参考文献,对托伐普坦管理心衰患者时高钠血症的发生率、危险因素、预后、预防及治疗进行系统回顾如下。
既往文献中因各研究中心对高钠血症的定义略有不同,且样本之间存在差异,所获得的高钠血症发生率也有所不同。本文检索到的文献中高钠血症的发生率介于1.69%~27.81%之间[11,15,16]。2018年,日本循环杂志发表的文章通过回顾3 349例心衰患者使用托伐普坦的治疗效果和安全性,分析了心衰患者应用托伐普坦治疗时高钠血症(定义为血钠浓度≥150 mmol/L)的发生率和相关危险因素,于可获得基线和治疗后血钠浓度数据的2 875例患者中,105例(3.65%)出现了高钠血症,其中90%的高钠血症发生在治疗过程的前7 d内。在发生高钠血症的患者中,经主治医师评估,14例出现了较为明显的临床症状如意识障碍等,称之为显著高钠血症,发生率为0.42%(14/3 349例),其中7例死亡,2例死亡原因考虑与高钠血症有强相关性(死亡原因为多脏器功能衰竭和严重心衰)[17]。2014年,在日本的一项多中心观察性研究中,通过观察不同剂量的托伐普坦对1 057例袢利尿剂治疗效果不佳的心衰患者的反应,来评价托伐普坦治疗心衰的安全性,其中40例(3.79%,40/1 056)发生了高钠血症(定义为血钠浓度≥150 mmol/L),且多数发生在开始托伐普坦治疗的前3 d内[10]。2016年,Hirai等[2]在欧洲临床药理学杂志上发表的文章回顾性分析了托伐普坦治疗371例患者的临床资料,来探讨长期应用托伐普坦的安全性和高钠血症发生的危险因素,该研究以血钠浓度147 mmol/L为界限定义高钠血症,入组的338例为心衰失代偿期患者,余为肝硬化患者。托伐普坦治疗的中位时间为13 d,33.20%和18.10%的患者使用托伐普坦治疗的时间分别大于1个月和3个月,初始剂量中位值和平均值均为7.5 mg/d。结果显示,94例(27.81%)心衰患者发生高钠血症,其中70例(20.71%)在开始托伐普坦治疗的7 d内发生(早期发病),24例(7.10%)在7 d后发生(迟发)。2014年,北印度的1项单中心观察性研究给予40例急性失代偿期心衰伴低钠血症(血钠浓度<125 mmol/L)患者服用托伐普坦15 mg/d共7 d,同时监测高钠血症(定义为血钠浓度>145 mmol/L)的发生率,结果显示10%的患者出现高钠血症[18]。本文对所检索到的文献相关数据进行荟萃分析,并进行异质性检验(I2=97.2%,P<0.000 1),因此选择随机效应模型,对应用托伐普坦治疗心衰时高钠血症的发生率得出较为准确的数据为6.84%(表1、图1)。
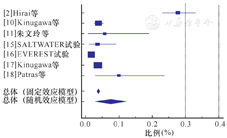

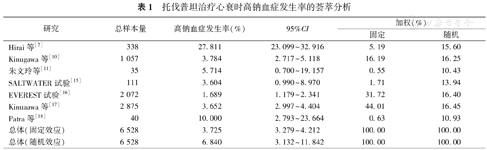
托伐普坦治疗心衰时高钠血症发生率的荟萃分析
托伐普坦治疗心衰时高钠血症发生率的荟萃分析
| 研究 | 总样本量 | 高钠血症发生率(%) | 95%CI | 加权(%) | |
|---|---|---|---|---|---|
| 固定 | 随机 | ||||
| Hirai等[2] | 338 | 27.811 | 23.099~32.916 | 5.19 | 15.60 |
| Kinugawa等[10] | 1 057 | 3.784 | 2.717~5.118 | 16.19 | 16.25 |
| 朱文玲等[11] | 35 | 5.714 | 0.700~19.157 | 0.55 | 10.43 |
| SALTWATER试验[15] | 111 | 3.604 | 0.990~8.970 | 1.71 | 13.94 |
| EVEREST试验[16] | 2 072 | 1.689 | 1.179~2.341 | 31.72 | 16.40 |
| Kinuaawa等[17] | 2 875 | 3.652 | 2.997~4.404 | 44.01 | 16.45 |
| Patra等[18] | 40 | 10.000 | 2.793~23.664 | 0.63 | 10.93 |
| 总体(固定效应) | 6 528 | 3.725 | 3.279~4.212 | 100.00 | 100.00 |
| 总体(随机效应) | 6 528 | 6.840 | 3.132~11.842 | 100.00 | 100.00 |
前述Kinugawa等[17]的研究显示,高钠血症的危险因素包括基线血钠浓度≥142 mmol/L、基线血钾浓度<3.8 mmol/L、托伐普坦起始剂量>15 mg/d和尿素氮/肌酐比值(BUN/Cr)>20,并应用这些数据开发了托伐普坦致高钠血症的危险评分,评分=0.125×血钠浓度(mmol/L)+0.032×[BUN(mg/dl)/Cr(mg/dl)]-0.436×血钾浓度(mmol/L)+0.014×年龄,并将评分≥17.8者定义为高危人群。从风险评分方程可以看出,基线血钠浓度是高钠血症发生的最重要危险因素,如患者基线血钠浓度≥145 mmol/L,使用托伐普坦前应仔细权衡利弊。也有学者提出,托伐普坦对血钠正常患者的血钠浓度无明显升高作用,但建议每位患者在应用前均应行风险评分,以确定最佳初始剂量、预防高钠血症的发生;而高危人群起始剂量应为3.75 mg/d,如预期效果差且耐受该药物者,可考虑将给药剂量增至7.5 mg/d[19]。前述Kinugawa等[10]的研究也得出了相似的结论,血钠浓度升高≥142 mmol/L(P<0.000 1)、托伐普坦起始剂量为15 mg/d(P=0.000 9)和血钾浓度降低<3.8 mmol/L(P=0.004 3)为高钠血症的独立预测因子,因此建议正常血钠和低血钾患者使用低剂量托伐普坦以预防高钠血症发生。前述Hirai等[2]的研究应用逐步分析法得出,基线血钠浓度≥140 mmol/L、托伐普坦起始剂量>7.5 mg/d和BUN/Cr≥20是早期(7 d内)发生高钠血症的独立危险因素,预测托伐普坦平均剂量>7.5 mg/d和年龄≥75岁是晚发(7 d后)高钠血症的危险因素。考虑老年患者口渴阈值较高,饮水相对减少,有效循环血容量较少,参与高钠血症的发生[20]。不过,2018年有学者通过比较大于80岁和小于80岁的充血性心衰患者应用托伐普坦的安全性发现,两组的托伐普坦致不良事件的总体发生率无显著差异,与小于80岁组比较,大于80岁组可能因渴觉降低致口渴发生率低,但高钠血症发生率并未增加[21]。
发生高钠血症的症状和体征主要表现为中枢神经系统功能障碍,尤其是血钠浓度升高幅度较大或升高速度较快时,其临床表现更为明显,包括肌肉抽搐、兴奋、烦躁不安、嗜睡和昏迷。高钠血症引起的脑萎缩可导致颅骨与脑皮质之间血管张力增加,静脉血管破裂,造成脑出血、蛛网膜下腔出血和永久性神经损伤或死亡[22,23]。
高钠血症导致的死亡率依病情的严重程度和发病快慢有很大差异,同时也很难将高钠血症与原有疾病造成的死亡分开。既往研究缺乏心衰患者应用托伐普坦时发生高钠血症对预后影响的数据,但有关高钠血症的相关研究显示,轻度高钠血症患者(150 mmol/L<血钠浓度≤155 mmol/L)和严重者(血钠浓度>155 mmol/L)的死亡风险分别为正常血钠患者的2.32倍和3.64倍[24]。国外一项对8 140例重症监护室患者的回顾性研究显示,出现高钠血症后患者的死亡率为46.20%[25];而国内的一项研究中重症监护室患者发生高钠血症后其死亡率高达71.40%[26]。
托伐普坦所致的高钠血症发生率低,但预后不良,为有效预防高钠血症,建议托伐普坦尽量用于住院患者,使用前应在了解病史的基础上,全面评估患者可能发生高钠血症的相关危险因素如年龄、血清钠、钾水平、有效循环血容量(如尿量小于1 000 ml/d、血压降低、皮肤黏膜苍白干燥、浅表静脉不充盈、脉搏弱及中心静脉压低,可一定程度上提示有效循环血容量降低)和肾功能等,根据高钠血症的危险评分评估托伐普坦的应用风险,以确定能否应用托伐普坦并选择合适的初始剂量。由于老年患者发生高钠血症的风险相对较高,建议使用低剂量托伐普坦,以小于7.5 mg/d为起始剂量,视患者反应而调整剂量。在托伐普坦大规模上市后,START研究[27]在监测其治疗肝硬化水肿的安全性和有效性中发现,托伐普坦在治疗肝硬化水肿患者时高钠血症的发生率较低(0.2%,1/453),分析其原因可能是相较于心衰患者,肝硬化患者几乎均给予了螺内酯口服,而螺内酯可提高血钾浓度。因此文中认为,醛固酮拮抗剂对高钠血症可能具有一定的预防作用。并且有学者推测,醛固酮拮抗剂如螺内酯可能通过抑制醛固酮诱导的钠重吸收而预防高钠血症发生[17],但仍需更多的研究来确定醛固酮拮抗剂在预防高钠血症中的作用。
高钠血症的治疗包括两方面:停用托伐普坦及其他可能导致血钠升高的药物,纠正当前的高钠血症。高钠血症发生后,组织液高渗状态引起细胞脱水收缩,主要表现在中枢神经系统。脱水收缩的脑细胞会迅速做出反应以对抗高渗状态的组织液对细胞的进一步损伤:数小时内组织间隙的电解质进入脑细胞(快速适应),阻止脑细胞继续脱水并携带水分子进入细胞,脑细胞容量部分恢复;数天内脑细胞通过产生并积累有机渗透物质(缓慢适应),减少细胞内外渗透压,使脑细胞容量正常化。此时尽管脑容量正常,但脑组织的高渗透压仍存在。对高渗状态的缓慢纠正,累积的电解质和有机渗透物质的耗散与水的充盈同步,可不引起脑组织水肿并重建正常的脑渗透压;相反,快速纠正可能会因脑细胞对水的吸收超过积累的电解质和有机渗透物质的消散而导致脑水肿,进而有发生更严重神经功能损害的风险[28,29]。
在托伐普坦应用过程中,临床医生会定期监测电解质变化,因此高钠血症的发生多为数小时内被发现,此时快速纠正高钠状态,脑细胞内积累的电解质会迅速从细胞中释放至组织间隙,可有效改善预后,且不会增加脑水肿的风险,血钠浓度可以每小时1 mmol/L的速度降低;而对于发生时间较长(数天)或时间未知的高钠血症者,纠正速度需缓慢,这种情况下建议以不高于每小时0.5 mmol/L的速度降低血钠浓度,防止脑水肿和抽搐发生。因此,Adrogué等[22]建议,对所有高钠血症患者均应有针对性地降低血钠浓度,不管何种类型(数小时或数天前发生)的高钠血症者,血钠浓度可每天均匀降低10 mmol/L,目标为降至145 mmol/L。降钠补液途径首选口服或管饲,如这两种方法均不可行,则行静脉输液。所应用液体应为低渗液,包括纯水、5%葡萄糖溶液、0.2%氯化钠溶液和0.45%氯化钠溶液(钠浓度分别为0、0、34和77 mmol/L),除出现明显的血容量不足外,一般不应用0.9%的氯化钠溶液。按照以下公式计算所需液体量:输注1 L液体对血钠的影响(mmol/L)=(所输液体的钠浓度-血钠浓度)/(体液总量+1),其中体液总量(L)是按体重(kg)的比例计算的,非老年男性这一比例为0.6,非老年女性为0.5,老年男性为0.5,老年女性为0.45。
托伐普坦用于治疗常规利尿药效果不佳的心衰患者,可发挥利尿、减轻水钠潴留的作用,虽其发生高钠血症并发症的可能性小,但预后差,与患者基础的血钠、血钾浓度,血清BUN/Cr,年龄以及起始托伐普坦剂量相关,主要导致中枢神经系统的功能障碍甚至死亡。结合相关文献数据,本文作者认为,在临床工作中使用托伐普坦前应详细评估高钠血症的发生风险,以小剂量起始应用,密切监测出入量、电解质、肝肾功能及血容量等重要指标,预防以及及时发现高钠血症,并迅速进行适宜处理以降低高钠血症造成的不良后果。
无



























